المجهر الإلكتروني الارتباطية الخفيفة (كليم) لتتبع وتصوير البروتينات الفيروسية المرتبطة الهياكل في الخلايا المعطل تداولها البرد
Summary
يتم تطبيق أسلوب ستتحقق خفيفة الميكروسكوب الإلكتروني (كليم) للصورة التي يسببها فيروس هياكل داخل الخلية عبر الميكروسكوب الإلكتروني (م) في الخلايا التي تم تحديدها سابقا عن طريق الخفيفة الميكروسكوب (LM). وضم كنهج تصوير هجين لتحقيق رؤية متكاملة للفيروس–المضيف التفاعلات LM وم.
Abstract
بسبب قرارها عالية، الميكروسكوب الإلكتروني (م) أداة لا غنى عنها لعلم. بيد أن إحدى الصعوبات الرئيسية عند تحليل الخلايا المصابة بالفيروسات أو ترانسفيكتيد عن طريق م هي الكفاءة المنخفضة للإصابة أو تعداء، التي تعوق النظر في هذه الخلايا. وللتغلب على هذه الصعوبة، يمكن أن يؤديها الخفيفة الميكروسكوب (LM) أولاً بتخصيص يتدنى الخلايا المصابة أو ترانسفيكتيد. وهكذا، مع استفادة استخدام البروتينات الفلورية (FPs) تنصهر فيها البروتينات الفيروسية، يستخدم LM هنا لتسجيل مواقف الخلايا “transfected إيجابية”، معربا عن FP والمتزايد على دعم مع نمط حروف. وفي وقت لاحق، الخلايا تجهز كذلك لطب الطوارئ عن طريق الضغط العالي تجميد (HPF)، تجميد الإحلال (خ)، وتضمين راتنج. خطوة التجميد السريع جداً يضمن الحفاظ على غشاء ممتازة من الخلايا المحددة التي يمكن تحليلها ثم على مستوى ultrastructural مجهر إلكتروني (TEM). هنا، يتم توفير سير عمل خطوة بخطوة ستتحقق خفيفة الميكروسكوب الإلكتروني (كليم)، تصف إعداد العينة والتصوير والعلاقة بالتفصيل. يمكن أيضا تطبيق التصميم التجريبي لمعالجة العديد من الأسئلة بيولوجيا الخلية.
Introduction
فكرة الجمع بين طريقتين الفحص المجهري للحصول على صورة أفضل لعملية بيولوجية محددة قديمة نوعا. ونشرت الدراسة الأولى عن الفيروسات باستخدام “ستتحقق مجهرية” وهكذا، في عام 1960 كمنشورات منفصلة اثنين1،2. في تلك الدراسة، حلل المؤلفون التغييرات في مورفولوجية نواة فعل غدية عن طريق تقنيات الفحص المجهري اثنين. في المنشور الأول، كانت الملاحظات الميكروسكوب الإلكتروني (م) وصف المورفولوجية التفاصيل المرتبطة بعدوى إتش1، المبلغ عنها. في منشور ثاني، كانت ترتبط هياكل مختلفة لاحظها م مع الصور الخفيفة الميكروسكوب (LM) أنماط المصبوغة histochemical، لتحديد طبيعة الهياكل التي لاحظها سابقا م2.
ومع ذلك، في هذه الدراسات المبكرة، أجريت ملاحظاتهم باستخدام مختلف الخلايا المصابة التي أعدت كتجارب مستقلة. “الارتباط”، يعني في الواقع، كمزيج المعلومات الآتية من طرائق التصوير اثنين لفهم ظاهرة معينة، مقارنة جميع النتائج التي تم الحصول عليها مع فحوصات مختلفة لفهم بيولوجية معينة عملية.
في الوقت الحاضر، المجهري يرتبط مصطلح، المعروف أيضا ستتحقق الضوء والمجهر الإلكتروني (كليم)، يتم تطبيقها على عدد متزايد من أساليب (إعادة النظر في الإشارات3،،من45)، مع تماثل أن تنفذ كل تقنيات التصوير (LM و EM) على العينة نفسها. المزيج من كلا الأسلوبين النتائج، وبالتالي، في تحليل النقل المتعدد الوسائط ومتعددة المستويات ومتعددة الأبعاد لأن عينة3. المزايا أن لم يمكن أن توفر استعراضاً واسع النطاق للعديد من الخلايا المختلفة، مما يتيح تحديد الفئات السكانية الفرعية خلية يعبر عن بروتين أو البروتينات ذات الاهتمام داخل خلية غير متجانسة سكان. طب الطوارئ ويتغلب على حد القرار LM، تقديم صورة دقة أعلى لحدث معين داخل الخلية. وعلاوة على ذلك، تمكن م تصور السياق غير الفلورية سوبسيلولار، بما في ذلك جميع العضيات غشاء ملزمة ومجمعات الجزيئات الكبيرة (مثل، ريبوسوم، centrioles، إلخ) والعناصر سيتوسكيليتال، وبالتالي توفير المعلومات المكانية إضافية، ما يسمى “مرجع الفضاء”6، وإعطاء السياق على الفور الفلورسنت الكشف عنها بواسطة LM.
وخلال السنوات القليلة الماضية، أصبح كليم أداة قوية ل علماء الأحياء الخلية5، بل أيضا اختصاصيو (استعرض في مرجع7) استعداد لفهم التفاعلات خلية الفيروس المعقدة التي تؤدي إلى نشر فيروسات ناجحة. وبالتالي، فهم كيفية تعديل الفيروسات أغشية الخلية والعضيات لمنفعتها الخاصة ضروري لتطوير عقاقير مضادة للفيروسات للقضاء على الفيروسات المسببة للأمراض.
هنا، يتم وصف أسلوب كليم التي تسمح الكشف عن ب LM الخلايا معربا عن البروتينات الفيروسية التي تنصهر فيها بروتين فلوري (FP). هذه الخلايا المعطل تداولها البرد في وقت لاحق، وكذلك استعداد لتحليل ultrastructural عن طريق مجهر إلكتروني (TEM) لاكتساب رؤى جديدة في كيفية التعبير عن هذه البروتينات ترتيب الأغشية داخل الخلايا (الشكل 1). وقد أجريت كليم مع خلايا ثابتة كيميائيا في معظم الدراسات علم الفيروسات التي نشرت بتاريخ8،،من910،11،،من1213،14 ،،من1516،17،،من1819. وهذا يرجع أساسا إلى الحاجة إلى تعطيل المواد المعدية لأسباب السلامة الأحيائية في مستوى السلامة الأحيائية-2 و-3 مختبرات (BSL-2 و BSL-3)، حيث البرد-تجميد الخلايا ليس من الممكن عادة. لتلك الأسئلة التي تتطلب الحفاظ على أغشية الخلية مثلى، التزجيج عن طريق الضغط العالي تجميد (HPF)، ومع ذلك، ينصح بشدة20. وفي هذه الحالات، يمكن تطبيق البروتوكول كليم الموصوفة هنا. من المثير للاهتمام، لا سيما عند التعامل مع العينات المعدية، يمكن إجراء هبف على العينات التي تم سابقا خامل كيميائيا، على سبيل المثال في مختبرات BSL-2، و BSL 3. مزيج التثبيت الكيميائية متبوعاً هبف إمكانية الربح على الأقل جزئيا من مزايا cryo–الحفاظ على أساليب21،22.
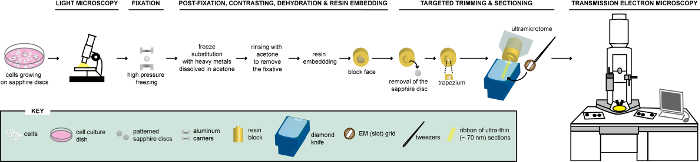
الشكل 1 : التمثيل التخطيطي لسير العمل لتحليل الخلايا عن طريق كليم. أولاً هي تحليل الخلايا التي تنمو على أقراص الياقوت منقوشة بواسطة LM لتعريب الخلايا معربا عن FPs قبل تجهيزها لطب الطوارئ. حالما يقع، فورا ثابتة الخلايا هبف وخ ليكون فيما بعد جزءا لا يتجزأ من الراتنج. عند بلمرة الراتنج، الدعم حيث كانت تنمو خلايا (= أقراص الياقوت) يجب إزالتها من كتلة الراتنج. يتم قطع كتلة تحتوي على خلايا مضمن إلى المعين صغيرة التي هي مقطوع الخلايا المتبقية، وإذ تعرب عن قوة حماية المنشآت، بسكين الماس. أقسام سامسونج تم جمعها على شبكات القمار وكذلك درست بال للحصول على معلومات ultrastructural من هذه الخلايا. هذا الرقم هو تكييفها وتعديلها بإذن من المرجع29. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم-
Protocol
Representative Results
Discussion
كليم المنهجية المقدمة هنا لدراسة أثر تعبير البروتينات الفيروسية في أغشية الخلايا وقد استخدمت بنجاح قبل توضيح سي المرتبطة النسخ المتماثل الهياكل، وأساساً غشاء مزدوج حويصلات (DMVs)21، وكذلك إلى تحديد اللبنات الحاسمة اللازمة لتشكيل هذه الهياكل التي يسببها فيروس التهاب الكبد جيم23. علما بأن عملنا أول استخدام كليم لدراسة فيروس التهاب الكبد جيم النسخ المتماثل21، تم تطبيق نسخة معدلة قليلاً من البروتوكول هو موضح هنا. في هذا الدراسة، أقراص الياقوت سميكة مم 0.05 التقليدية، دون نمط أبجدية رقمية، واستخدمت فيها نمط مرجع أنشأتها الكربون طلاء لهم مع شبكة باحث على أعلى (انظر الجدول للمواد). ويمكن في نهاية المطاف تطبيق هذا الإصدار من البروتوكول الحالي، مع ميزة أن الناقل “” عن هبف يمكن استخدامها مباشرة، دون الحاجة إلى قطع كما في الشكل 3ألف. وبدلاً من ذلك، كما ورد في البروتوكول، أكثر سمكا “A” الناقل يمكن الاستفادة منها (انظر الجدول للمواد) مع أقراص الياقوت منقوشة، دون الحاجة للناقل “ب”.
من المثير للاهتمام، ويمكن تطبيق هذا البروتوكول ليس فقط لدراسة عينات BSL-1، مثل الخلايا transfected مع البروتينات الفيروسية كما هو موضح هنا وفي أماكن أخرى23من19،، ولكن أيضا لدراسة الخلايا المصابة بالفيروسات. على الرغم من أن العمل مع مسببات الأمراض البشرية يقتصر عادة على مختبرات BSL-2، و BSL 3، في بعض البلدان لا يزال من الممكن القيام بالتثبيت البرد في ظل هذه الظروف السلامة الأحيائية. في BSL-2 ومختبرات BSL-3 حيث التزجيج ليس ممكناً، بسبب اللوائح المحلية أو عدم وجود جهاز هبف، الخلايا المصابة بالفيروسات يمكن لا تزال إعداد باستخدام هذا الأسلوب إذا نفذ التثبيت الكيميائي مع الألدهيدات في وقت مبكر، أي قبل مغادرة المرافق BSL-2 أو BSL 3. وعلاوة على ذلك، الألدهيدات بحاجة إلى أن تطفئ مباشرة بعد التثبيت للحفاظ الأسفار، بينما باقي البروتوكول مماثلة لتلك المذكورة هنا. يمكن اعتبار هذا الأسلوب زائدة عن الحاجة لأن يتم إصلاح الخلايا مرتين وكيميائيا وعبر عمليات التزجيج. ومع ذلك، يؤدي هذا البروتوكول تثبيت مزدوج الواقع كثير أفضل الحفاظ على DMVs التي يسببها فيروس التهاب الكبد جيم بالمقارنة مع DMVs الموجودة في الخلايا التي تتعرض للتثبيت الكيميائية وحدها21.
لمزيد من التعديلات واستكشاف الأخطاء وإصلاحها للقارئ هو المشار إليها وتلاحظ في جميع أنحاء الجزء بروتوكول لهذه المخطوطة. وتصف هذه الملاحظات لتجنب المزالق، فضلا عن بدائل للتغلب على الصعوبات المفترضة التي قد تنشأ عند تنفيذ هذا الأسلوب.
الرئيسية المطلوبة لتطبيق هذا الأسلوب جهاز هبف. عندما شل حركة cryo الخلايا عن طريق هبف ليس ممكناً (نظراً لعدم وجود جهاز هبف) أو غير مطلوب (عندما لا تحتاج إلى الحفاظ على غشاء الأمثل)، خلايا يمكن كيميائيا ثابتة وبعد ذلك أعد وتحليلها بواسطة م8، 9،10،11،،من1213،،من1415،16،17،18 ،19. لا يتطلب هذا الخيار استخدام الأقراص الياقوت، لكن خلية ثقافة الأطباق مع أنماط الشبكية لنقل الخلايا أو مجموعات خلايا. والميزة الرئيسية لاستخدام هذه الأطباق هو قطرها أكبر بالمقارنة مع الأقراص الياقوت، السماح بفحص المناطق السطحية أكبر. وهكذا، تطبيق هذا البروتوكول كليم طبقت بنجاح لدراسة أثر مجمع المضادة للفيروسات ضد فيروس التهاب الكبد جيم15 أو لتصور ترتيبات جديدة الغشاء الناجم عن البروتينات نونستروكتورال نوروفيروسيس19. والمسألة الأخرى التي يمكن أن تحد من أداء هذا الأسلوب هو عدم وجود جهاز خ التجارية. وفي هذه الحالة، يمكن أن تستخدم نظم خ محلية الصنع الأساسية بدلاً من ذلك. على الرغم من أن آلات خ قد تقلل من التعامل مع الحوادث المؤسفة، أجهزة محلية الصنع وتستخدم بنجاح على سبيل المثال في كينت ماكدونالد30 ومختبرات بول فالتر.
فيما يتعلق بالتثبيت الكيميائي، يضمن البروتوكول الموصوفة هنا الحفاظ على هياكل داخل الخلايا20أمثل. ولذلك، في حالة الأجهزة هبف وخ المذكورة أعلاه متاحة، فيتريفيينج الخلايا للفائدة سيكون المفضل.
وتشمل البدائل المستقبلية لهذا النهج كليم إمكانية استخدام هذا الأسلوب ليس فقط إلى الحصول على معلومات ثنائية الأبعاد على مستوى ultrastructural، ولكن أيضا للحصول على معلومات ثلاثية الأبعاد عن العمارة من الغشاء وعضيه التعديلات الناجمة عن الفيروسات. أساليب م 3D، بما في ذلك التصوير المقطعي الإلكترون (ET) وأيون تركيز شعاع المسح الميكروسكوب الإلكتروني (التعزيز-وزارة شؤون المرأة) (وصف على نطاق واسع في29)، يمكن أن تطبق أيضا على الخلايا التي تم إعدادها بعد هذا الحالي بروتوكول21، 31. وباﻹضافة إلى ذلك، 3D يمكن أيضا الحصول على معلومات على مستوى LM، عند استخدام مجهر [كنفوكل]، الذي يتيح الحصول على مكدسات z. في الواقع، هذا الخيار هو يوصي بشدة عندما يكون ارتباط دقيق بين مجموعات البيانات LM وم المطلوب (انظر على سبيل المثال17). المعلومات التي يتضمنها الإيدز مكدسات z ثلاثية الأبعاد لتحسين العلاقة مع الصور ال 2D. وهكذا، في مثل هذا سيناريو، أفضل تركيب الصور LM وم يمكن تحديدها وثم تعرض لواحد من الارتباط البرامج المتاحة، مثل البرنامج المساعد ec-كليم الجليدية (http://icy.bioimageanalysis.org/)32 أو المساعد “المرسلات معلما” من الصورة ي (http://imagej.net/Landmark_Correspondences)، أدى إلى توليد تداخل الصور لم م.
عند الحاجة إلى معلومات الزمانية لفهم الحركية لحدث معين، يمكن استخدام التصوير بمرور الزمن لرصد ديناميات الخلايا الحية في تركيبة مع م. خلال هذا حدث الفائدة، خلايا ثابتة على الفور، توليد “لقطة مجمدة” التي يمكن تحليلها في وقت لاحق عن طريق طب الطوارئ، وتوفير معلومات ultrastructural مفصلة حول تلك اللحظة بالذات في وقت التثبيت. من أجل الحصول على تلك “اللقطة مجمدة”، بعد الملاحظة في الوقت الحقيقي، يمكن أن تكون الخلايا ثابتة كيميائيا33 أو المعطل تداولها البرد6. حيث تحدث العديد من العمليات الخلوية أسرع من عمليات نشر التثبيت الكيميائي، إذا كان ذلك ممكناً، ينبغي أن يجري تجميد فائقة السرعة. ومع ذلك، من المهم أن تأخذ في الاعتبار أن الآلات هبف تختلف في القرار الفعال للوقت على34.
وعلاوة على ذلك، على الرغم من أن تم تصميم هذا البروتوكول لتضمين الخلايا في راتنج الإيبوكسي، الخلايا يمكن أن تكون أيضا جزءا لا يتجزأ من راتنجات اللزوجة منخفضة، مثل لوويكريلس، ل. ر الأبيض أو الذهب LR. استخدام هذه الوسائط التضمين تمكن من الحفاظ على أنتيجينيسيتي35،36، فضلا عن الأسفار37،38 ، وذلك، تستخدم في الغالب لما بعد تضمين إيمونولابيلينج في الباب39 , 40 وفي قسم كليم41،42،43،44، حيث لم يتم بعد تضمين. كلا النهجين (م المناعية وكليم في القسم) يجب أن تكون حاسمة بالنسبة لتلك التجارب التي هياكل غير مميزة يمكن يمكن العثور عليها بسهولة عبر تيم و/أو كعنصر تحكم ضد ميسكوريليشن بين LM وم إشارات. وبالمثل، وضع العلامات مع الأجسام المضادة التي يمكن تصور بكل طرائق التصوير (LM و EM) يمكن الاضطلاع بها45 من أجل التعرف على سبيل المثال، transfected الخلايا في LM (تضمين ما قبل المرحلة) وتحقيق تعريب أكثر دقة بكثير من بروتينات فلورية خضراء إشارة عبر به العلامات المحددة قبل م المناعية (مرحلة ما بعد التضمين). فإنه يجب أن تؤخذ في الحسبان، بيد أن permeabilization يجري قبل LM للسماح وصول الأجسام إلى الفضاء داخل الخلايا، مما قد يؤدي إلى حفظ دون المستوى أمثل من العمارة خلية على مستوى م. من المثير للاهتمام، هذا البروتوكول أيضا مناسبة تماما لتجارب متعددة الألوان التي يمكن أن تتحقق باستخدام العلامات الفلورية الأخرى، عدا التجارة والنقل (كما هو موضح هنا). وفي الختام، هناك الكثير من الاحتمالات المفترضة للتكيف مع هذا البروتوكول، على حد سواء على لم و/أو على جانبي م، اعتماداً على الأسئلة التي تعالج. للحصول على وصف شامل لبروتوكولات أخرى بديلة ويحال القارئ إلى5،46. بغض النظر عن كيف يتم الجمع بين طرائق الفحص المجهري، معا والنتيجة مكسب للمعلومات، مما يسمح لنا بفهم أفضل لكيفية تفاعل الفيروسات وعلى البروتينات مع مضيفيهم في الحياة الحقيقية.
أن الخطوة الأكثر أهمية ضمن هذا الأسلوب هو مجموعة مقاطع المسلسل من الخلايا للفائدة. كما أبرز في قسم النتائج التمثيلية، وهذا يتطلب موظفين ذوي خبرة، فضلا عن الكثير من الصبر. الأهم من ذلك، هذه الخطوة غير ضرورية لإيجاد الخلايا مرة أخرى على مستوى م لسببين. أولاً، في هذا النوع من البروتوكول كليم استخدام قبل تضمين LM، الإحداثيات مرئية فقط في مستوى LM وعلى وجهة كتلة راتنج بعد تضمين. ومع ذلك، أنها لن تكون مرئية على الأقسام التي تيم. ولذلك، يجب إنجازها التشذيب المستهدفة على الوجه كتلة أسفل إلى المناطق ذات الاهتمام (رويس) بعناية مع شفرة حلاقة لضمان احتواء الخلايا معربا عن FP معطى المقاطع التي يتم الحصول عليها في وقت لاحق. ثانيا، “المسح الضوئي” عدة أقسام من الضروري إيجاد أفضل التراكب بين LM والشراء م. وفي هذه الحالة تراكب LM م ليست دقيقة حتى خلافا للأساليب التي تؤدي فيها LM في مرحلة ما بعد الدمج،. دقة منخفضة تراكب نتيجة للاختلافات في القرار المحوري بين LM وم، تقلص أثناء معالجة عينة من م، وضغط أثناء تقطيع42. ومع ذلك، أساليب تتبع الكفاءة، مثل استخدام المعالم، تساعد على العثور على الخلايا مرة أخرى. ويشمل هذا موقف خلية واحدة إلى آخر، وكذلك الشكل من الخلايا، ونواة هذه. وفي هذا الصدد، كما هو موضح في البروتوكول، الصور DIC تقديم معلومات “التشريحية” الخلايا ذات الأهمية الحاسمة لتحسين العلاقة. بدلاً من ذلك، النواة أو العضيات الأخرى خلية التعرف عليها جيدا (مثل الميتوكوندريا أو الدهن قطرات) يمكن الملون قبل LM واستخدامها كمعالم.
أخيرا، من الجدير أن نذكر أنه على الرغم من أن تركز هذه المخطوطة على استخدام هذه التقنية لدراسات علم الفيروسات، يمكن توسيع نطاق هذا التصميم التجريبي لمعالجة المسائل البيولوجية العامة أكثر.
Disclosures
The authors have nothing to disclose.
Acknowledgements
ونحن ممتنون جداً للموظفين الميكروسكوب الإلكتروني الأساسية مرافق (امكف) في EMBL (هايدلبرغ) وفي جامعة هايدلبرغ. أيضا نود أن نشكر اولريكي هيريان، ستيفاني كليس واندريا وهيلويج (جامعة هايدلبرغ)، فضلا عن ايبرهارت شميت ورينات كونز (جامعة أولم) لخبراء المساعدة التقنية. عمل سنغ وفريقه (U.H. والإسلامية-باء) أيده الأوقيانوغرافية الألمانية، SFB1129، TP11، و TRR83، TP13.
Materials
| UV Crosslinker | Stratagene | 400072 | Stratalinker 1800, 230Vac, equipped with 254-nm UV light bulbs, 8-watts/each. |
| Patterned sapphire discs | Engineering Office M. Wohlwend, Sennwald, Switzerland | 627 | They have a 0.3-mm diameter and are 0.16-mm thick, as well as an an etched alphanumeric pattern to allow for re-location of the cells. They can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| Slim and long tweezers | Electron Microscopy Sciences, Hatfield, PA, USA | 72919-SS | "Style SS", for handling sapphire discs. |
| Cell culture medium | Thermo Fisher Scientific, Waltham, MA, USA | 41965-062 | Dulbecco's modified Eagle medium (DMEM) supplemented with 2 mM L-glutamine, nonessential amino acids, 100 units penicillin per ml, 100 µg streptomycin per ml and 10% fetal calf serum (DMEM complete, see below). Package containing 10 bottles, 500 ml/each. |
| L-glutamine | Thermo Fisher Scientific, Waltham, MA, USA | 25030-123 | Package containing 20 bottles of 100 ml/each. |
| Nonessential amino acids | Thermo Fisher Scientific, Waltham, MA, USA | 11140-068 | Package containing 20 bottles of 100 ml/each. |
| Penicillin/Streptomycin | Thermo Fisher Scientific, Waltham, MA, USA | 15140-163 | Package containing 20 bottles of 100 ml/each. |
| Fetal calf serum | Sigma Aldrich, St. Louis, MI, USA | F7524 | Bottle of 50 ml. |
| Inverted microscope | Olympus Deutschland, Hamburg, Germany | CKX41 | It is an inverted microscope with trinocular head options and fluorescence upgrade capability. |
| Huh7-Lunet cells stably expressing the T7 RNA-polymerase | Avaliable at Prof. Dr. Ralf Bartenschlager laboratory | Not available | Contact Prof. Bartenschlager at: ralf.bartenschlager@med.uni-heidelberg.de. |
| Mirus TransIT-LT1 Transfection Reagent | Mirus Bio LLC, Madison, USA | MIR 2304 | Broad spectrum, low toxicity, DNA transfection reagent. Vial of 0.4 ml. |
| Inverted widefield fluorescence microscope | Carl Zeiss Microscopy GmbH, Germany | Zeiss Observer.Z1 | Inverted fluorescence microscope for experiments involving living cell cultures. |
| 1-hexadecene | Merck, Darmstadt, Germany | 8220640100 | Bottle of 100 ml. |
| "A" aluminium holders for high pressure frezing (HPF) | Engineering Office M. Wohlwend, Sennwald, Switzerland | 241 | This is the holder that has been used for this protocol and has 2 different depths of 0.1 and 0.2-mm. It can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| "B" aluminium holders for HPF | Engineering Office M. Wohlwend, Sennwald, Switzerland | 242 | This is the holder that has been used for this protocol.It is 0.3-mm thick.They can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| "A" aluminium holder for HPF (special for working with patterned sapphire discs) | Engineering Office M. Wohlwend, Sennwald, Switzerland | 737 | This is the holder than can be used alone with the patterned sapphire disc (as an alternative to the current protocol), without the need of a "B" holder or the edition of the "A" holder. It is 0.84-mm thick. It can be only ordered per e-mail: martin-wohlwend@bluewin.ch. |
| Sapphire discs | Engineering Office M. Wohlwend, Sennwald, Switzerland | 405 | These sapphires discs are the "conventional" one, with a 0.3-mm diameter and a thickness of 0.05 mm . They can be also used for CLEM as an alternative instead of patterned sapphire discs. |
| Finder grids | Electron Microscopy Sciences, Hatfield, Philadelphia, USA | LF135-Cu | These 135 mesh grids are used to create an alphanumeric pattern on "conventional" sapphire discs (described above) via carbon coating, so that they can be used for CLEM. 100 grids/vial. |
| HPF machine | ABRA Fluid AG, Widnau, Switzerland | HPM 01 | This HPF machine has been used for this protocol. |
| HPF machine | Leica Microsystems, Vienna, Austria | EMPACT 2 | "EMPACT 2", as an alternative to the use of the HPM machine that it has been used in this protocol (described above). |
| Cryo-tubes | Thermo Fisher Scientific, Waltham, MA, USA | Z763667-500EA | For long term-storage of cryo-immobilized samples in liquid nitrogen. Package containing 500 cryovials. |
| Liquid nitrogen dewar | Cole-Parmer GmbH, Wertheim, Germany | GZ-05094-60 | For long term-storage of cryo-immobilized samples in liquid nitrogen, equipped with cryo-racks with a capacity of 1600 cryo-tubes. |
| Automatic freeze substitution (AFS) machine | Leica Microsystems, Vienna, Austria | EM AFS2 | This machine performs freeze substitution and progressive lowering of temperature (PLT) techniques and allows low temperature embedding and polymerization of resins. |
| Osmium tetroxide (OsO4) | Electron Microscopy Sciences, Hatfield, PA, USA | 19150 | 4% aqueous solution, one box containing 10 x 2 ml ampules. |
| Uranyl-Acetate (UA) | Serva, Heidelberg, Germany | 77879.01 | Bottle containing 25 grs of (UA)-2 H2O. |
| Sonicator | Bandelin Electronic, Berlin, Germany | 329 | "Sonorex Super RK 31" is a high-power ultrasonic cleaning bath for aqueous cleaning solution that is used in this protocol to mix OsO4 and Ua when preparing the FS medium. |
| Glass-distilled acetone | Electron Microscopy Sciences, Hatfield, PA, USA | 10015 | Bottle of 100 ml. |
| Stereomicroscope | Leica Microsystems, Vienna, Austria | Leica M80 | Routine stereomicroscope for daily inspections, equipped with a camera for capturing images. |
| Epoxy resin | Electron Microscopy Sciences, Hatfield, PA, USA | 14120 | Embed 812 is a kit containing several components that must be mix together in the proportions given by the manufacturers. |
| Flow through rings | Leica Microsystems, Vienna, Austria | 16707157 | Package containing 100 pieces. |
| Reagent baths | Leica Microsystems, Vienna, Austria | 16707154 | Package containing 100 pieces. |
| Ultramicrotome | Leica Microsystems, Vienna, Austria | Leica EM UC7 | Ultramicrotome for preparation of semi- and ultrathin sections at room temperature. |
| Ultra 35° diamond knife | Diatome Ltd., Nidau Switzerland |
AGG339-735 | This knife have an edge length of 3 mm. |
| Ultra fine tweezers | Electron Microscopy Sciences, Hatfield, PA, USA | E78318 | "Style 3X", for handling EM grids. |
| EM slot grids | Electron Microscopy Sciences, Hatfield, PA, USA | G2010-Cu | 100 grids/vial. |
| EM grid storage box | Electron Microscopy Sciences, Hatfield, PA, USA | 71155 | It has capacity for 100 grids. |
References
- Morgan, C., Godman, G. C., Breitenfeld, P. M., Rose, H. M. A correlative study by electron and light microscopy of the development of type 5 adenovirus. I. Electron microscopy. Journal of Experimental Medicine. 112, 373-382 (1960).
- Godman, G. C., Morgan, C., Breitenfeld, P. M., Rose, H. M. A correlative study by electron and light microscopy of the development of type 5 adenovirus. II. Light microscopy. Journal of Experimental Medicine. 112, 383-402 (1960).
- Caplan, J., Niethammer, M., Taylor, R. M., Czymmek, K. J. The power of correlative microscopy: multi-modal, multi-scale, multi-dimensional. Current Opinion in Structural Biology. 21, 686-693 (2011).
- de Boer, P., Hoogenboom, J. P., Giepmans, B. N. Correlated light and electron microscopy: ultrastructure lights up. Nature Methods. 12, 503-513 (2015).
- Müller-Reichert, T., Verkade, P. . Correlative light and electron microscopy III, First edition. , (2017).
- Brown, E., Mantell, J., Carter, D., Tilly, G., Verkade, P. Studying intracellular transport using high-pressure freezing and Correlative Light Electron Microscopy. Seminars in Cell and Developmental Biology. 20, 910-919 (2009).
- Bykov, Y. S., Cortese, M., Briggs, J. A., Bartenschlager, R. Correlative light and electron microscopy methods for the study of virus-cell interactions. FEBS Letters. , (2016).
- Spuul, P., et al. Assembly of alphavirus replication complexes from RNA and protein components in a novel trans-replication system in mammalian cells. Journal of Virology. 85, 4739-4751 (2011).
- Nagel, C. H., Dohner, K., Binz, A., Bauerfeind, R., Sodeik, B. Improper tagging of the non-essential small capsid protein VP26 impairs nuclear capsid egress of herpes simplex virus. PLoS One. 7, 44177 (2012).
- Sharma, M., Kamil, J. P., Coughlin, M., Reim, N. I., Coen, D. M. Human cytomegalovirus UL50 and UL53 recruit viral protein kinase UL97, not protein kinase C, for disruption of nuclear lamina and nuclear egress in infected cells. Journal of Virology. 88, 249-262 (2014).
- Kallio, K., et al. Template RNA length determines the size of replication complex spherules for Semliki Forest virus. Journal of Virology. 87, 9125-9134 (2013).
- Martinez, M. G., Snapp, E. L., Perumal, G. S., Macaluso, F. P., Kielian, M. Imaging the alphavirus exit pathway. Journal of Virology. 88, 6922-6933 (2014).
- Lebrun, M., et al. Varicella-zoster virus induces the formation of dynamic nuclear capsid aggregates. Virology. 454-455, 311-327 (2014).
- Madela, K., et al. A simple procedure to analyze positions of interest in infectious cell cultures by correlative light and electron microscopy. Methods in Cell Biology. 124, 93-110 (2014).
- Berger, C., et al. Daclatasvir-like inhibitors of NS5A block early biogenesis of hepatitis C virus-induced membranous replication factories, independent of RNA replication. Gastroenterology. 147, 1094-1105 (2014).
- van der Schaar, H. M., et al. Illuminating the Sites of Enterovirus Replication in Living Cells by Using a Split-GFP-Tagged Viral Protein. mSphere. 1, (2016).
- Vale-Costa, S., et al. Influenza A virus ribonucleoproteins modulate host recycling by competing with Rab11 effectors. Journal of Cell Science. 129, 1697-1710 (2016).
- Wang, L., et al. Visualization of HIV T Cell Virological Synapses and Virus-Containing Compartments by Three-Dimensional Correlative Light and Electron Microscopy. Journal of Virology. 91, (2017).
- Doerflinger, S. Y., et al. Membrane alterations induced by nonstructural proteins of human norovirus. PLOS Pathogens. 13, 1006705 (2017).
- Dahl, R., Staehelin, L. A. High-pressure freezing for the preservation of biological structure: theory and practice. Journal of Electron Microscopy Technique. 13, 165-174 (1989).
- Romero-Brey, I., et al. Three-dimensional architecture and biogenesis of membrane structures associated with hepatitis C virus replication. PLOS Pathogens. 8, 1003056 (2012).
- Sosinsky, G. E., et al. The combination of chemical fixation procedures with high pressure freezing and freeze substitution preserves highly labile tissue ultrastructure for electron tomography applications. Journal of Structural Biology. 161, 359-371 (2008).
- Romero-Brey, I., et al. NS5A Domain 1 and Polyprotein Cleavage Kinetics Are Critical for Induction of Double-Membrane Vesicles Associated with Hepatitis C Virus Replication. MBio. 6, 00759 (2015).
- Dixit, R., Cyr, R. Cell damage and reactive oxygen species production induced by fluorescence microscopy: effect on mitosis and guidelines for non-invasive fluorescence microscopy. The Plant Journal. 36, 280-290 (2003).
- Jou, M. J., Jou, S. B., Guo, M. J., Wu, H. Y., Peng, T. I. Mitochondrial reactive oxygen species generation and calcium increase induced by visible light in astrocytes. Annals of the New York Academy of Sciences. 1011, 45-56 (2004).
- McDonald, K. L., Morphew, M., Verkade, P., Muller-Reichert, T. Recent advances in high-pressure freezing: equipment- and specimen-loading methods. Methods in Molecular Biology. 369, 143-173 (2007).
- Walther, P., Ziegler, A. Freeze substitution of high-pressure frozen samples: the visibility of biological membranes is improved when the substitution medium contains water. Journal of Microscopy. 208, 3-10 (2002).
- White, J. G., Southgate, E., Thomson, J. N., Brenner, S. The structure of the nervous system of the nematode Caenorhabditis elegans. Philosophical Transactions of the Royal Society B: Biological Sciences. 314, 1-340 (1986).
- Romero-Brey, I., Bartenschlager, R. Viral Infection at High Magnification: 3D Electron Microscopy Methods to Analyze the Architecture of Infected Cells. Viruses. 7, 6316-6345 (2015).
- McDonald, K. L., Webb, R. I. Freeze substitution in 3 hours or less. Journal of Microscopy. 243, 227-233 (2011).
- Villinger, C., Neusser, G., Kranz, C., Walther, P., Mertens, T. 3D Analysis of HCMV Induced-Nuclear Membrane Structures by FIB/SEM Tomography: Insight into an Unprecedented Membrane Morphology. Viruses. 7, 5686-5704 (2015).
- Paul-Gilloteaux, P., et al. eC-CLEM: flexible multidimensional registration software for correlative microscopies. Nature Methods. 14, 102-103 (2017).
- Polishchuk, R. S., Mironov, A. A. Correlative video light/electron microscopy. Current Protocols in Cell Biology Supplement. , 8 (2001).
- McDonald, K. L. A review of high-pressure freezing preparation techniques for correlative light and electron microscopy of the same cells and tissues. Journal of Microscopy. 235, 273-281 (2009).
- Newman, G. R., Jasani, B., Williams, E. D. A simple post-embedding system for the rapid demonstration of tissue antigens under the electron microscope. The Histochemical Journal. 15, 543-555 (1983).
- Schwarz, H., Humbel, B. M. Influence of fixatives and embedding media on immunolabelling of freeze-substituted cells. Scanning Microscopy. 3, 57-63 (1989).
- Luby-Phelps, K., Ning, G., Fogerty, J., Besharse, J. C. Visualization of identified GFP-expressing cells by light and electron microscopy. Journal of Histochemistry and Cytochemistry. 51, 271-274 (2003).
- Nixon, S. J., et al. A single method for cryofixation and correlative light, electron microscopy and tomography of zebrafish embryos. Traffic. 10, 131-136 (2009).
- McDonald, K. L. Rapid embedding methods into epoxy and LR White resins for morphological and immunological analysis of cryofixed biological specimens. Microscopy and Microanalysis. 20, 152-163 (2014).
- Webster, P., Schwarz, H., Griffiths, G. Preparation of cells and tissues for immuno EM. Methods in Cell Biology. 88, 45-58 (2008).
- Kukulski, W., et al. Correlated fluorescence and 3D electron microscopy with high sensitivity and spatial precision. Journal of Cell Biology. 192, 111-119 (2011).
- Peddie, C. J., et al. Correlative and integrated light and electron microscopy of in-resin GFP fluorescence, used to localise diacylglycerol in mammalian cells. Ultramicroscopy. 143, 3-14 (2014).
- Hampoelz, B., et al. Pre-assembled Nuclear Pores Insert into the Nuclear Envelope during Early Development. Cell. 166, 664-678 (2016).
- Lemercier, N., et al. Microtome-integrated microscope system for high sensitivity tracking of in-resin fluorescence in blocks and ultrathin sections for correlative microscopy. Scientific Reports. 7, 13583 (2017).
- Takizawa, T., Powell, R. D., Hainfeld, J. F., Robinson, J. M. FluoroNanogold: an important probe for correlative microscopy. Journal of Biological Chemistry. 8, 129-142 (2015).
- Romero-Brey, I., Yamauchi, Y. 3D electron microscopy (EM) and correlative light electron microscopy (CLEM) methods to study virus-host interactions. Methods in Molecular Biology: Influenza Virus Methods & Protocols. , (2018).

