ביצוע מדידות FRET מדויקות ומדויקות באמצעות smfBox קוד פתוח
Summary
מאמר זה מספק הוראות שלב אחר שלב לביצוע מדידות FRET מדויקות מתוקנות במלואן על ביומולקולים בודדים, המפזרים בחופשיות באמצעות קוד פתוח, smfBox זול, החל מהפעלת, דרך יישור ומיקוד, לאיסוף וניתוח נתונים.
Abstract
ה- smfBox הוא מכשיר חסכוני וחסכוני בקוד פתוח להעברת אנרגיה בתהודה של Förster חד-מולקולתי (smFRET), מה שהופך את המדידות על ביומולקולות מפוזרות בחופשיות לנגישות יותר. סקירה זו כוללת פרוטוקול שלב אחר שלב לשימוש במכשיר זה כדי לבצע מדידות של יעילות FRET מדויקת בדגימות DNA דופלקס, כולל פרטים על הכנת המדגם, הגדרת המכשיר ויישור, רכישת נתונים, ושגרות ניתוח מלא. הגישה המוצגת, הכוללת כיצד לקבוע את כל גורמי התיקון הנדרשים למדידות מרחק מדויקות שמקורן ב- FRET, מתבססת על גוף גדול של עבודה משותפת שנערכה לאחרונה ברחבי קהילת FRET, שמטרתה לקבוע פרוטוקולים סטנדרטיים וגישות ניתוח. פרוטוקול זה, הניתן להתאמה בקלות למגוון מערכות ביומולקולריות, מוסיף למאמצים הגוברים בדמוקרטיזציה של smFRET עבור הקהילה המדעית הרחבה יותר.
Introduction
העברת אנרגיית תהודה של מולקולה אחת של Förster (smFRET) היא טכניקה המודדת את יעילות FRET בין שני צבעים- תורם לבין מקבל – ברמה של מולקולות בודדות. FRET הוא תהליך פוטופיזי הנובע מפרטטרום האנרגיה החופף של שני צבעים: התורם מתרגש לאור אורך גל מסוים ומעביר אנרגיה ללא רדיקליבית למקבל, וכתוצאה מכך פליטה מן המקבל. היעילות של העברה זו היא ביחס הפוך לכוח השישי של המרחק בין שני הצבעים, כך יעילות ההעברה משתנה עם מרחק1. לכן, יעילות FRET זו יכולה לשמש כדי לקבוע מידע מרחבי על המולקולות(s)2 שאליהן מחוברים הצבעים, בטווח של 3-10 ננומטר. קנה מידה זה, והעובדה ששינויים ביעילות FRET רגישים לתנועות מולקולריות אנגסטרום3, הופכים את הטכניקה למתאים היטב לחקירת מידע מבני על ביומולקולות – כגון חומצות גרעין וחלבונים – ללא סיבוכים של הרכב ממוצע של 4,5,6. בעוד ששינויים ביעילות FRET יחסית יכולים לשמש לניטור אינטראקציות ביומולקולריות ודינמיקה קונפורמציה, שופכים אור על תהליכים תאיים מרכזיים כגון קיפול חלבונים (un),שעתוק ושכפול ותיקון DNA, יעילות FRET מוחלטת שימשו לקביעת מרחקים מדויקים לקביעת מבנה ביומולקולרי7,8,9,10,11 התגברות על הצורך בגיבש או הקפאה כנדרש בשיטות מבניות אחרות4,12.,
ניסויי smFRET בדרך כלל לוקחים שתי צורות, קונפוקלית או מיקרוסקופיית פלואורסצנטיות השתקפות פנימית כוללת (TIRF). בין שתי הגישות ניתן לחקור בדרך כלל את הדינמיקה המולקולרית של הביומולקולות על צירי זמן מפיקו עד אלפית השנייה (מולקולות קונפוקליות, מתפזרות בחופשיות) עד אלפית השנייה לשעות (TIRF, מולקולות משותקות פני השטח). הסיבה לכך היא ההגדרות השונות המעורבות בכל טכניקה. במיקרוסקופיה של TIRF, מולקולות משותקות על פני השטח של שקופית ונרגשות מגל אוונסנטי (איור 1A). כאן, לעומת זאת, ההתמקדות היא במיקרוסקופיה קונפוקלית מכיוון שזה הפורמט של ה- smfBox. במיקרוסקופיה קונפוקלית, מולקולות אינן משותקות ובמקום זאת מפוזרות בחופשיות באמצעות תנועה בראונית דרך נפח הקונפוקלי (~1 fL), שנוצר על ידי מיקוד קרן לייזר דרך עדשת צמצם מספרי גבוה לנקודה בעומק ייעודי כלשהו בתוך הפתרון (איור 1B). הפליטה המתקבלת ממוקדת בחזרה דרך אותו צמצם ומסוננת דרך מראה דיכרואית (איור 1C לקבלת סכמטי מלא). לאחר מכן הוא מתמקד דרך חור סיכה על מנת להסיר כל אור מחוץ למיקוד ועל פוטודיודה מפולת שלגים (APD). כאשר APD מזהה פוטון, הוא פולק פעימת TTL, התזמון שלה ניתן להקליט ברזולוציה של עד picosecond. זמן התצפית של מולקולות אלה המתפזרות בחופשיות בקרבת נפח הקונפוקלי הוא בדרך כלל בסדר אלפיות השנייה.
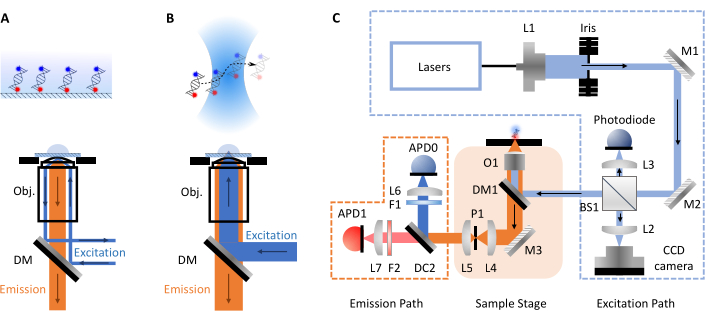
איור 1: שרטוטים המציגים עקרונות של מיקרוסקופיה והגדרת smfBox. (A) עקרון מיקרוסקופיה של השתקפות פנימית כוללת (TIRF): אור עירור מכוון לקצה המטרה (Obj.) ועובר השתקפות פנימית מוחלטת בממשק חיץ הכיסויים היוצר שדה התקוה מתפורר באופן אקספוננציאלי כדי לרגש מולקולות המחוברות לפני השטח. (B) מיקרוסקופיה קונפוצלית: מולקולות מתפזרות בחופשיות מתרגשות מנקודה כמעט מוגבלת עקיפה המתמקדת במדגם. (ג) הגדרת smfBox המשמשת בפרוטוקול זה, המציגה את כל רכיבי המפתח: פוטודיודות מפולת שלגים (APD), מפצל קרן (BS), מראות דיכרויות (DM), מסננים (F), מראות (M), מטרה (O) וחור סיכה (P). אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
לאחרונה, טכניקות smFRET שילבו שתי עירור צבעים, שבו לייזרים התואמים את התורם ואת אורכי גל עירור קבלה לסירוגין5. זה יכול להיעשות באחת משתי דרכים, הראשונה על ידי לווסן לייזרי גל רציפים בציר הזמן KHz, אשר ידוע בשם עירור לייזר לסירוגין (ALEX)13,14. השיטה השנייה משלבת פולסים מהירים בציר הזמן של MHz; זהו ננו-שניות-ALEX15 או עירור משולב פעמו (PIE)16. בכל הגישות הללו, מידע מהלייזר המקבל מוביל לחישוב מה שמכונה סטויצ’ומטריה, אשר יכול להפלות בין מולקולות עם יעילות FRET נמוכה לבין אלה חסרים מקבל (או באמצעות תיוג לא שלם או ליבנה). שימוש PIE /ns-ALEX בנוסף נותן גישה לכל החיים פלואורסצנטי ברמת המולקולה הבודדת, ואניסוטרופיות ניתן למדוד כאשר בשילוב עם אופטיקה מקוטבת. שילוב זה של מדידות ידוע בשם זיהוי פלואורסצנטיות רב-תכליתי (MFD)9.
למרות היתרונות הרבים של smFRET, הוא אינו נמצא בשימוש נרחב מחוץ למעבדות מומחים בשל העלויות הגבוהות של מכשירים מסחריים והיעדר חלופות פשוטות, בבנייה עצמית. מגמה הולכת וגוברת לקראת פיתוח של מיקרוסקופיה opensource בעלות נמוכה מתרחשת ופלטפורמות אחרות הופיעו לאחרונה, כולל פלנקטוסקופ17, OpenFlexure מיקרוסקופ18, Flexiscope19, miCube20, liteTIRF21, ו Squid22. במחקר מוערך הפרוטוקול לשימוש ב-smfBox, מערך קונפוקלי חסכוני שפותח לאחרונה ומסוגל למדוד את יעילות FRET בין שני צבעים על מולקולות בודדות המפזרות בחופשיות. הוראות בנייה מפורטות וכל התוכנות התפעוליות הדרושות זמינות בחופשיות ב: https://craggslab.github.io/smfBox/ 23. הסידור האופטי של ה- smfBox מורכב מרכיבים זמינים שנרכשו מיצרני אלומיניום במחירים נוחים ונגישים באופן נרחב, בעוד גוף המיקרוסקופ (האחראי על רוב ההוצאה במערך קונפוקלי סטנדרטי) הוחלף בקופסת אנודייז-אלומיניום הדוקה במיוחד (המאפשרת לבצע מדידות בתנאי תאורת סביבה). תיבה זו מאכלסת רכיבים אופטיים מרכזיים, כולל דיכרואי עירור, מטרה וחור סיכה, ושולב לייזר מכני, המאפשר את פעולתו הבטוחה כמוצר לייזר Class I (ראה איור 1C לקבלת שרטוט מלא). ה- smfBox משתמש ב- ALEX כדי לאמת את סטויצ’ומטריית הצבע ולקבוע גורמי תיקון FRET מדויקים. הוא מופעל באמצעות תוכנת קוד פתוח (smOTTER) שנכתבה בהתאמה אישית, השולטת בכל ההיבטים של רכישת הנתונים ומפיקה את הנתונים בתבנית פוטון-HDF5 בקוד פתוח24, התואמת לכלי ניתוח רבים של צד שלישי. smfBox ופרוטוקולי הרכישה וניתוח הנתונים נבדקו לאחרונה מול >20 מכשירים אחרים (הן קונפוקלי והן TIRF) במחקר עיוור רב-מעבדות25. יעילות FRET שהושגו היו בהסכמה מצוינת עם כל המכשירים האחרים, למרות smfBox עולה רק חלק קטן ממחיר של הגדרות זמינות מסחרית.
כאן, פרוטוקול שלב אחר שלב מתאר לרכישה וניתוח של יעילות FRET מדויקת ומוחלטת על דופלקסים DNA מפוזרים בחופשיות באמצעות smfBox, כל הדרך מהפעלת, דרך יישור ומיקוד, לאיסוף וניתוח נתונים. הדגימות המשמשות כאן הן שלוש DNAs דופלקס (המציגים יעילות גבוהה, בינונית ונמוכה FRET, ראה טבלה 1) שנבדקו במחקר עיוור ברחבי העולם25; עם זאת, השיטה ניתנת להתאמה למערכות מולקולריות רבות, כולל חלבונים וחומצות גרעין אחרות. התקווה היא כי פרוטוקול מפורט כזה, יחד עם הוראות הבנייה הקיימות כבר עבור smfBox23, יסייע להפוך טכניקה חזקה זו אפילו יותר נגיש למגוון רחב של מעבדות.
Protocol
Representative Results
Discussion
השלבים הקריטיים ביותר בפרוטוקול הם יישור המיקרוסקופ והתאמת ריכוז המדגם לדילול הנכון. אם היישור כבוי, אז ייתכן שאין מספיק אות כדי לזהות התפרצויות התוויית היסטוגרמה, ואם אי התאמה מתרחשת בין דגימות אז תיקון FRET מדויק עלול להיכשל עקב שינויים דליפת וזיהוי / יעילות עירור. השימוש בריכוז מתאים חשוב גם הוא, ריכוז גבוה מדי ייתן פרצים מקריים, המכילים מולקולות מרובות עם יעילות FRET שונה או תיוג סטויצ’יומטריות. ריכוז נמוך מדי ייתן מעט מדי התפרצויות לניתוח נתונים חזק.
הפרוטוקול המתואר כאן הוא למדידת מרחקים במיני FRET יחיד סטטי. אם המדגם יש יותר משיא אחד בהיסטוגרמה יעילות FRET, או פסגות מופיעות רחב (אשר יכול לקרות עם מינים דינמיים), אז התפרצויות נוספות עשויות להיות נחוצות כדי להתאים היסטוגרמה לאותה מידה של דיוק. עבור שתי פסגות מופרדות היטב אז בערך פי שניים יותר נתונים יהיה צורך, אבל אם האוכלוסיות חופפות מעט אז אפילו יותר נתונים נדרשים.
אם שתי האוכלוסיות יתחברו בסולם הזמן של הניסוי, הדינמיקה והקינטיקה של המערכת עשויות להיקבע. בדיקות כגון BVA27 ו- 2CDE28 יכולות לאשר כי התפרצויות הביניים הן דינמיות בטבען, בעוד שניתוחים כולל dPDA29,30 או H2MM31 יכולים לקבוע את שיעורי ההסתה ההדדית. מחשבים ניידים של Jupyter עבור BVA ו- 2CDE זמינים באתר האינטרנט FRETBursts26, והתוכנה מבוססת MATLab PAM32 יכולה להפעיל ניתוחי BVA, 2CDE ו- PDA.
קונפוקל מולקולה אחת FRET יכול בקלות להתבונן מצבים הרבה יותר קצר חי (~ 1 ms) מאשר TIRF; עם זאת, זמני התצפית הקצרים, המוגבלים על ידי דיפוזיה, אינם מעניקים היסטוריה מולקולרית, ולכן אינם יכולים לקבוע זמני התעכבות ארוכים יותר, או רשתות מעבר מורכבות באופן שבו ניסויים משותקים על פני השטח יכולים.
כאשר הפרוטוקול מודד מולקולות מפוזרות בחופשיות בריכוז נמוך מאוד, הוא פועל בצורה הטובה ביותר בעת מדידת מרחקים תוך-עיניים על אותה מולקולה. ניתן למדוד מרחקים בין-מולקולות קשורות ארעיות בתנאי שניתן למדוד את ה– Kd של שתי המולקולות נמוך מספיק כדי שהמכלול קיים בכמות משמעותית בריכוז העבודה הנמוך הנדרש על ידי הניסוי (~ 100 pM). אם Kd הוא הרבה יותר גבוה מזה, אז רק מולקולות מסומנות יחיד יראו. ניתן להתגבר על בעיה זו באמצעות microfluidics לערבב את שני הרכיבים המסומנים יחד בריכוז גבוה ולאחר מכן דילול מהיר וזורם מעל המטרה לפני המורכב dissociates33,34.
למדידת יעילות FRET ברמת המולקולה הבודדת יש יתרון משמעותי על פני טכניקות הרכב, כפי שהוא מודיע על תת-אוכלוסין הטרוגניים, אשר בניסוי הרכב יהיה ממוצע. יתר על כן, FRET מולקולה אחת עם ALEX נותן גישה יעילות FRET מדויק, אשר ניתן להמיר למרחקים מדויקים. זה מאפשר קביעת מידע מבני מפורט יותר ולא רק לבחן שינויים יחסיים במרחק. ה- smfBox נושא את כל היתרונות והיכולות הללו אך ניתן לבנות אותו בתקציב נמוך בהרבה ממיקרוסקופים זמינים מסחרית דומים המסוגלים לקונפוקל smFRET23.
ה- smfBox מהווה מחסום כניסה נמוך בהרבה לטכניקות smFRET, ומאפשר לחוקרים למדוד שינויים קונפורמציה, ומרחקים מדויקים בתוך ובין חלבונים וחומצות גרעין7,8,9,10,11,35.
Disclosures
The authors have nothing to disclose.
Acknowledgements
המחברים מכירים בהכרת תודה במקורות המימון הבאים: BBSRC (BB/T008032/1); EPSRC (סטודנט לתואר ראשון) ו- MRC (סטודנט לא.ר.ט.
Materials
| Amino modified oligonucleotide | Eurogentec | N/A | May be ordered from various suppliers or synthesised; amino modification enables labeling with NHS-ester modified dyes |
| Avalanche photodiode (APD) | Excelitas | SPCM-AQRH-14 | Two APDs are required for the smfBox setup |
| Bovine Serum Albumin (BSA) | Merck | A2153 | System dependant; imaging buffer component (0.1 mg/mL in buffer) |
| Compact Laser Combiner | OMICRON | LightHUB-2 | 515 nm (80 mW) and 638 nm (100 mW) lasers |
| Coverglass | VWR | 630-2742 | Thickness: 0.17 ± 0.01 mm, LxW: 22×22 mm |
| Cy3B | Cytiva | PA63101 | 1 mg, PA63100 (5 mg), PA96106 (25 mg) |
| FRETBursts Python Package | N/A | N/A | Open-source python package for burst analysis of freely-diffusing single-molecule FRET data: https://fretbursts.readthedocs.io |
| Imaging Buffer | N/A | System dependant; 5 mM NaCl, 20 mM MgCl2, 5 mM Tris pH 7.5 and 0.1 mg/mL BSA | |
| Immersion Oil | Olympus | IMMOIL-F30CC | |
| Jupyter notebooks | Project Jupyter | N/A | Open-source web application to create and share documents that contain live code, equations, visualizations and text; data analysis notebooks for smfBox can be found in the SI |
| Lens Tissue | ThorLabs | MC-5 | MC-50E is same item in bulk |
| Magnesium Chloride | Merck | M2670 | System dependant; imaging buffer component (20 mM in buffer) |
| MilliQ/Ultrapure water | N/A | ||
| Nanopoistioner | Piezoconcept | FOC300 | Nanopositioner for accurate positioning of microscope objective |
| NHS-ester modified ATTO-550 | ATTO-TEC | AD 550-31 | 1 mg, AD 550-35 (5 mg) |
| NHS-ester modified ATTO-647N | ATTO-TEC | AD 647N-31 | 1 mg, AD 647N-35 (5 mg) |
| Objective lens | Olympus | N1480700 | Olympus objective series from orignal smfBox discontinued; replaced by N5702300 |
| OMICRON Control Center (OCC)- laser control center | OMICRON | N/A | v3.5.34 – OMICRON laser driver software |
| Press-To-Seal silicone isolator | Grace Bio-Labs | 664201 | 8-9 mm Diameter x 1.7 mm Depth |
| smOTTER | N/A | N/A | Open-source acquisition software for the Craggs Lab smfBox: https://github.com/craggslab/smOTTER |
| Sodium Chloride | Merck | S7653 | System dependant; imaging buffer component (5 mM in buffer) |
| Tris base | Merck | 93362 | System dependant; imaging buffer component (5 mM, pH 7.5 in buffer) |
| Type I ultrapure water | Merck | ZIQ7000T0 | Milli-Q® IQ 7000 Ultrapure Water System |
References
- Forster, T. Intermolecular energy migration and fluorescence. Annals of Physics. 437 (1-2), 55-75 (1948).
- Stryer, L., Haugland, R. P. Energy transfer: a spectroscopic ruler. Proceedings of the National Academy of Sciences. 58 (2), 719-726 (1967).
- Hohlbein, J., et al. Conformational landscapes of DNA polymerase I and mutator derivatives establish fidelity checkpoints for nucleotide insertion. Nature Communications. 4 (1), 2131 (2013).
- Lerner, E., et al. Toward dynamic structural biology: Two decades of single-molecule Förster resonance energy transfer. Science. 359 (6373), (2018).
- Hohlbein, J., Craggs, T. D., Cordes, T. Alternating-laser excitation: single-molecule FRET and beyond. Chemical Society Reviews. 43 (4), 1156-1171 (2014).
- Lerner, E., et al. The FRET-based structural dynamics challenge — community contributions to consistent and open science practices. arXiv. , (2020).
- Hellenkamp, B., Wortmann, P., Kandzia, F., Zacharias, M., Hugel, T. Multidomain structure and correlated dynamics determined by self-consistent FRET networks. Nature Methods. 14 (2), 174-180 (2017).
- Craggs, T. D., et al. Substrate conformational dynamics facilitate structure-specific recognition of gapped DNA by DNA polymerase. Nucleic Acids Research. 47 (20), 10788-10800 (2019).
- Tsytlonok, M., et al. Dynamic anticipation by Cdk2/Cyclin A-bound p27 mediates signal integration in cell cycle regulation. Nature Communications. 10 (1), 1676 (2019).
- Nagy, J., et al. Complete architecture of the archaeal RNA polymerase open complex from single-molecule FRET and NPS. Nature Communications. 6 (1), 6161 (2015).
- LeBlanc, S. J., et al. Coordinated protein and DNA conformational changes govern mismatch repair initiation by MutS. Nucleic Acids Research. 46 (20), 10782-10795 (2018).
- Segal, M., et al. High-throughput smFRET analysis of freely diffusing nucleic acid molecules and associated proteins. Methods. 169, 21-45 (2019).
- Kapanidis, A. N., et al. Fluorescence-aided molecule sorting: Analysis of structure and interactions by alternating-laser excitation of single molecules. Proceedings of the National Academy of Sciences. 101 (24), 8936-8941 (2004).
- Kapanidis, A. N., et al. Alternating-laser excitation of single molecules. Accounts of Chemical Research. 38 (7), 523-533 (2005).
- Müller, B. K., Zaychikov, E., Brauchle, C., Lamb, D. C. Pulsed interleaved excitation. Biophysical Journal. 89 (5), 3508-3522 (2005).
- Laurence, T. A., Kong, X., Jager, M., Weiss, S. Probing structural heterogeneities and fluctuations of nucleic acids and denatured proteins. Proceedings of the National Academy of Sciences of the United States of America. 102 (48), 17348-17353 (2005).
- Pollina, T., et al. PlanktonScope: Affordable modular imaging platform for citizen oceanography. bioRxiv. , 056978 (2020).
- Collins, J. T., et al. Robotic microscopy for everyone: the OpenFlexure microscope. Biomedical Optics Express. 11 (5), 2447-2460 (2020).
- Courtney, A., Alvey, L. M., Merces, G. O. T., Burke, N., Pickering, M. The Flexiscope: a low cost, flexible, convertible and modular microscope with automated scanning and micromanipulation. Royal Society Open Science. 7 (3), 191949 (2020).
- Martens, K. J. A., et al. Visualisation of dCas9 target search in vivo using an open-microscopy framework. Nature Communications. 10 (1), 3552 (2019).
- Auer, A., et al. Nanometer-scale multiplexed super-resolution imaging with an economic 3D-DNA-PAINT microscope. ChemPhysChem. 19 (22), 3024-3034 (2018).
- Li, H., et al. Squid: Simplifying quantitative imaging platform development and deployment. bioRxiv. , 424613 (2020).
- Ambrose, B., et al. The smfBox is an open-source platform for single-molecule FRET. Nature Communications. 11 (1), 5641 (2020).
- Ingargiola, A., Laurence, T., Boutelle, R., Weiss, S., Michalet, X. Photon-HDF5: An open file format for timestamp-based single-molecule fluorescence experiments. Biophysical Journal. 110 (1), 26-33 (2016).
- Hellenkamp, B., et al. Precision and accuracy of single-molecule FRET measurements-a multi-laboratory benchmark study. Nature Methods. 15 (9), 669-676 (2018).
- Ingargiola, A., Lerner, E., Chung, S., Weiss, S., Michalet, X. FRETBursts: An open source toolkit for analysis of freely-diffusing single-molecule FRET. PLOS One. 11 (8), 0160716 (2016).
- Torella, J. P., Holden, S. J., Santoso, Y., Hohlbein, J., Kapanidis, A. N. Identifying molecular dynamics in single-molecule FRET experiments with burst variance analysis. Biophysical Journal. 100 (6), 1568-1577 (2011).
- Tomov, T. E., et al. Disentangling subpopulations in single-molecule FRET and ALEX experiments with photon distribution analysis. Biophysical Journal. 102 (5), 1163-1173 (2012).
- Santoso, Y., Torella, J. P., Kapanidis, A. N. Characterizing single-molecule FRET dynamics with probability distribution analysis. ChemPhysChem. 11 (10), 2209-2219 (2010).
- Kalinin, S., Valeri, A., Antonik, M., Felekyan, S., Seidel, C. A. M. Detection of structural dynamics by FRET: A photon distribution and fluorescence lifetime analysis of systems with multiple states. The Journal of Physical Chemistry B. 114 (23), 7983-7995 (2010).
- Pirchi, M., et al. Photon-by-photon hidden Markov model analysis for microsecond single-molecule FRET kinetics. The Journal of Physical Chemistry B. 120 (51), 13065-13075 (2016).
- Schrimpf, W., Barth, A., Hendrix, J., Lamb, D. C. PAM: A framework for integrated analysis of imaging, single-molecule, and ensemble fluorescence data. Biophysical Journal. 114 (7), 1518-1528 (2018).
- Zijlstra, N., et al. Rapid microfluidic dilution for single-molecule spectroscopy of low-affinity biomolecular complexes. Angewandte Chemie International Edition. 56 (25), 7126-7129 (2017).
- Hellenkamp, B., Thurn, J., Stadlmeier, M., Hugel, T. Kinetics of transient protein complexes determined via diffusion-independent microfluidic mixing and fluorescence stoichiometry. The Journal of Physical Chemistry B. 122 (49), 11554-11560 (2018).
- Bennet, I. A., et al. Regional conformational flexibility couples substrate specificity and scissile phosphate diester selectivity in human flap endonuclease 1. Nucleic Acids Research. 46 (11), 5618-5633 (2018).

