Bakteriell uttrykk og rensing av human matrise Metalloproteinase-3 ved hjelp av affinitet kromatografi
Summary
Hans-tag rensing, dialyse og aktivering brukes til å øke utbyttet av løselig, aktiv matrise metalloproteinase-3 katalytisk domene protein uttrykk i bakterier. Proteinfraksjoner analyseres via SDS-PAGE geler.
Abstract
Matrix metalloproteinaser (MLP)-er tilhører familien av metzincinproteaser med sentrale roller i ekstracellulær matrise (ECM) nedbrytning og ombygging, samt interaksjoner med flere vekstfaktorer og cytokiner. Overekspressering av spesifikke MMP-er er ansvarlig i flere sykdommer som kreft, nevrodegenerative sykdommer og kardiovaskulær sykdom. MMP-er har vært sentrum for oppmerksomheten den siste tiden som mål om å utvikle terapeutiske behandlinger som kan behandle sykdommer som er korrelert med MMP-overekspression.
For å studere MMP-mekanismen i løsning, er det nødvendig med mer facile og robuste rekombinante proteinuttrykk og rensemetoder for produksjon av aktive, oppløselige MMP-er. Det katalytiske domenet til de fleste MMP-er kan imidlertid ikke uttrykkes i Escherichia coli (E. coli) i løselig form på grunn av mangel på posttranslasjonsmaskineri, mens pattedyruttrykkssystemer vanligvis er kostbare og har lavere utbytter. MMP-inkluderingsorganer må gjennomgå den kjedelige og arbeidskrevende prosessen med omfattende rensing og omfolding, noe som reduserer utbyttet av MMP-er betydelig i innfødt konformasjon. Dette dokumentet presenterer en protokoll ved hjelp av Rosetta2(DE3)pLysS (heretter referert til som R2DP) celler for å produsere matrise metalloproteinase-3 katalytisk domene (MMP-3cd), som inneholder en N-terminal His-tag etterfulgt av pro-domene (Hisx6-pro-MMP-3cd) for bruk i affinitetsrensing. R2DP-celler forbedrer uttrykket av eukaryote proteiner gjennom en kloramfenikolresistent plasmid som inneholder codons som normalt er sjeldne i bakterielle uttrykkssystemer. Sammenlignet med den tradisjonelle cellelinjen for rekombinant proteinuttrykk, BL21 (DE3), forbedret rensing ved hjelp av denne nye stammen utbyttet av renset Hisx6-pro-MMP-3cd. Ved aktivering og avsalting er pro-domenet spaltet sammen med N-terminalen His-tag, og gir aktiv MMP-3cd for umiddelbar bruk i utallige in vitro-applikasjoner . Denne metoden krever ikke dyrt utstyr eller komplekse fusjonsproteiner og beskriver rask produksjon av rekombinante menneskelige MMP-er i bakterier.
Introduction
De fleste komplekse eukaryote proteiner gjennomgår forseggjorte posttranslasjonelle modifikasjoner etter uttrykk, noe som krever svært assistert proteinfolding og kofaktorer for å være funksjonelle1. Å produsere store mengder løselig humant protein i en bakteriell vert er fortsatt en betydelig utfordring på grunn av høye kostnader og mangel på robuste uttrykks- og rensemetoder, selv for mindre laboratorieforsøk2,3. MLP-er, humane endopeptidaser med stor molekylvekt, uttrykkes vanligvis som uoppløselige inklusjonslegemer når de uttrykkes i E. coli. Utvinning av løselige menneskelige MMP-er fører ofte til en arbeidskrevende, tidkrevende løsnings- og omfoldingsprosess4.
MMP-er har kritiske roller i både fysiologiske og patogene prosesser. Humane MMP-er er en familie på 23 sink endopeptidaser, kategorisert etter struktur og substratspesifisitet, og differensialt uttrykt til tross for et høyt bevart katalytisk domene5,6. MMP-er utskilles som inaktive zymogener, regulert via posttranslasjonell aktivering og deres endogene hemmere, vevshemmere av metalloproteinaser (TIMPs) 7,8,9,10. Selv om de først ble anerkjent for sin rolle i ECM-omsetning, har MMP-er også vært involvert i utvikling, morfogenese, vevsreparasjon og ombygging8. Dysregulering av MMP-er har særlig vært knyttet til kreft sammen med blant annet nevrodegenerative, kardiovaskulære og fibrotiske sykdommer.
Utviklingen av robuste MMP-produksjonsmetoder i stor skala er avgjørende for å sikre suksess for fremtidige studier av MMP-mekanismer gjennom biokjemiske og cellebaserte analyser. Ulike MMP-er har tidligere blitt uttrykt i bakterier11, inkludert Hisx6-taggede MMPer, uten å endre MMP-aktivitet12,13,14,15. Imidlertid inkluderer disse metodene kjedelige, lange trinn som kan være vanskelige å gjenskape.
Pattedyrceller kan også brukes til å uttrykke mange forskjellige menneskelige proteiner samtidig som de sikrer riktige posttranslasjonelle modifikasjoner16. Selv om pattedyruttrykkssystemet er et ideelt valg for å produsere rekombinante menneskelige proteiner med riktige postoversettelsesendringer, er de viktigste ulempene ved denne metoden innledende lave utbytter, kostbare vekstmedier og reagenser, lange tidslinjer for å nå stabile uttrykkslinjer og risiko for forurensning med andre arter som sopp eller bakterier2,11 . Videre gir MMP-produksjon i pattedyrcellelinjer urenheter fra tilknyttede cellulære proteiner som TIMPer eller fibronectins11. I motsetning til den langsomme celleveksten som observeres i pattedyrceller, tilbyr bakterieuttrykkssystemet storskala proteinproduksjon på kort tid sammen med enklere medier og vekstkrav. På grunn av mangel på andre assosierte cellulære proteiner (dvs. TIMPer) i bakterielle uttrykkssystemer, er aktive MMP-er ved høyere konsentrasjoner utsatt for nedbrytning gjennom autoproteolyse, noe som resulterer i dårlig MMP-utbytte17.
Dette dokumentet beskriver en detaljert metode for bakteriell uttrykk, rensing og aktivering av rekombinant Hisx6-pro-MMP-3cd ved hjelp av E. coli som uttrykksvert på grunn av sin overkommelige pris, enkelhet og suksess med å produsere høyere utbytter av MMPs2,3,18. Siden E. coli mangler protein folding maskiner og posttranslational behandling som kreves for rekombinante MMP og andre komplekse proteiner, mange E. coli stammer har blitt konstruert for å overvinne disse begrensningene, noe som gjør E. coli en mer egnet vert for uttrykk for rekombinant menneskelig MMP-3cd, 19,20 . For eksempel forbedrer R2DP-stammen som brukes i denne studien eukaryotisk uttrykk ved å levere en kloramfenikolresistent plasmid som inneholder codons som sjelden brukes i E. coli.
Som beskrevet i denne protokollen, etter overekspressering av relativt rene inklusjonslegemer fra pET-3a-vektoren (figur 1) i R2DP-celler, blir Hisx6-pro-MMP-3 katalytiske domene (MMP-3cd) proteiner ekstrahert og denaturert4. Hisx6-pro-MMP-3cd3,19 ble renset ved hjelp av affinitetsmerkekromatografi. Ved omfolding og dialyse ble pro-MMP-3cd (zymogen) aktivert av 4-aminofenylmercuric acetat (APMA), og SDS-PAGE analyse brukes til å evaluere utbytter og behovet for ytterligere rensing5,21. Denne protokollen beskriver uttrykk, rensing og aktivering av løselig MMP-3cd som et eksempel. Det kan imidlertid også brukes som en veiledning for uttrykk for andre MMP-er og menneskelige proteaser med lignende uttrykk, og aktiveringsmekanismer (figur 2). For andre proteiner enn MMP-3cd anbefales leseren å bestemme optimale buffersammensetninger og metoder for deres målprotein før du prøver denne protokollen.
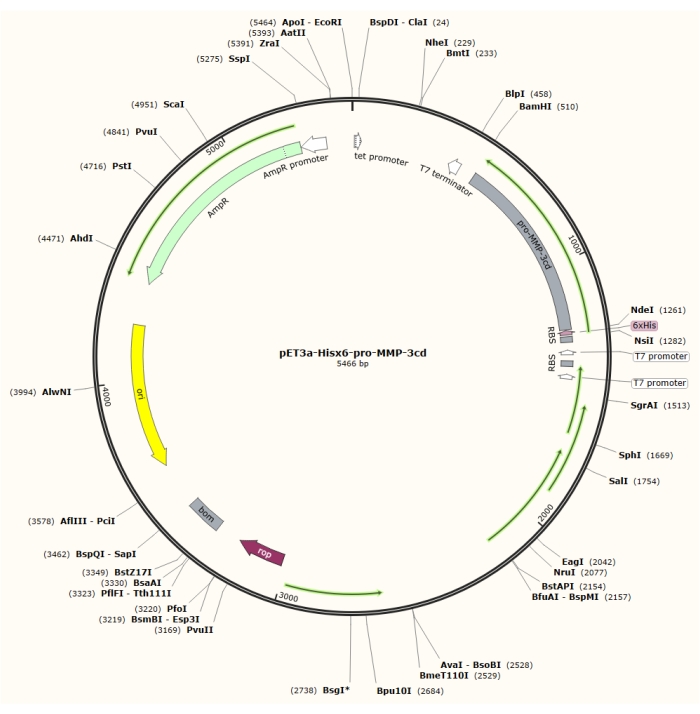
Figur 1: Plasmidkart over pET-3a-Hisx6-pro-MMP-3cd plasmid. PET-3a-vektoren inneholder et ampicillinresistensgen. En N-terminal Hisx6-tag-sekvens klones inn i den pET-3a-baserte vektoren, inkludert pro-MMP-3cd, for å gi pET-3a-Hisx6-pro-MMP-3cd-konstruksjonen under kontroll av T7-promotoren mellom BamHI og NdeI-begrensningssteder. Klikk her for å se en større versjon av denne figuren.
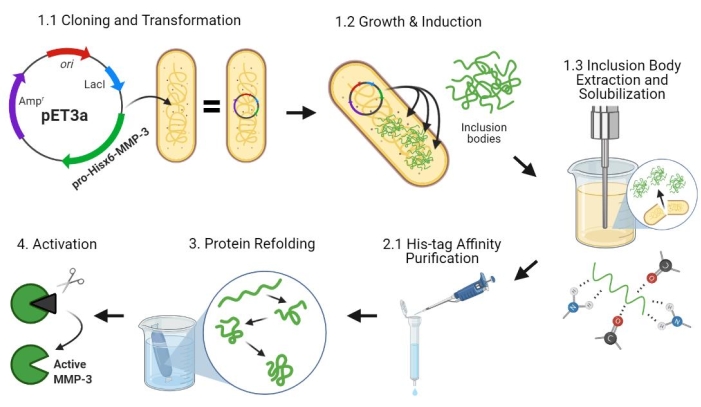
Figur 2: Bakteriell uttrykk for pro-MMP-3cd, rensing, bretting og aktivering. 1.1: pET-3a-Hisx6-pro-MMP-3cd plasmid ble forvandlet til BL21(DE3) eller R2DP Cells. 1.2: Pro-MMP-3cd proteinuttrykk ble indusert ved hjelp av IPTG. 1.3: Kjemisk lysis og sonikering brukes til å trekke ut Hisx6-pro-MMP-3cd proteiner som hovedsakelig er uoppløselige og finnes i inklusjonslegemene. Urea ble brukt til å denaturere og løse protein fra inklusjonslegemer. 2.1. Denaturert Hisx6-pro-MMP-3cd protein ble renset via affinitet kromatografi rensing. 3. Den eluted Hisx6-pro-MMP-3cd ble sakte omdelt under dialyse gjennom gradvis fjerning av urea fra bufferen. 4. Til slutt ble refoldet MMP-3cd protein aktivert ved hjelp av APMA ved å fjerne N-terminal pro-peptiddomenet. APMA fjernes senere fra løsningen gjennom avsalting. Tallene tilsvarer protokolldelene som beskriver disse trinnene. Forkortelser: MMP-3cd = Matrix metalloproteinase-3 katalytisk domene; APMA = 4-aminofenylmercuric acetat. Klikk her for å se en større versjon av denne figuren.
Protocol
Representative Results
Discussion
Den store produksjonen av løselige, menneskelige, rekombinante MMP-er er fortsatt en utfordrende oppgave. Pattedyrceller kan uttrykke funksjonelle MPS til høye kostnader og lange ventetider, mens E. coli raskt produserer høye mengder MMP-inkluderingsorganer som må renses og brettes på nytt11,16. R2DP-celler øker utbyttet av MMP-inkluderingsorganer betydelig, noe som muliggjør en mer kostnadseffektiv og produktiv MMP-omfoldingsprosess. Imidlertid m…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Forfatterne ønsker å anerkjenne Dr. Evette Radisky og Alexandra Hockla ved Mayo Clinic i Jacksonville, Florida, for å ha gitt pET-3a-pro-MMP-3cd plasmid som mal for kloning av Hisx6pro-MMP-3cd-genet, og deres kommentarer, sammen med Dr. Paul Hartley fra Nevada Genomics Center ved University of Nevada, Reno, for DNA-sekvensering. Forfatterne vil også takke Cassandra Hergenrader for å ha hjulpet til med en del av proteinuttrykket. M.R.-S. vil takke NIH-P20 GM103650-COBRE Integrative Neuroscience grant og UNR R&D mICRO SEED Grant Award.
Materials
| 0.22 µm sterile filter | Sigma Aldrich | SLGP033RS | Used to remove some contaminants from the protein extract before purification, and prevent the Ni-NTA column from clogging |
| 1 L Erlenmeyer flasks | Thermo Fisher Scientific | S76106F | n/a |
| 1 L glass bottles | Thermo Fisher Scientific | 06-414-1D | n/a |
| 1.5 mL microfuge tubes | Thermo Fisher Scientific | 02-682-002 | n/a |
| 15 mL conical tubes | Thermo Fisher Scientific | 339650 | n/a |
| 18 G, 1-in. beveled needle | Amazon | B07S7VBHM2 | Used in combination with the dialysis casette |
| 2 mL desalting column | Thermo Fisher Scientific | 89890 | Removes APMA following activation |
| 2-(N-Morpholino)ethanesulfonic acid (MES) | Thermo Fisher Scientific | AAA1610422 | n/a |
| 250 mL conical bottle cushions | Thermo Fisher Scientific | 05-538-53A | Stabilize conical bottles during large-volume centrifugation |
| 250 mL conical bottles | Thermo Fisher Scientific | 05-538-53 | n/a |
| 400 mL stirred cell | Sigma Aldrich | UFSC40001 | Re-concentrates a much larger volume than the centrifugal filter unit. Rosetta2(DE3)pLysS cells produce high volumes of protein that may exceed the 15 mL limit of the centrifugal filter unit |
| 4-aminophenylmercuric acetate (APMA) | Sigma Aldrich | A9563-5G | Activates MMP-3 by cleaving the propeptide |
| 5 mL syringe | Thermo Fisher Scientific | NC0829167 | Used in combination with the dialysis casette |
| 50 mL conical tubes | Thermo Fisher Scientific | 339650 | Used for storage in many purification steps |
| 50 mL re-concentration tube | Sigma Aldrich | UFC901024D | Used for re-concentrating protein samples after dialysis or removing contaminants |
| Agar | Thermo Fisher Scientific | BP1423-500 | Buffer ingredient that solidifies autoclaved LB media upon cooling |
| Ampicillin | Thermo Fisher Scientific | BP1760-25 | Antibiotic used with pET3a vector; used at 100 µg/mL in LB media |
| BamHI | NEB | R3136S | Restriction enzyme to be used with the pET3a vector |
| Calcium chloride (CaCl2) | Thermo Fisher Scientific | 600-30-23 | The calcium ion stabilizes MMP structure |
| Cell spreaders | Thermo Fisher Scientific | 50-189-7544 | Can be used to spread cells across a petri dish after transformation |
| Chloramphenicol | Thermo Fisher Scientific | 22-055-125GM | Antibiotic used with pET3a vector; used at 34 µg/mL in LB media |
| Dialysis Buffer 1 | n/a | n/a | 20 mM Tris-HCl (pH 8.0), 150 mM NaCl, 10 mM CaCl2, 1 µM ZnCl2, 4 M Urea. |
| Dialysis Buffer 2 | n/a | n/a | 20 mM Tris-HCl (pH 8.0), 150 mM NaCl, 10 mM CaCl2, 1 µM ZnCl2, 2 M Urea. |
| Dialysis Buffer 3 | n/a | n/a | 20 mM Tris-HCl (pH 8.0), 150 mM NaCl, 10 mM CaCl2 , 1 µM ZnCl2. |
| Dialysis clips | Thermo Fisher Scientific | 68011 | Used in combination with snakeskin dialysis tubing |
| Dialysis tubing | Thermo Fisher Scientific | 88243 | Alternative dialysis method that holds much larger sample volumes, but with higher risk of sample loss |
| Digest buffer | NEB | B7204S | Buffer used in digesting the pET3a vector |
| Disposable cuvettes | Thermo Fisher Scientific | 21-200-257 | Used to measure the bacterial culture OD during growth and expression |
| Dithiothreitol (DTT) | Thermo Fisher Scientific | D107125G | Assists with protein denaturation by reducing any disulfide bonds |
| DNA assembly mix | NEB | E2621S | Used to ligate the Hisx6-pro-MMP-3cd PCR product and digested pET3a vector |
| DNase I | NEB | M0303S | Endonuclease for degrading unfavorable DNA contaminants that could later affect protein purification |
| Ethanol | Thermo Fisher Scientific | A995-4 | n/a |
| Ethylenediaminetetraacetic acid (EDTA) | Thermo Fisher Scientific | J15694-AE | Used in denaturation. Prevents oxidation and subsequent formation of disulfide bonds |
| Gel recovery kit | Promega | A9281 | Isolates and purifies DNA from agarose gels |
| Glycerol | Thermo Fisher Scientific | G33-500 | Used for making glycerol stocks, which are frozen at -80 °C |
| Gravity flow column | BioRad | 7321010 | Used for Ni-NTA purification of recombinantly His-tagged proteins |
| Guanidine hydrochloride (GdnHCl) | Thermo Fisher Scientific | AAA135430B | Second chaotropic agent used for disrupting protein secondary structure. |
| High-transformation efficiency cells | NEB | C2987 | High-transformation efficiency cells with greater chance of success for cloning the N-terminal His-tag into the pET3a-pro-MMP-3cd construct |
| HT Elution Buffer | n/a | n/a | 20 mM Tris-HCl (pH 8.0), 50 mM NaCl, 6 M urea, 250 mM imidazole. Adjust pH to 7.4 |
| HT Equilibration Buffer | n/a | n/a | 20 mM Tris-HCl (pH 8.0), 50 mM NaCl, 6 M urea. Adjust pH to 7.4 |
| HT Regeneration Buffer | n/a | n/a | 20 mM MES, 0.1 M NaCl. Adjust pH to 5.0 |
| HT Wash Buffer | n/a | n/a | 20 mM Tris-HCl (pH 8.0), 50 mM NaCl, 6 M urea, 25 mM imidazole. Adjust pH to 7.4 |
| Hydrochloric acid (HCl) | Thermo Fisher Scientific | A144C-212 | Used to pH buffers |
| Imidazole | Thermo Fisher Scientific | AAA1022122 | Mimics the histidine side group. Used to separate non-specifically binding proteins from the his-tagged target protein |
| Inclusion Body Buffer | n/a | n/a | 20 mM Tris-HCl (pH 8.0), 1 mM EDTA, 100 mM NaCl, 5 mM DTT, 2% v/v Triton X 100, 0.5 M Urea. Adjust pH to 8.0 |
| Isopropyl-ß-D-thiogalactopyranoside (IPTG) | Thermo Fisher Scientific | FERR0392 | A reagent that induces target gene expression in pET3a. Make 0.5 mL 1 M aliquots, filter sterilize and store in -20 °C |
| LB Amp CamR media | n/a | n/a | To be poured into a sterible 1 L bottle or 1 L flask. For 1 L, add 25 g LB Broth. Sterilize by autoclaving. Once cooled to below 50 °C, add ampicillin to 100 µg/mL and chloramphenicol to 34 µg/mL |
| LB Amp CamR plates | n/a | n/a | To be poured into sterile petri dishes. Pour until the petri dish lid is completely covered. 1 L of media yields 40-60 plates. For 1 L: 25 g LB Broth, 16 g Agar. Sterilize by autoclaving. Once cooled to below 50 °C, add ampicillin to 100 µg/mL and chloramphenicol to 34 µg/mL |
| LB Broth | Thermo Fisher Scientific | BP1426-2 | Pre-mixed with tryptone, yeast extract, and sodium chloride |
| Lysis Buffer | n/a | n/a | 50 mM Tris-HCl (pH 8.0), 1 mM EDTA, 100 mM NaCl, 0.133 g/mL lysozyme, 0.49% v/v Triton X-100. Adjust pH to 8.0 |
| Lysozyme | MP Biomedicals | 195303 | Used in protein extraction. Enzyme that lyses bacterial cell walls |
| Miniprep kit | Promega | A1330 | If successful, extracts the pET3a-pro-MMP-3cd construct from transformants |
| NdeI | NEB | R0111S | Restriction enzyme to be used with the pET3a vector |
| Ni-NTA resin | Thermo Fisher Scientific | PI88221 | Used to bind recombinant his-tagged proteins. This strong interaction can be displaced with higher concentrations of imidazole |
| PCR mix | NEB | M0492S | A PCR reagent for inserting an N-terminal his-tag into the pET3a-pro-MMP-3cd vector |
| pET plasmid | Addgene | n/a | The pET3a vector offers ampicillin resistance, inducible expression of a target gene, and sequencing with T7 primers |
| Petri dishes | VWR | 25384-342 | Used for plating transformants on LB agar media |
| R2DP cells | Novagen | 714033 | BL21 derivatives with enhanced expression of eukaryotic proteins. Contain tRNAs of codons found to be rare in e. coli |
| SOC growth media | NEB | B9020S | Non-selective growth media for rapid growth during transformation |
| Sodium chloride (NaCl) | Thermo Fisher Scientific | BP358-1 | Used in buffers and helps with protein stability |
| Sodium deoxycholate | Thermo Fisher Scientific | PI89905 | Detergent used in protein extraction. Lyses cell walls |
| Solubilization Buffer | n/a | n/a | 20 mM Tris-HCl (pH 8.0), 50 mM NaCl, 10 mM DTT, 6 M Urea. Adjust pH to 8.0 |
| Tris base | Thermo Fisher Scientific | BP152-1 | Common buffer used in the physiological pH range. Temperature-sensitive |
| Triton X-100 | Thermo Fisher Scientific | M1122980101 | Detergent used for cell lysis |
| Urea | Thermo Fisher Scientific | AAJ75826A7 | First chaotropic agent for disrupting protein secondary structure |
| Zinc chloride (ZnCl2) | Thermo Fisher Scientific | AAA162810E | Stabilizes MMP structure. The zinc ion is found in the catalytic site of MMP-3 |
References
- Portolano, N., et al. Recombinant protein expression for structural biology in HEK 293F suspension cells: A novel and accessible approach. Journal of Visualized Experiments: JoVE. (92), e51897 (2014).
- Subedi, G. P., Johnson, R. W., Moniz, H. A., Moremen, K. W., Barb, A. High yield expression of recombinant human proteins with the transient transfection of HEK293 cells in suspension. Journal of Visualized Experiments: JoVE. (106), e53568 (2015).
- Nilvebrant, J., Alm, T., Hober, S. Orthogonal protein purification facilitated by a small bispecific affinity tag. Journal of Visualized Experiments: JoVE. (59), e3370 (2012).
- Yang, Z., et al. Highly efficient production of soluble proteins from insoluble inclusion bodies by a two-step-denaturing and refolding method. PLoS One. 6 (7), 22981 (2011).
- Hu, X., Beeton, C. Detection of functional matrix metalloproteinases by zymography. Journal of Visualized Experiments: JoVE. (45), e2445 (2010).
- Radisky, E. S., Raeeszadeh-Sarmazdeh, M., Radisky, D. C. Therapeutic potential of matrix metalloproteinase inhibition in breast cancer. Journal of Cellular Biochemistry. 118 (11), 3531-3548 (2017).
- Raeeszadeh-Sarmazdeh, M., Do, L. D., Hritz, B. G. Metalloproteinases and their inhibitors: Potential for the development of new therapeutics. Cells. 9 (5), 1313 (2020).
- Nagase, H., Visse, R., Murphy, G. Structure and function of matrix metalloproteinases and TIMPs. Cardiovascular Research. 69 (3), 562-573 (2006).
- Raeeszadeh-Sarmazdeh, M., et al. Directed evolution of the metalloproteinase inhibitor TIMP-1 reveals that its N- and C-terminal domains cooperate in matrix metalloproteinase recognition. Journal of Biological Chemistry. 294 (24), 9476-9488 (2019).
- Batra, J., et al. Matrix metalloproteinase-10 (MMP-10) interaction with tissue inhibitors of metalloproteinases TIMP-1 and TIMP-2. Journal of Biological Chemistry. 287 (19), 15935-15946 (2012).
- Singh, K. K., Jain, R., Ramanan, H., Saini, D. K., Galea, C. A. Expression and purification of matrix metalloproteinases in Escherichia coli. Matrix Metalloproteases. , 3-16 (2017).
- Manka, S. W., et al. Structural insights into triple-helical collagen cleavage by matrix metalloproteinase 1. Proceedings of the National Academy of Sciences of the United States of America. 109 (31), 12461-12466 (2012).
- Gomis-Ruth, F. X., et al. Mechanism of inhibition of the human matrix metalloproteinase stromelysin-1 by TIMP-1. Nature. 389 (6646), 77-81 (1997).
- Shirian, J., et al. Converting a broad matrix metalloproteinase family inhibitor into a specific inhibitor of MMP-9 and MMP-14. FEBS Letters. 592 (7), 1122-1134 (2018).
- Li, C., et al. Purification of recombinant histidine-tagged catalytic domain of MMP-13 in one step using affinity column and renaturation of it with histidine tag. Journal of Liquid Chromatography & Related Technologies. 37 (15), 2118-2130 (2014).
- Aydin, H., Azimi, F. C., Cook, J. D., Lee, J. E. A convenient and general expression platform for the production of secreted proteins from human cells. Journal of Visualized Experiments: JoVE. (65), e4041 (2012).
- McNiff, M. L., Haynes, E. P., Dixit, N., Gao, F. P., Laurence, J. S. Thioredoxin fusion construct enables high-yield production of soluble, active matrix metalloproteinase-8 (MMP-8) in Escherichia coli. Protein Expression and Purification. 122, 64-71 (2016).
- Maity, R., et al. GST-His purification: A two-step affinity purification protocol yielding full-length purified proteins. Journal of Visualized Experiments: JoVE. (80), e50320 (2013).
- Stefan, A., Ceccarelli, A., Conte, E., Montón Silva, A., Hochkoeppler, A. The multifaceted benefits of protein co-expression in Escherichia coli. Journal of Visualized Experiments: JoVE. (96), e52431 (2015).
- Yadavalli, R., Sam-Yellowe, T. HeLa based cell free expression systems for expression of Plasmodium rhoptry proteins. Journal of Visualized Experiments: JoVE. (100), e52772 (2015).
- Zeytuni, N., Zarivach, R. Purification of the M. magneticum strain AMB-1 magnetosome associated protein MamAΔ41. Journal of Visualized Experiments: JoVE. (37), e1844 (2010).

