Bestrahlungsplanungsassistent - Ein webbasiertes Tool zur Unterstützung einer qualitativ hochwertigen Strahlentherapie in Kliniken mit begrenzten Ressourcen
Summary
Dieses Protokoll beschreibt eine Reihe automatisierter Tools, die für die hochwertige Autokonturierung und Autoplanung der Strahlentherapie entwickelt wurden und in einen webbasierten Service verpackt werden, um die Robustheit und Skalierbarkeit zu maximieren und gleichzeitig die Betriebskosten zu minimieren.
Abstract
Der Zugang zur Strahlentherapie ist weltweit begrenzt. Der Radiation Planning Assistant (RPA) ist ein vollautomatisches, webbasiertes Tool, das entwickelt wird, um Kliniken mit begrenzten Ressourcen vollautomatische Tools zur Planung von Strahlentherapiebehandlungen anzubieten. Ziel ist es, klinische Teams dabei zu unterstützen, ihre Bemühungen zu skalieren und so mehr Krebspatienten zu erreichen. Der Benutzer stellt über eine Webseite eine Verbindung zum RPA her, füllt eine Serviceanfrage (Rezept und Informationen über die Strahlentherapieziele) aus und lädt das CT-Bildset des Patienten hoch. Die RPA bietet zwei Ansätze für die automatisierte Planung. Bei der einstufigen Planung generiert das System anhand der Serviceanfrage und des CT-Scans automatisch die notwendigen Konturen und den Behandlungsplan. Bei der zweistufigen Planung überprüft und bearbeitet der Anwender die automatisch generierten Konturen, bevor die RPA mit der Erstellung eines volumenmodulierten Arc-Therapieplans fortfährt. Der endgültige Plan wird von der RPA-Website heruntergeladen und in das lokale Behandlungsplanungssystem des Benutzers importiert, wo die Dosis für den lokal in Betrieb genommenen Linac neu berechnet wird. Bei Bedarf wird der Plan vor der Zulassung für den klinischen Einsatz überarbeitet.
Introduction
Es wird erwartet, dass die weltweite Zahl der Krebsfälle bis 2030 auf etwa 24,6 Millionen ansteigen wird, wobei die größte Belastung in Ländern mit niedrigem und mittlerem Einkommen (LMICs)1 zu verzeichnen sein wird. Die Strahlentherapie ist eine kostengünstige, kurative und palliative Behandlung von Krebs, die etwa 50 % der Krebspatienten und 60-70 % in Ländern mit niedrigem Einkommen, in denen die Patienten mit größerer Wahrscheinlichkeit in einem späten Stadium vorstellig werden, Vorteile bietet 2,3. Der Zugang zur Strahlentherapie ist jedoch weltweit begrenzt4; So verfügt beispielsweise kein Land in Afrika über die Strahlentherapiekapazitäten, um den geschätzten Bedarf zu decken5. In mehreren Studien wurden diese drohenden Engpässe und die zur Deckung des künftigen Bedarfs erforderlichen Faktoren abgeschätzt 6,7.
Die Lancet Oncology Commission argumentierte überzeugend, dass Investitionen in die Verbesserung der Strahlentherapiekapazitäten nicht nur Leben retten, sondern auch positive wirtschaftliche Vorteile mit sich bringen würden3. Sie wiesen auch ausdrücklich darauf hin, dass die Automatisierung der Strahlentherapie-Konturierung und der Behandlungsplanung klinischen Teams helfen kann, ihre Bemühungen zu skalieren, indem sie die Zeit, die Onkologen bzw. Physiker für diese Aufgaben aufwenden, erheblich reduziert und die Ziele leichter erreichbar macht.
Unsere Forschungsgruppe hat in Zusammenarbeit mit klinischen Teams bei MD Anderson und in Krankenhäusern auf der ganzen Welt an der Entwicklung webbasierter automatisierter Tools gearbeitet. Diese Suite von Tools (RPA genannt) bietet auf künstlicher Intelligenz basierende Konturierung (Umrisse von Tumoren und nahe gelegenen Organen auf CT-Scans) und eine Strahlentherapie-Behandlungsplanung (die genau definiert, wie die Strahlung abgegeben wird). Diese webbasierte Plattform bietet den Vorteil, dass weniger Zeit und Ressourcen benötigt werden, um qualitativ hochwertige Pläne für jeden Patienten zu erstellen.
Unsere Erfahrung mit einer frühen Version eines KI-basierten Tools bei MD Anderson hat gezeigt, dass die automatisierte Konturierung bis zu 2 Stunden pro Patient einsparen kann – eine erhebliche Rationalisierung des Arbeitsablaufs. Dies bedeutet, dass das derzeitige klinische Personal in der Lage sein wird, seinen Aufwand zu skalieren und mehr Patienten mit einer qualitativ hochwertigeren Strahlentherapie zu behandeln. Indem wir diese Tools über einen vollautomatischen, webbasierten Service (Radiation Planning Assistant [RPA], RPA.mdanderson.org) anbieten, können wir die Kosten für die Patienten und Anbieter minimieren und die Reichweite dieses Tools maximieren.
Wir entwickeln die RPA seit 6 Jahren, und seit der ersten Veröffentlichung der RPA-Workflows8 wurden mehrere bedeutende Änderungen vorgenommen. Dazu gehört die Weiterentwicklung der RPA zu einem webbasierten Tool, wodurch die Kosten für Installation und Wartung gesenkt und die Robustheit des Systems verbessert werden. Zu den weiteren Verbesserungen gehören Änderungen an den Benutzeroberflächen, um die Benutzerfreundlichkeit zu verbessern und das Risiko von Fehlernzu verringern 9 sowie die Erweiterung der Behandlungsmöglichkeiten (insbesondere die Planung der Strahlentherapie für Brust nach Mastektomie10 und Metastasen im Gehirn11). Damit ist das hier beschriebene Protokoll wesentlich weiter fortgeschritten als die bisher veröffentlichte Ausgangsversion.
Die RPA verwendet einen einstufigen Prozess zur Erstellung von Konturen und Plänen in Situationen, in denen eine Bearbeitung der Konturen in der Regel nicht erforderlich ist, um den Behandlungsplan zu erstellen. Dazu gehören die Vier-Felder-Box-Behandlungsplanung für Gebärmutterhalskrebs (basierend auf knöchernen Landmarken oder automatisch generierten Weichteilkonturen)12,13,14,15, tangentiale oder supraklavikuläre Felder für Brustkrebs nach Mastektomie11 und entgegengesetzte laterale Felder für Ganzhirnbehandlungen16. Wir gehen davon aus, dass wir in naher Zukunft Schädelspinalbehandlungen für pädiatrische Krebserkrankungen17, Dreifeldbehandlungen für Rektumkarzinome18 und Behandlungsplanung für verschiedene palliative Fälle (Wirbelkörper, Hüften und Rippen)19 sowie Lungen- und Blasenkrebs hinzufügen werden. Derzeit erfordern fortgeschrittenere Behandlungen, insbesondere die volumenmodulierte Arc-Therapie (VMAT), einen zweistufigen Prozess, bei dem automatisch generierte Konturen vor der Behandlungsplanung bearbeitet werden13,20. Die Qualität des Deep-Learning-basierten Autocontouring ist jedoch so hoch, dass wir davon ausgehen, dass wir diese Planungsansätze in Zukunft auf einen einstufigen Prozess umstellen werden. Dieses Protokoll konzentriert sich auf die einstufige Planung.
Abbildung 1 zeigt den gesamten Arbeitsablauf für die Erstellung eines Strahlentherapie-Behandlungsplans mit dem RPA, mit weiteren Details zu den verschiedenen Aufgaben, die in Tabelle 1 aufgeführt sind. Zusammenfassend lässt sich sagen, dass die RPA eine ausgefüllte Serviceanfrage (die Informationen wie die Dosisverschreibung und den Behandlungsansatz enthält) und den individuellen CT-Scan eines Patienten erfordert. Die Serviceanfrage muss von einem Radioonkologen angenommen werden. Der CT-Scan muss von einem klinischen Benutzer akzeptiert werden, um sicherzustellen, dass die RPA-Berechnungen auf dem richtigen CT-Scan durchgeführt werden. Sobald die RPA einen Plan erstellt hat, sollte er von der RPA-Website heruntergeladen und in das Behandlungsplanungssystem des Benutzers importiert werden, wo die Dosis neu berechnet werden sollte. Dies ist notwendig, da die RPA Pläne für Standardträger (verfügbar für mehrere Linac-Modelle) berechnet, die möglicherweise nicht genau mit den Balkeneigenschaften des lokalen Linacs übereinstimmen. Dieser Ansatz wurde gewählt, um die Kosten zu senken, obwohl eine Anpassung erforderlich sein kann, wenn sich die lokalen Träger erheblich von unseren Standardträgern unterscheiden. Die Benutzer (Behandlungsplaner und Radioonkologe) können Änderungen am Plan vornehmen. Der Plan gibt dann den typischen klinischen Arbeitsablauf des Benutzers ein, einschließlich lokaler Qualitätssicherungsprüfungen. Schließlich sollte der Benutzer seinen endgültigen (neu berechneten und bearbeiteten) Plan auf die RPA-Website hochladen, wo ein automatisierter Vergleich zwischen dem endgültigen Plan und dem RPA-Plan durchgeführt wird. Dies ist eine sinnvolle Überprüfung der Datenintegrität im gesamten Workflow.
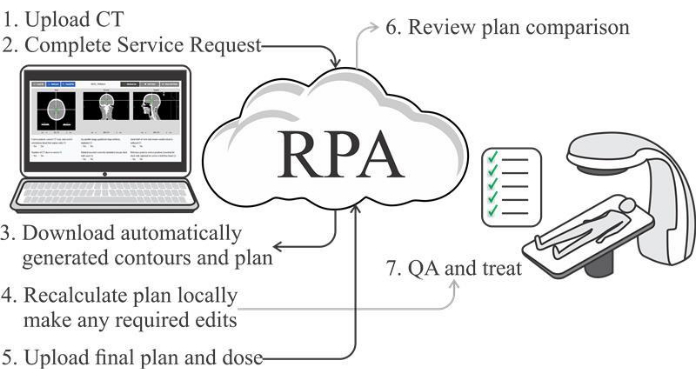
Abbildung 1: Ablauf des automatisierten Behandlungsplanungsprozesses. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
| Aufgabe # in Abbildung 1 | Aufgabenbeschreibung | Ort | |||
| Überprüfen Sie den Status früherer Patienten | Haupt-Dashboard | ||||
| 1 | Füllen Sie eine Serviceanfrage auf der RPA-Website aus | Dashboard für Serviceanfragen | |||
| 2 | Laden Sie einen CT-Scan auf die RPA-Website hoch | CT-Scan-Dashboard | |||
| 3 | Überprüfen Sie den Status des Patienten | Haupt-Dashboard | |||
| RPA-Plan prüfen und herunterladen | Haupt-Dashboard | ||||
| 4 | Importieren Sie den Plan in das TPS des Benutzers, berechnen Sie die Dosis neu und nehmen Sie bei Bedarf Änderungen vor | Lokales TPS | |||
| 5, 6 | Laden Sie den endgültigen Plan auf die RPA-Website hoch | Dashboard für den Planvergleich | |||
| Überprüfen Sie den automatischen Vergleich des endgültigen Plans und des RPA-Plans | Dashboard für den Planvergleich | ||||
| – | Der Plan geht in den klinischen Routineablauf des Anwenders ein, einschließlich der regelmäßigen Qualitätssicherung | Eigene Software des Benutzers | |||
Tabelle 1: Übersicht über die Aufgaben, die bei der Erstellung eines RPA-Plans mit dem 1-Schritt-Workflow anfallen. Lokales TPS: Behandlungsplanungssystem des Benutzers.
Dieses Manuskript beschreibt diesen einstufigen Workflow für die RPA und präsentiert einige Beispielergebnisse des Behandlungsplanungsprozesses. Derzeit verwenden die folgenden Planungsansätze diesen einstufigen Arbeitsablauf: i) Vier-Felder-Box-Behandlungspläne für Gebärmutterhalskrebspatientinnen (knöcherne Landmarken-basierte Öffnungen); ii) Vierfeld-Box-Behandlungspläne für Patientinnen mit Gebärmutterhalskrebs (weichteilbasierte Feldöffnungen); iii) tangentiale und supraklavikuläre Behandlungspläne für Brustwandpatienten; iv) Behandlungspläne für das gesamte Gehirn.
Protocol
Representative Results
Discussion
Dieses Protokoll beschreibt die Schritte zur Erstellung automatisierter Behandlungspläne mithilfe der RPA. Die wichtigsten Schritte sind (1) CT-Upload und -Genehmigung, (2) Ausfüllen und Genehmigen von Serviceanfragen, (3) Herunterladen und Importieren des Plans in das TPS des Benutzers und Neuberechnung der Dosis und Planbearbeitung sowie (4) Hochladen des endgültig bearbeiteten Plans zum Vergleich mit dem RPA-Plan. Die Reihenfolge der CT-Genehmigung und der Service-Request-Genehmigung ist austauschbar. Einige Pläne, insbesondere volumenmodulierte Arc-Therapiepläne für Kopf-Hals- und Gebärmutterhalskrebs, werden in einem zweistufigen Prozess erstellt, in dem zusätzliche Benutzerinteraktionen und die Konturen und Pläne separat generiert werden. Insgesamt sind die Prozesse jedoch ähnlich, und wir gehen davon aus, dass diese fortschrittlichen Ansätze der Behandlungsplanung in Zukunft auf einen einstufigen Prozess umgestellt werden können. Die allgemeine klinische Akzeptanz, die von diesen Werkzeugen und von Werkzeugen, die sich in der Entwicklung für zukünftige Versionen befinden, erwartet werden kann, finden Sie in unserer veröffentlichten Arbeit 10,12,14,15,16,17,18,19,20,21,22.
Diese Werkzeuge weisen mehrere Einschränkungen auf, wie in unserer früheren Arbeit beschrieben, in der das Risiko beim Einsatz des Bestrahlungsplanungsassistenten in Strahlentherapiekliniken untersuchtwurde 9,23. Obwohl die Benutzeroberfläche so gestaltet wurde, dass das Risiko einer unangemessenen Dateneingabe minimiert wird, wie z. B. CT-Bilder mit unzureichendem Sichtfeld oder Fehler bei der manuellen Dateneingabe, besteht dennoch ein Fehlerpotenzial. Insbesondere menschliches Versagen, Automatisierungsverzerrung (übermäßiges Vertrauen in die Ergebnisse) und Softwarefehler sind von Belang9. Eine sorgfältige Überprüfung und ggf. Bearbeitung der automatisch generierten Konturen und Pläne ist für die sichere Nutzung des Bestrahlungsplanungsassistenten unerlässlich. Im Allgemeinen sollten diese Überprüfungen dem gleichen Verfahren folgen wie bei der Überprüfung klinischer Pläne durch Physiker und Radioonkologen, obwohl dies durch die Verwendung von Checklisten unterstützt werden kann, die speziell entwickelt wurden, um die manuelle Überprüfung automatisch erstellter Behandlungspläne zu ergänzen24.
Es gibt Situationen, in denen die RPA nicht in der Lage ist, einen Plan zu erstellen und dem Benutzer einen Fehler meldet. In fast allen Fällen wird dies dadurch verursacht, dass die RPA auf unerwartete Daten stößt, die sie nicht interpretieren kann, wie z. B. ein unzureichendes Sichtfeld oder eine unzureichende Patientenpositionierung (z. B. wenn ein CT-Bild in Rückenlage aufgenommen wurde, der Patient jedoch in Bauchlage). Der Benutzer kann das Problem möglicherweise anhand des Ortes identifizieren, an dem der Fehler gemeldet wird. In den meisten Fällen können diese Situationen nur durch manuelles Konturieren oder Planen behoben werden. Das RPA-Team kann möglicherweise auch Protokolldateien überprüfen, um das Problem zu identifizieren.
Das RPA wurde speziell entworfen und entwickelt, um Kliniken mit begrenzten Ressourcen, insbesondere in Ländern mit niedrigem und mittlerem Einkommen, hochwertige Autokonturierungs- und Autoplanungstools zur Verfügung zu stellen. Wir arbeiten derzeit an den regulatorischen, rechtlichen und administrativen Prozessen, die dazu führen werden, dass die RPA klinisch eingesetzt wird. Sobald dies geschieht, gehen wir davon aus, dass wir die Nutzung sorgfältig überwachen und Änderungen am Workflow oder an den Benutzeroberflächen vornehmen, um auf unvorhergesehene Risiken oder anderes Benutzerfeedback zu reagieren. Ziel ist es, Tools zur Unterstützung von Strahlentherapiediensten bereitzustellen, so dass lokale klinische Teams ihre Bemühungen skalieren und den Zugang zu qualitativ hochwertigen, konsistenten Strahlentherapieplänen verbessern können. Wir hoffen, dass dies zu verbesserten Patientenergebnissen sowie zu kürzeren Wartezeiten führen wird. Obwohl sich das derzeitige Portfolio auf Krebserkrankungen des Kopfes und Halses, der Brust und des Gebärmutterhalses sowie auf die Bestrahlung des gesamten Gehirns bei Hirnmetastasen beschränkt, arbeiten wir an zusätzlichen Behandlungen, die in zukünftigen Versionen17, 18, 19 enthalten sein werden.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Diese Arbeit wurde vom National Cancer Institute und dem Wellcome Trust finanziert, mit zusätzlicher Unterstützung von Varian Medical Systems. Unser aktuelles System verwendet Eclipse für die Behandlungsplanung. Wir möchten uns auch bei Ann Sutton von Editing Services, Research Medical Library, UT MD Anderson Cancer Center bedanken. Zusätzlich zu den institutionellen Mitteln für die RPA-Entwicklung erhalten unsere Forschungsteams Mittel vom Cancer Prevention and Research Institute of Texas (CPRIT) und dem Fund for Innovation in Cancer Informatics, The University of Texas MD Anderson Cancer Center.
References
- Ferlay, J., et al. Cancer incidence and mortality worldwide: Sources, methods and major patterns in GLOBOCAN 2012. International Journal of Cancer. 136 (5), E359-E386 (2015).
- Elmore, S. N. C., et al. Global palliative radiotherapy: a framework to improve access in resource-constrained settings. Annals of Palliative Medicine. 8 (3), 274-284 (2019).
- Atun, R., et al. Expanding global access to radiotherapy. The Lancet. Oncology. 16 (10), 1153-1186 (2015).
- Yap, M. L., Zubizarreta, E., Bray, F., Ferlay, J., Barton, M. Global access to radiotherapy services: have we made progress during the past decade. Journal of Global Oncology. 2 (4), 207-215 (2016).
- Elmore, S. N. C., et al. C. al. Radiotherapy resources in Africa: an International Atomic Energy Agency update and analysis of projected needs. The Lancet. Oncology. 22 (9), e391-e399 (2021).
- Datta, N. R., Samiei, M., Bodis, S. Radiation therapy infrastructure and human resources in low- and middle-income countries: present status and projections for 2020. International Journal of Radiation Oncology, Biology, Physics. 89 (3), 448-457 (2014).
- Ward, Z. J., Scott, A. M., Hricak, H., Atun, R. Global costs, health benefits, and economic benefits of scaling up treatment and imaging modalities for survival of 11 cancers: a simulation-based analysis. The Lancet. Oncology. 22 (3), 341-350 (2021).
- Court, L. E., et al. Radiation Planning Assistant – a streamlined, fully automated radiotherapy treatment planning system. Journal of Visualized Experiments. (134), e57411 (2018).
- Nealon, K. A., et al. Using failure mode and effects analysis to evaluate risk in the clinical adoption of automated contouring and treatment planning tools. Practical Radiation Oncology. 12 (4), e344-e353 (2022).
- Kisling, K., et al. Automated treatment planning of postmastectomy radiotherapy. Medical Physics. 46 (9), 3767-3775 (2019).
- Xiao, Y., et al. Customizable landmark-based field aperture design for automated whole-brain radiotherapy treatment planning. Journal of Applied Clinical Medical Physics. 24 (3), e13839 (2022).
- Kisling, K., et al. Fully automatic treatment planning for external-beam radiation therapy of locally advanced cervical cancer: a tool for low-resource clinics. Journal of Global Oncology. 5, 1-9 (2019).
- Rhee, D. J., et al. Clinical acceptability of fully automated external beam radiotherapy for cervical cancer with three different beam delivery techniques. Medical Physics. 49 (9), 5742-5751 (2022).
- Rhee, D. J., et al. Automated radiation treatment planning for cervical cancer. Seminars in Radiation Oncology. 30 (4), 340-347 (2020).
- Rhee, D. J., et al. Automatic contouring system for cervical cancer using convolutional neural networks. Medical Physics. 47 (11), 5648-5658 (2020).
- Xiao, Y., et al. Automated WBRT treatment planning via deep learning auto-contouring and customizable landmark-based field aperture design. arXiv. , (2022).
- Hernandez, S., et al. Automating the treatment planning process for 3D-conformal pediatric craniospinal irradiation therapy. Pediatric Blood & Cancer. 70 (3), e30164 (2023).
- Huang, K., et al. Automation of radiation treatment planning for rectal cancer. Journal of Applied Clinical Medical Physics. 23 (9), e13712 (2022).
- Netherton, T. J., et al. An automated treatment planning framework for spinal radiation therapy and vertebral-level second check. International Journal of Radiation Oncology, Biology, Physics. 114 (3), 516-528 (2022).
- Olanrewaju, A., et al. Clinical acceptability of automated radiation treatment planning for head and neck cancer using the Radiation Planning Assistant. Practical Radiation Oncology. 11 (3), 177-184 (2021).
- Rhee, D. J., et al. Automatic contouring QA method using a deep learning-based autocontouring system. Journal of Applied Clinical Medical Physics. 23 (8), e13647 (2022).
- Rhee, D. J., et al. Automatic detection of contouring errors using convolutional neural networks. Medical Physics. 46 (11), 5086-5097 (2019).
- Kisling, K., et al. A risk assessment of automated treatment planning and recommendations for clinical deployment. Medical Physics. 46 (6), 2567-2574 (2019).
- Nealon, K. A., Court, L. E., Douglas, R. J., Zhang, L., Han, E. Y. Development and validation of a checklist for use with automatically generated radiotherapy plans. Journal of Applied Clinical Medical Physics. 23 (9), e13694 (2022).

