Kitle Spektrometrik Liyofilize Toz Protein Yapısı ve Etkileşimler Eğitim Yaklaşımları
Summary
Here, we present detailed protocols for solid-state amide hydrogen/deuterium exchange mass spectrometry (ssHDX-MS) and solid-state photolytic labeling mass spectrometry (ssPL-MS) for proteins in solid powders. The methods provide high-resolution information on protein conformation and interactions in the amorphous solid-state, which may be useful in formulation design.
Abstract
Kütle spektrometrik analizi ve ardından amid hidrojen / döteryum değişimi (ssHDX-MS) ve yan zincir fotolitik etiketleme (Sspl-MS), protein terapötiklerinin liyofilize formülasyonlan karakterize edilmesi için yararlı olabilir. Uygun proteolitik sindirme ile, ardından etiketleme protein yapısı ve etkileşimleri peptid seviyesi çözünürlüğü ile eşlenmesi sağlar. Protein yana yapı elemanları, ana zincirleri ve amino asitler, amino asit rezidüleri atomu spesifik etiketleme proteininin yapısı ve biçimi görmemizi sağlar yan zincirleri kimyasal bağların bir ağ tarafından stabilize edilir. Liyofilize katıların (örneğin, FTIR), ssHDX-MS-MS ve Sspl nicel ve site özgü bilgi proteinleri incelemek için kullanılan rutin yöntemlerin aksine. döteryum Kuruluş ve kinetik parametrelerin ölçüde hızlı ve yavaş amid havuzları alışverişi ile ilgili olabilir (N hızlı, N yavaş) ve doğrudan C yansıtırLiyofilize formülasyonlar protein katlanması ve yapısı ree. Kararlı fotolitik etiketleme arka değişimi, ssHDX-MS üzerinde bir avantaj uğramaz. Burada, trehaloz ya da sorbitol ya içeren liyofilize formülasyonlarda bir model protein olarak miyoglobin (Mb) kullanılarak ssHDX-MS ve Sspl-MS hem de ayrıntılı protokolleri sağlar.
Introduction
Protein ilaçlar biofarmasötik endüstrisinin en hızlı büyüyen sektör olan ve hormonal bozukluklar, kanser ve otoimmün hastalıklar 1 olmak üzere daha önce inatçı hastalıklar için umut verici yeni tedaviler sunuyoruz. 2012 yılında, küresel Biyoterapötikler pazarı 138.000.000.000 $ ulaştı ve yıl 179.000.000.000 $ ulaşması bekleniyor 2018 2. Proteinler büyük ve geleneksel küçük molekül ilaçların daha kırılgan ve böylece bozulması 3 birçok türleri daha hassastır. (Örneğin, dondurularak kurutulmuş) bir katı madde tozlar liyofilize yeterli raf ömrü ve stabilitesini sağlamak için, protein ilaçlar genellikle formüle edilir. Bununla birlikte, bir protein yine doğal yapısı Liyofilizasyon işlemi esnasında 4,5 'korunmaz, özellikle katı halde bozulma tabi olabilir. Bu yapı muhafaza edilmiştir sağlanması sufficien ile katı halde protein yapısını sondalamak analitik yöntem bulunmaktadır geçerli olabilmesit çözünürlüğü.
NMR spektroskopisi 6 ve X-ışını kristalografisi 7 çözüm ve kristallerin 8 protein yapısını değerlendirmek için yaygın olarak kullanılan yüksek çözünürlüklü yöntemleri vardır. Için yardımcı maddeler ve kullanılan işleme yöntemlerinin doğası, iyofilleştirilmiş protein, formülasyonlar, genellikle amorf yerine 9 kristaldir. homojenlik ve mikroskopik seviyede olmaması şekilsiz katılar proteinler için, yukarıda belirtilen teknikler kullanışsız hale getirir. Fourier kızılötesi spektroskopi (FTIR) 10 dönüşümü, Raman spektroskopisi 11 ve yakın kızılötesi spektroskopi (NIR) 12 düzenli yerli çözüm devlet yapısının buna liyofilize tozlar protein ikincil yapısını karşılaştırmak için biofarmasötik endüstrisi tarafından kullanılmaktadır. Ancak, bu yöntemlerin düşük çözünürlüklü ve sadece ikincil yapı küresel değişimler hakkında bilgi verebilir. FTIR kullanılarak katı-hal yapısal karakterizasyonuUzun vadeli depolama stabilitesi zayıf 13,14 veya kötü 15 korelasyon ya göstermiştir. Bu sınırlamalar uygun yüksek çözünürlüklü yöntemleri solid-state protein yapısal tedirginlikler tanımlamak için ihtiyaç vurgulayın.
Proteoliz ve kütle spektrometrik analiziyle birlikte kimyasal etiketleme, sulu çözelti içinde, protein yapısı ve molekül etkileşimleri izlenmesi için güçlü bir yaklaşım haline gelmiştir. İlaç gelişmede, HDX-MS protein ilaçların 19 uyum post-translasyonel modifikasyonlar etkilerini izlemek için, reseptör-ilaç etkileşimleri 18 harita ve karşılaştırmak için, antijen-antikor etkileşimleri 16,17 epitop haritalama için kullanılır olmuştur biyobenzerlerin 20 gelişmekte olan partiden partiye varyasyonu. Benzer şekilde, foto-aktifleştirilebilen ligandlar ilaç hedeflerini tanımlamak ve bağlanma afinitesini ve ilaç-reseptör etkileşimleri 21,22 özgüllüğünü belirlemek için kullanılmıştır. Extend liyofilize formülasyonlar bu yöntemlerin uygulanması, bizim grup geliştirdi katı-hal hidrojen döteryum değişim kütle spektrometresi (ssHDX-MS) ve katı-hal fotolitik etiketleme kütle spektrometresi (Sspl-MS) liyofilize örneklerinde protein konformasyonlar ve yardımcı madde etkileşimleri çalışmak için Yüksek çözünürlükte.
SsHDX-MS ve Sspl-MS Her iki protein, liyofilize katı madde ideal tepkime koşulları altında işaretlenir, ve numuneler daha sonra tekrar oluşturulmuş ve veya proteolitik sindirim olmayan kütle spektrometresi ile analiz edilir. Sspl-MS yan zincirlerinin çevre bilgileri (Şekil 1) içerir ise ssHDX-MS, döteryum buhar ana zincir maruz hakkında bilgi sağlar. iki yöntem böylece katı halde protein yapısındaki hakkında tamamlayıcı bilgiler sağlayabilir. Burada, biz Mb, (Şekil 2) ssHDX-MS ve Sspl-MS kullanılarak liyofilize katı proteinleri okuyan kullanımı için genel bir protokol sağlamakbir model, bir protein. Iki farklı yardımcı maddeler ile formülasyonlar farkını ayırt etme iki yöntemden kabiliyetini gösterir.
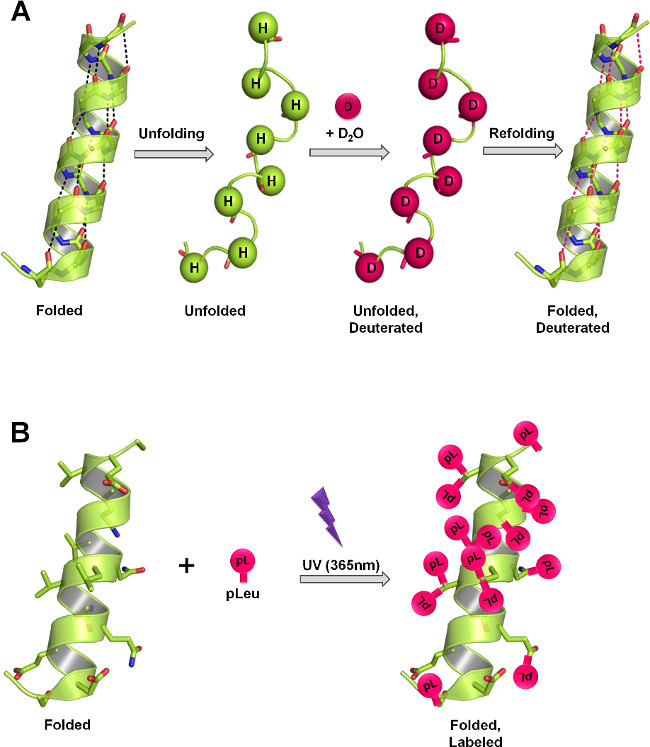
Şekil 1:., Farklı etiket mekanizmalarla liyofilize katılar ssHDX ve Sspl ölçer protein yapı (A) 'HDX olarak, omurga amid, bir protein yapısı ve fonksiyonu ve D 2 O erişim olarak döteryum ile değişimi hidrojenlerin. Katı halde, hızı ve döteryum değişimi derecesi D 2 O sorpsiyon protein hareketlilik (yayılan ve olayları tekrar katlama) ve katı bir matris içinde mevcut katkı maddelerinin doğası düzeyine bağlıdır. PLeu bölgesinin diazirine işlevsel grup ara ürün, bir reaktif karben oluşumunu başlatır ve bir XH bağı (X, herhangi bir atomu olması durumunda) veya reklama spesifik olmayan sokulur mil PL (B), 365 UV ışınlamayakın çevresinde bir C = C bağı boyunca pro-. Katı halde ise bu oran ve etiketleme ölçüde lokal işaretleme maddesi konsantrasyonu, uygulama süresi, protein yapısı ve katı bir matris içinde mevcut katkı maddelerinin doğasına bağlıdır. Paneller A ve B proteininin, sırasıyla omurga ve yan zincirler üzerinde oluşabilecek maksimum teorik etiketleme göstermektedir.
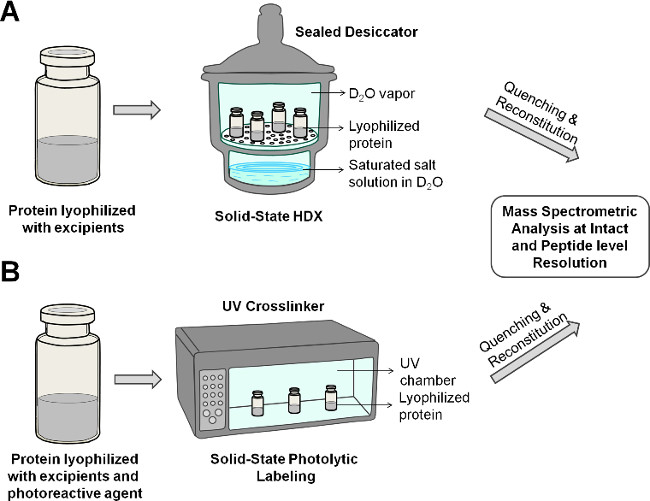
Şekil 2: şematik gösterimi katı hal HDX-MS (A) ve liyofilize edilmiş bir formülasyona protein PL-MS (B) gerçekleştirildi.
Protocol
Representative Results
Discussion
Çeşitli çalışmalar liyofilize örneklerinde yerel çevre proteini bozulmasını 5,29,30 etkilediğini düşündürmektedir. Ancak, katı halde protein yapısı ve istikrar arasında doğrudan bir ilişki kurarak, yüksek çözünürlüklü analitik yöntemlerin eksikliği mümkün olmamıştır. liyofilize tozlar böyle HDX ve PL gibi mevcut yüksek çözünürlüklü yöntemlerinin uygulama çözümü protokolleri ve dikkatli veri yorumlama değişiklik gerektirir. HDX-MS ve PL-MS arda katı halde protein konformasyonlar izlemek için kabul edilmiştir. Sonuçlar Burada sunulan ve başka 27,28,31-33 katı ortamda yüksek çözünürlüklü protein yapısını izlemek için bu yöntemlerin yeteneğini göstermiştir. Veri analizinde kritik adımlar çözelti 34-36 etiketleme farklılık olmasa da, deney düzeneği ve veri yorumlama sırasında önemli hususlar katı-hal kemi için gereklidircal etiketleme.
Etiketleme reaktif seçimi boyutu ve etiketleme mekanizmasına dayalı olmalıdır. döteryum küçük boyutlu pLeu görece büyük boyutlu yan zincirlere etiketleme sınırlar ise peptid omurgası, kolaylıkla araştırılabilir sağlar. Bu etiketleme sadece matris omurgada hem de yan zincir maruz bağlıdır, böylece ssHDX ve Sspl ikisi de herhangi bir amino asidi için tercih gösterir. Etkin bir solid-state protein konformasyonlar prob, etiketleme sürecini etkileyen dış faktörler dikkatle kontrol edilmelidir. toplam miktarı ve liyofilize katı olarak işaretleme maddesi alansal dağılımı, sulu çözeltiler farklıdır.
SsHDX olarak, katı bir matris içinde D 2 O miktarı açılma protein oranı (veya kısmi açılması), yeniden katlama ve döteryum değişimi etkileyebilir. Bu protein, örneği, normal olarak, D 2 O geniş bir hacmi ile seyreltilmiş halde bir çözelti HDX, durum böyle değildirSsHDX oranı hidrasyon etkilerinin dikkatli bir şekilde tarama doğru RH koşullarının seçimi bilgilendirebilir. Nem sorpsiyon hızını kontrol ve higroskopik yardımcı maddeler (örneğin, sakaroz ve trehaloz) ihtiva eden formülasyonlar tozun çökmesini önlemek için, ssHDX soğutulmuş koşullar altında gerçekleştirilebilir (2-8 ° C). Beklendiği gibi hidrasyon etkileri üzerine önceki çalışmamızda, nem içeriğinin artması ile döviz kurunu ve kapsamını artış gösterdi. Çalışmalarımız, 5 ° C sıcaklıkta% 43 oranında bir ara RH 'nın büyük bir bölümünde, makul bir süre 24 formülasyonlan ayırt ideal olduğu kanıtlanmıştır. bir plato elde edilene kadar reaksiyon genellikle gerçekleştirilir. Bu katı madde halinde nem emiş ve difüzyon HDX hızını kontrol yok olmasını sağlar. ≤2 ml önceden liyofilizasyon hacmi küçük katı numune boyutları kullanımı da, D 2 O buharı emilmesi, erken dönemde değişimi esas itibarıyla tamamlandığında sağlamaya yardımcı olur. Olsa ssHDX-MS içerirKatı-devlet proteinin yapısındaki kantitatif bilgiler, verilerin yorumlanması tamamen yalnız ssHDX çalışmaya dayanarak olamaz belirli koşullar vardır. Bu azalma döteryum alımı nedeniyle, protein yapısının en yüksek tutma ve numune içinde mevcut bulunan protein unsurlarının önemli miktarda olabilir (kontrol ile karşılaştırıldığında) bir numunede gözlemlenen mümkündür. Böyle bir durumda, ssHDX verilerin yorumlanması diğer tamamlayıcı yöntemler sonuçları gerektirir. Döteryumlu kütle spektrumları zirve genişleme birkaç Mb formülasyonlar 27,28 gözlenmiştir. Bu D 2 O konsantrasyonu numune kısmen katlanmamış protein nüfus, mekansal heterojenlik varlığı veya mekansal geçişlerini gibi çeşitli faktörlere bağlı olabilir. Ancak, bu faktörler ssHDX-MS ayırt ve daha fazla araştırma ihtiyacı değildi.
Sspl-MS nispeten yeni olduğu gibi diğer yöntemlerle, sürekli öğrenme ab göreuygulamaları ve sınırlamaları dışında gerekmektedir. Sspl olarak, foto-çapraz-bağlayıcı protein ile liyofilize edilir. nem eksikliği katı matris içindeki bileşenlerin hareketliliğini kısıtlar ve ssHDX nem emilimi ile oluşabilecek kısmi yapısal gevşeme Sspl bir fenomen değildir. Bu foto-çapraz bağlayıcı hemen yakınında için Sspl olarak etiketleme sınırlar. Bununla birlikte, HDX-MS, tortu seviyesi yapısal bilgiler elde edilebilir kovalent olarak işaretlenmiş proteinin, MS / MS analizi farklı. Sspl etiketleme kovalent ve geri dönüşü olmayan bir olduğu için, geri değişimi meydana gelmez ve numuneler hazırlanmış ve etiketin kaybı göz önüne alınmadan analiz edilebilir. Işaretleme maddesi difüzyonunu kolaylaştırmak ve katı matris içinde etiketleme verimliliğini artırmak için, Sspl artan% RH ile gerçekleştirilebilir. pLeu alınmasından da fotoreaktif ajanın artan konsantrasyonu ile geliştirilebilir. istenildiği gibi pLeu proteinin mol oran isteğe göre ayarlanabilir. Genel olarak, pro pLeu bir 100x mol fazlasıproteindir yeterli etiketleme sağlayacaktır. Bununla birlikte, yüksek pLeu konsantrasyonu katı matris protein üçüncül yapısının kaybına neden olabilir. Bu nedenle, etiket kinetik ve formülasyon bileşimine ek olarak, pLeu konsantrasyonu seçimi aynı zamanda, protein, yapısal bütünlüğünü muhafaza dayanmalıdır. PLeu seçilmeden XH etiketler gibi grup, bu mümkün (X = C, N, O nerede) benzer etiketleme siteleri ile yardımcı maddeler büyük ölçüde protein etiketleme düzeyini etkileyebilir. Protein etiketleme için pLeu mevcudiyetindeki eksipiyan parazit henüz karakterize hale getirilecektir. Bu diazirine aktivasyonu üretilen karben tortu özgü olmadığı bilinmektedir, ancak bir çalışma Asp ve Glu 36 doğru önyargı bildirir. Bu tortu, spesifik etkileşimleri hakkında bilgi edinmek için iyi olsa da, peptid seviyesi bilgiler de yararlıdır ve katı halde, yüksek matris maruz bölgeleri bloke etme yardımcı maddeleri tasarlamak için de kullanılabilir. Sspl-MS Ancak, detaylı niteliksel bilgi sağlarnicel veriler elde edilmesi gerekiyor ve sağlam ölçütler liyofilize sistemleri çeşitli genelinde formülasyon farklılıklarını analiz etmek geliştirilmesi gerekmektedir.
MS / MS analizi ile birlikte, bir tortu, spesifik etiketin kullanımı, ayrıca aşağıdaki amino asit seviyesine çözünürlüğünü artırabilir. Örneğin 2,3-bütandion olarak etiketleme ayıraçları, Arg, Cys Lys ve N -alkylmaleimide türevleri, N-hidroksisukinimid türevleri tam da liyofilize toz moleküler etkileşimlerini eşleştirmek üzere kullanılabilir etiket. Bununla birlikte, bu reaktifler pH değerine bağımlı ve reaksiyon katı-halde fotolitik etiketleme gibi iyi kontrol olmayabilir. Bir alternatif yaklaşım, oksotrofik hücre çizgileri, mevkiye yönelik mutagenez ya da yan zincir türetme kullanımı ile protein dizisi olarak foto-çapraz bağlayıcı dahil etmektir.
Daha önceki ssHDX-MS, Sspl-MS çalışmalar proteinin etiketlenmesi eksipiyan doğasına ve miktarına bağlı olduğunu göstermiştir24,27,28,31-33,37,38 kullanılır. Mb düşük molekül ağırlığı 32 şeker ile-liyofilize ko daha Mb ssHDX-MS guanidin hidroklorür (Gdn.HCl) ile birlikte liyofilize eş daha döteryum alımını göstermektedir. Gdn.HCl sakaroz 33 ile Mb'den fotolitik etiketleme karşı daha fazla koruma gösterdi ayrı bir Sspl-MS çalışmasında, Mb-liyofilize eş. Bundan başka, ssHDX-MS sayısal ölçümler yüksek uzun süreli depolama sırasında 28 protein stabilitesi ile ilişkilendirilmiştir. Bu çalışmalar, protein ssHDX veya Sspl liyofilize toz bulunan proteininin yapısal tutma derecesini yansıtır düşündürmektedir. Biz liyofilize tozlar ikincil yapının tutma yan zinciri pLeu ile etiketleme ve döteryum değişiminden amid hidrojen korunması için elverişli bir ortam oluşturduğuna inanıyoruz. Bununla birlikte, bu yöntem ile ilgili bilgi içeriğinin detaylı karşılaştırma gelecekte yapılması gerekmektedir. SsHDX-MS ve Sspl-MS programı kuran rağmenBir formülasyon tarama aracı olarak birçok proteinler uygulanabilir sonuçta gerektirir, son çalışmaların sonuçları daha geniş benimsenmesini desteklemektedir. Daha da geliştirilmesi, bu yöntem, ilaç endüstrisinin katı-hal protein formülasyonlan karakterize etmek için yaygın olarak faydalı olması beklenmektedir.
Declarações
The authors have nothing to disclose.
Acknowledgements
The authors gratefully acknowledge financial support from NIH R01 GM085293 (PI: E. M. Topp) and from the College of Pharmacy at Purdue University.
Materials
| Name of Material/ Equipment | Company | Catalog Number | Comments/Description |
| Equine myoglobin | Sigma-Aldrich | M0630-5G | |
| D-(+)-Trehalose dihydrate | Sigma Aldrich | #T9531 | |
| D-Sorbitol | Sigma Aldrich | #240850 | |
| L-Photo-leucine | Thermo Scientific | #22610 | |
| Potassium phosphate monobasic | Sigma-Aldrich | #P0662 | |
| Potassium phosphate dibasic | Sigma-Aldrich | #P3786 | |
| Deuterium Oxide | Cambridge Isotope Laboratories | #DLM-4-PK | Alternate (Cat. No.: 151882, Sigma-Aldrich) |
| Immobilized pepsin | Applied Biosystems | #2-3132-00 | |
| Trypsin | Promega | #V511A | Chymotrypsin (Cat. No.: #V1062, Promega) can be additionally used |
| Water, Optima LC/MS grade | Fisher Chemical | #7732-18-5 | |
| Acetonitrile | Sigma-Aldrich | #34998 | |
| Formic acid | Thermo Scientific | #28905 | |
| ESI-TOF Calibrant | Agilent Technologies | #G1969-85000 | Highly flammable liquid |
| Protein microtrap | Michrom Bioresources | TR1/25108/03 | |
| Peptide microtrap | Michrom Bioresources | TR1/25109/02 | |
| Analytical column | Agilent Technologies | Zorbax 300SB-C18 | |
| Freeze dryer | VirTis AdVantage Plus | ||
| Stratalinker equipped with five 365 nm lamps | Stratagene Corp. | Stratalinker 2400 | |
| HPLC | Agilent Technologies | 1200 series LC | Refrigerated LC system for HDX-MS |
| ESI-qTOF MS | Agilent Technologies | 6520 qTOF | |
| HDExaminer (HDX-MS data analysis software) | Sierra Analytics | http://www.massspec.com/HDExaminer.html |
Referências
- Lawrence, S. Billion dollar babies–biotech drugs as blockbusters. Nat. Biotechnol. 25 (4), 380-382 (2007).
- . . Global Markets and Manufacturing Technologies for Protein Drugs. , BIO021D (2013).
- Lai, M. C., Topp, E. M. Solid-state chemical stability of proteins and peptides. J. Pharm. Sci. 88 (5), 489-500 (1999).
- Carpenter, J. F., Pikal, M. J., Chang, B. S., Randolph, T. W. Rational design of stable lyophilized protein formulations: some practical advice. Pharm. Res. 14 (8), 969-975 (1997).
- Carpenter, J. F., Chang, B. S., Garzon-Rodriguez, W., Randolph, T. W. Rational design of stable lyophilized protein formulations: theory and practice. Pharm. Biotechnol. 13, 109-133 (2002).
- Wüthrich, K. Protein structure determination in solution by NMR spectroscopy. J. Biol. Chem. 265 (36), 22059-22062 (1990).
- Ilari, A., Savino, C. Protein structure determination by x-ray crystallography. Methods. Mol. Biol. 452, 63-87 (2008).
- Brunger, A. T. X-ray crystallography and NMR reveal complementary views of structure and dynamics. Nat. Struct. Biol. 4, 862-865 (1997).
- Yu, L. Amorphous pharmaceutical solids: preparation, characterization and stabilization. Adv Drug. Deliv. Rev. 48 (1), 27-42 (2001).
- Manning, M. C. Use of infrared spectroscopy to monitor protein structure and stability. Expert. Rev. Proteomics. 2 (5), 731-743 (2005).
- Grohganz, H., Gildemyn, D., Skibsted, E., Flink, J. M., Rantanen, J. Rapid solid-state analysis of freeze-dried protein formulations using NIR and Raman spectroscopies. J. Pharm. Sci. 100 (7), 2871-2875 (2011).
- Bai, S., Nayar, R., Carpenter, J. F., Manning, M. C. Noninvasive determination of protein conformation in the solid state using near infrared (NIR) spectroscopy. J. Pharm. Sci. 94 (9), 2030-2038 (2005).
- Pikal, M. J., et al. Solid state chemistry of proteins: II. The correlation of storage stability of freeze-dried human growth hormone (hGH) with structure and dynamics in the glassy solid. J. Pharm. Sci. 97 (12), 5106-5121 (2008).
- Wang, B., Tchessalov, S., Cicerone, M. T., Warne, N. W., Pikal, M. J. Impact of sucrose level on storage stability of proteins in freeze-dried solids: II. Correlation of aggregation rate with protein structure and molecular mobility. J. Pharm. Sci. 98 (9), 3145-3166 (2009).
- Schule, S., Friess, W., Bechtold-Peters, K., Garidel, P. Conformational analysis of protein secondary structure during spray-drying of antibody/mannitol formulations. Eur. J. Pharm. Biopharm. 65 (1), 1-9 (2007).
- Baerga-Ortiz, A., Hughes, C. A., Mandell, J. G., Komives, E. A. Epitope mapping of a monoclonal antibody against human thrombin by H/D-exchange mass spectrometry reveals selection of a diverse sequence in a highly conserved protein. Protein. Sci. 11 (6), 1300-1308 (2002).
- Coales, S. J., Tuske, S. J., Tomasso, J. C., Hamuro, Y. Epitope mapping by amide hydrogen/deuterium exchange coupled with immobilization of antibody, on-line proteolysis, liquid chromatography and mass spectrometry. Rapid. Commun. Mass. Spectrom. 23 (5), 639-647 (2009).
- Pacholarz, K. J., Garlish, R. A., Taylor, R. J., Barran, P. E. Mass spectrometry based tools to investigate protein-ligand interactions for drug discovery. Chem. Soc. Rev. 41 (11), 4335-4355 (2012).
- Houde, D., Peng, Y., Berkowitz, S. A., Engen, J. R. Post-translational modifications differentially affect IgG1 conformation and receptor binding. Mol. Cell. Proteomics. 9 (8), 1716-1728 (2010).
- Houde, D., Berkowitz, S. A., Engen, J. R. The utility of hydrogen/deuterium exchange mass spectrometry in biopharmaceutical comparability studies. J. Pharm. Sci. 100 (6), 2071-2086 (2011).
- Dorman, G., Prestwich, G. D. Using photolabile ligands in drug discovery and development. Trends. Biotechnol. 18 (2), 64-77 (2000).
- Robinette, D., Neamati, N., Tomer, K. B., Borchers, C. H. Photoaffinity labeling combined with mass spectrometric approaches as a tool for structural proteomics. Expert. Rev. Proteomics. 3 (4), 399-408 (2006).
- Greenspan, L. Humidity fixed points of binary saturated aqueous solutions. Journal of Research of the National Bureau of Standards. 81A (1), 8 (1977).
- Sophocleous, A. M., Zhang, J., Topp, E. M. Localized hydration in lyophilized myoglobin by hydrogen-deuterium exchange mass spectrometry. 1. Exchange mapping. Mol. Pharm. 9 (4), 718-726 (2012).
- Keppel, T. R., Jacques, M. E., Young, R. W., Ratzlaff, K. L., Weis, D. D. An efficient and inexpensive refrigerated LC system for H/D exchange mass spectrometry. J. Am. Soc. Mass. Spectrom. 22 (8), 1472-1476 (2011).
- Gasteiger, E., et al. ExPASy: The proteomics server for in-depth protein knowledge and analysis. Nucleic. Acids. Res. 31 (13), 3784-3788 (2003).
- Sophocleous, A. M., Topp, E. M. Localized hydration in lyophilized myoglobin by hydrogen-deuterium exchange mass spectrometry. 2. Exchange kinetics. Mol. Pharm. 9 (4), 727-733 (2012).
- Moorthy, B. S., Schultz, S. G., Kim, S. G., Topp, E. M. Predicting Protein Aggregation during Storage in Lyophilized Solids Using Solid State Amide Hydrogen/Deuterium Exchange with Mass Spectrometric Analysis (ssHDX-MS). Mol. Pharm. 11 (6), 1869-1879 (2014).
- Wang, W. Lyophilization and development of solid protein pharmaceuticals. Int. J. Pharm. 203 (1-2), 1-60 (2000).
- Sarciaux, J. M., Mansour, S., Hageman, M. J., Nail, S. L. Effects of buffer composition and processing conditions on aggregation of bovine IgG during freeze-drying. J. Pharm. Sci. 88 (12), 1354-1361 (1999).
- Li, Y., Williams, T. D., Schowen, R. L., Topp, E. M. Characterizing protein structure in amorphous solids using hydrogen/deuterium exchange with mass spectrometry. Anal. Biochem. 366 (1), 18-28 (2007).
- Sinha, S., Li, Y., Williams, T. D., Topp, E. M. Protein conformation in amorphous solids by FTIR and by hydrogen/deuterium exchange with mass spectrometry. Biophys. J. 95 (12), 5951-5961 (2008).
- Iyer, L. K., Moorthy, B. S., Topp, E. M. Photolytic labeling to probe molecular interactions in lyophilized powders. Mol. Pharm. 10 (12), 4629-4639 (2013).
- Hentze, N., Mayer, M. P. Analyzing protein dynamics using hydrogen exchange mass spectrometry. J. Vis. Exp. (81), e50839 (2013).
- Kaltashov, I. A., Bobst, C. E., Abzalimov, R. R. H/D exchange and mass spectrometry in the studies of protein conformation and dynamics: is there a need for a top-down approach. Anal. Chem. 81 (19), 7892-7899 (2009).
- Jumper, C. C., Schriemer, D. C. Mass spectrometry of laser-initiated carbene reactions for protein topographic analysis. Anal. Chem. 83 (8), 2913-2920 (2011).
- Li, Y., Williams, T. D., Topp, E. M. Effects of excipients on protein conformation in lyophilized solids by hydrogen/deuterium exchange mass spectrometry. Pharm. Res. 25 (2), 259-267 (2008).
- Li, Y., Williams, T. D., Schowen, R. L., Topp, E. M. Trehalose and calcium exert site-specific effects on calmodulin conformation in amorphous solids. Biotechnol. Bioeng. 97 (6), 1650-1653 (2007).

