Sistema Induzível de Expressão Multigênica mediada por polimerização T7 de T7, pMGX
Summary
Este estudo descreve métodos para a co-expressão mediada por T7 de múltiplos genes de um único plasmídeo em Escherichia coli usando o sistema de plasmídeo pMGX.
Abstract
A co-expressão de múltiplas proteínas é cada vez mais essencial para a biologia sintética, estudando complexos proteína-proteína e caracterizando e aproveitando os caminhos biossintéticos. Neste manuscrito, descreve-se o uso de um sistema altamente eficaz para a construção de operões sintéticos multigenes sob o controle de uma polimerase de ARN T7 induzível. Este sistema permite que muitos genes sejam expressos simultaneamente a partir de um plasmídeo. Aqui, um conjunto de quatro vetores relacionados, pMGX-A, pMGX-hisA, pMGX-K e pMGX-hisK, com o marcador selecionável por resistência à ampicilina ou kanamicina (A e K) e possuindo ou não uma hexahistidina N-terminal A tag (his) é divulgada. São fornecidos protocolos detalhados para a construção de operões sintéticos usando este sistema de vetores juntamente com os dados correspondentes, mostrando que um sistema baseado em pMGX contendo cinco genes pode ser facilmente construído e usado para produzir todas as cinco proteínas codificadas em Escherichia coli . Este sistemaEm e protocolo permite que os pesquisadores rotineiramente expressam módulos complexos de múltiplos componentes e caminhos em E. coli .
Introduction
A co-expressão de múltiplas proteínas é cada vez mais essencial, particularmente em aplicações de biologia sintética, onde vários módulos funcionais devem ser expressos 1 ; No estudo dos complexos proteína-proteína, onde a expressão e função muitas vezes requerem co-expressão 2 , 3 ; E na caracterização e aproveitamento de caminhos biossintéticos, onde cada gene na via deve ser expresso 4 , 5 , 6 , 7 , 8 . Vários sistemas foram desenvolvidos para coexpressão, particularmente no organismo hospedeiro Escherichia coli , o cavalo de trabalho para a expressão de proteína recombinante em laboratório 9 . Por exemplo, múltiplos plasmídeos com diferentes marcadores selecionáveis podem ser usados para expressar proteínas individuais usando uma riqueza de diferentes ex Vetores de pressão 10 , 11 . Os sistemas plasmídicos únicos para expressão múltipla de proteínas utilizaram múltiplos promotores para controlar a expressão de cada gene 10 , 12 ; Operões sintéticos, onde múltiplos genes são codificados em uma única transcrição 2 , 13 ; Ou, em alguns casos, um único gene que codifica um polipéptido que é processado de forma proteolítica, produzindo as proteínas desejadas de interesse 14 .
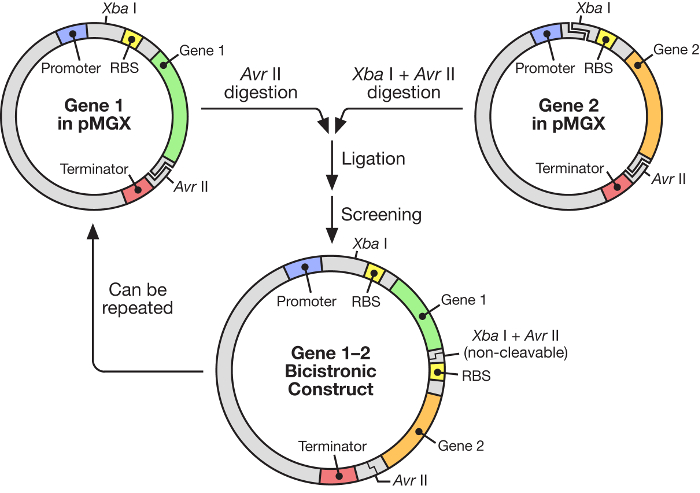
Figura 1: fluxo de trabalho pMGX que mostra a construção de um vetor policristão. O sistema pMGX fornece uma estratégia flexível e fácil de usar para a construção de operões sintéticos sob o controle de um promotor T7 indutível.E.com/files/ftp_upload/55187/55187fig1large.jpg "target =" _ blank "> Clique aqui para ver uma versão maior deste número.
Neste manuscrito, é descrito o uso de um sistema altamente eficaz para a construção de operões sintéticos multigene sob o controle de uma ARN polimerase T7 indutível ( Figura 1 ). Este sistema permite que muitos genes sejam expressos simultaneamente a partir de um plasmídeo. É baseado em um sistema de plasmídeo, originalmente chamado pKH22, que foi utilizado com sucesso para várias aplicações diferentes 6 , 7 , 8 . Aqui, este conjunto de plasmídeo é expandido para incluir quatro vetores relacionados: pMGX-A, um vetor de expressão que não possui quaisquer marcas C ou N-terminal e com o marcador de resistência à ampicilina; PMGX-hisA, um vetor de expressão que codifica uma etiqueta de hexahistidina N-terminal e com o marcador de resistência à ampicilina; PMGX-K, um vetor de expressão lObtendo quaisquer tags C ou N-terminal e com o marcador de resistência à kanamicina; E pMGX-hisK, um vetor de expressão que codifica uma etiqueta de hexahistidina N-terminal e com o marcador de resistência à canamicina. Neste estudo, o método para a geração de um vetor policristão contendo cinco genes usando o sistema pMGX, especificamente pMGX-A, é demonstrado juntamente com a produção bem-sucedida de cada proteína individual em Escherichia coli .
Protocol
Representative Results
Discussion
A co-expressão de múltiplos genes é cada vez mais essencial, particularmente na caracterização e reconstituição das vias metabólicas complexas multigênicas 3 , 4 , 5 . O sistema pMGX faz co-expressão multigene na rotina 6 , 7 , 8 de E. coli e acessível a diversos pesquisadores. Neste estudo, mostraram-se cinco prote…
Declarações
The authors have nothing to disclose.
Acknowledgements
Este trabalho foi apoiado pelo Conselho de Pesquisa em Ciências Naturais e Engenharia do Canadá.
Materials
| Enzymes | |||
| Alkaline Phosphatase, Calf Intestinal (CIP) | New England Biolabs | M0290S | |
| AvrII | New England Biolabs | R0174S | |
| EcoRI | New England Biolabs | R0101S | |
| NdeI | New England Biolabs | R0111S | |
| XbaI | New England Biolabs | R0145S | |
| Herculase II Fusion DNA Polymerase | Agilent Technologies | 600677 | |
| T4 DNA Ligase | New England Biolabs | M0202S | |
| Name | Company | Catalog Number | Comments |
| Reagents | |||
| 1 kb DNA ladder | New England Biolabs | N3232L | |
| 4-20% Mini-PROTEAN TGX Stain-Free Protein Gels | Bio-Rad | 456-8095 | |
| 50 x TAE | Fisher Thermo Scientific | BP1332-4 | |
| Agar | Fisher Thermo Scientific | BP1423-500 | |
| Agarose | Fisher Thermo Scientific | BP160-500 | |
| Ampicilin | Sigma-Alrich | A9518-5G | |
| BL21 (DE3) chemically comeptent cells | Comeptent cell prepared in house | ||
| B-PER Bacterial Protein Extraction Reagent | Fisher Thermo Scientific | PI78243 | |
| dNTP mix | Agilent Technologies | Supplied with polymerase | |
| Gel Extraction Kit | Omega | D2500-02 | E.Z.N.A Gel Extraction, supplied by VWR Cat 3: CA101318-972 |
| Glycine | Fisher Thermo Scientific | BP381-1 | |
| His Tag Antibody [HRP], mAb, Mouse | GenScript | A00612 | |
| Immobilon Western Chemiluminescent HRP Substrate | EMD Millipore | WBKLS0100 | |
| IPTG | Sigma-Alrich | 15502-10G | |
| LB | Fisher Thermo Scientific | BP1426-500 | |
| Methanol | Fisher Thermo Scientific | A411-20 | |
| Pasteurized instant skim milk powder | Local grocery store | No-name grocery store milk is adequate | |
| Nitrocellulose membrane | Amersham Protran (GE Healthcare Life Sciences) | 10600007 | Membrane PT 0.45 µm 200 mm X 4 m, supplied by VWR Cat #: CA10061-086 |
| Plasmid DNA Isolation Kit | Omega | D6943-02 | E.Z.N.A Plasmid DNA MiniKit I, supplied by VWR Cat #: CA101318-898 |
| pMGX | Boddy Lab | Request from the Boddy Lab Contact cboddy@uottawa.ca | |
| Primers | Intergrated DNA Technologies | Design primers as needed for desired gene | |
| Synthetic Gene | Life Technologies | Design and optimize as needed | |
| Thick Blot Filter Paper | Bio-Rad | 1703932 | |
| Tris base | BioShop | TRS001.1 | |
| Tween-20 | Sigma-Alrich | P9416-50ML | |
| XL1-Blue chemically competent cells | Comeptent cell prepared in house | ||
| Name | Company | Catalog Number | Comments |
| Equipment | |||
| BioSpectrometer | Eppendorf | RK-83600-07 | |
| Gel box – PAGE | Bio-Rad | 1658005 | Mini-PROTEIN Tetra Vertical Electrophoresis Cell |
| Gel Imager | Alpha Innotech | AlphaImager EC | |
| Incubator-oven | Fisher Thermo Scientific | 11-690-650D | Isotemp |
| Incubator-shaker | Fisher Thermo Scientific | SHKE6000-7 | MaxQ 6000 |
| Personna Razors | Fisher Thermo Scientific | S04615 | |
| Power Pack | Bio-Rad | S65533Q | FB300 |
| Transilluminator | VWR International | M-10E,6W | |
| Thermocylcer | Eppendorf | Z316091 | Mastercycler Personal, supplied by Sigma |
| UV Face-Shield | 18-999-4542 | ||
| Waterbath | Fisher Thermo Scientific | 15-460-2SQ | |
| Western Transfer Apparatus | Bio-Rad | 1703935 | Mini-Trans Blot Cell |
Referências
- Purnick, P. E. M., Weiss, R. The second wave of synthetic biology: from modules to systems. Nat. Rev. Mol. Cell Biol. 10 (6), 410-422 (2009).
- Bieniossek, C., et al. Automated unrestricted multigene recombineering for multiprotein complex production. Nat. Methods. 6 (6), 447-450 (2009).
- Jochimsen, B., et al. Five phosphonate operon gene products as components of a multi-subunit complex of the carbon-phosphorus lyase pathway. Proc. Natl. Acad. Sci. USA. 108 (28), 11393-11398 (2011).
- Martin, V. J. J., Pitera, D. J., Withers, S. T., Newman, J. D., Keasling, J. D. Engineering a mevalonate pathway in Escherichia coli for production of terpenoids. Nat. Biotechnol. 21 (7), 796-802 (2003).
- Ajikumar, P. K., et al. Isoprenoid pathway optimization for Taxol precursor overproduction in Escherichia coli. Science. 330 (6000), 70-74 (2010).
- Boddy, C. N., Hotta, K., Tse, M. L., Watts, R. E., Khosla, C. Precursor-directed biosynthesis of epothilone in Escherichia coli. J. Am. Chem. Soc. 126 (24), 7436-7437 (2004).
- Lundgren, B. R., Boddy, C. N. Sialic acid and N-acyl sialic acid analog production by fermentation of metabolically and genetically engineered Escherichia coli. Org. Biomol. Chem. 5 (12), 1903-1909 (2007).
- Horsman, M. E., Lundgren, B. R., Boddy, C. N. N-Acetylneuraminic Acid Production in Escherichia coli Lacking N-Acetylglucosamine Catabolic Machinery. Chem. Eng. Commun. 203 (10), 1326-1335 (2016).
- Romier, C., et al. Co-expression of protein complexes in prokaryotic and eukaryotic hosts: experimental procedures, database tracking and case studies. Acta Crystallogr. D, Biol. Crystallogr. 62 (Pt 10), 1232-1242 (2006).
- Tolia, N. H., Joshua-Tor, L. Strategies for protein coexpression in Escherichia coli. Nat. Methods. 3 (1), 55-64 (2006).
- Chanda, P. K., Edris, W. A., Kennedy, J. D. A set of ligation-independent expression vectors for co-expression of proteins in Escherichia coli. Protein Expr. Purif. 47 (1), 217-224 (2006).
- Kim, K. -. J., et al. Two-promoter vector is highly efficient for overproduction of protein complexes. Protein Sci. 13 (6), 1698-1703 (2004).
- Tan, S., Kern, R. C., Selleck, W. The pST44 polycistronic expression system for producing protein complexes in Escherichia coli. Protein Expr. Purif. 40 (2), 385-395 (2005).
- Chen, X., Pham, E., Truong, K. TEV protease-facilitated stoichiometric delivery of multiple genes using a single expression vector. Protein Sci. 19 (12), 2379-2388 (2010).
- Lorenz, T. C. Polymerase chain reaction: basic protocol plus troubleshooting and optimization strategies. J. Vis. Exp. (63), e3998 (2012).
- Lee, P. Y., Costumbrado, J., Hsu, C. -. Y., Kim, Y. H. Agarose gel electrophoresis for the separation of DNA fragments. J. Vis. Exp. (62), (2012).
- Sukumaran, S. Concentration determination of nucleic acids and proteins using the micro-volume BioSpec-nano-spectrophotometer. J. Vis. Exp. (48), (2011).
- JoVE Science Education Database. Basic Methods in Cellular and Molecular Biology. Molecular Cloning. J. Vis. Exp Available from: https://www.jove.com/science-education/5074/molecular-cloning (2016)
- JoVE Science Education Database. Basic Methods in Cellular and Molecular Biology. The Western Blot. J. Vis. Exp Available from: https://www.jove.com/science-education/5065/the-western-blot (2016)
- Laible, M., Boonrod, K. Homemade site directed mutagenesis of whole plasmids. J. Vis. Exp. (27), (2009).

