Análise por citometria de fluxo de biomarcadores apoptóticos em células de câncer cervical SiHa tratadas com Actinomicina D
Summary
A apoptose pode ser caracterizada pela análise por citometria de fluxo de biomarcadores apoptóticos precoce e tardio. A linhagem celular de câncer cervical, SiHa, foi analisada para biomarcadores de apoptose após tratamento com Actinomicina D usando citômetro de fluxo de bancada.
Abstract
Biomarcadores de apoptose foram investigados em células de câncer cervical SiHa tratadas com actinomicina D usando um citômetro de fluxo de bancada. Biomarcadores precoces (anexina V e potencial de membrana mitocondrial) e biomarcadores tardios (caspases 3 e 7 e danos ao DNA) de apoptose foram medidos em culturas experimental e controle. As culturas foram incubadas por 24 horas em estufa umidificada a 37 °C com 5% de CO2. As células foram então destacadas com tripsina e enumeradas por citometria de fluxo. As células foram posteriormente analisadas para apoptose usando um ensaio de anexina V, um ensaio de potencial transmembrana eletroquímico mitocondrial, um ensaio de caspase 3/7 e um ensaio de danos ao DNA. Este artigo fornece uma visão geral da apoptose e citometria de fluxo tradicional, e elabora protocolos de citometria de fluxo para processamento e análise de células SiHa. Os resultados descrevem dados experimentais positivos, negativos e subótimos. Também são discutidas interpretações e ressalvas na realização da análise por citometria de fluxo da apoptose utilizando esta plataforma analítica. A análise por citometria de fluxo fornece uma medida precisa de biomarcadores precoces e tardios para apoptose.
Introduction
A apoptose, classificada como morte celular programadatipo 1, garante o equilíbrio entre proliferação e morte celular2. A apoptose é essencial durante o desenvolvimento humano, pós-lesão e para a prevenção de doenças como o câncer3. As vias de sinalização da morte celular apoptótica intrínseca e extrínseca4 causam alterações bioquímicas e morfológicas intracelulares sequenciais 2,5,6. As características apoptóticas morfológicas podem ser identificadas por microscopia, e a perturbação bioquímica pode ser analisada por ensaios bioquímicos, incluindo citometria de fluxo (FC)7.
A análise por citometria de fluxo para identificar a apoptose e entender os mecanismos intracelulares associados tem surgido nas últimas duas décadas8. A CF é uma metodologia científica que analisa células em um fluido que passa por lasers mono ou multicanais (Figura 1)9,10,11. As células do fluido são focalizadas em um único arquivo pelo sistema fluídico do citômetro de fluxo usando focalização hidrodinâmica. À medida que as células passam pelo laser, a luz é espalhada ou emitida pelas células. A luz espalhada pode estar na direção para frente (dispersão para frente) ou para o lado (dispersão lateral) e fornece informações sobre o tamanho da célula e granularidade da célula ou estruturas internas, respectivamente.
Além disso, reagentes fluorescentes, como corantes fluorescentes ou anticorpos marcados com fluoróforos, detectam estruturas ou moléculas específicas de superfície ou intracelulares. Quando o laser excita os fluoróforos, a luz é emitida em um comprimento de onda específico. Os detectores – geralmente tubos fotomultiplicadores – quantificam a luz espalhada e emitida a partir de amostras celulares. Os detectores produzem uma corrente quantificável que é proporcional à dispersão de luz e emissão de fluorescência. A saída eletrônica é convertida em sinais digitais por meio de um software computacional para identificar populações celulares com base no tamanho celular, granularidade celular e fluorescência relativa de moléculas marcadas com fluoróforos 9,12,13.
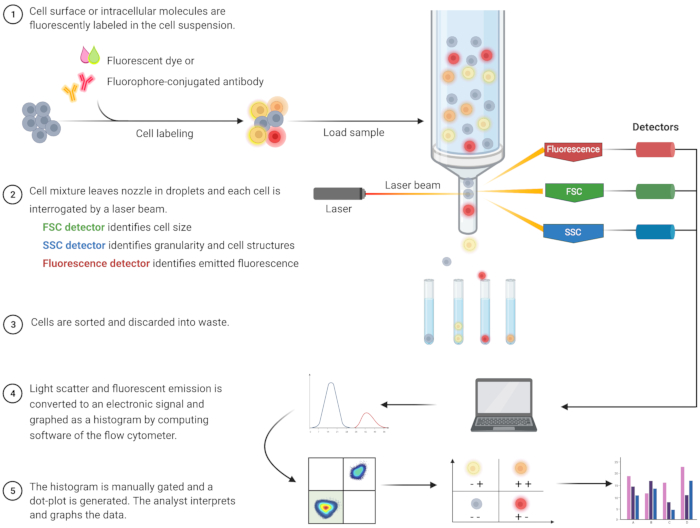
Figura 1: Esquema descrevendo o funcionamento técnico e o fluxo de trabalho da citometria de fluxo tradicional. As células são coradas com reagentes fluorescentes e sondadas por laser. Os sinais de fluorescência gerados são detectados e convertidos em uma saída eletrônica, que é posteriormente digitalizada e analisada por programas de computador e programas estatísticos. Abreviações: FSC = forward scatter; SSC = dispersão lateral. Clique aqui para ver uma versão maior desta figura.
FC é usado em pesquisa e diagnóstico de saúde. Os dois objetivos da CF em necrobiologia são a elucidação das propriedades moleculares e funcionais da morte celular e a discriminação dos vários modos de morte celular14,15,16,17,18. As aplicações da FC incluem enumeração celular, classificação de populações celulares, imunofenotipagem, detecção de biomarcadores (por exemplo, biomarcadores de apoptose), estudos de toxicidade e engenharia de proteínas12. Além disso, a CF é comumente aplicada em diagnósticos de saúde para auxiliar no diagnóstico e acompanhamento de pacientes com neoplasias hematológicas. Avanços em instrumentação, detecção de fluoróforos e sistemas de detectores estão expandindo as aplicações de FC para incluir citometria de imagem, citometria de massa e citometria espectral com aplicações de pesquisa maisamplas 12.
A análise por citometria de fluxo da apoptose oferece vantagens sobre as técnicas tradicionais utilizadas na avaliação da saúde celular. A CF pode analisar várias células isoladas em uma amostra heterogênea de forma rápida e reprodutível para estimar a apoptose 3,5. A capacidade da CF de fornecer informações quantitativas sobre fenótipos celulares em uma base celular individual, e evitar análises em massa, oferece sensibilidade superior às técnicas de Western blotting, ensaios imunoenzimáticos (ELISAs), fluorometria e espectrofotometria utilizadas na análise da apoptose 8,19. Além disso, a relativa facilidade da análise de CF em contraste com os passos manuais pesados e pouco reprodutíveis de Western blots e ELISAs é vantajosa. A análise reprodutível, precisa e de alto rendimento da CF é, portanto, benéfica na pesquisa do câncer20.
A CF também permite a análise simultânea de parâmetros do ciclo celular de populações de células apoptóticas saudáveis e anormais21. Como a apoptose é um processo dinâmico, diferentes métodos podem produzir resultados variáveis e são dependentes do momento em que as células são colhidas22. A avaliação quantitativa simultânea de múltiplos parâmetros do fenótipo celular permite a detecção de subpopulações menores com alta acurácia, por exemplo, subpopulações celulares raras com baixa frequência de 0,01% podem ser detectadas23. A análise multiparamétrica da CF é especialmente útil, pois a morte apoptótica ocorre ao longo de um espectro de alterações bioquímicas precoces e tardias com células em vários pontos ao longo do contínuo apoptótico. Por exemplo, o uso de dupla coloração usando anexina V e iodeto de propídio na análise de CF de células apoptóticas permite a categorização de células apoptóticas precoces, células apoptóticas tardias e célulasmortas24. A detecção precisa de apoptose em múltiplos estágios evita erros de classificação e resultados falso-negativos. Assim, a análise multiparamétrica por CF melhora a especificidade geral da detecção de fenótipos celulares e evita o erro de classificação de populações menores. Além disso, a triagem celular por CF permite o isolamento de populações celulares com alta pureza para posterioranálise7.
A desvantagem da CF inclui o uso de células em suspensão, o que pode ser desafiador na análise tecidual, pois a desagregação do tecido em células pode alterar a função celular19. Além disso, a falta de padronização da configuração do instrumento de CF, análise de dados e relatórios de ensaios pode causar variação nos resultados19, enfatizando a necessidade de treinamento otimizado dos operadores de CF para executar, analisar e relatar dados. Por exemplo, a capacidade da CF de discriminar debris apoptóticos verdadeiros de núcleos apoptóticos requer i) configurações de aquisição adequadas, ii) o uso de esferas de calibração para identificar um pico de DNA diploide e iii) controles celulares negativos e positivos que são específicos para células3. Além disso, a análise multiparamétrica é limitada pelo número de detectores, e compensações ótimas precisam ser realizadas para evitar resultados inespecíficos e transbordamento de emissão fluorescente ao usar múltiplos reagentes fluorescentes25. Os avanços na tecnologia de instrumentos e fluoróforos melhoraram a detecção de parâmetros para 30 parâmetros12.
A identificação da morte celular apoptótica nem sempre é simples7, e biomarcadores sensíveis e específicos devem ser considerados. O Comitê de Nomenclatura de Morte Celular (DCNT) recomenda que mais de um ensaio seja utilizado para estudar e quantificar o processo de apoptose26. A análise microscópica para características apoptóticas clássicas26 também é recomendada para confirmar a apoptose e evitar resultados falso-positivos7. Quatro características bioquímicas cardinais que abrangem eventos apoptóticos precoces e tardios são: (1) perda de assimetria da membrana celular; (2) potencial de membrana mitocondrial de dissipação (ΔΨm); (3) ativação de caspases; e (4) danos ao DNA26.
Durante a apoptose precoce, a fosfatidilserina é exteriorizada para a membrana celular externa 27 e pode ser detectada pela anexina V marcada fluorescentemente com ficoeritrina27,28,29. Além disso, a dupla coloração com o corante fluorescente ligante de DNA, 7-aminoactinomicina D (7-AAD), distingue células vivas, apoptóticas tardias e mortas. Portanto, as células apoptóticas precoces são positivas para a anexina V e negativas para o 7-AAD, em contraste com as células apoptóticas tardias, que são positivas para ambos os corantes24.
Sinais apoptóticos intrínsecos induzem a dissipação do potencial de membrana mitocondrial (ΔΨm). A ruptura do ΔΨm provoca a liberação precoce de proteínas pró-apoptóticas do espaço intermembrana mitocondrial para o citosol27,29,30. A alteração no ΔΨm pode ser avaliada pela dupla coloração com o corante lipofílico carregado positivamente, éster etílico tetrametilrodamina, TMRE e 7-AAD. O corante TMRE se acumula dentro da membrana interna das mitocôndrias intactas quando o potencial de membrana é alto. As mitocôndrias despolarizadas demonstram diminuição da fluorescência. Células vivas com mitocôndrias polarizadas (membrana mitocondrial intacta) coram positivo para TMRE e negativo para 7-AAD. Células mortas com mitocôndrias despolarizadas são negativas para TMRE e positivas para 7-AAD31.
As caspases são uma família de proteases intracelulares que, quando ativadas, sinalizam e executam a apoptose26,27. As caspases do executor terminal (3,6,7) afetam a apoptose tardia 29,32,33. As atividades da caspase-3 e -7 podem ser medidas por um substrato fluorescentemente marcado que, quando clivado, liga-se ao DNA e emite um sinal fluorescente. Além disso, qualquer comprometimento da integridade da membrana celular pode ser avaliado pela coloração com 7-AAD. As células apoptóticas são positivas para o corante ligante de DNA, mas negativas para 7-AAD. Células mortas e apoptóticas tardias são positivas para ambos os corantes34.
A apoptose tardia é caracterizada por danos ao DNA27,29,35, que podem ser avaliados por ataxiatelangiectasia fosforilada, quinase mutada (ATM) e histona H2A.X. Quebras de DNA de fita dupla (DSBs) causam fosforilação de H2A.X. Anticorpos fluorescentemente marcados contra ATM e H2A. X pode determinar danos no DNA. Detecção negativa de ATM e H2A. X indica ausência de danos ao DNA, enquanto a detecção de ambos os corantes indica a presença de quebras de fita dupla no DNA36.
A actinomicina D é um potente indutor de apoptose e age ligando-se ao DNA para bloquear eventos de transcrição e tradução37. Este estudo teve como objetivo avaliar a apoptose bioquímica induzida pela actinomicina D na linhagem celular SiHa, analisando biomarcadores de apoptose em estágio inicial e tardio. Quatro biomarcadores bioquímicos de apoptose avaliaram as etapas sequenciais da cascata apoptótica que incluíram perda de assimetria da membrana celular, alteração no potencial de membrana mitocondrial, ativação de caspases terminais e danos ao DNA.
Protocol
Representative Results
Discussion
Neste estudo, células SiHa tratadas com actinomicina D analisadas por FC revelaram biomarcadores precoces e tardios significativos para apoptose. Condições subótimas para preparo, enumeração e coloração celular identificaram resultados imprecisos, enfatizando a necessidade de estreita aderência às instruções do fabricante ao realizar a CF.
Este estudo da apoptose por meio da identificação precoce e tardia de biomarcadores está de acordo com as diretrizes da DCNT1 para investigação de apoptose. Culturas de SiHa tratadas com actinomicina D demonstraram biomarcadores positivos para estágios apoptóticos precoce e tardio. O ensaio de Anexina V/PI e o ensaio de permeabilidade mitocondrial mostraram que a actinomicina D induziu um padrão PS-flip e dissipação da transição da membrana mitocondrial, respectivamente. Uma vez que as células apoptóticas atingem o ponto de não retorno induzido pela perturbação mitocondrial, as caspases terminais são ativadas 3,7. A ativação das caspases terminais 3 e 7 observada neste estudo indica apoptose tardia. Além disso, a ativação da caspase terminal causa clivagem internucleossômica do DNA e extensa fragmentação do DNA, o que classicamente tem sido relatado como um padrão de escada observado por eletroforese em gel28,38.
Os danos nucleares com o ATM e H2A. O ensaio de danos ao DNA do X FC mostrou quebras de fita dupla no DNA e danos totais ao DNA. Estes resultados confirmaram o dano nuclear apoptótico clássico induzido pela caspase a jusante (cariorrexe e cariorrlise) em culturas experimentais. O uso de múltiplos biomarcadores de citometria de fluxo detectou, assim, os eventos sequenciais em múltiplos estágios na apoptose e identificou de forma precisa e reprodutível populações celulares nos estágios apoptóticos iniciais e tardios. Esses achados são consistentes com as conhecidas características pró-apoptóticas da actinomicina D no tratamento do câncer em humanos 37,39,40,41 e apoiam ainda mais o uso da actinomicina D como controle positivo em experimentos de cultura de células FC que investigam apoptose.
O confinamento das populações celulares neste estudo foi informado por meio negativo e controles solventes, que separaram células apoptóticas de células saudáveis. Alternativamente, uma mistura de populações de controles positivos e negativos também pode ser usada para definir populações de células vivas e apoptóticas para estabelecer portões populacionais celulares 7,9. Uma vez que os estados celulares doentes e saudáveis são definidos e controlados, as configurações do modelo podem ser aplicadas a todas as culturas experimentais e de controle subsequentes.
A adesão rigorosa ao protocolo de CF é essencial para evitar falsos resultados. Durante a otimização do protocolo, os seguintes problemas foram observados: (1) baixa concentração celular, (2) alta concentração celular, (3) aglomeração celular, (4) coloração prolongada e (5) mau manuseio da amostra. Esses problemas podem ser evitados pela estrita adesão aos requisitos otimizados do protocolo. Isso enfatiza a natureza crucial das etapas pré-analíticas e analíticas para que a CF obtenha dados precisos. Durante a preparação celular, tripsinização, pipetagem, centrifugação e diluições devem ser conduzidas com cuidado. A tripsinização excessiva e a pipetagem vigorosa podem resultar em cisalhamento químico e mecânico das células, respectivamente. A centrifugação prolongada e de alta velocidade pode resultar em degradação celular e altas contagens de detritos celulares. A concentração celular ideal é necessária para minimizar a aquisição incorreta de eventos celulares. Portanto, as suspensões celulares primárias devem ser diluídas para obter a concentração celular ótima.
Além disso, ao manusear amostras, deve-se tomar cuidado para evitar aglomeração e fragmentação celular e garantir que as células permaneçam em suspensão durante a análise. O manuseio da amostra para evitar a aglomeração de células permite o fluxo de células laminares únicas, evita o bloqueio mecânico da tubulação capilar do instrumento e reduz os índices espúrios de tamanho de células grandes. Outra ressalva é proteger as culturas contra a luz para evitar foto-oxidação e extinção dos fluoróforos nos ensaios para evitar resultados falso-negativos. Deve-se tomar cuidado para garantir uma exposição mínima à luz na etapa de coloração das células e etapas subsequentes de processamento. Além disso, tempos prolongados de imunomarcação podem resultar em resultados falso-positivos, uma vez que as proteínas são coradas não especificamente. Portanto, a adesão aos períodos de incubação prescritos pelo fabricante é importante.
Em resumo, a CF pode detectar com precisão a apoptose e discriminar entre biomarcadores de apoptose precoce e tardia em cultura celular. Além disso, os avanços na tecnologia levaram à fabricação de citômetros de fluxo de bancada para cientistas não especialistas estudarem a saúde celular e vias complexas de sinalização intracelular.
Declarações
The authors have nothing to disclose.
Acknowledgements
O estudo foi financiado pela National Research Foundation (NRF) e pelo South African Medical Research Council (SAMRC). Gostaríamos de agradecer ao Serviço Nacional de Laboratório de Saúde (NHLS) pela compra do Analisador de Células de Goiaba. Todas as figuras desta publicação foram criadas com Biorender.com.
Materials
| 6-well plates | Lasec | P1PLA044C-000006 | |
| Dimethyl Sulfoxide | Sigma-Aldrich | D8418 | |
| DMEM | ThermoFisher | 41966052 | |
| Glutamine | Sigma-Aldrich | P10-040500 | |
| Guava Muse Cell Analyzer | Luminex | 0500-3115 | |
| Microcentrifuge tubes/Eppendorf | Merck | EP0030122208-200EA | |
| Muse Annexin V kit | Merck | MCH100105 | |
| Muse Caspase-3/7 kit | Merck | MCH100108 | |
| Muse Count and Viability kit | Merck | MCH600103 | |
| Muse DNA Damage kit | Merck | MCH200107 | |
| Muse MitoPotential kit | Merck | MCH100110 | |
| PBS Buffer | ThermoFisher | 70013065 | |
| Pen-strep | Sigma-Aldrich | P4333 | |
| SiHa cells | ATCC | CRL-1550 | |
| T25 culture flasks | Sigma-Aldrich | C6231 | |
| Trypsin | Pan Biotech | P10-040500 |
Referências
- Galluzzi, L., et al. Molecular mechanisms of cell death: Recommendations of the Nomenclature Committee on Cell Death 2018. Cell Death and Differentiation. 25 (3), 486-541 (2018).
- Kerr, J. F., Wyllie, A. H., Currie, A. R. Apoptosis: a basic biological phenomenon with wide-ranging implications in tissue kinetics. British journal of cancer. 26 (4), 239-257 (1972).
- Riccardi, C., Nicoletti, I. Analysis of apoptosis by propidium iodide staining and flow cytometry. Nature Protocols. 1 (3), 1458-1461 (2006).
- Edinger, A. L., Thompson, C. B. Death by design: apoptosis, necrosis and autophagy. Current Opinion in Cell Biology. 16 (6), 663-669 (2004).
- Arends, M. J., Morris, R. G., Wyllie, A. H. Apoptosis. The role of the endonuclease. The American journal of pathology. 136 (3), 593-608 (1990).
- Majno, G., Joris, I. Apoptosis, oncosis, and necrosis. An overview of cell death. Am J Pathol. 146 (1), 3-15 (1995).
- Darzynkiewicz, Z., Traganos, F., Al-Rubeai, M. . Apoptosis. , 33-73 (1998).
- Wlodkowic, D., Skommer, J., Darzynkiewicz, Z. Flow cytometry-based apoptosis detection. Methods in molecular biology. 559, 19-32 (2009).
- . Introduction to Flow Cytometry Basics Available from: https://www.bio-rad-antibodies.com/introduction-to-flow-cytometry.html (2021)
- Telford, W. G., Komoriya, A., Packard, B. Z. Detection of localized caspase activity in early apoptotic cells by laser scanning cytometry. Cytometry. 47 (2), 81-88 (2002).
- Castedo, M., et al. Quantitation of mitochondrial alterations associated with apoptosis. J Immunol Methods. 265 (1-2), 39-47 (2002).
- McKinnon, K. M. Flow Cytometry: An Overview. Current protocols in immunology. 120, 1-11 (2018).
- Macey, M. G. Flow cytometry: principles and clinical applications. Med Lab Sci. 45 (2), 165-173 (1988).
- Darzynkiewicz, Z., et al. Features of apoptotic cells measured by flow cytometry. Cytometry. 13 (8), 795-808 (1992).
- Darzynkiewicz, Z., et al. Cytometry in cell necrobiology: Analysis of apoptosis and accidental cell death (necrosis). Cytometry. 27 (1), 1-20 (1997).
- Ormerod, M. G. The study of apoptotic cells by flow cytometry. Leukemia. 12 (7), 1013-1025 (1998).
- van Engeland, M., Nieland, L. J., Ramaekers, F. C., Schutte, B., Reutelingsperger, C. P. Annexin V-affinity assay: a review on an apoptosis detection system based on phosphatidylserine exposure. Cytometry. 31 (1), 1-9 (1998).
- Vermes, I., Haanen, C., Reutelingsperger, C. Flow cytometry of apoptotic cell death. Journal of Immunological Methods. 243 (1), 167-190 (2000).
- Jahan-Tigh, R. R., Ryan, C., Obermoser, G., Schwarzenberger, K. Flow cytometry. J Invest Dermatol. 132 (10), 1-6 (2012).
- Lövborg, H., Gullbo, J., Larsson, R. Screening for apoptosis-classical and emerging techniques. Anti-cancer drugs. 16 (6), 593-599 (2005).
- Vorobjev, I. A., Barteneva, N. S. Multi-parametric imaging of cell heterogeneity in apoptosis analysis. Methods. 112, 105-123 (2017).
- Telford, W. G., Komoriya, A., Packard, B. Z. Multiparametric analysis of apoptosis by flow and image cytometry. Methods in molecular biology. 263, 141-160 (2004).
- Kagami, S., Rizzo, H. L., Lee, J. J., Koguchi, Y., Blauvelt, A. Circulating Th17, Th22, and Th1 cells are increased in psoriasis. J Invest Dermatol. 130 (5), 1373-1383 (2010).
- . Muse® Annexin V & Dead Cell Kit Available from: https://www.luminexcorp.com/muse-annexin-v-dead-cell-kit/ (2019)
- Roederer, M. Spectral compensation for flow cytometry: visualization artifacts, limitations, and caveats. Cytometry. 45 (3), 194-205 (2001).
- Kroemer, G., et al. Classification of cell death: recommendations of the Nomenclature Committee on Cell Death. Cell Death and Differentiation. 12 (2), 1463-1467 (2005).
- Apoptosis assays and markers guide. Abcam Available from: https://www.abcam.com/kits/apoptosis-assays (2021)
- Vermes, I., Haanen, C., Steffens-Nakken, H., Reutelingsperger, C. A novel assay for apoptosis. Flow cytometric detection of phosphatidylserine expression on early apoptotic cells using fluorescein labelled Annexin V. Journal of Immunological Methods. 184 (1), 39-51 (1995).
- Elmore, S. Apoptosis: A Review of Programmed Cell Death. Toxicologic Pathology. 35 (4), 495-516 (2007).
- Saelens, X., et al. Toxic proteins released from mitochondria in cell death. Oncogene. 23 (16), 2861-2874 (2004).
- Muse™ MitoPotential Kit User’s Guide. Luminex Corporation Available from: https://www.luminexcorp.com/muse-mitopotential-kit (2013)
- McIlwain, D. R., Berger, T., Mak, T. W. Caspase functions in cell death and disease. Cold Spring Harbor Perspectives in Biology. 5 (4), 008656 (2013).
- Wigdal, S. S., Kirkland, R. A., Franklin, J. L., Haak-Frendscho, M. Cytochrome c release precedes mitochondrial membrane potential loss in cerebellar granule neuron apoptosis: lack of mitochondrial swelling. Journal of Neurochemistry. 82 (5), 1029-1038 (2002).
- Muse® Caspase-3/7 Kit. Luminex Corporation Available from: https://www.luminexcorp.com/muse-caspase-3-7-kit/#overview (2019)
- Häcker, G. The morphology of apoptosis. Cell and Tissue Research. 301 (1), 5-17 (2000).
- Muse® Multi-Color DNA Damage Kit User’s Guide. Luminex Corporation Available from: https://www.luminexcorp.com/muse-multi-color-dna-damage-kit/#overview (2020)
- Kleeff, J., Kornmann, M., Sawhney, H., Korc, M. Actinomycin D induces apoptosis and inhibits growth of pancreatic cancer cells. International journal of cancer. 86 (3), 399-407 (2000).
- Wlodkowic, D., Skommer, J., Darzynkiewicz, Z. Cytometry of apoptosis. Historical perspective and new advances. Experimental oncology. 34 (3), 255-262 (2012).
- Szeberenyi, J. The effect of actinomycin D on RNA metabolism in human cells. Biochem Mol Biol Educ. 34 (1), 50-51 (2006).
- Ginell, S., Lessinger, L., Berman, H. M. The crystal and molecular structure of the anticancer drug actinomycin D–some explanations for its unusual properties. Biopolymers. 27 (5), 843-864 (1988).
- Hou, M. H., Robinson, H., Gao, Y. G., Wang, A. H. Crystal structure of actinomycin D bound to the CTG triplet repeat sequences linked to neurological diseases. Nucleic Acids Res. 30 (22), 4910-4917 (2002).

