用于体外评估药物诱导肝毒性的人肝脏微生理系统
Summary
药物性肝损伤(DILI)是药物失败的主要原因。已经开发了一种协议来使用肝脏微生理系统(MPS)准确预测化合物的DILI责任。肝脏模型使用原代肝细胞的共培养和翻译相关终点来评估细胞对治疗的反应。
Abstract
DILI是药物开发中损耗的主要原因,已知有1000多种FDA批准的药物可能导致人类DILI。不幸的是,DILI往往在药物达到临床阶段时才被发现,危及患者的安全,并给制药行业带来重大损失。考虑到标准2D模型在检测DILI方面存在局限性,因此必须开发更具预测性的体外模型以提高数据可转换性。为了详细了解DILI的因果关系和机制方面,已经开发了一种由人原代肝实质和非实质细胞(NPC)组成并在灌注下在工程支架上的3D微组织中培养的人肝脏MPS。将冷冻保存的原代人肝细胞(PHHs)和Kupffer细胞(HKCs)作为微组织在MPS平台中共培养长达两周,并且每种感兴趣的化合物以七种测试浓度重复加样到肝脏微组织中长达四天。分析功能性肝脏特异性终点(包括临床生物标志物,如丙氨酸氨基转移酶,ALT)以评估肝功能。通过比较对单剂量和多剂量微组织的反应,可以评估急性和慢性暴露于各种严重程度的DILI化合物。该方法已通过广泛的严重和轻度肝毒性化合物进行了验证。在这里,我们显示了吡格列酮和曲格列酮的数据,这些众所周知的肝毒性化合物因导致肝功能衰竭而从市场上撤出。总体而言,肝脏MPS模型可以成为评估DILI及其与肝功能变化关联的有用工具。该模型还可用于评估新化合物在不同患者亚群中的行为以及毒性特征如何受到肝病状态(例如病毒性肝炎,脂肪肝)的影响。
Introduction
DILI仍然是美国和欧洲急性肝衰竭的最常见原因,也是药物开发过程中化合物损耗的主要原因1。几乎所有类别的药物都会引起肝毒性,中枢神经系统药物和抗生素是迄今为止导致患者DILI的最常见治疗方法2。药物诱导的肝毒性是由遗传、非遗传和环境因素的复杂相互作用引起的,导致肝细胞和其他肝细胞类型(包括胆管细胞和内皮细胞)死亡1,3。
DILI致病因子可以分为两种方式:引起可预测剂量依赖性肝损伤的药物或引起特异质性DILI的药物,这种药物很少见,并且独立于药物剂量、途径或给药持续时间而发展,但在美国,高达六分之一的急性肝衰竭仅占4。不幸的是,在药物进入药物开发过程的临床阶段之前,DILI通常不会被检测到。药物性肝损伤等级(或DILIrank)由一千多种FDA批准的药物组成,根据其引起DILI的可能性分为四类,并且必须密切监测其在患者中的使用5。
研究药物肝毒性的机制仍然非常具有挑战性,因此,已经开发了许多临床前模型来探索DILI的机制。目前用于预测临床前开发中DILI的体外和体内模型在提供对活体人体中复杂,多方面相互作用的见解方面存在一些局限性。在2D中培养的癌性肝细胞系(即HepG2,HepaRG)仍然用于药物开发的早期阶段,以评估候选化合物的毒性6。即便如此,这些细胞系来自单个供体,肝功能水平异常,并且并不总是对检测DILI7,8表现出高灵敏度。作为癌性肝细胞系的替代品,如果在体外适当培养,PHHs可以更好地代表人类肝脏生理学,尽管它们的培养存在一些局限性,例如药物孵育时间短,寿命相对较短,肝基因表达丧失以及药物代谢功能改变9,10,11.PHHs可以在标准2D细胞培养板中的细胞外基质蛋白上培养,但缺点是其功能的快速下降意味着它们对DILI预测的灵敏度较低(<50%)12。
另一方面,对动物模型的测试缓慢,昂贵,并且需要跨物种翻译才能将预测推断到人类。大多数新开发的药物未能获得批准,这使得这一过程成本高昂且风险很大5。此外,为了测试新的人类特异性模式,由于基因序列或免疫反应与人类的差异,动物模型不太合适13。
因此,对更先进的三维(3D)体 外 肝脏模型的兴趣呈指数级增长。将PHHs培养为由悬挂液滴或超低附着表面上的重力聚集产生的球状结构,代表了评估复合负债的高通量方法14。PHH 球状体已用于评估疾病背景下的 DILI(例如脂肪变性和胆汁淤积)15。已经开发了各种各样的模型,包括肝细胞与基质成纤维细胞的电镀微图案共培养16,3D生物打印肝组织17,有或没有肝非实质细胞的3D球状体培养物15。然而,所有这些方法仍然存在缺点,在更具生理相关性的微环境中培养PHH可以长时间为它们提供更高水平的功能,以便能够长期暴露于潜在的肝毒物。此外,为了提高任何先进的 体外 PHH培养物的翻译相关性,必须利用临床相关的功能终点或毒性输出生物标志物来比较 体内 或临床场景的数据18。
在这项研究中,我们评估了MPS,也称为器官芯片(OOC)体外肝脏模型是否可用于了解肝毒性的详细机制方面。MPS先前已被证明可以在流动下维持功能强大的3D肝脏微组织长达4周19。该系统最近经过FDA测试,并显示出在进行药物毒性,代谢和细胞内积累时具有高可重复性20。此外,与球状体和夹心培养物相比,该系统在检测几种药物的毒性方面具有更稳定的功能和更高的灵敏度20。迄今为止,MPS已被广泛用于ADME 21,疾病建模(HBV22,NAFLD 23,24,25)和药物相互作用26,可能使其非常适合评估急性和慢性DILI。这里介绍的技术提供了一种替代方案,可以缩小更传统的细胞培养和动物模型与人体临床试验之间的差距,朝着模拟人类生物学条件的方向发展,以支持在药物开发过程的临床前阶段评估候选化合物的肝毒性。
Protocol
Representative Results
Discussion
MPS旨在在 体外重现 人体器官的功能单位,并已开发用于解决传统3D细胞培养模型的局限性27。肝脏是使用MPS建模最多的器官之一,并且已经开发了各种各样的系统。人肝负责药物代谢和有毒药物代谢物的产生,其功能是药物开发模型的关键要素,包括评估化合物28的DILI责任。在这里,我们介绍了一种使用肝脏MPS评估DILI的新方法;该方案能够为每种化合物寻求机理见解,以确定其如何引起DILI,并且是一种高度灵敏和稳健的测定。肝脏微组织在MPS板中形成,MPS板是PHH和HKCs的共培养物,与标准 体外 肝脏模型20相比,具有高水平的白蛋白和尿素产生以及高CYP3A4活性。
虽然这里描述的DILI模型可以作为药物开发过程中临床前测试后期的有用工具,但它也有一些局限性。作为目前市场上的大多数MPS,它是一个低通量平台,因此更难用于大规模的药物筛选活动。DILI模型由通过共培养PHH和HKC形成的微组织组成,也不能完全捕获人类肝脏的复杂性,通过结合不同类型的细胞(例如免疫细胞)进行进一步优化将有利于为现有模型增加价值。这种单器官MPS还可以与其他器官平台相结合,这些平台可以共享一个共同的介质,并允许细胞或内分泌水平的器官串扰,这有助于更好地理解毒性的机制见解,而不仅仅是肝脏本身。此外,与任何相对较新的技术一样,它可能被认为是昂贵的,因此可及性有限。
MPS是一个用于开发单个或多个人体组织的器官型模型的平台。该系统由控制器、脐带电缆和插入板的 MPS 驱动器组成(图 5A)。每个肝脏MPS板都有12个独立的开放孔,用于在工程支架上以3D方式培养原代肝细胞。总之,该系统经过QC检查,并在第-1天启动板,在第0天将PHH和HKC接种在平板上(图5B,见1)。嵌入式微泵促进细胞培养基通过支架的循环,以促进3D微组织的形成(图5B,见2)。形成的微组织在第4天进行QC处理,每48小时给药一次不同浓度的每种化合物,持续4天,并在第8天测定终点生物标志物(图5C)。MPS板中DILI测定的实验时间表如图 5D所示。
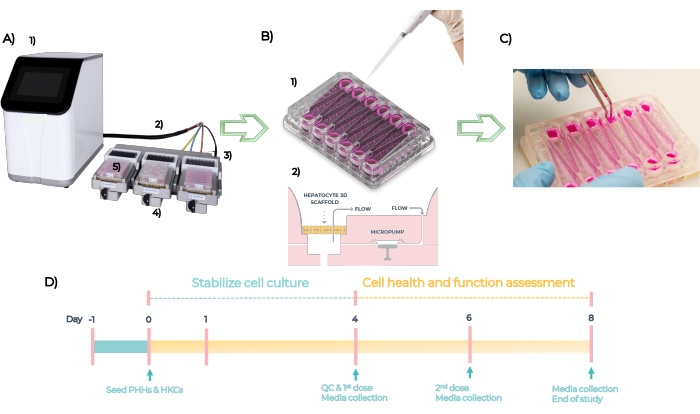
图5:标准DILI测定的微生理系统和实验时间表。 (A)微生理系统及其组件:控制器(1),脐带电缆(2),扩展坞(3),MPS驱动器(4)和LC12板(5)。(B)在第1天(1)将PHH和HKCs接种在LC12板上,嵌入式微泵促进细胞培养基以可调流速通过接种在支架上的3D微组织循环(2)。(C)在研究结束时取下脚手架。(四)实验时间表。 请点击此处查看此图的大图。
执行实验方案时,重要的是在启动之前进行可靠的系统质量控制检查,检查系统是否气动运行正常,并且对耗材板进行目视检查和有效底漆,以确保所有孔的功能均匀。拥有高质量的原代人细胞对于该协议至关重要,已知肝细胞在细胞培养实验中始终如一地粘附并形成3D相互作用。解冻这些细胞也是一个关键步骤,因为原代肝细胞不应通过移液作用重悬,因为这会迅速导致细胞死亡。细胞活力高于85%对于成功接种至关重要,因为大量的细胞碎片会干扰3D微组织的形成。在第4天对形成的肝脏微组织进行QC检查也很重要,用户需要确保测量可接受的LDH和尿素水平,因为超出范围的参数可能表明组织形成质量差,并允许直接排除故障。最后,细胞培养基中使用的氢化可的松必须在使用当天新鲜制备,以防止任何可能影响细胞培养功能的不必要的降解,因为它是维持肝细胞代谢功能所必需的。
尽管具有显着的复杂性,但肝脏MPS并不包含人类肝脏的所有细胞类型。可以向模型24,29添加更多细胞类型以增加生理相关性,但这些细胞类型只能在使用上下文的明确理由下添加。对于研究帝力PHH是关键细胞类型,在该模型中掺入HKCs可以确定一些免疫反应。还应该注意的是,从人肝脏中分离的PHHs和市售的冷冻保存PHHs往往在批次之间表现出一些差异。我们在这里已经证明,当与高质量的细胞制剂一起使用时,该协议会产生可重复的结果。然而,预计会有一些批次间的变化,这可以通过使用多个捐赠者的合并批次来进一步克服。这些限制可以通过使用与iPSC分化的肝细胞样细胞来克服,这些细胞概括了PHH的许多功能特性,并已用于药物开发过程30。HKC还显示出很大的批次间变异性和解冻后高水平的活化;因此,HKC供体在用于实验细胞培养(与经过验证的PHHs共培养)之前,在内部进行了预先验证,并且解冻后的活化水平必须较低;这是通过测量生物标志物IL-6和TNF-α来评估的(见补充材料)。
此处提供的数据证实,该测定可以准确检测DILI,有助于识别2D10,11甚至某些3D模型可能无法检测到的肝毒物。由于缺乏过程标准化和协调性,包括站点间重现性,MPS生成的数据仍未被制药行业用作监管提交或药物筛选目的的标准20。这里展示的数据和实验方法解决了这个问题,表明肝脏模型可以在DILI筛查中常规和稳健地使用,以准确预测新化合物的责任。
通过测量一系列终点以产生“肝毒性特征”,帮助识别具有不同程度的DILI关注的化合物(包括其他体外方法无法检测到的化合物)及其毒性机制。该技术可以缩小传统细胞培养和动物模型与人体临床试验之间的差距,作为药物开发过程的一部分,朝着模拟人类生物学条件的方向发展,以进行肝毒性的临床前评估。
Declarações
The authors have nothing to disclose.
Acknowledgements
CN Bio Innovations Ltd.资助了这项研究。
Materials
| 24 well cell culture cluster plates flat bottom | Corning | 3524 | |
| 96 well clear assay plates, flat bottom clear plastic | Greiner | 655101 | |
| 96 well plates black flat bottom | Corning | 3915 | |
| 96 Well White/Clear Bottom Plate, TC Surface | ThermoScientific | 165306 | |
| Advanced DMEM (1x) | Gibco | 12491015 | Cell culture media. |
| AssayMax Albumin ELISA Kit | AssayPro | EA3201-1 | Dilution 1:250. Time point Day 4, 6, and 8. |
| Cell Maintenance Cocktail B, (Primary Hepatocyte Maintenance Supplements) | Gibco | CM4000 | |
| CellTiter-Glo 3D Cell Viability Assay | Promega | G9682 | Dilution 1:1. Time point Day 8. |
| Chlorpromazine HCl | Sigma Aldrich | C8138 | |
| Chromacol blue lids, 9 mm Autosampler Vial Screw Thread Caps | ThermoScientific | 9-SCK(B)-ST1 | glass vial |
| Chromacol vials, 9 mm Clear Glass Screw Thread Vials | ThermoScientific | 2-SVW | |
| Class 2 Microbiological Safety Cabinets – Trimat2 1500 exhaust | Contained Air Solutions | ||
| Conical tubes 50 mL | Greiner | 227261 | |
| Cryopreserved Hepatocyte Recovery Medium (CHRM) | ThermoFisher Scientific | Gibco CM7000 | |
| Cryopreserved primary human hepatocytes | BioIVT Europe | Lot. RAS | |
| CytoTox 96 Cytotoxicty (LDH) Assay Kit | Promega | G1781 | Dilution – none. Time point Day 4, 6 and 8 |
| >Data analysis model used to generate the graph and EC:50 curves was nonlinear regression (curve fit) asymmetric sigmoidal, 5PL, where X is log(concentration | GraphPad Prism 9 | ||
| Disposable PES Filter Units 500mL | Fisher Scientific | 15913307 | |
| Disposable Pipette Basins 50ml | Fisher Scientific | 12369175 | |
| DMSO (Dimethyl sulfoxide) | Sigma-Aldrich | Sigma D2650 | |
| Dulbeco’s Phosphate Buffered Saline without Ca2+ and Mg2+ (D-PBS) | ThermoFisher Scientific | 14190-144 | |
| Easy Reader Conical Polypropylene Centrifuge Tubes 15 mL | Fisher Scientific | 11889640 | |
| Foetal bovine serum | Gibco | 10500064 | |
| Human ALT ELISA Kit | Abcam | ab 234578 | Dilution 1:5. Time point Day 6 and 8. |
| Human Cryopreserved Kupffer Cells | Lonza Europe | Lot. 190088KC | |
| hydrocortisone | Merck | H0888-1G | |
| Incubators models: New Brunswick Galaxy 170 S, New Brunswick Galaxy 170 R and CellXpert® C170. | Eppendorf | All serviced yearly; paperwork available upon request. | |
| Inverted Microscope | Leica DMIL LED | ||
| MPS know as Organ-on-a-Chip (OOC) | CN Bio Innovations Ltd. | ||
| MPS LC-12 plate | CN Bio Innovations Ltd. | ||
| Neubauer Improved C-Chip Disposable Haemocytometer (2 channel) | Cambridge Bioscience | DHC-N01-50 | |
| P450-Glo CYP3A4 Assay and Screening System | Promega | V9002 | Dilution – none. Time point Day 8 |
| PhysioMimix MPS platform | CN Bio Innovations Ltd. | ||
| Pioglitazone | MedChemExpress Tocris | HY-13956/CS-1700 | |
| Quantichrom Urea Assay Kit – Bioassay systems | Bioassay Systems | DY970-05 | Dilution 1:2 if initial reading is too high. Time point Day 4, 6 and 8. |
| Silica gel | Sigma-Aldrich | S7625 | |
| Software used to analyse and generate all the graphs was | GraphPad Prism 9 | ||
| Stripettes 10 mL | Fisher Scientific | 11839660 | |
| Stripettes 25 mL | Fisher Scientific | 11839181 | |
| Thawing plate Cocktail A, (Primary Hepatocyte Thawing and Plating Supplements) | Gibco | CM3000 | |
| Troglitazone | MedChemExpress Tocris | 97322-87-7 | |
| Trypan Blue Solution, 0.4% | Gibco | 15250061 | |
| Tubes 1.5 mL | Greiner | 616201 | |
| Weighing balance – model PA214C and AV213C | Ohaus Corp |
Referências
- Lisi, D. M. Drug-induced liver injury: An overview. US Pharmacist. 41 (12), 30-34 (2016).
- Kuna, L., et al. Models of drug induced liver injury (DILI)-current issues and future perspectives. Current Drug Metabolism. 19 (10), 830-838 (2018).
- Katarey, D., Verma, S. Drug-induced liver injury. Clinical Medicine. 16 (6), 104-109 (2016).
- Kullak-Ublick, G. A., et al. Drug-induced liver injury: recent advances in diagnosis and risk assessment Recent advances in clinical practice. Gut. 66, 1154-1164 (2017).
- Dirven, H., et al. Performance of pre-clinical models in predicting drug-induced liver injury in humans: a systematic review. Scientific Reports. 11 (1), 6403 (2021).
- Donato, M. T., Lahoz, A., Castell, J. V., Gomez-Lechon, M. J. Cell lines: a tool for in vitro drug metabolism studies. Current Drug Metabolism. 9 (1), 1-11 (2008).
- Wilkening, S., Stahl, F., Bader, A. Comparison of primary human hepatocytes and hepatoma cell line HepG2 with regard to their biotransformation properties. Drug Metabolism and Disposition. 31 (8), 1035-1042 (2003).
- Gerets, H. H. J., et al. Characterization of primary human hepatocytes, HepG2 cells, and HepaRG cells at the mRNA level and CYP activity in response to inducers and their predictivity for the detection of human hepatotoxins. Cell Biology and Toxicology. 28 (2), 69-87 (2012).
- Grainger, C. I., Greenwell, L. L., Lockley, D. J., Martin, G. P., Forbes, B. Culture of Calu-3 cells at the air interface provides a representative model of the airway epithelial barrier. Pharmaceutical Research. 23 (7), 1482-1490 (2006).
- Li, F., Cao, L., Parikh, S., Zuo, R. Three-dimensional spheroids with primary human liver cells and differential roles of kupffer cells in drug-induced liver injury. Journal of Pharmaceutical Sciences. 109 (6), 1912-1923 (2020).
- Proctor, W. R., et al. Utility of spherical human liver microtissues for prediction of clinical drug-induced liver injury. Archives of Toxicology. 91 (8), 2849-2863 (2017).
- Lin, C., Khetani, S. R. Advances in engineered liver models for investigating drug-induced liver injury. BioMed Research International. 2016, 1829148 (2016).
- Olson, H., et al. Concordance of the toxicity of pharmaceuticals in humans and in animals. Regulatory Toxicology and Pharmacology. 32 (1), 56-67 (2000).
- Bell, C. C., et al. Comparison of hepatic 2D sandwich cultures and 3D spheroids for long-term toxicity applications: A multicenter study. Toxicological Sciences. 162 (2), 655-666 (2018).
- Bell, C. C., et al. Characterization of primary human hepatocyte spheroids as a model system for drug-induced liver injury, liver function and disease. Scientific Reports. 6, 25187 (2016).
- Khetani, S. R., et al. Use of micropatterned co-cultures to detect compounds that cause drug-induced liver injury in humans. Toxicological Sciences. 132 (1), 107-117 (2013).
- Ma, X., et al. Deterministically patterned biomimetic human iPSC-derived hepatic model via rapid 3D bioprinting. Proceedings of the National Academy of Sciences of the united States of America. 113 (8), 2206-2211 (2016).
- Dieterle, P. Y. M., Dieterle, F. Tissue-specific, non-invasive toxicity biomarkers: translation from pre-clinical safety assessment to clinical safety monitoring. Expert Opinion on Drug Metabolism & Toxicology. 5 (9), 1023-1038 (2009).
- Rowe, C., et al. Perfused human hepatocyte microtissues identify reactive metabolite-forming and mitochondria-perturbing hepatotoxins. Toxicology in Vitro. 46, 29-38 (2018).
- Rubiano, A., et al. Characterizing the reproducibility in using a liver microphysiological system for assaying drug toxicity, metabolism, and accumulation. Clinical and Translational Science. 14 (3), 1049-1061 (2021).
- Tsamandouras, N., Kostrzewski, T., Stokes, C. L., Griffith, L. G., Hughes, D. J., Cirit, M. Quantitative assessment of population variability in hepatic drug metabolism using a perfused three-dimensional human liver microphysiological system. Journal of Pharmacology and Experimental Therapeutics. 360 (1), 95-105 (2017).
- Ortega-Prieto, A. M., et al. 3D microfluidic liver cultures as a physiological pre-clinical tool for hepatitis B virus infection. Nature Communications. 9 (1), 682 (2018).
- Kostrzewski, T., et al. Three-dimensional perfused human in vitro model of non-alcoholic fatty liver disease. World Journal of Gastroenterology. 23 (2), 204-215 (2017).
- Kostrzewski, T., et al. A microphysiological system for studying nonalcoholic steatohepatitis. Hepatology Communications. 4 (1), 77-91 (2020).
- Vacca, M., et al. Bone morphogenetic protein 8B promotes the progression of non-alcoholic steatohepatitis. Nature Metabolism. 2 (6), 514-531 (2020).
- Long, T. J., et al. Modeling therapeutic antibody-small molecule drug-drug interactions using a three-dimensional perfusable human liver co-culture platforms. Drug Metabolism and Disposition. 44, 1940-1948 (2016).
- Bai, J., Wang, C. Organoids and microphysiological systems: New tools for ophthalmic drug discovery. Frontiers in Pharmacology. 11, 407 (2020).
- Ribeiro, A. J. S., Yang, X., Patel, V., Madabushi, R., Strauss, D. G. Liver microphysiological systems for predicting and evaluating drug effects. Clinical Pharmacology & Therapeutics. 106 (1), 139-147 (2019).
- Clark, A. M., et al. A microphysiological system model of therapy for liver micrometastases hhs public access. Experimental Biology and Medicine (Maywood). 239 (9), 1170-1179 (2014).
- Qosa, H., Ribeiro, A. J. S., Hartman, N. R., Volpe, D. A. Characterization of a commercially available line of iPSC hepatocytes as models of hepatocyte function and toxicity for regulatory purposes. Journal of Pharmacological and Toxicological Methods. 110, 107083 (2021).

