5.1:
Pressione e misurazione della pressione
5.1:
Pressione e misurazione della pressione
La pressione del gas è causata dalla forza esercitata da molecole di gas che si scontrano con le superfici degli oggetti. Sebbene la forza di ogni collisione sia molto piccola, qualsiasi superficie di un’area apprezzabile sperimenta un gran numero di collisioni in breve tempo, il che può causare alta pressione.
In generale, la pressione è definita come la forza esercitata su una data area:
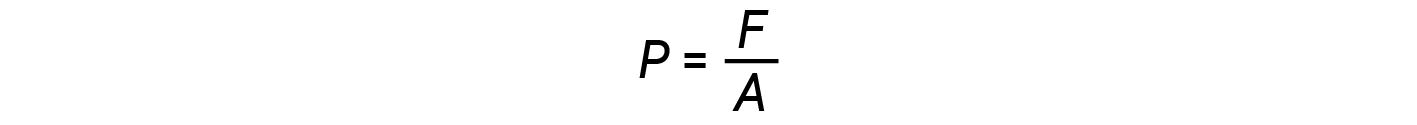
La pressione è direttamente proporzionale alla forza e inversamente proporzionale all’area. Pertanto, la pressione può essere aumentata aumentando la quantità di forza o diminuendo l’area su cui viene applicata; pressione può essere diminuita diminuendo la forza o aumentando l’area.
L’unità di pressione SI è il pascal (Pa), con 1 Pa = 1 N/m2, dove N è il newton, un’unità di forza definita come 1 kg·m/s2. Un pascal è una piccola pressione; in molti casi, è più conveniente utilizzare unità di kilopascal (1 kPa = 1000 Pa) o bar (1 bar = 100.000 Pa). La pressione può anche essere misurata utilizzando l’atmosfera unitaria (atm).
Pressione di misura
La pressione atmosferica, la forza esercitata dall’atmosfera sulla superficie terrestre, viene misurata con un barometro. Un barometro è un tubo di vetro che viene chiuso ad un’estremità, riempito con un liquido non volontario, come il mercurio, e quindi invertito e immerso in un contenitore di quel liquido. L’atmosfera esercita pressione sul liquido all’esterno del tubo, la colonna di liquido esercita pressione all’interno del tubo e la pressione sulla superficie liquida è la stessa all’interno e all’esterno del tubo. L’altezza del liquido nel tubo è quindi proporzionale alla pressione esercitata dall’atmosfera.
Nel barometro, il mercurio è la scelta preferita rispetto all’acqua, poiché è 13,5 volte più denso dell’acqua. La pressione atmosferica può sostenere una colonna di mercurio alta solo circa 0,760 m, mentre una colonna d’acqua dovrebbe essere alta 10,3 m. Questo rende una colonna di mercurio un modo conveniente per misurare la pressione.
La pressione atmosferica standard di 1 atm al livello del mare (101.325 Pa) corrisponde a una colonna di mercurio alta circa 760 mm. La pressione esercitata da un fluido a causa della gravità è nota come pressione idrostatica, p:
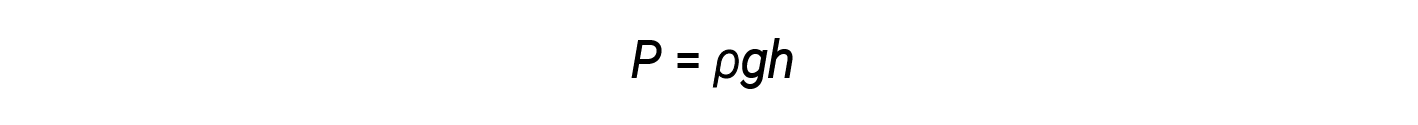
dove h è l’altezza del fluido, ρ è la densità del fluido, e g è l’accelerazione dovuta alla gravità.
Un manometro è un dispositivo utilizzato per misurare la pressione di un gas intrappolato in un contenitore. Un manometro chiuso è un tubo a forma di U con un braccio chiuso, un braccio che si collega al gas da misurare e mercurio nel mezzo. La distanza tra i livelli di liquido nei due bracci del tubo, h, è proporzionale alla pressione del gas nel contenitore. In un manometro open-end, un braccio del tubo è aperto all’atmosfera. In questo caso, la distanza tra i livelli di liquido corrisponde alla differenza di pressione tra il gas nel contenitore e l’atmosfera.
Questo testo è adattato da Openstax, Chimica 2e, Sezione 9.1: Pressione del gas.
