Caracterização dos Efeitos de recombinação em uma Câmara de ionização líquido usado para a dosimetria de um Acelerador Radiosurgical
Summary
Um número cada vez maior de dispositivos de terapia de radiação oferecem a vantagem de proporcionar a dose muito pequenas através de vigas para o tumor, permitindo uma maior conformidade e doses mais altas por fracção. Muitos detectores diferentes pode ser usado para a dosimetria desses pequenos campos. No presente estudo, o efeito da recombinação de iões é investigada para uma câmara de ionização líquida, usando um sistema de radioterapia estereotáxica.
Abstract
A maioria dos modernos dispositivos de terapia de radiação permite a utilização de muito pequenas áreas, ou através de terapia de radiação beamlets Intensidade Modulada (IMRT) ou através de radioterapia estereotáxica, onde a precisão de posicionamento permite a entrega de doses muito elevadas por fracção num pequeno volume do paciente. Medições dosimétricas em aceleradores médicos são convencionalmente realizado utilizando câmaras de ionização com ar. No entanto, em pequenos feixes estes estão sujeitos aos efeitos de perturbação nonnegligible. Este estudo centra-se em câmaras de ionização líquidos, que oferecem vantagens em termos de resolução espacial e baixa perturbação influência. Efeitos de recombinação de íons são investigados pelo detector microLion (PTW) usado com o sistema Cyberknife (Accuray). O método consiste na realização de uma série de medições do tanque de água a diferentes distâncias fonte de superfície, e a aplicação de correcções para as leituras de detectores líquidas à base de medições simultâneas detectores gasosos. Esta abordagem facilitadortes isolando os efeitos de recombinação decorrentes da alta densidade do meio sensível líquido e obtenção de fatores de correção para aplicar às leituras do detector. A principal dificuldade reside na obtenção de um nível suficiente de precisão na configuração de ser capaz de detectar pequenas mudanças na resposta de câmara.
Introduction
Dosimetria em radioterapia foi realizada utilizando câmaras de ionização gasosos por muitos anos. Estes detectores de bom desempenho, tanto quanto a terapia de radiação "convencional" está em causa, isto é, grandes campos homogéneos (ou lentamente variável) são usadas. No entanto, muitos dispositivos recentes, tais como a Cyberknife (Figura 1) do sistema estudados neste trabalho, oferecem a possibilidade de utilização de campos muito pequenos (abaixo de 5 mm). Outros dispositivos produzir perfis feixe altamente modulados, como em Intensidade Modulada Radioterapia (IMRT). Detectores cheios de ar convencionais não estão bem adequados para estas técnicas 1; , a fim de alcançar uma resolução espacial aceitável o volume da cavidade teria de ser reduzido a um tamanho em que a resposta câmara iria tornar-se demasiado baixo. Diodos oferecem a vantagem de volumes menores e sensíveis que são amplamente utilizados em pequena dosimetria do feixe. No entanto, eles apresentam outras limitações, tais como efeitos de espalhamentodecorrente da sua blindagem metálica 12,13.
Em uma câmara de ionização líquida 2 (LIC), a densidade de ionização é muito mais elevado e assim é possível a redução do volume sensível, sem comprometer a resposta do detector. Além disso, o meio sensível tem uma densidade próxima da da água, reduzindo as perturbações de fluência associados com uma cavidade de ar. Estes aspectos tornam o LIC um candidato interessante para pequenas feixe dosimetria 3-5.
Há, no entanto, algumas questões a resolver antes de ser capaz de realizar medições de dosimetria de rotina com PBR. Em primeiro lugar, devido a uma densidade de ionização mais elevado dos efeitos de recombinação são mais importantes do que nas câmaras cheias de ar 6-8. A recombinação pode ser inicial (um elétron recombina com seu íon mãe) ou geral (dois íons provenientes de diferentes eventos de ionização recombinar). O último é dependente da taxa de dose incidente no detector; tseus meios que medições de dose relativa (por exemplo, perfis de dose, doses de profundidade percentual, fatores de saída) pode potencialmente sofrer desvios devido à mudança na taxa de dose. Recombinação é caracterizada pela eficiência de recolha geral, definida como a razão entre a carga medida para a carga produzida pela radiação incidente e escapando recombinação inicial: f = Q C / Q 0. Em detectores gasosos efeitos de recombinação são avaliadas utilizando o método de duas tensão a partir da teoria das Boag 9,10, o que não pode ser aplicado em PBR 11.
Uma alternativa pode ser encontrado na utilização do método da taxa de duas doses de 8, que consiste em variar a taxa de dose para isolar a influência de recombinação geral e medir a eficiência de recolha através da relação geral 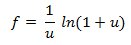
onde u é defined como 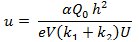
com α sendo o coeficiente de recombinação, Q 0 a quantidade de carga que escapa recombinação inicial, h a separação do eletrodo, E a carga elementar, V o volume sensível da câmara, k 1 e k 2 as mobilidades das cargas positivas e negativas, e L a tensão aplicada. Ao medir a diferentes doses por impulsos, é possível obter o parâmetro de retorno e, portanto, a eficiência de recolha, f. A dose por impulsos é dado pela relação 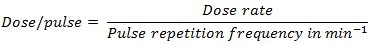
Todas as medições são realizadas nas condições de referência do Cyberknife (fonte-superfície Distância SSD = 78,5 centímetros, 1,5 cm de profundidade, 60 mm colimador). A utilização de um grande alo colimadorws evitando os efeitos de volume associados com pequenos raios. Dada a taxa de dose é de 800 MU / min e a frequência de repetição é de 150 Hz, o que resulta em uma dose de 0,89 mGy / pulso (nas condições de referência, de 1 MU corresponde a uma dose de 1 cGy). Quando a frequência de repetição de pulso é mantida constante, a dose por impulso só depende da taxa de dose de Gy / min, o que está relacionado com o SSD através da lei distância inversa-quadrado: 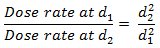
para dois SSDs d 1 e d 2.
Protocol
Representative Results
Discussion
Os métodos apresentados acima permitem avaliar os efeitos de recombinação em um LIC sobre uma grande variedade de doses (0,14-1,58 mGy / pulso). Método A é simples, mas é associado com mais incertezas do que o método B, que fornece valores bastante precisos (e absoluta) de eficiência de coleta, f. A recombinação é responsável pela perda de aproximadamente 2% no sinal em toda a faixa investigada, mas este intervalo é maior do que o que geralmente é medido durante as medições de rotina. O maior erro em um factor de saída é de 0,35%, e atinge 1% para uma medição de dose em profundidade percentagem como foi mostrado na secção de resultados.
O elemento crítico para a realização do protocolo é a configuração inicial da experiência, como todas as medições são realizadas em relação à posição inicial da cabeça de tratamento. Assim, deve-se ter cuidado com a medida exata do SSD inicial para ser capaz de relacionar as leituras do detector para cadadosar por pulso. Isto também é verdadeiro para o posicionamento do detector em água; deve ser tomado cuidado de que o ponto efectivo de medição (situado a 1 mm atrás da janela de entrada, no caso de o detector microLion) está posicionado a 1,5 cm abaixo da superfície. O atraso de 1 hora e a dose pré-irradiação são também essenciais para estabilizar o fornecimento de 800 V e à temperatura.
A taxa de repetição do acelerador linear impacta diretamente a dose por pulso. A 800 MU / min e com uma frequência de 150 Hz, a dose por pulso é 0,89 mGy / pulso. Esta freqüência deve ser fixada para todas as medidas para garantir que a distância é o único fator variável ter uma influência sobre a dose por pulso. O método pode ser utilizado no caso de uma viga contínua com algumas adaptações 7. Em outros dispositivos onde a SSD não pode ser variada movendo directamente a cabeça de tratamento, a taxa de repetição pode ser modificada para introduzir a dose por variação de impulsos. Se este parâmetro éfixo, bem como, o SSD pode ainda ser modificada movendo o PBR e a superfície da água no tanque, mas a exactidão dessa aproximação seria provavelmente mais baixa do que o movimento da cabeça de tratamento utilizado no presente estudo.
O próximo passo na caracterização do LIC para o seu uso em pequenas dosimetria campo é para investigar os outros factores que induzem a perturbação da resposta, tal como os materiais do detector e o efeito do volume (isto é, o facto de que o volume não é sensível pequena em comparação com as dimensões do feixe). Isto é possível através da utilização de simulações de Monte Carlo 5. Com estes aspectos levados em conta factores de correcção global podem ser aplicados para as leituras LIC obtidos nas medições de rotina clínica (factores de saída, doses percentuais de profundidade, perfis de dose), a fim de eliminar completamente as perturbações.
Após a completa caracterização e correção destes efeitos perturbating, tLIC ele pode ser usado como um detector adicional para dosimetria pequeno feixe, permitindo que uma verificação independente dos perfis, as doses percentuais de profundidade e os factores de saída medidos por outros detectores. É muito alta resolução espacial na direção longitudinal também seria adequado para a dosimetria de campos retangulares, com apenas uma pequena dimensão (por exemplo, TomoTherapy.)
Disclosures
The authors have nothing to disclose.
Acknowledgements
Os autores não têm confirmações.
Materials
| MicroLion chamber | PTW | 31018 | http://www.ptw.de/2263.html |
| Unidos Webline dosimeter | PTW | http://www.ptw.de/unidos_webline_dosemeter_rt0.html | |
| HV supply | PTW | http://www.ptw.de/2265.html | |
| MP3 water scanning system | PTW | http://www.ptw.de/2032.html | |
| 0.125 cm3 SemiFlex chamber | PTW | 31010 | http://www.ptw.de/semiflex_chambers0.html?&cId=6069 |
| Cyberknife | Accuray |
References
- Das, I. J., Din, G. X., Ahnesjö, A. Small fields: non-equlibrium radiation dosimetry. Med. Phys. 35 (1), 206-215 (2008).
- Wickmann, G., Nystrom, H. The use of liquids in ionization chambers for high precision radiotherapy dosimetry. Phys. Med. Biol. 37 (9), 1789-1812 (1992).
- Chung, E., Soisson, E., Seuntjens, J. Dose homogeneity specification for reference dosimetry of nonstandard fields. Med. Phys. 39 (1), 407-414 (2011).
- Francescon, P., Kilby, W., Satariano, N., Cora, S. Monte Carlo simulated correction factors for machine specific reference field dose calibration and output factor measurement using fixed and iris collimators on the Cyberknife system. Phys. Med. Biol. 57 (12), 3741-3758 (2012).
- Wagner, A., Crop, F., Lacornerie, T., Vandevelde, F., Reynaert, N. Use of a liquid ionization chamber for stereotactic radiotherapy dosimetry. Phys. Med. Biol. 58 (8), 2445-2459 (2013).
- Johansson, B., Wickman, G., Bahar-Gogani, J. General collection efficiency for liquid iso-octane and tetramethylsilane in pulsed radiation. Phys. Med. Biol. 42 (10), 1929-1938 (1997).
- Andersson, J., Tölli, H. Application of the two-dose-rate method for general recombination correction for liquid ionization chambers in continuous beams. Phys. Med. Biol. 56 (2), 299-314 (2010).
- Sjgren, R., Wendelsten, M. A two-dose-rate method for general recombination correction for liquid ionization chambers in pulsed beams. Phys. Med. Biol. 55 (15), 4247-4260 (2010).
- Boag, J. W. Ionization measurements at very high intensities: part I. Pulsed radiation beams. Br. J. Radiol. 23 (274), 601-611 (1950).
- Boag, J. W. The saturation curve for ionization measurements in pulsed radiation beams. Br. J. Radiol. 25 (300), 649-650 (1952).
- Stewart, K. J., Elliott, A., Seuntjens, J. P. Development of a guarded liquid ionization chamber for clinical dosimetry. Phys. Med. Biol. 52 (11), 3089-3104 (2007).
- Yin, Z., Hugtenburg, R. P., Beddoe, H. Response corrections for solid-state detectors in megavoltage photon dosimetry. Phys. Med. Biol. 49 (11), 3691-3702 (2004).
- Griessbach, I., Lapp, M., Bohsung, J., Gademann, G., Harder, D. Dosimetric characteristics of a new unshielded silicon diode and its application in clinical photon and electron beams. Med. Phys. 32, 3750-3754 (2005).
- . . Accuray Inc., Physics Essentials Guide P/N 032515A-ENG. Accuray Inc. , (2010).

