次世代シーケンシングのフルレングスの HIV-1 Proviruses 近くの増幅
Summary
潜在性の決定の増幅とフルレングス (そのまま、欠陥) HIV-1 の proviruses の近くの 1 つのシーケンスに効率的かつ高スループット方法を提供でき、フルレングス個々 プロウイルス シーケンス (反転)レプリケーション能力。反転は、潜在的な HIV 1 貯水池をシーケンス処理する設計されています以前の試金の限界を克服します。
Abstract
フルレングス個々 プロウイルス シーケンス (反転) アッセイはフルレングス (そのまま、欠陥)、HIV-1 の proviruses の近くの 1 つのシーケンスを増幅しに設計されている効率的かつ高スループット方法。反転では、統合された hiv-1 細胞集団内の遺伝的組成の決定ことができます。有害な停止コドン/超変異、フレーム シフト突然変異および代理要素 cis 諸国における突然変異/削除が必要な大規模な内部の削除など、逆のトランスクリプションの間に起こる HIV 1 プロウイルス シーケンス内の欠陥を識別してウイルス粒子成熟の反転は、統合 proviruses 複製することができないを識別できます。反転法は、これらの欠陥がない、したがって潜在的レプリケーション主務 HIV-1 proviruses を識別するために利用できます。反転のプロトコル: HIV-1 感染細胞の換散は、フルレングスの HIV-1 proviruses 近くの PCR を入れ子になった (HIV 1 5 を対象としたプライマーを使用して ‘ と 3’ LTR)、DNA 精製と定量、ライブラリの準備のため次世代シーケンス (NGS)、NGS、プロウイルス コンティグとレプリケーション主務 proviruses を識別するための簡単な消去法のde novoアセンブリ。反転は、シーケンスに設計された従来の方法上の利点統合単一プロウイルス シーケンスなどの HIV-1 proviruses を提供します。反転増幅未定、複製能力を有効にフルレングスの proviruses 近くのシーケンスし、も少ない増幅プライマー、プライマーの不一致の結果を防止を使用します。反転特に潜在貯留層内での統合の HIV-1 proviruses の遺伝的風景を理解するための便利なツール、ただし、その利用を統合された hiv-1 遺伝的組成が必要である、任意のアプリケーションに拡張できます。
Introduction
長期的な抗レトロ ウイルス療法 (ART) の個人で解決しない、潜在的な HIV 1 貯水池の遺伝学的解析が統合された proviruses の大半の欠陥と複製無能な1を理解することが重要されています。,2。 統合プロウイルス順序逆のトランスクリプションのプロセス中にエラーが発生します。欠陥プロウイルスのシーケンスを生成するいくつかのメカニズムは、間違いやすい 1 HIV 逆転写酵素酵素34、および/または APOBEC 誘起超変異5,6の切り替えテンプレート。二最近の研究が発見した遺伝子そのまま潜在的レプリケーション有能な長期的なアートの個人から分離された HIV-1 proviruses の約 5%、HIV 1 血中アートの停止時の急回復に貢献するかもしれない1,2,7. 以前の研究は、レプリケーション主務の HIV-1 proviruses が世間知らずとは別のメモリー cd4 陽性で存続することを識別した+ T 細胞サブセット (中央、経過とエフェクター メモリー T 細胞を含む) の重要性を示すこれらをターゲット細胞将来的に撲滅戦略2,8,9です。
早い洞察力分布、動態と潜在 HIV 1 貯水池の維持を実現した HIV 1 ゲノム10 のサブ ゲノム領域の遺伝的特性を示す単一プロウイルス シーケンス (SPS) 法の活用、11,12,13。SPS は、単一 HIV 1 provirus からの 1 つの感染した細胞をシーケンスすることができる汎用性の高いツールです。ただし、SPS ではそれだけ系列のプライマー結合部位内で大きな欠失を含むサブ ゲノム領域とミスの proviruses proviruses のレプリケーション能力を特定できません。前の研究は、SPS がによるレプリケーション有能な貯留層のサイズを過大評価を実証して 13 〜 17 倍を介して選択的にそのままサブ ゲノム領域2のシーケンスします。
SPS、Hoらの制限に対処するため4ブルーナーら1は、フルレングスの HIV-1 proviruses 近くのシーケンスにアッセイを開発しました。これは決定する長期的なアートの個人の遺伝子そのままと潜在的レプリケーション主務の HIV-1 proviruses の周波数を許可しました。これらの試金は増幅し、塩基配列 (サンガーを介してシーケンス) 取得 (そのまままたは欠陥) のシーケンス HIV 1 provirus 組み立てられた、サブ ゲノムの領域。このアプローチの 3 つの制限: 1) 複数配列のプライマーの使用が誤ってプロウイルスのシーケンスに欠陥を導入するリスクを増加し、2) プライマーの不一致は、増幅を防ぐことができます特定の proviruses と 3) は、しばしば、プロウイルス シーケンス全体は、これらのメソッドの専門性のため解決できません。
既存のフルレングス HIV 1 プロウイルス シーケンス試金の制限を克服するためにFull –Length私個々Proviral Sequencing (反転) アッセイを開発しました。反転は次世代シーケンサー (NGS)-ベースのアッセイを増幅し、高スループットかつ効率的にフルレングス (そのまままたは不良) HIV-1 の proviruses に近いシーケンスします。反転前の試金、上の利点を提供は、プライマーが使用数が制限したがって、プライマーを proviruses の人口を制限する可能性があります不一致キャプチャまたは誤ってウイルス シーケンスに欠陥が生じる可能性が低くなります。反転前の試金よりより少なく技術的に難しいもとメインの手順を 6: 1) 換散の HIV-1 感染細胞、2) nested pcr 法の限界希釈の非常に節約された特異的なプライマーで実行を介して単一の HIV-1 proviruses の増幅HIV-1 5′ と 3′ U5 LTR 地域 (図 1 a)、3) 浄化と 4 増幅産物の定量) NGS、5 のため増幅された proviruses の図書館準備) NGS、6) それぞれのコンティグを取得するシーケンス proviruses のde novoアセンブリ個々 の provirus。
反転から生成される系列は、遺伝子そのままと潜在的レプリケーション主務 (図 1)2であるそれらを識別して除去の厳格なプロセスを受けることができます。そのまま遺伝子 proviruses は、複製無能な provirus 生成の結果すべての既知の欠陥を欠いています。これらの欠陥があります: 5′ 信号または主要な包装の変異や frameshifts、超変異/有害な停止コドンとなる大規模な内部削除反転シーケンス スプライス ドナー (MSD) のサイト。
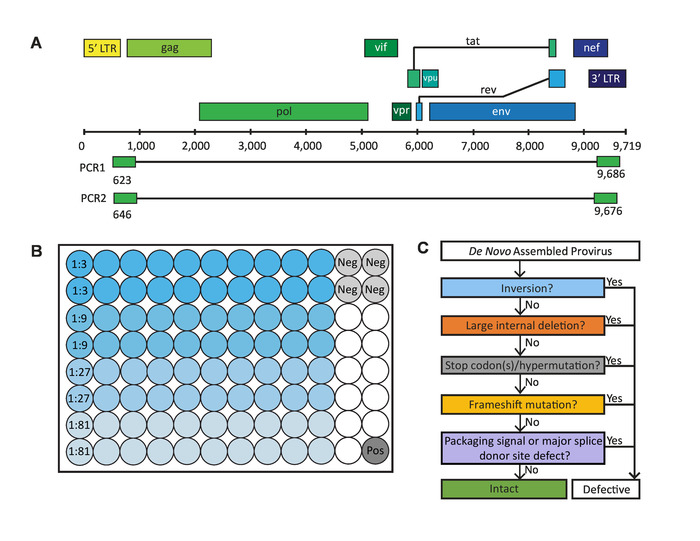
図 1: フルレングス個々 プロウイルス シーケンス (反転) アッセイで重要な手順です。(A) HIV 1 DNA ゲノム nested pcr 法によるフルレングス (欠陥とそのまま) HIV-1 proviruses 近く増幅に反転で使用する 5′ と 3′ の U5 LTR 地域のプライマー結合部位を持つ。(B) 80 サンプル井戸 (各希釈用 20 井戸)、4 のネガティブ コントロール井戸 1 肯定的な制御をも含む 96 ウェル PCR プレートのレイアウト。(C) 遺伝子そのままと潜在的レプリケーション主務の HIV-1 proviruses を識別するために使用される除去のプロセスです。この図は、Hienerらから変更されています。2.この図の拡大版を表示するのにはここをクリックしてください。
Protocol
Representative Results
Discussion
反転アッセイは、増幅し、シーケンス シングル、フルレングスの HIV-1 proviruses 近くの効率的かつ高スループット方法です。複数の要因とプロトコル数と得られるシーケンスの質に影響を与える重要な手順は、識別されています。まず、セル数、セルの人口の HIV-1 感染頻度増幅 proviruses の数に影響します。たとえば、前の文書約半分として多くのシーケンスの+ T ナイーブ cd4 陽性の同じ数から得られた細胞エフェクター メモリー CD4 と比較して+ T 細胞。ナイーブ細胞通常エフェクター記憶細胞2より低い感染頻度があるためにです。第二に、セル換散抽出プロセスの DNA を失うリスクがないゲノム DNA を取得する列を用いた抽出メソッドをお勧めします。最後に、任意の pcr アッセイと汚染を防止するは、重要です。ポジティブ コントロール、DNA の浄化と定量化、およびライブラリの準備の追加ゲノムの DNA の処理、マスター ミックスを準備するため分離クリーン エリアを指定必要があります。これは、ここに示してなどシングル コピーの試金のため特に重要です。
反転法の実装は、参加者のサンプルではなく、pNL4 3 プラスミドなど肯定的な制御を実行しているを含める必要があります最初。これは HIV 1 肯定的な細胞の使用に任意のトラブルシューティングの前の得られるシーケンスは、これらのプラスミッドのための利用可能な参照の配列と比較することとなります。1 HIV 陽性細胞を使用すると、ほとんどない proviruses が増幅される場合 hiv-1 サブタイプ (フリップが B のサブタイプに固有のために設計したプライマー) および細胞集団の感染頻度を考慮することが重要です。プライマー シーケンスは、他のサブタイプを一致するように変更/再設計することができます。さらに、肯定的な制御を含んでいるもが実行ごとの PCR に含まれます。
反転は、SPS を含む、以前のシーケンス試金の制限を克服しています。増幅とフルレングスの HIV-1 proviruses 近くのシーケンス、反転は、HIV-1 の proviruses の潜在的な複製能力を判断できます。これは SPS のみサブ ゲノム領域をシーケンスし、したがってそのままプライマー結合部位とシーケンスの選択を使用して可能ではなかった。さらに、反転は、以前フルレングス シーケンス試金1,4で採用された複数の増幅と配列のプライマーを利用しながらに関連付けられている制限を克服します。PCR NGS と組み合わせて HIV 1 LTR 地域の 2 回は、フリップは、数と必要なプライマーの複雑さを減少します。反転はプライマーの不一致、すなわち欠陥 proviruses の誤同定と集団内のいくつかの proviruses を増幅することができないことの結果を受けにくいため。反転プロトコルも効率的であり、シーケンスの前の方法よりもの高いスループットを実現できます。
明らかに、反転は、HIV-1 proviruses の遺伝的組成を決定する既存の方法上の利点を提供します。ただし、反転の限界を認識することが重要です。まず、反転法は開発されていない潜在的な HIV 1 貯蔵所のサイズを測定するためのツールとして反転増幅すべて HIV 1 provirus 細胞集団内に存在かどうかを決定するための解析が完了するいないと。反転は代わりに異なる細胞集団2間貯留層の組成の相対的な比較を行うために役立ちます。第二に、そのまま HIV-1 proviruses のレプリケーション能力は体内の分析では、Hoらによって実行されるものなどを行わなければ確実性を特定できません。4. 第三に、反転は、HIV-1 proviruses の統合サイトを決定する設計されていません。
反転プロトコルへのマイナーな変化は、そのアプリケーションを増やすことができます。たとえば、シーケンスが異なるできるプライマーで増幅し、塩基配列に複数の hiv-1 サブタイプ変更します。プラズマ 1 HIV ウイルス粒子の配列は、nested pcr 法の前に cDNA 合成添加を介して可能です。単一分子配列方法の将来利用de novoアセンブリの必要性がなくなります。
統合の HIV-1 proviruses の遺伝子配列は、潜在的な HIV 1 貯水池の私達の理解を増加しています。反転は、組成と潜在的な貯留層の分布の解明、将来の研究のための重要なツールです。ただし、反転のアプリケーションは、貯水池を超えて拡張することができます。将来の研究利用 CRISPR Cas 技術は、特定のターゲットを判断したり、コーディングの識別を支援する反転とウイルスにより逆にエージェントの待機時間に対応する非コーディングの地域。ウイルスゲノム組換えは、大きな内部欠失のジャンクション サイト見てによってよりよく理解可能性があります。
Disclosures
The authors have nothing to disclose.
Acknowledgements
この作品が支持された (1U19AI096109 および 1UM1AI126611-01) の治療法を見つけるにデラニー エイズ研究企業 (あえて)amfAR HIV 撲滅 (ARCHE) 共同研究助成 (amfAR 108074-50-RGRL); エイズ研究財団からの研究コンソーシアムオーストラリア センター HIV や肝炎ウイルスの研究 (ACH2);UCSF GIVI センター エイズ研究 (P30 AI027763);オーストラリア国立保健医療研究審議会 (AAP1061681)。博士ジョーイ ライ、ウエストミード ライブラリの準備および彼の施設の使用の彼の訓練のための医学研究所ゲノム施設マネージャー、ゲノミクス (大学のニュー ・ サウス ・ ウェールズ、シドニー、オーストラリア) の Ramaciotti センターに感謝したいと思いますシーケンスを行う。我々 はこの研究のサンプルを寄付者に感謝の気持ちで認めます。
Materials
| UltraPure 1 M Tris-HCI, pH 8.0 | Invitrogen | 15568025 | Dilute to 5 mM for nested PCR |
| Nonidet P 40 Substitute solution | Sigma | 98379 | |
| Tween-20 | Sigma | P9416 | |
| Proteinase K Solution (20 mg/mL) | Promega | AM2548 | |
| 96 well thermocycler | Any 96 well thermocycler can be used | ||
| Platinum Taq DNA Polymerase High Fidelity | Invitrogen | 11304011 | |
| 10X High Fidelity Buffer [600 mM Tris-SO4 (pH 8.9), 180 mM (NH4)2SO4] | Invitrogen | 11304011 | |
| 50 mM MgSO4 | Invitrogen | 11304011 | |
| PCR Nucleotide Mix, 10 mM | Promega | C1141 | |
| Ultrapure H2O | Invitrogen | 10977023 | |
| PCR1 and PCR2 Primers | Desalted. Dilute to (100 M) with H2O | ||
| PCR Plate 96 Well, Half Skirt, Single Notch Corner, Clear | Axygen | PCR-96M2-HS-C | |
| Microseal 'B' Adhesive Seals | BioRad | MSB1001 | Required to seal 96 well PCR plates |
| HIV-1 NL4-3 Infectious Molecular Clone (pNL4-3) | The following reagent was obtained through the NIH AIDS Reagent Program, Division of AIDS, NIAID, NIH: HIV-1 NL4-3 Infectious Molecular Clone (pNL4-3) from Dr. Malcolm Martin (Cat# 114). | Diluted to 10^5 copies/mL and used as positive control | |
| PCR plate spinner or benchtop centrifuge | |||
| E-GEL 48 1% Agarose | Invitrogen | G800801 | Precast 1% agarose gels (two gels used per 96 well plate). Any 1% agarose gel can be substituted. Contains ethidium bromide. |
| DirectLoad Wide Range DNA Marker | Sigma | D7058 | Any ladder with a range up to 10 kb can be substituted |
| Mother E-Base device | Invitrogen | EBM03 | Required for running precast 48 well 1% agarose gels |
| Gel Doc EZ Gel Documentation System | BioRad | 1708270 | Any visualisation system for ethidium bromide containing agarose gels can be used |
| PlateMax Peelable Heat Sealing | Axygen | HS-200 | Heat sealing film for long term storage |
| 96 Well 0.8 mL Storage Plate | ThermoFisher Scientific | AB0765 | 0.8 mL 96 well plate required for magnetic bead based PCR purification |
| Agencourt AMPure XP (PCR purification kit) | Beckman Coulter | A63880 | Magnetic bead based PCR purification kit. Other PCR purification kits can be substitued here (e.g. QIAquick PCR Purification Kit (Qiagen Cat#28106) |
| Ethyl alcohol, Pure. 200 proof, for molecular biology | Sigma | E7023 | |
| Magnetic Stand-96 | Invitrogen | AM10027 | |
| Microplate shaker | Optional | ||
| Buffer EB | Qiagen | 19086 | Elution buffer |
| Quant-iT PicoGreen dsDNA Assay Kit | Invitrogen | P11496 | A fluorescence based stain for measuring dsDNA concentration |
| Microplate reader | |||
| Nextera XT DNA Library Preparation Kit | Illumina | FC-131-1096 | |
| Nextera XT Index Kit | Illumina | FC-131-2001 | |
| Hard-Shell 96-Well PCR Plates | Biorad | HSP9601 | Required for Nextera XT DNA library preparation kit |
| Library Quantification Kit – Illumina/Universal | Kapa Biosystems | KK4824 | Other library quantification kits can be substitued (e.g. JetSeq DNA Library Quantification Lo-Rox Kit (Bioline Cat#BIO-68029) |
| 2100 Bioanalyzer | Agilent Technology | Automated electrophoresis system . Use in conjunction with a High Sensistivity DNA kit | |
| High Sensistivty DNA kit | Agilent Technology | 5067-4626 | |
| Illumina MiSeq Platform | Illumina |
References
- Bruner, K. M., et al. Defective proviruses rapidly accumulate during acute HIV-1 infection. Nature Medicine. 22 (9), 1043-1049 (2016).
- Hiener, B., et al. Identification of Genetically Intact HIV-1 Proviruses in Specific CD4(+) T Cells from Effectively Treated Participants. Cell Reports. 21 (3), 813-822 (2017).
- Abram, M. E., Ferris, A. L., Shao, W., Alvord, W. G., Hughes, S. H. Nature, position, and frequency of mutations made in a single cycle of HIV-1 replication. Journal of Virology. 84 (19), 9864-9878 (2010).
- Ho, Y. C., et al. Replication-competent noninduced proviruses in the latent reservoir increase barrier to HIV-1 cure. Cell. 155 (3), 540-551 (2013).
- Harris, R. S., et al. DNA deamination mediates innate immunity to retroviral infection. Cell. 113 (6), 803-809 (2003).
- Lecossier, D., Bouchonnet, F., Clavel, F., Hance, A. J. Hypermutation of HIV-1 DNA in the absence of the Vif protein. Science. 300 (5622), 1112 (2003).
- Chun, T. W., et al. Rebound of plasma viremia following cessation of antiretroviral therapy despite profoundly low levels of HIV reservoir: implications for eradication. AIDS. 24 (18), 2803-2808 (2010).
- Chomont, N., et al. HIV reservoir size and persistence are driven by T cell survival and homeostatic proliferation. Nature Medicine. 15 (8), 893-900 (2009).
- Soriano-Sarabia, N., et al. Quantitation of replication-competent HIV-1 in populations of resting CD4+ T cells. Journal of Virology. 88 (24), 14070-14077 (2014).
- Josefsson, L., et al. The HIV-1 reservoir in eight patients on long-term suppressive antiretroviral therapy is stable with few genetic changes over time. Proceedings of the National Academy of Sciences USA. 110 (51), E4987-E4996 (2013).
- Evering, T. H., et al. Absence of HIV-1 evolution in the gut-associated lymphoid tissue from patients on combination antiviral therapy initiated during primary infection. Public Library of Science Pathogens. 8 (2), e1002506 (2012).
- von Stockenstrom, S., et al. Longitudinal Genetic Characterization Reveals That Cell Proliferation Maintains a Persistent HIV Type 1 DNA Pool During Effective HIV Therapy. Journal of Infectious Diseases. 212 (4), 596-607 (2015).
- Palmer, S., et al. Multiple, linked human immunodeficiency virus type 1 drug resistance mutations in treatment-experienced patients are missed by standard genotype analysis. Journal of Clinical Microbiology. 43 (1), 406-413 (2005).
- . CLC Genomics Version 10 Available from: https://www.qiagenbioinformatics.com/products/clc-genomics-workbench (2018)
- . FastQC: a quality control tool for high throughput sequence data Available from: https://www.bioinformatics.babraham.ac.uk/projects/fastqc/ (2010)
- Bolger, A. M., Lohse, M., Usadel, B. Trimmomatic: a flexible trimmer for Illumina sequence data. Bioinformatics. 30 (15), 2114-2120 (2014).
- Martin, M. Cutadapt removes adapter sequences from high-throughput sequencing reads. EMBnet.journal. 17 (1), (2011).
- Magoc, T., Salzberg, S. L. FLASH: fast length adjustment of short reads to improve genome assemblies. Bioinformatics. 27 (21), 2957-2963 (2011).
- Langmead, B., Salzberg, S. L. Fast gapped-read alignment with Bowtie 2. Nature Methods. 9 (4), 357-359 (2012).
- Bankevich, A., et al. SPAdes: a new genome assembly algorithm and its applications to single-cell sequencing. Journal of Computational Biology. 19 (5), 455-477 (2012).
- Kumar, S., Stecher, G., Tamura, K. MEGA7: Molecular Evolutionary Genetics Analysis Version 7.0 for Bigger Datasets. Molecular Biology and Evolution. 33 (7), 1870-1874 (2016).
- Katoh, K., Standley, D. M. MAFFT multiple sequence alignment software version 7: improvements in performance and usability. Molecular Biology and Evolution. 30 (4), 772-780 (2013).
- . HIV Sequence Database – Gene Cutter tool Available from: https://www.hiv.lanl.gov/content/sequence/GENE_CUTTER/cutter.html (2018)
- Foster, J. L., Garcia, J. V. Role of Nef in HIV-1 replication and pathogenesis. Advances in Pharmacology. 55, 389-409 (2007).
- . HIV Sequence Database – Consensus Maker tool Available from: https://www.hiv.lanl.gov/content/sequence/CONSENSUS/consensus.html (2018)
- . HIV Sequence Database – Hypermut tool Available from: https://www.hiv.lanl.gov/content/sequence/HYPERMUT/hypermut.html (2018)
- Yu, G., Smith, D. K., Zhu, H., Guan, Y., Lam, T. T. Y. ggtree: an r package for visualization and annotation of phylogenetic trees with their covariates and other associated data. Methods in Ecology and Evolution. , (2016).

