Protein Topografya Değişikliklerinin Belirlenmesinde Proteinlerin Hızlı Fotokimyasal Oksidasyonlarında Gerçek Zamanlı Telafinin Sağlanması
Summary
Proteinlerin hızlı fotokimyasal oksidasyonu proteinlerin yapısal karakterizasyonu için ortaya çıkan bir tekniktir. Farklı solvent katkı maddeleri ve ligandlar çeşitli hidroksil radikal atma özelliklerine sahiptir. Farklı koşullarda protein yapısını karşılaştırmak için reaksiyonda oluşan hidroksil radikallerinin gerçek zamanlı telafisi reaksiyon koşullarını normalleştirmek için gereklidir.
Abstract
Proteinlerin hızlı fotokimyasal oksidasyonu (FPOP), proteinlerin çözücüye erişilebilen yüzey alanını araştıran kütle spektrometresi temelli yapısal biyoloji tekniğidir. Bu teknik, amino asit yan zincirlerin çözeltide serbestçe difüzyon olan hidroksil radikalleri ile reaksiyonuna dayanır. FPOP hidrojen peroksit lazer fotolizi ile yerinde bu radikalleri oluşturur, bir mikrosaniye sırasına göre tükenmiş hidroksil radikallerin bir patlama oluşturma. Bu hidroksil radikalleri bir çözücü erişilebilir amino asit yan zincir ile reaksiyona girdiğinde, reaksiyon ürünleri ölçülebilir ve kütle spektrometresi ile ölçülen ve ölçülen bir kütle kayması sergiler. Bir amino asitin reaksiyon oranı kısmen o amino asitin ortalama çözücü erişilebilir yüzeyine bağlı olduğundan, bir proteinin belirli bir bölgenin oksidasyon miktarındaki ölçülen değişiklikler, farklı konformasyonlar arasındaki bölgenin çözücü erişilebilirliğindeki değişikliklerle doğrudan ilişkili olabilir (örn. ligand bağlı vs. ligand-vs. agrega, monomer vs. agrega, vb.) FPOP biyolojide protein-protein etkileşimleri, protein konformasyonel değişiklikleri ve protein-ligand bağlanması gibi bir dizi sorunda uygulanmıştır. Hidroksil radikallerinin mevcut konsantrasyonu FPOP deneyindeki birçok deneysel koşula bağlı olarak değiştiğinden, protein analitinin maruz kaldığı etkili radikal dozu izlemek önemlidir. Bu izleme, FPOP reaksiyonundan gelen sinyali ölçmek için sıralı bir dosimetre nin biraraya gelmesiyle etkin bir şekilde sağlanır ve istenilen miktarda oksidasyon elde etmek için gerçek zamanlı olarak ayarlanmış lazer fluence ile sağlanır. Bu kompansasyon ile, protein topografyasında konformasyonel değişiklikleri, ligand-bağlayıcı yüzeyleri ve/veya protein-protein etkileşim arayüzlerini yansıtan değişiklikler nispeten düşük örneklem miktarları kullanılarak heterojen örneklerde belirlenebilir.
Introduction
Proteinlerin hızlı fotokimyasal oksidasyonu (FPOP), proteinlerin solvente maruz kalan yüzey alanının ultra hızlı kovalent modifikasyonu ve ardından LC-MS1tarafından saptanması ile protein topografik değişikliklerinin belirlenmesinde ortaya çıkan bir tekniktir. FPOP hidrojen peroksit UV lazer flaş fotoliz ihda hidroksil radikallerin yüksek konsantrasyon üretir. Bu hidroksil radikalleri çok reaktif ve kısa ömürlü, FPOP koşulları altında kabaca bir mikrosaniye zaman ölçeğinde tüketilen2. Bu hidroksil radikalleri su yoluyla yayılır ve genellikle hızlı (~106 M-1 s-1)difüzyon kontrollü3arasında değişen kinetik oranlarda çözelti çeşitli organik bileşenleri okside . Hidroksil radikal bir protein yüzeyi karşılaştığında, radikal protein yüzeyinde amino asit yan zincirleri okside edecek, bu amino asit bir kitle kayması ile sonuçlanan (en yaygın bir oksijen atomunun net eklenmesi)4. Herhangi bir amino asit oksidasyon reaksiyonu oranı iki faktöre bağlıdır: bu amino asit doğal reaktivite (yan zincir ve dizi bağlamına bağlıdır)4,5 ve difüzyon hidroksil radikal bu yan zincirin erişilebilirlik, hangi yakından ortalama ortalama çözücü erişilebilir yüzey alanı ile ilişkilidir6,7. Glisin dışındaki tüm standart amino asitler, fpop deneylerinde bu son derece reaktif hidroksil radikalleri tarafından etiketlenmiş olarak gözlenmiştir, çok farklı verimde de olsa; uygulamada, Ser, Thr, Asn ve Ala nadiren yüksek radikal dozlar altında dışında çoğu örnekte oksitlenmiş olarak görülür ve dikkatli ve hassas hedefli ETD parçalanma8,,9ile tanımlanır. Oksidasyondan sonra, hidrojen peroksit ve sekonder oksidanları (süperoksit, tek oksijen, peptidil hidroperoksitler vb.) çıkarmak için numuneler söndürülür. Söndürülen numuneler daha sonra oksitlenmiş peptidlerin karışımlarını oluşturmak için proteolytically sindirilir, burada yapısal bilgiler çeşitli peptidlerin oksidasyon ürünlerinin desenlerinde kimyasal bir “anlık” olarak dondurulur(Şekil 1). Kütle spektrometresi (LC-MS) ile birleşen sıvı kromatografisi, bu peptidin okside ve oksitlenmemiş versiyonlarının göreceli yoğunluklarına göre belirli bir proteolitik peptiddeki amino asitlerin oksidasyon miktarını ölçmek için kullanılır. Farklı konformasyonel koşullar altında elde edilen aynı proteinin bu oksidatif ayak izini karşılaştırarak (örn. ligand bağlı karşı ligand-free), proteinin belirli bir bölgenin oksidasyon miktarındaki farklılıklar doğrudan o bölgenin solvent erişilebilir yüzey alanında farklılıklar ile ilişkili olabilir6,7. Protein topografik bilgi sağlamak için yeteneği FPOP proteinlerin yüksek sıralı yapı belirlenmesi için cazip bir teknoloji yapar, protein terapötik keşif ve geliştirme dahil10,11.
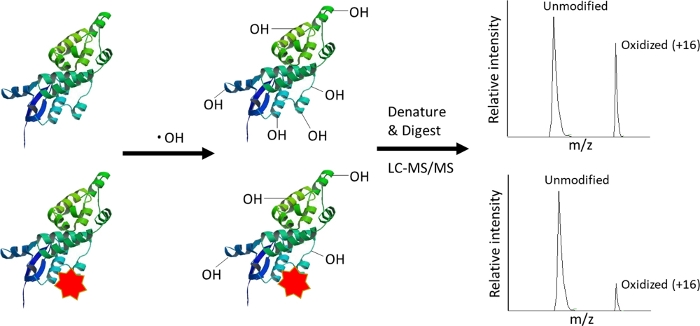
Şekil 1: FPOP’a genel bakış. Proteinin yüzeyi son derece reaktif hidroksil radikalleri tarafından kovalent olarak modifiye edilir. Hidroksil radikalleri kuvvetle yan zincirin solvent erişilebilirlik etkilenir bir oranda proteinamino asit yan zincirleri ile tepki verecektir. Topografik değişiklikler (örneğin, yukarıda gösterildiği gibi bir ligand bağlanması nedeniyle) hidroksil radikalleri ile reaksiyona etkileşim bölgesinde amino asitler koruyacak, LC-MS sinyalinde modifiye peptit yoğunluğunda bir azalmaya neden. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
FPOP çözeltisinde bulunan farklı bileşenler (örn. ligandlar, eksipiyanlar, tamponlar) hidrojen peroksit3’ünlazer fotolizisi üzerine üretilen hidroksil radikallerine karşı farklı atma aktivitesine sahiptir. Benzer şekilde, peroksit konsantrasyonu küçük bir değişiklik, lazer fluence, ve tampon kompozisyon etkili radikal dozu değiştirebilir, örnekler arasında ve farklı laboratuvarlar arasında zorlu FPOP verilerinin çoğaltılması yapma. Bu nedenle, birkaç mevcut hidroksil radikal doz12,,13,1412,,15,16kullanarak her örnekte protein ile reaksiyona mevcut hidroksil radikal dozu karşılaştırmak mümkün olması önemlidir. Hidroksil radikal dosimetreler hidroksil radikalleri havuzu için analit (ve çözelti tüm çöpçüler ile) ile rekabet ederek hareket; hidroksil radikallerin etkin dozu dozimetreoksidasyon miktarı ölçülerek ölçülür. “Etkili hidroksil radikal doz” hidroksil radikal üretilen ilk konsantrasyonu ve radikal yarı ömrü hem de bir fonksiyonu olduğunu unutmayın. Bu iki parametre kısmen birbirine bağımlı dır ve teorik kinetik modellemeyi biraz karmaşık hale getirirler(Şekil 2). İki örnek, oluşan hidroksil radikalin ilk konsantrasyonunu değiştirerek aynı etkili radikal dozu korurken çılgınca farklı ilk radikal yarı yaşamlara sahip olabilir; onlar hala aynı ayak izleriüretecek 17. Adenin13 ve Tris12 uygun hidroksil radikal dozimetrelerdir çünkü oksidasyon düzeyleri UV spektroskopisi ile gerçek zamanlı olarak ölçülebiliyor, bu da araştırmacıların etkili hidroksil radikal dozda bir sorun olduğunda hızlı bir şekilde belirlemelerine ve problemlerini çözmelerine olanak sağlıyor. Bu sorunu çözmek için, akış sisteminde bulunan ve ışınlama bölgesinden hemen sonra bulunan ve adenin emicilik değişikliklerinden gelen sinyali gerçek zamanlı olarak izleyebilen bir sıralı dosimetre önemlidir. Bu tamponlar veya hidroksil radikal atma kapasitesi17geniş ölçüde farklı seviyelerde başka bir eksipiyan FPOP deneyleri yürütülmesinde yardımcı olur. Bu radikal doz telafisi gerçek zamanlı olarak yapılabilir, etkili radikal doz ayarlayarak aynı konformer için istatistiksel olarak ayırt edilemez sonuçlar veren.
Bu protokolde, bir iç optik radikal dosimetre olarak adenin kullanarak radikal dozaj telafisi ile tipik bir FPOP deney icra etmek için ayrıntılı prosedürler var. Bu yöntem, araştırmacıların gerçek zamanlı olarak tazminat gerçekleştirerek farklı atma kapasitesine sahip FPOP koşulları arasında ayak izlerini karşılaştırmalarına olanak tanır.
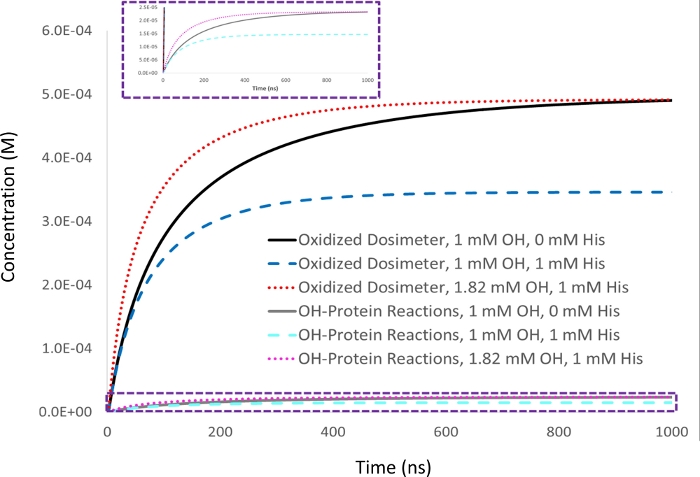
Şekil 2: Dozimetri bazlı kompanzasyonun kinetik simülasyonu. 1 mM adenin dosimetre yanıtı 5 mm ilk hidroksil radikal konsantrasyonu (▪OH t t1/2=53 ns) ile 5 μM lizozim analyit cinsinden ölçülür ve hedef dosimetre yanıtı (siyah) olarak ayarlanır. 1 mM’lik ekskavatif histidin eklenmesi yle, dosimetre yanıtı (mavi) protein oksidasyonu miktarı ile birlikte orantılı bir şekilde azalır (siyan. Hidroksil radikalinin yarı ömrü de azalır (▪OH t1/2=39 ns). Üretilen hidroksil radikal miktarı, 1 mM histidin çöpçü ile numunede oksidasyonlu dosimetrenin eşdeğer verimini vermek için arttırıldığında, çöpçü (kırmızı) yokluğunda 1 mM hidroksil radikal ile elde edilen protein oksidasyonu miktarı benzer şekilde aynı hale gelirken (macenta), hidrosil radikal yarı ömrü daha da azalır (▪OH t1/2=29 n9). Sharp J.S., Am Pharmaceut Rev 22, 50-55, 2019 izniyle uyarlanmıştır. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Protocol
Representative Results
Discussion
Hidrojen-döteryum değişimi, kimyasal çapraz bağlama, kovalent etiketleme ve yerli sprey kütle spektrometresi ve iyon hareketliliği gibi kütle spektrometresi tabanlı yapısal teknikler, esneklikleri, duyarlılıkları ve karmaşık karışımları idare etme yetenekleri nedeniyle hızla popülerlik kazanmıştır. FPOP kütle spektrometresi tabanlı yapısal teknikler alanında popülaritesini artırdı çeşitli avantajlara sahiptir. Çoğu kovalent etiketleme stratejileri gibi, çoğu post-labeling süreçleri …
Disclosures
The authors have nothing to disclose.
Acknowledgements
Biz Ulusal Genel Tıp Bilimleri Enstitüsü hibe R43GM125420-01 bir benchtop FPOP cihaz ve R01GM127267 yüksek enerjili FPOP için standardizasyon ve dozimetre protokollerinin geliştirilmesi için ticari gelişimini desteklemek için araştırma finansmanı kabul ediyoruz.
Materials
| Adenine | Acros Organics | 147440250 | Soluble in water upto 3.5 mM |
| Aperture | Edmund Optics | 39-905 | 1000 μm Aperture Diameter, Gold-Plated Copper Aperture |
| Aperture holder | Edmund Optics | 53-287 | 25.8mm Outer Diameter, Precision Pinhole Mount |
| Catalse | Sigma Aldrich | C-40 | Catalase from bovine liver, lyophilized powder, ≥10,000 units/mg protein |
| COMPex Pro laser | Coherent | 1113836 | COMPexPRO 102, F-Vversion, KrF laser, No XeCl |
| Dithiotheitol (DTT) | Promega | V3151 | DTT, Molecular Grade (DL-Dithiothreitol) |
| Fraction collector | GenNext Technologies, Inc. | N/A | Automated fraction collector |
| Fused silica capillay | Molex | 1068150023 | Polymicro Flexible Fused Silica Capillary Tubing, Inner Diameter 100 µm, Outer Diameter 375 µm, TSP100375 |
| Glutamine | Acros Organics | 119951000 | L(+)-Glutamine, 99% |
| Holder for lens | Edmund Optics | 03-668 | 53 mm Outer Diameter, Three-Screw Adjustable Ring Mount |
| Hydrogen peroxide | Fisher Scientific | H325-100 | Hydrogen Peroxide, 30% (Certified ACS), Fisher Chemical |
| LC-MS/MS system | Thermo Scientific | IQLAAEGAAPFADBMBCX | Dionex Ultimate 3000 coupled to Orbitap Fusion Tribrid mass spectrometer |
| Mas spec grade Acetonitrile | Fisher Scientific | A955-1 | Acetonitrile, Optima LC/MS Grade, Fisher Chemical |
| Mass spec grade formic acid | Fisher Scientific | A117-50 | Formic Acid, 99.0+%, Optima™ LC/MS Grade, Fisher Chemical |
| Mass spec grade water | Fisher Scientific | W6-4 | Water, Optima LC/MS Grade, Fisher Chemical |
| MES buffer | Sigma Aldrich | M0164 | MES hemisodium salt |
| Methionine amide | Bachem | 4000594.0005 | H-met-NH2.HCl |
| Micro V clamp | Thor Labs | VK250 | Micro V-clamp with stainless steel blades |
| Motorized stage | Edmund Optics | 68-638 | 50mm Travel Motorized Stage System with Manual Control |
| Nano C18 colum | Thermo Scientific | 164534 | Acclaim PepMap 100 C18 HPLC Columns |
| Optical bench | Edmund Optics | 56-935 | 18" x 18" breadboard |
| Pioneer FPOP Module System | GenNext Technologies, Inc. | N/A | Inline FPOP Radical Dosimetry System |
| Post holder | Edmund Optics | 58-979 | 3" Length, ¼-20 Thread, Post Holder |
| Sodium phosphate dibasic | Fisher Scientific | BP331-500 | Sodium Phosphate Dibasic Heptahydrate (Colorless-to-White Crystals), Fisher BioReagents |
| Sodium phosphate monobasic | Fisher Scientific | BP330-500 | Sodium Phosphate Monobasic Monohydrate (Colorless-to-white Crystals), Fisher BioReagents |
| Syringe | Hamilton | 81065 | 100 µL, Model 1710 RN SYR, Small Removable NDL, 22s ga, 2 in, point style 3 |
| Syringe pump | KD Scientific | 788101 | Legato 101 syringe pump |
| Trap C18 column | Thermo Scientific | 160454 | Thermo Scientific Acclaim PepMap 100 C18 HPLC Columns |
| Tris | Sigma Aldrich | 252859 | Tris(hydroxymethyl)aminomethane |
| Trypsin | Promega | V5111 | Sequencing Grade Modified Trypsin |
| UV plano convex lens | Edmund Optics | 84-285 | 30 mm Dia. x 120 mm FL Uncoated, UV Plano-Convex Lens |
References
- Kaur, P., Kiselar, J., Yang, S., Chance, M. R. Quantitative protein topography analysis and high-resolution structure prediction using hydroxyl radical labeling and tandem-ion mass spectrometry (MS). Molecular & Cellular Proteomics. 14 (4), 1159-1168 (2015).
- Hambly, D. M., Gross, M. L. Laser flash photolysis of hydrogen peroxide to oxidize protein solvent-accessible residues on the microsecond timescale. Journal of the American Society for Mass Spectrometry. 16 (12), 2057-2063 (2005).
- Buxton, G. V., Greenstock, C. L., Helman, W. P., Ross, A. B. Critical review of rate constants for reactions of hydrated electrons, hydrogen atoms and hydroxyl radicals (·OH/·O- in Aqueous Solution. Journal of Physical and Chemical Reference Data. 17 (2), 513 (1988).
- Xu, G., Chance, M. R. Radiolytic modification and reactivity of amino acid residues serving as structural probes for protein footprinting. Analytical Chemistry. 77 (14), 4549-4555 (2005).
- Sharp, J. S., Tomer, K. B. Effects of anion proximity in peptide primary sequence on the rate and mechanism of leucine oxidation. Analytical Chemistry. 78 (14), 4885-4893 (2006).
- Huang, W., Ravikumar, K. M., Chance, M. R., Yang, S. Quantitative mapping of protein structure by hydroxyl radical footprinting-mediated structural mass spectrometry: a protection factor analysis. Biophysical Journal. 108 (1), 107-115 (2015).
- Xie, B., Sood, A., Woods, R. J., Sharp, J. S. Quantitative protein topography measurements by high resolution hydroxyl radical protein footprinting enable accurate molecular model selection. Scientific Reports. 7 (1), 4552 (2017).
- Li, Z., et al. High structural resolution hydroxyl radical protein footprinting reveals an extended Robo1-heparin binding interface. Journal of Biological Chemistry. 290 (17), 10729-10740 (2015).
- Li, X., et al. Structural analysis of the glycosylated intact HIV-1 gp120-b12 antibody complex using hydroxyl radical protein footprinting. Biochemistry. 56 (7), 957-970 (2017).
- Li, K. S., Shi, L., Gross, M. L. Mass spectrometry-based fast photochemical oxidation of proteins (FPOP) for higher order structure characterization. Accounts of Chemical Research. 51 (3), 736-744 (2018).
- Li, J., Chen, G. The use of fast photochemical oxidation of proteins coupled with mass spectrometry in protein therapeutics discovery and development. Drug Discovery Today. 24 (3), 829-834 (2019).
- Roush, A. E., Riaz, M., Misra, S. K., Weinberger, S. R., Sharp, J. S. Intrinsic buffer hydroxyl radical dosimetry using Tris(hydroxymethyl)aminomethane. Journal of the American Society for Mass Spectrometry. 31 (2), 169-172 (2020).
- Xie, B., Sharp, J. S. Hydroxyl radical dosimetry for high flux hydroxyl radical protein footprinting applications using a simple optical detection method. Analytical Chemistry. 87 (21), 10719-10723 (2015).
- Niu, B., Zhang, H., Giblin, D., Rempel, D. L., Gross, M. L. Dosimetry determines the initial OH radical concentration in fast photochemical oxidation of proteins (FPOP). Journal of the American Society for Mass Spectrometry. 26 (5), 843-846 (2015).
- Niu, B., et al. Incorporation of a reporter peptide in FPOP compensates for adventitious scavengers and permits time-dependent measurements. Journal of the American Society for Mass Spectrometry. 28 (2), 389-392 (2017).
- Garcia, N. K., Sreedhara, A., Deperalta, G., Wecksler, A. T. Optimizing hydroxyl radical footprinting analysis of biotherapeutics using internal standard dosimetry. Journal of the American Society for Mass Spectrometry. 31 (7), 1563-1571 (2020).
- Sharp, J. S., Misra, S. K., Persoff, J. J., Egan, R. W., Weinberger, S. R. Real time normalization of fast photochemical oxidation of proteins experiments by inline adenine radical dosimetry. Analytical Chemistry. 90 (21), 12625-12630 (2018).
- Zhang, B., Cheng, M., Rempel, D., Gross, M. L. Implementing fast photochemical oxidation of proteins (FPOP) as a footprinting approach to solve diverse problems in structural biology. Methods. 144, 94-103 (2018).
- Konermann, L., Stocks, B. B., Czarny, T. Laminar flow effects during laser-induced oxidative labeling for protein structural studies by mass spectrometry. Analytical Chemistry. 82 (15), 6667-6674 (2010).
- Gau, B. C., Sharp, J. S., Rempel, D. L., Gross, M. L. Fast photochemical oxidation of protein footprints faster than protein unfolding. Analytical Chemistry. 81 (16), 6563-6571 (2009).
- Li, K. S., et al. Hydrogen-Deuterium exchange and hydroxyl radical footprinting for mapping hydrophobic interactions of human bromodomain with a small molecule Inhibitor. Journal of the American Society for Mass Spectrometry. 30 (12), 2795-2804 (2019).
- Espino, J. A., Jones, L. M. Illuminating biological interactions with in vivo protein footprinting. Analytical Chemistry. 91 (10), 6577-6584 (2019).
- Charvatova, O., et al. Quantifying protein interface footprinting by hydroxyl radical oxidation and molecular dynamics simulation: application to galectin-1. Journal of the American Society for Mass Spectrometry. 19 (11), 1692-1705 (2008).
- Gau, B., Garai, K., Frieden, C., Gross, M. L. Mass spectrometry-based protein footprinting characterizes the structures of oligomeric apolipoprotein E2, E3, and E4. Biochemistry. 50 (38), 8117-8126 (2011).
- Gau, B. C., Chen, J., Gross, M. L. Fast photochemical oxidation of proteins for comparing solvent-accessibility changes accompanying protein folding: Data processing and application to barstar. Biochimica et Biophysica Acta. 1834 (6), 1230-1238 (2013).
- Garrison, W. M. Reaction mechanisms in the radiolysis of peptides, polypeptides, and proteins. Chemical Reviews. 87 (2), 381-398 (1987).
- Xu, G., Chance, M. R. Radiolytic modification of sulfur-containing amino acid residues in model peptides: fundamental studies for protein footprinting. Analytical Chemistry. 77 (8), 2437-2449 (2005).
- Xu, G., Chance, M. R. Radiolytic modification of acidic amino acid residues in peptides: probes for examining protein-protein interactions. Analytical Chemistry. 76 (5), 1213-1221 (2004).
- Xu, G., Takamoto, K., Chance, M. R. Radiolytic modification of basic amino acid residues in peptides: probes for examining protein-protein interactions. Analytical Chemistry. 75 (24), 6995-7007 (2003).
- Misra, S. K., Orlando, R., Weinberger, S. R., Sharp, J. S. Compensated hydroxyl radical protein footprinting measures buffer and excipient effects on conformation and aggregation in an adalimumab biosimilar. AAPS Journal. 21 (5), 87 (2019).
- Simmons, D. A., Konermann, L. Characterization of transient protein folding intermediates during myoglobin reconstitution by time-resolved electrospray mass spectrometry with on-line isotopic pulse labeling. Biochemistry. 41 (6), 1906-1914 (2002).
- Vahidi, S., Konermann, L. Probing the time scale of FPOP (fast photochemical oxidation of proteins): radical reactions extend over tens of milliseconds. Journal of the American Society for Mass Spectrometry. 27 (7), 1156-1164 (2016).
- Chance, M. R. Unfolding of apomyoglobin examined by synchrotron footprinting. Biochemical and Biophysical Research Communications. 287 (3), 614-621 (2001).
- Xu, G., Chance, M. R. Hydroxyl radical-mediated modification of proteins as probes for structural proteomics. Chemical Reviews. 107 (8), 3514-3543 (2007).
- Zhang, Y., Rempel, D. L., Zhang, H., Gross, M. L. An improved fast photochemical oxidation of proteins (FPOP) platform for protein therapeutics. Journal of the American Society for Mass Spectrometry. 26 (3), 526-529 (2015).
- Cornwell, O., Radford, S. E., Ashcroft, A. E., Ault, J. R. Comparing hydrogen deuterium exchange and fast photochemical oxidation of proteins: a structural characterisation of wild-type and ΔN6 β(2)-microglobulin. Journal of the American Society for Mass Spectrometry. 29 (2), 2413-2426 (2018).
- Xie, B., Sharp, J. S. Relative Quantification of sites of peptide and protein modification using size exclusion chromatography coupled with electron transfer dissociation. Journal of the American Society for Mass Spectrometry. 27 (8), 1322-1327 (2016).
- Srikanth, R., Wilson, J., Vachet, R. W. Correct identification of oxidized histidine residues using electron-transfer dissociation. Journal of Mass Spectrometry. 44 (5), 755-762 (2009).
- Li, X., Li, Z., Xie, B., Sharp, J. S. Improved identification and relative quantification of sites of peptide and protein oxidation for hydroxyl radical footprinting. Journal of the American Society for Mass Spectrometry. 24 (11), 1767-1776 (2013).
- Li, X., Li, Z., Xie, B., Sharp, J. S. Supercharging by m-NBA Improves ETD-Based Quantification of Hydroxyl Radical Protein Footprinting. Journal of the American Society for Mass Spectrometry. 26 (8), 1424-1427 (2015).
- Khaje, N. A., Sharp, J. S. Rapid quantification of peptide oxidation isomers from complex mixtures. Analytical Chemistry. 92 (5), 3834-3843 (2020).

