En modell membran plattform for rekonstituere mitokondrie membran dynamikk
Summary
Mitokondriefusjon er en viktig homeostatisk reaksjon underliggende mitokondriedynamikk. Beskrevet her er et in vitro rekonstitueringssystem for å studere mitokondrie indre membran fusjon som kan løse membran tethering, docking, hemifusjon, og pore åpning. Allsidigheten til denne tilnærmingen i å utforske cellemembransystemer diskuteres.
Abstract
Mitokondriedynamikk er avgjørende for organelles ulike funksjoner og cellulære reaksjoner. Den overfylte, romlig komplekse, mitokondriemembranen er et utfordrende miljø for å skille regulatoriske faktorer. Eksperimentell kontroll av protein- og lipidkomponenter kan bidra til å svare på spesifikke spørsmål om regulering. Likevel er kvantitativ manipulering av disse faktorene utfordrende i cellulære analyser. For å undersøke den molekylære mekanismen for mitokondrier indre membranfusjon introduserte vi en in vitro rekonstitueringsplattform som etterligner lipidmiljøet i mitokondrie indre membran. Her beskriver vi detaljerte trinn for å forberede lipid bilayers og rekonstituere mitokondriemembranproteiner. Plattformen tillot analyse av mellomprodukter i mitokondrie indre membranfusjon, og kinetikken for individuelle overganger, på en kvantitativ måte. Denne protokollen beskriver fabrikasjon av bilayers med asymmetrisk lipidsammensetning og beskriver generelle hensyn for rekonstituering av transmembraneproteiner til en polstret bilayer. Metoden kan brukes til å studere andre membransystemer.
Introduction
Membran compartmentalization er et kjennetegn på eukaryotiskeceller 1 (Figur 1A). Biologiske membraner blir i økende grad anerkjent som mer enn et todimensjonalt løsningsmiddel, og regnes som et miljø som spiller kritiske roller i å regulere proteinfunksjon og makromolekylær kompleksmontering 2,,3. Innfødte lipider er ligands som regulerer membranproteinaktivitet3,4. Membran romlig organisasjon og evnen til membraner som skal skulptureres i ulike former er viktige fysiske egenskaper for å velge nyefunksjoner 3,5.
Modell membran plattformer er biomimetiske systemer som kan hjelpe oss å forstå cellulær membranstruktur, dynamikk,og funksjon 6,7,8. Modellmembraner består vanligvis av en lipidblanding av veldefinert sammensetning, med definerte biofysiske egenskaper (stivhet, tykkelse og elastisitet). Sammenlignet med fluorescens bildebehandling, modell membran plattformer tillate kvantitativ analyse av membranstruktur og funksjon 9,10,11. Lipid bilayer rekonstitueringsstrategier har blitt brukt til å studere SNARE-mediert membranfusjon9,,10,DNA-mediert membranfusjon12og viralfusjon 11,,13. En fordel med slike metoder er potensialet til å få kinetisk informasjon for mellomliggende trinn før en observerbar reaksjonshendelse14.
Plasmamembranen har blitt grundig studert ved hjelp av modellmembraner. Bilayers med lipid fase separasjon er utviklet for å studere lipid flåte strukturer viktig i cellulær signalisering11,,15,,16. Mikropatterned lipid planar bilayers17,18 har blitt brukt til å undersøke organiseringen av cellereseptorer. Polymer- eller gelstøttede membraner har blitt brukt som biomimetiske systemer for å studere membran-cytoskeleton-organisasjonen, membranproteinpartisjonering under cellesignalering og migrasjon ved cellecellekontakter19.
Kunstige membransystemer brukes også til å studere subcellulære organeller20. Organeller har karakteristiske morfologier som skaper distinkte undermiljøer. Den endoplasmaiske reticulum (ER) nettverk er ett eksempel. Ved rekonstituering av reticulons til liposomer dannes rørformede membranstrukturer med egenskaper som ligner på cellulære ER21. Tilsetning av atlastin, et ER fusion protein, kan indusere lipid tubuli fra liposomer for å danne et nettverk20. Dette er et eksempel på hvordan proteoliposomer kan gi funksjonell innsikt i organelle morfologi og dynamikk.
Mitokondriemembranfusjon og fisjon er avgjørende for helsen til mitokondriepopulasjonen22,23,,24,,25., Et sett med dynaamin familie GTPases katalyserer mitokondrier membran fusjon. Mfn 1/2 katalyserer ytre membranfusjon. Opa1 medierer indremembranfusjon 26 (figur 1B). Opa1 har to former: en lang form (l-Opa1), transmembrane-forankret til mitokondrie indre membran, og en “løselig” kortform (s-Opa1), tilstede i mellommembrane rommet. Forholdet mellom de to Opa1-skjemaene reguleres av aktiviteten til to proteaser, Oma1 og Yme1L27,,28,,29,,30. Viktige spørsmål i Opa1 regulering inkluderer: hvordan de to formene for Opa1, (kort og lang) megle membran fusjon og deres regulatoriske samspill28,,29,,31,,32,,33.
Her beskriver vi en rekonstitueringsstrategi som ble brukt til å undersøke mitokondrie indre membranfusjon som klargjorde rollene til l- og s-Opa1 i indre membranfusjon. Vi utviklet en plattform som etterlignet mitokondrie indre membran ved hjelp av en polymer-bundet lipid bilayer og 200 nm unilamellar vesikler. Fordelene med en polymer tether under lipid bilayer inkluderer følgende. For det første bevarer det rekonstituerte transmembraneproteinet, som ellers kan bli forstyrret av nærheten til glasslysbildet34. For det andre tjener det et tykt vannlag mellom lipid bilayer og glasssubstrat, noe som letter studier av poreåpning9, og for det tredje tillater viskoelastisk natur peg polymer membran krumningendringer 35. Vi brukte tre-farge fluorescens imaging å karakterisere trinn i membran fusjon (Figur 1C-F).
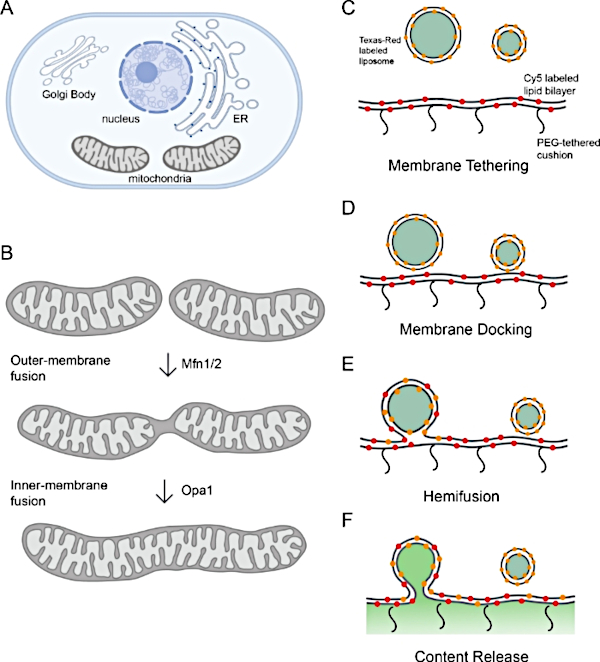
Figur 1: Overvåking av mitokondriemembranfusjon.
Organellerer cellulære membranrom. (B)Sekvensielle trinn av mitokondriemembranfusjon. Fusjon av den ytre membranen av mitokondrier er katalysert av Mfn1 og/ eller Mfn2, mens indre membranfusjon er mediert av Opa1. (C-F) Skjematisk av in vitro rekonstitueringsplattformen for å studere mitokondriemembranfusjon. Plattformen inneholder to deler: en proteoliposom og en polymer-bundet lipid bilayer, begge med rekonstituert l-Opa1. Fluorescerende etiketter, inkludert to forskjellige fluorescerende membranfargestoffer og en innholdsmarkør, bidrar til å skille trinn under membranfusjon. De to membranmarkørene (Cy5-PE (rød) og TexasRed PE (oransje) lager et FRET-par, som kan rapportere om tett membrandokking. Diffusjon av TexasRed-PE som merker proteoliposome er en indikator på lipid demixing (hemifusjon). Innholdsutgivelse overvåkes gjennom dequenching av calcein signalet (vist i grønt). Panel A og B opprettet ved hjelp av Biorender. Vennligst klikk her for å se en større versjon av denne figuren.
Protocol
Representative Results
Discussion
In vitro modell-membransystemer kan beskrive komplekse membranprosesser under veldefinerte forhold. Disse systemene kan skille mellom minimale komponenter som er nødvendige for komplekse molekylære prosesser for å avdekkemolekylære mekanismer 6,,15,,20,,38. For membranproteiner er liposomer og planarstøttede bilayers vanlige rekonstitueringssystemer. I motsetning til solid-støttet lipid bilayers, polymer pute mellom substratet og støttet membran i polymer-bundet bilayers tillater fri mobilitet av store membranproteiner, og transmembran-proteiner å diffuse og montere fritt34. Disse funksjonene hjalp oss med å undersøke kinetikken til mitokondrier indre membranfusjon36.
Vi utarbeidet en polymer-bundet lipid bilayer ved hjelp av Langmuir-Blodgett / Langmuir-Schaefer (LB / LS) teknikker. Dette gjør at vi kan forberede en bilayer med asymmetriske lipidkomponenter. Cellulære membraner har asymmetrisk brosjyresammensetning, og LB / LS-tilnærmingen tillater studiet av slike bilayers. Med Schaefer-overføring kan et helt glasssubstrat dekkes av en lipid bilayer. Det er viktig å forberede en ren overflate for bilayer forberedelse. I tillegg kreves det praksis å utføre en Schaefer-overføring riktig. Mislykket Schaefer overføring kan skape uønskede defekter i en lipid bilayer. I denne protokollen gjelder trykket som legges til filmbalansen for en bilayer som inneholder 20% kardiolipin. For bilayers med andre komponenter, se overflaten trykk-området isotherm av de viktigste komponentene. En alternativ metode er Langmuir-Blodgett / vesicle fusion (LB / VF) metoden, hvor bunnen lipid monolayer overføres fra luft-vann grensesnittet til en Langmuir trau på et rent substrat, deretter liposomer sikring til toppen av støttet lipid monolayer og danner den endelige bilayer39. Rekonstituering av membranproteiner ved hjelp av LB/VF-metoden er enklere enn LB/LS, da rekonstituering kan utføres gjennom fusjon av proteoliposomer. Vesikkelfusjon krever imidlertid tilsetning av overflødige liposomer, noe som kan komplisere studiet av membranhendelser avhengig av konsentrasjonsavhengige proteinproteininteraksjoner.
Den vellykkede rekonstituering av transmembraneproteiner i både polymer-bundet lipid bilayers og liposomer i en foretrukket funksjonell orientering er viktig, men vanskelig å håndheve. Eksperimentelle kontroller er nødvendig for å ta hensyn til dette. For polymer-bundet lipid bilayers, er det også viktig å opprettholde integriteten til lipid bilayer under rekonstituering. Overflateaktive konsentrasjoner må holdes relativt lave for å forhindre oppløsning av lipid bilayer, men høy nok til å forhindre denaturation av protein av interesse37,40. Metoden som er beskrevet her er ideell for rekonstituering av membranproteiner for enkeltmolekylstudier, men er ikke nødvendigvis skalerbar for større studier. Overflateaktivt valg er en annen viktig vurdering. Ofte er overflateaktivt middel som brukes til rensing og lagring et godt utgangspunkt. Maksimal konsentrasjon av overflateaktivt middel er vanligvis ~ 200 ganger mindre av CMC36, i et område hvor overflateaktivt middel opprettholder proteinstabilitet og forhindrer proteinaggregasjon, samtidig som integriteten tilmembranen 36. Cocktailer som inneholder 2 eller 3 overflateaktive stoffer kan vurderes. For rekonstituering i liposomer er det ikke nødvendig med lav konsentrasjon av overflateaktivt middel. Imidlertid er overflateaktive konsentrasjoner under CMC å foretrekke å opprettholde jevn størrelse og morfologifordeling for liposomer. For å forhindre lekkasje av innhold fargestoff, er det nødvendig å dialyze mot en fargestoffholdig buffer.
I motsetning til liposomenbaserte fusjonsanalyser, gir plattformen vi etablerte en tilnærming for å undersøke kinetikken til hvert trinn av membranfusjon. Denne metoden gir muligheten til å studere transmembrane fusjonsproteiner under nesten innfødte forhold. Modell membran plattformer kan brukes til å studere membran protein montering og oligomerisering, membran “sculpting”, og protein-lipid interaksjoner av proteiner i subcellulære miljøer, som mitokondrie indre membran. Denne metoden tillater også utforskning av viktige fysiologiske forhold i membran-protein samspillet, for eksempel bilayer sammensetning asymmetri. Rollen som en viktig mitokondrielipid, kardiolipin, i bilayeregenskapene til både liposomer og polymerstøttede bilayers gjenstår å definere. Egenskaper som ionisk styrke, membrantykkelse, membranstivhet, membrankrumning og membranelastisk viskositetsegenskaper kan alle påvirke proteinenes evne til å monteres i spesifikke funksjonelle tilstander. Fremtidige studier kreativt bruker modell membran systemer har potensial til å avdekke nye aspekter av membran protein organisasjon og funksjon.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Forfatterne anerkjenner støtten fra Charles H. Hood Foundation Child Health Research Award og sjenerøs støtte fra Institutt for molekylærbiologi ved Massachusetts General Hospital.
Materials
| 1,2-dioleoyl-sn-glycero-3-phosphoethanolamine-N-(Cyanine 5) | Avanti polar lipid | Cat #: 810335C1mg | membrane fluorescent markers |
| 1,2-dioleoyl-sn-glycero-3-phosphoethanolamine-N-[methoxy(polyethylene glycol)-2000] (ammonium salt) | Avanti Polar lipids | Cat #: 880130P | lipid molecules |
| 1',3'-bis[1,2-dioleoyl-sn-glycero-3-phospho]-glycerol (sodium salt) | Avanti Polar lipids | Cat #: 710335P | lipid molecules |
| 18:1 (Δ9-Cis) PC (DOPC) | Avanti Polar lipids | Cat #: 850375P | lipid molecules |
| 1-palmitoyl-2-oleoyl-sn-glycero-3-phosphoethanolamine | Avanti Polar lipids | Cat #: 850757P | lipid molecules |
| Alexa Fluor 488 Antibody Labeling Kit | ThermoFisher Scientific | A20181 | |
| Amber vial with PTFE liner | Fisher scientific | 14-955-332 | sample vials to keep lipid solutions |
| Calcein | Sigma-Aldrich | Cat #: C0875; PubChem Substance ID: 24892279 | fluorescent dye |
| Chloroform | Fisher scientific | 298-500/ C295-4 | Fisher brand Chloroform is usually quite reliable for lipid works. |
| Concavity slide (1 well) | Electron Microscopy Science | 71878-05 | applied as Schaefer Slide |
| FCS analysis tool | Smith Lab, University of Akron | software tool | |
| Fiji /ImageJ | Fiji | SCR_002285 | software tool |
| Fisherbrand Cover Glasses: Circles | Fisher scientific | 12-545-102 | Cover glass for solid supported lipid bilayers, the item is now discontinued as authors prepared the manuscript. An alternative is Fisher brand premium cover glass with catalog number: 12-548-5M |
| GTP Disodium salt | SIGMA-ALDRICH INC | Cat #: 10106399001 | |
| Langmuir & Langmuir-Blodgett Trough | Biolin Scientifc | KN2002 | |
| L-α-lysophosphatidylinositol (Liver, Bovine) (sodium salt) | Avanti Polar lipids | Cat #: 850091P | lipid molecules |
| Mini Extruder | Avanti Polar lipids | 610020 | |
| n-Dodecyl-β-D-Maltopyranoside | Anatrace | Cat #: D310 25 GM | surfactant for reconstitution |
| n-Octyl-α-D-Glucopyranoside | Anatrace | Cat #: O311HA 25 GM | surfactant for reconstitution |
| PC Membranes 0.2μm | Avanti Polar Lipids | 610006 | |
| Rabbit Anti-Opa1 antibody | NOVUS BIOLOGICALS | Cat #: NBP2-59770 | antibody for Opa1 C-terminal detection |
| Slidebook | Intelligent imaging | RRID: SCR_014300 | software tool |
| Teflon threaded seal tape | Fisher Scientific | NC0636085 | taflon tape for sample storage |
| Texas Red 1,2-Dihexadecanoyl-sn-Glycero-3-Phosphoethanolamine, Triethylammonium Salt (Texas Red DHPE) | ThermoFisher Scientific | Cat #: T1395MP | membrane fluorescent markers |
References
- Sackmann, E., Lipowsky, R., Sackmann, E. Biological membranes architecture and function. Structure and Dynamics of Membranes. 1, 1-63 (1995).
- Rajendran, L., Simons, K. Lipid rafts and membrane dynamics. Journal of Cell Science. 118, 1099-1102 (2005).
- Schink, K. O., Tan, K. W., Stenmark, H. Phosphoinositides in Control of Membrane Dynamics. Annual Review of Cell and Developmental Biology. 32, 143-171 (2016).
- Gu, R. X., Ingolfsson, H. I., de Vries, A. H., Marrink, S. J., Tieleman, D. P. Ganglioside-Lipid and Ganglioside-Protein Interactions Revealed by Coarse-Grained and Atomistic Molecular Dynamics Simulations. Journal of Physical Chemistry B. 121 (15), 3262-3275 (2017).
- Schafer, D. A. Coupling actin dynamics and membrane dynamics during endocytosis. Current Opinion in Cell Biology. 14 (1), 76-81 (2002).
- Chan, Y. H., Boxer, S. G. Model membrane systems and their applications. Current Opinion in Chemical Biology. 11 (6), 581-587 (2007).
- Biswas, K. H., Groves, J. T. Hybrid Live Cell-Supported Membrane Interfaces for Signaling Studies. Annual Reviews in Biophysics. 48, 537-562 (2019).
- Pick, H., Alves, A. C., Vogel, H. Single-Vesicle Assays Using Liposomes and Cell-Derived Vesicles: From Modeling Complex Membrane Processes to Synthetic Biology and Biomedical Applications. Chemical Reviews. 118 (18), 8598-8654 (2018).
- Kiessling, V., Domanska, M. K., Tamm, L. K. Single SNARE-mediated vesicle fusion observed in vitro by polarized TIRFM. Biophysical Journal. 99 (12), 4047-4055 (2010).
- Kiessling, V., et al. Rapid fusion of synaptic vesicles with reconstituted target SNARE membranes. Biophysical Journal. 104 (9), 1950-1958 (2013).
- Yang, S. T., Kiessling, V., Tamm, L. K. Line tension at lipid phase boundaries as driving force for HIV fusion peptide-mediated fusion. Nature Communication. 7, 11401 (2016).
- Rawle, R. J., van Lengerich, B., Chung, M., Bendix, P. M., Boxer, S. G. Vesicle fusion observed by content transfer across a tethered lipid bilayer. Biophysical Journal. 101 (8), 37 (2011).
- Chao, L. H., Klein, D. E., Schmidt, A. G., Pena, J. M., Harrison, S. C. Sequential conformational rearrangements in flavivirus membrane fusion. Elife. 3, 04389 (2014).
- Floyd, D. L., Harrison, S. C., van Oijen, A. M. Analysis of kinetic intermediates in single-particle dwell-time distributions. Biophysical Journal. 99 (2), 360-366 (2010).
- Sezgin, E., Schwille, P. Model membrane platforms to study protein-membrane interactions. Molecular Membrane Biology. 29 (5), 144-154 (2012).
- Ge, Y., Gao, J., Jordan, R., Naumann, C. A. Changes in Cholesterol Level Alter Integrin Sequestration in Raft-Mimicking Lipid Mixtures. Biophysical Journal. 114 (1), 158-167 (2018).
- Dutta, D., Kam, L. C. Micropatterned, multicomponent supported lipid bilayers for cellular systems. Methods in Cell Biology. 120, 53-67 (2014).
- Groves, J., Ferrari, M., Desai, T., Bhatia, S. Supported Lipid Bilayers as Mimics for Cell Surfaces and as Tools in Biotechnology. BioMEMS and Biomedical Nanotechnology. , (2006).
- Shoaib, T., Nalam, P. C., He, Y., Chen, Y., Espinosa-Marzal, R. M. Assembly, Morphology, Diffusivity, and Indentation of Hydrogel-Supported Lipid Bilayers. Langmuir. 33 (28), 7105-7117 (2017).
- Wang, N., Rapoport, T. A. Reconstituting the reticular ER network – mechanistic implications and open questions. Journal of Cell Science. 132 (4), 227611 (2019).
- Powers, R. E., Wang, S., Liu, T. Y., Rapoport, T. A. Reconstitution of the tubular endoplasmic reticulum network with purified components. Nature. 543 (7644), 257-260 (2017).
- Chan, D. C. Fusion and fission: interlinked processes critical for mitochondrial health. Annual Reviews of Genetics. 46, 265-287 (2012).
- Nunnari, J., Suomalainen, A. Mitochondria: in sickness and in health. Cell. 148 (6), 1145-1159 (2012).
- Wai, T., Langer, T. Mitochondrial Dynamics and Metabolic Regulation. Trends in Endocrinology Metabolism. 27 (2), 105-117 (2016).
- Westermann, B. Mitochondrial fusion and fission in cell life and death. Nature Reviews Molecular Cell Biology. 11 (12), 872-884 (2010).
- Chen, H., et al. Mitofusins Mfn1 and Mfn2 coordinately regulate mitochondrial fusion and are essential for embryonic development. Journal of Cell Biology. 160 (2), 189-200 (2003).
- Ishihara, N., Fujita, Y., Oka, T., Mihara, K. Regulation of mitochondrial morphology through proteolytic cleavage of OPA1. EMBO Journal. 25 (13), 2966-2977 (2006).
- Anand, R., et al. The i-AAA protease YME1L and OMA1 cleave OPA1 to balance mitochondrial fusion and fission. Journal of Cell Biology. 204 (6), 919-929 (2014).
- Mishra, P., Carelli, V., Manfredi, G., Chan, D. C. Proteolytic cleavage of Opa1 stimulates mitochondrial inner membrane fusion and couples fusion to oxidative phosphorylation. Cell Metabolism. 19 (4), 630-641 (2014).
- Baker, M. J., et al. Stress-induced OMA1 activation and autocatalytic turnover regulate OPA1-dependent mitochondrial dynamics. EMBO Journal. 33 (6), 578-593 (2014).
- DeVay, R. M., et al. Coassembly of Mgm1 isoforms requires cardiolipin and mediates mitochondrial inner membrane fusion. Journal of Cell Biology. 186 (6), 793-803 (2009).
- Rainbolt, T. K., Lebeau, J., Puchades, C., Wiseman, R. L. Reciprocal Degradation of YME1L and OMA1 Adapts Mitochondrial Proteolytic Activity during Stress. Cell Reports. 14 (9), 2041-2049 (2016).
- Ban, T., et al. Molecular basis of selective mitochondrial fusion by heterotypic action between OPA1 and cardiolipin. Nature Cell Biology. 19 (7), 856-863 (2017).
- Tanaka, M., Sackmann, E. Polymer-supported membranes as models of the cell surface. Nature. 437 (7059), 656-663 (2005).
- Shilts, K., Naumann, C. A. Tunable cell-surface mimetics as engineered cell substrates. Biochimica Biophysica Acta Biomembrane. 1860 (10), 2076-2093 (2018).
- Ge, Y., et al. Two forms of Opa1 cooperate to complete fusion of the mitochondrial inner-membrane. Elife. 9, 50973 (2020).
- Ge, Y., Siegel, A. P., Jordan, R., Naumann, C. A. Ligand binding alters dimerization and sequestering of urokinase receptors in raft-mimicking lipid mixtures. Biophysical Journal. 107 (9), 2101-2111 (2014).
- Simons, K., Vaz, W. L. Model systems, lipid rafts, and cell membranes. Annual Review of Biophysics and Biomolecular Structure. 33, 269-295 (2004).
- Kiessling, V., Liang, B., Tamm, L. K. Reconstituting SNARE-mediated membrane fusion at the single liposome level. Methods in Cell Biology. 128, 339-363 (2015).
- Siegel, A. P., Kimble-Hill, A., Garg, S., Jordan, R., Naumann, C. A. Native ligands change integrin sequestering but not oligomerization in raft-mimicking lipid mixtures. Biophysics Journal. 101 (7), 1642-1650 (2011).

