Platsstyrd φC31-medierad integration och kassettutbyte i Anopheles vektorer av malaria
Summary
Protokollet beskriver hur man uppnår platsstyrda modifieringar i genomet av Anopheles malariamyggor med hjälp av φC31-systemet . De ändringar som beskrivs omfattar både integration och utbyte av transgena kassetter i arvsmassan hos attP-bärande dockningslinjer.
Abstract
Funktionell genomisk analys och relaterade strategier för genetisk kontroll av malaria förlitar sig på validerade och reproducerbara metoder för att exakt modifiera genomet av Anopheles myggor. Bland dessa metoder möjliggör φC31-systemet exakt och stabil platsstyrd integrering av transgener, eller ersättning av integrerade transgena kassetter via rekombinerasmedierat kassettutbyte (RMCE). Denna metod bygger på verkan av Streptomyces φC31 bakteriofagintegras för att katalysera rekombination mellan två specifika fästpunkter som betecknas attP (härlett från fag) och attB (härledd från värdbakterien). Systemet använder en eller två attP-platser som tidigare har integrerats i mygggenomet och attB-platserna i donatormallens DNA. Här illustrerar vi hur man stabilt modifierar genomet av attP-bärande Anopheles dockningslinjer med hjälp av två plasmider: en attB-märkt donator som bär integrations- eller utbytesmallen och en hjälpare plasmid som kodar φC31 integrase. Vi rapporterar två representativa resultat av φC31-medierade plats-riktade modifiering: den enda integrationen av en transgenic kassett i An. stephensi och RMCE i An. gambiae myggor. φC31-medierad genommanipulation erbjuder fördelen med reproducerbara transgene uttryck från validerade, fitness neutrala genomiska platser, vilket möjliggör jämförande kvalitativa och kvantitativa analyser av fenotyper. Integrationens platsstyrda karaktär förenklar också avsevärt valideringen av det enskilda insättningsstället och parningssystemet för att erhålla en stabil transgen linje. Dessa och andra egenskaper gör φC31-systemet till en viktig komponent i den genetiska verktygslådan för transgen manipulation av malariamyggor och andra insektsvektorer.
Introduction
Förmågan att modifiera arvsmassan hos myggvektorer av sjukdomar på ett tillförlitligt och reproducerbart sätt har stärkt in vivo funktionell validering av gener och öppnat dörrarna till realiserbara genetiska vektorkontrollstrategier, till exempel de som riktar sig mot Anopheles myggor som överför malaria1.
Tidig mygggenomredigering förlitade sig enbart på transponerbar element (TE)-medierad omvandling, där piggyBac var den vanligaste transposonen i Anopheles2,3,4. Te-integrationens slumpmässiga karaktär kan dock leda till oönskade modifieringar såsom gen knockouts (insertional mutagenesis) och betydande positionseffekter på transgeneuttryck5,6,7,8. Flera infogningar är också vanliga när du använder piggyBac5,9, vilket gör valideringen och isoleringen av transgena linjer med enstaka infogningar mödosamma. Andra nackdelar inkluderar deras potentiella remobilisering, som observerats i bakterien av Anopheles stephensi när de tillhandahåller en källa till piggyBac transposase10,11,12, och deras begränsade storlek på DNA-last (10-15 kb i längd) med omvandling effektivitet minskar med ökande storlek på givaren plasmid13,14.
Webbplatsstyrda integrationsmetoder infördes för att kringgå dessa frågor. Den vanligaste platsstyrda genommodifieringen hos myggor är den som förmedlas av φC31-systemet (figur 1a). Detta drivs av en viral integras som katalyserar rekombinationen mellan två heterospecific anknytning (att) platser som förekommer naturligt i genomet av bakteriofag φC31 (attP) och i Streptomyces bacterium värd (attB)15. Rekombinationen av de två platserna är enkelriktad och resulterar i bildandet av hybridplatser (attL och attR). Rekombinationen av sådana hybridplatser (som leder till DNA-excision) skulle kräva inte bara närvaron av ett aktivt viralt integras utan också en annan fagerkodad rekombinationsfaktor16,17. En stabil integrationsplats skapas därmed som avlastar frågan om potentiell oönskad remobilisering15. Dessutom gör systemet det möjligt att integrera stora laster (t.ex. integrering av >100 kb-konstruktioner rapporterades i D. melanogaster18), vilket avsevärt ökar bärkapaciteten. Integration sker i en enda fördefinierad genomisk locus som kraftigt förenklar valideringen av insättning och parningssystemet för att erhålla en stabil transgen linje. Slutligen tillåter den platsstyrda karaktären av integrationen normalisering av uttryck eftersom alternativa transgener ligger i samma locus och regleras därför inom samma närliggande genomiska sammanhang. En av de viktigaste tillämpningarna av tekniken är den direkta jämförelsen av fenotyper som ges av olika transgener efter införandet i en identisk locus.
Att uppnå φC31-medierad integration innebär två faser: fas I är skapandet av transgena dockningslinjer som transporterar attP-anläggningar, och fas II är den platsstyrda integrationen av en attB-flankerad last i dockningslinjen19. Skapandet av fas I-dockningslinjer har förlitat sig på te-medierad slumpmässig integration av attP-märkta konstruktioner och därmed involverat en inledande mödosam process (inklusive södra blot och omvända PCR-analyser på en-kvinnliga avkomma) för att isolera och validera transgena linjer som bär en enda integrationshändelse i unika, transkriptionellt aktiva och fitnessneutrala genomiska platser. Ändå har flera dockningslinjer för φC31-medierad enkel integration utvecklats och validerats i An. gambiae19,20,21,22 och i An. stephensi23,24,25 (tabell 1). Var och en av dessa linjer varierar när det gäller dockningsplatsens genomiska läge och den stamspecifika genetiska bakgrunden och från dem kan en stor variation av nya transgena linjer skapas. Den komplexa valideringen av TE-medierade integrationer för tillverkning av dockningslinjer kan nu kringgås med CRISPR/Cas9-tekniken26. Detta förlitar sig dock på a priori kunskap om neutral lokus att vara mål och deras omgivande sekvenser.
φC31-medierad integration har tillämpats i stor utsträckning på insektsgenomredigering från modellorganismen D. melanogaster27, till myggorna Aedes aegypti13,28, Ae. albopictus29, An. gambiae19 och An. stephensi24, liksom andra insekter inklusive Ceratitis capitata30 och Bombyx mori31.
En begränsning av φC31-medierad integration, särskilt med tanke på potentiella fältutsläpp för vektorkontroll, är integrationen i mygggenomet hos hela attB-bärande donatorplasmid, inklusive oönskade sekvenser som genmarkörer för antibiotikaresistens och plasmid stamnätkomponenter av bakteriellt ursprung. För att ta itu med detta genomfördes en ändring av standardsystemet, rekombinerasmedierat kassettutbyte (RMCE), som gör det möjligt att exakt ersätta en tidigare integrerad transgen kassett med ett nytt donator-DNA (figur 1b). Detta uppnås genom att använda två inverterade att platser flankerar donator- och mottagarkassetterna i varje ände, vilket driver två oberoende rekombinationshändelser att äga rum samtidigt som det resulterar i kassettutbyte utan integration av plasmid ryggrad. Denna förbättrade konstruktion kringgår integrationen av oönskade sekvenser och utökar tillämpningen av φC31-system till att till exempel omfatta integrering av omärkta DNA-laster genom screening för förlust av en tidigare integrerad fluorescerande markör32.
RMCE uppnåddes först med D. melanogaster32 och tillämpades senare framgångsrikt på icke-modell insekter inklusive An. gambiae9,26,33, Ae. aegypti34, Plutella xylostella34 och B. mori35. Flera dockningslinjer för RMCE har utvecklats och validerats i An. gambiae5,9,26 (tabell 1). Såvitt vi vet har RMCE ännu inte utforskats i andra Anopheles vektorarter.
Hittills har φC31-systemet använts i stor utsträckning i Anopheles myggor för att introducera och studera en mängd olika molekyler, inklusive antimalaria-effektorer19,24,36, komponenter i GAL4/ UAS-systemet för att överuttrycka och slå ner gener för insekticidresistensstudier9,33, regulatoriska element, reportergener5,21,37 och gendrivelement26 ,38.
Detta protokoll beskriver hur man utför 1) platsstyrd integration av en attB-flankerad last och 2) RMCE av en konstruktion flankerad av inverterade attB-platser i genomet av Anopheles dockningslinjer. Detta uppnås med hjälp av två plasmider: en givaren attB-märkt plasmid som bär transgenen av intresse och en hjälpare plasmid som uttrycker φC31 integrase. De stora malariavektorerna An. gambiae och An. stephensi används som specifika exempel, men dessa protokoll är tillämpliga på andra Anopheles arter.
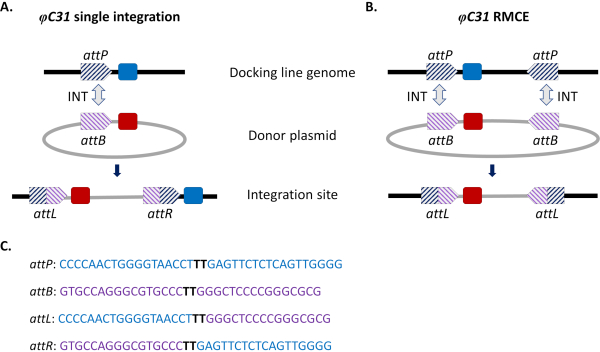
Figur 1. Platsstyrda genomändringar, enkel integrering och rekombinerad kassettutbyte (RMCE) med hjälp av φC31-systemet. φC31 integrase (INT, grå dubbelpil) katalyserar rekombinationen mellan attB-platserna (lila randiga) som finns i en donatorplasmid och attP-platserna (blå randiga) som finns i en mottagningsdockningslinje, vilket resulterar i bildandet av hybridplatser attL och attR. A) Integration uppnås när enstaka attB- och attP-platser kombineras och resulterar i närvaron av två integrerade markörer (blå och röd). B) RMCE inträffar när två attB/P-platser kombineras samtidigt och resulterar i att kassetten byts ut mellan dockningslinjens (blå markör) med den som bärs av donatorplasmiden (röd markör). C) Partiella nukleotidsekvenser av attP (blå) och attB (lila) och hybridplatserna attL/R. Rekombination sker mellan “TT”-kärnsekvenserna markerade i fet svart. Klicka här för att se en större version av den här figuren.
Protocol
Representative Results
Discussion
Den exakta utformningen av attB-märkta plasmider som är kompatibla med dockningslinjen är av största vikt för experimentets framgång. Man måste noga överväga valet av den markör som används för screening av transformanter, inklusive fluorescensfärgen och dess uttrycksmönster, som kommer att omfattas av det mönster som redan finns i dockningslinjen. Det är nödvändigt att använda fluorescerande markörer som är lätta att urskilja: bra markörkombinationer inkluderar RFP (röd)/CFP (cyan), RFP (röd)/GFP (grön), RFP (röd)/YFP (gul) och YFP (gul)/CFP (cyan), medan kombinationer att undvika är YFP (gul)/GFP (grön) och CFP (cyan)/GFP (grön). 3xP3 promotorn39, specifik för ögon och nervsladd, är den vanligaste för att driva uttrycket av fluorescerande markörer för myggtransgenes. Faktum är att alla Anopheles dockningslinjer som för närvarande är tillgängliga använder denna promotor. Alternativa regleringsregioner är den för An. gambiae polyubiquitin genen (PUBc)5 eller viral promotor IE120, som driver uttryck i flera vävnader. När de används tillsammans med 3xP3 skulle dessa promotorer utöka de möjliga färgkombinationerna och till och med användningen av samma fluorofor. De angivna promotorerna är aktiva under hela mygglivscykeln vilket möjliggör screening och fluorescensövervakning i alla livsstadier. En ytterligare faktor vid plasmidkonstruktion är storleken på den last som ska integreras eller bytas ut. Även om φC31-systemet har anmärkningsvärd bärförmåga18, bör det anses att storleken på donatorplasmiden i allmänhet korrelerar negativt med omvandlingseffektiviteten22.
I det beskrivna protokollet är källan till integrase en hjälpare plasmid som uttrycker enzymet allestädes närvarande40. Den allestädes närvarande närvaron av integrasen kan leda till omvandling av somatiska celler om mikroinjektioner inte exakt riktas till det område där könscellerna bildas. Medan sådana omvandlingshändelser kommer att gå förlorade eftersom de inte är ärftliga, kan somatiska effekter minska konditionen hos injicerade individer. För att undvika detta och öka omvandlingseffektiviteten kan integrasuttrycket begränsas till bakterien, till exempel genom att använda vasapromotorn22,26. Andra protokoll beskriver användningen av in vitro transkriberad budbärar-RNA (mRNA) som källa till φC31 integrase19,24,43. Detta innebär dock mödosam förberedelse av mRNA och kräver noggrann hantering av injektionsblandningen och användning av RNase fria reagenser för att undvika nedbrytning. Plasmid källor av integrase har visats i både An. gambiae9,21,22,26,33,37 och An. stephensi (A.A. personlig kommunikation) att vara tillförlitlig och leda till effektiv omvandling, och är därmed vårt föredragna alternativ. Ett annat alternativ för integrase-leverans är dess in vivo-produktion i självdockande hjälplinjer. Sådana linjer skapades i An. gambiae som uttrycker φC31 integrase under regleringen av de bakteriespecifika promotorn nanos och befanns leda till en förbättrad överlevnad och omvandling effektivitet20. Potentiella träningsbelastningar som införs av in vivo-produktionen av integrasenzymet på hjälplinjen måste dock övervägas.
Liksom med andra transgena tekniker måste särskild omsorg förbehållas uppfödning och korsning av individer som härrör från injicerade embryon för att maximera chanserna att återvinna transformanter. Individer som stabilt har ärvt transgenen kan först återvinnas vid G1-avkomman. Tidiga tecken på potentiell omvandling kan dock utvärderas genom förekomsten av transienta episomala uttryck av fluorescerande markör i anal papiller och/eller nerv sladden av G0 första och andra instar larver när du använder 3xP3 promotorn43. Medan förekomsten av transient fluorescence föreslår framgångsrika plasmid leverans, garanterar det inte ärftliga könsceller omvandling. På samma sätt utesluter bristen på tillfälliga uttryck inte framgångsrik omvandling. Det har dock observerats att övergående positiva individer är mer benägna att ge transgena avkomma jämfört med övergående negativa43,48. I experthänder kan uppfödning och korsning av endast positiva individer vara ett alternativ för att minska myggantalet. Men med tanke på vikten och bräckligheten hos små G0-larver är minsta mängd manipulering fortfarande tillrådligt och uppfödning av alla G0-individer rekommenderas alltid.
Parningsschemat som rapporteras i det här protokollet är utformat för att maximera risken för parning och för att isolera oberoende omvandlingshändelser. Men om insektsutrymme eller personaltillgänglighet är ett problem kan G0 vuxna slås samman efter kön i enstaka burar om tillräckligt många individer av motsatt kön tillhandahålls. En sådan inställning kommer inte att tillåta diskriminering mellan flera omvandlingshändelser som inträffar hos individer från samma bur. Beroende på den experimentella installationen förväntas närvaron av en dubbel (enkel integration) eller en enda (RMCE) markör under screeningprocessen. I enskilda integrationsexperiment är det viktigt att verifiera närvaron av den ursprungliga markören från dockningslinjen, medan det i RMCE är viktigt att verifiera förlusten av den tidigare integrerade markören. Det är faktiskt inte ovanligt i RMCE-konstruktioner att återvinna transformanter där en enda integration i stället för utbyte inträffade på grund av rekombinationen av en enda attP-plats9,33. I sådana individer är både fluorescerande markörer närvarande samt hela givaren plasmid ryggraden belyser vikten av att genomföra en grundlig screening för båda fluorescerande markörer.
Medan förekomsten av förväntade fluorescensmönster indikerar framgångsrik omvandling, måste molekylär karakterisering av insättningsstället genomföras. För att göra detta är utarbetandet av exakta kartor över den förutsedda införing locus, inklusive de flankerande genomiska regionerna i dockningslinjen, avgörande för utformningen av adekvata diagnostiska oligonukleotidprimrar för genförstärkningsanalyser. Enskilda integrationshändelser resulterar i bildandet av attR – och attL-hybridplatser vid korsningen mellan det nyligen integrerade DNA:t och den tidigare insatta kassetten. Dessa platser kan riktas för validering av insättningswebbplats. I RMCE-konstruktioner kan införandet av donatorkassetten ske i två alternativa riktningar med avseende på den genomiska locus, så fyra primers kan användas i alternativa PCR-kombinationer för att upptäcka vilken orientering linjen bär. Eftersom orienteringen av kassett insättning kan påverka transgene uttryck, i jämförande gen uttryck analys är det viktigt att använda linjer som bär samma orientering av insättning.
När man arbetar med lågt antal transformanter kanske det inte är önskvärt att offra hela individer för molekylär analys. Ett alternativ till detta är att genomföra molekylär analys på DNA extraheras från en vuxens ben46 eftersom benförlust inte påverkar en vuxen kvinnlig förmåga att para sig och oviposit49. Det finns dock risk för att skada individen i processen för benborttagning. Framgång har erhållits med hjälp av kasserade pupal fall (L. Grigoraki personlig kommunikation), men det säkraste tillvägagångssättet är att utföra molekylär analys på G2 föräldrar efter att ha erhållit livskraftiga G3 avkomma.
Under de senaste åren har CRISPR/Cas9 revolutionerat sättet att utföra platsspecifik genomredigering26,41,50,51. Till skillnad från platsstyrda RMCE är CRISPR/Cas9-medierade genintegrationer (knock-ins) oberoende av förekomsten av förinsatta rekombinationsplatser med endast en omvandlingshändelse i ett steg som behövs. Crispr/Cas9-systemet förlitar sig dock på närvaron av stora kända genomiska sekvenser som flankerar den önskade insättningsplatsen för framgångsrik homologi riktad reparation samt på effektiv webbplatsigenkänning förmedlad av guide RNAs. Dessa villkor kan inte alltid uppfyllas eller kan vara mödosamma att felsöka och med tanke på tillgången till flera dockningslinjer i An. gambiae och An. stephensi och linjer som härrör från dem, är φC31-systemet fortfarande ett mycket värdefullt verktyg för att utföra direkta fenotypiska jämförelser mellan transgener på samma genomiska platser.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi är tacksamma mot Kiona Parker (UCI) för att ha tillhandahållit bilder av transgena An. stephensi larver, och till Fraser Colman (LSTM) och Beth Poulton (LSTM) för att tillhandahålla transgena An. gambiae larver. Beth Poulton (LSTM) gav också värdefull hjälp under avbildningen av An. gambiae larver. Detta arbete finansierades av Tata Institute for Genetics and Society (TIGS) och LSTM: s Director Catalyst Fund tilldelad A.A. (DCF2014AA). A.A.J. är en Donald Bren professor vid University of California, Irvine.
Materials
| 1.5 mL eppendorf tubes | |||
| 8-well microslides | VWR | MARI1216690 | |
| DNeasy Blood & Tissue Kit | Qiagen | 69504 | |
| EndoFree Plasmid Maxi Kit (10) | Qiagen | 12362 | |
| Ethanol, Absolute, Molecular Biology Grade | |||
| Filter set CFP for Leica MZ FLIII Excitation 436/20 nm, extinction 480/40 nm | Leica | 10446363 | |
| Filter set dsRED for Leica MZ FLIII Excitation 545/30 nm, extinction 620/60 nm | Leica | 10447079 | |
| Filter set YFP customised for Leica MZ FLIII | Omega Optical | 500QM25, 500QM35 | |
| Halocarbon oil 27 | Sigma | H8773 | |
| Halocarbon oil 700 | Sigma | H8898 | |
| Petri dishes | |||
| Potassium chloride | |||
| Sodium Chloride | |||
| Sodium phosphate dibasic | |||
| Sodium Acetate Solution (3 M), pH 5.2 | Thermo Fisher Scientific (Life Technologies) | R1181 | |
| Stable brush Size 0 |
References
- Adolfi, A., Lycett, G. J. Opening the toolkit for genetic analysis and control of Anopheles mosquito vectors. Current Opinion in Insect Science. 30, 8-18 (2018).
- Grossman, G. L., Rafferty, C. S., Clayton, J. R., Stevens, T. K., Mukabayire, O., Benedict, M. Q. Germline transformation of the malaria vector, Anopheles gambiae, with the piggyBac transposable element. Insect Molecular Biology. 10 (6), 597-604 (2001).
- Nolan, T., Bower, T. M., Brown, A. E., Crisanti, A., Catteruccia, F. piggyBac-mediated germline transformation of the malaria mosquito Anopheles stephensi using the red fluorescent protein dsRED as a selectable marker. Journal of Biological Chemistry. 277 (11), 8759-8762 (2002).
- Perera, O. P., Harrell, R. A., Handler, A. M. Germ-line transformation of the South American malaria vector, Anopheles albimanus, with a piggyBac/EGFP transposon vector is routine and highly efficient. Insect Molecular Biology. 11 (4), 291-297 (2002).
- Adolfi, A., Pondeville, E., Lynd, A., Bourgouin, C., Lycett, G. J. Multi-tissue GAL4-mediated gene expression in all Anopheles gambiae life stages using an endogenous polyubiquitin promoter. Insect Biochemistry and Molecular Biology. 96, 1-9 (2018).
- Carballar-Lejarazú, R., Jasinskiene, N., James, A. Exogenous gypsy insulator sequences modulate transgene expression in the malaria vector mosquito, Anopheles stephensi. Proceedings of the National Academy of Sciences of the United States of America. 110 (18), 7176-7181 (2013).
- Galizi, R., et al. A synthetic sex ratio distortion system for the control of the human malaria mosquito. Nature Communications. 5, 3977 (2014).
- Nolan, T., Petris, E., Müller, H. M., Cronin, A., Catteruccia, F., Crisanti, A. Analysis of two novel midgut-specific promoters driving transgene expression in Anopheles stephensi mosquitoes. PLoS ONE. 6 (2), 16471 (2011).
- Lynd, A., Balabanidou, V., Vontas, J., Lycett, G. J. Development of a functional genetic tool for Anopheles gambiae oenocyte characterisation: appliction to cuticular hydrocarbon synthesis. BioRxiv. , (2019).
- O’Brochta, D. A., Alford, R. T., Pilitt, K. L., Aluvihare, C. U., Harrell, R. A., Harrell, R. A. piggyBac transposon remobilization and enhancer detection in Anopheles mosquitoes. Proceedings of the National Academy of Sciences of the United States of America. 108 (39), 16339-16344 (2011).
- O’Brochta, D. A., Pilitt, K. L., Harrell, R. A., Aluvihare, C., Alford, R. T. Gal4-based enhancer-trapping in the malaria mosquito Anopheles stephensi. G3. 2 (11), 1305-1315 (2012).
- Macias, V. M., et al. nanos-Driven expression of piggyBac transposase induces mobilization of a synthetic autonomous transposon in the malaria vector mosquito, Anopheles stephensi. Insect Biochemistry and Molecular Biology. 87, 81-89 (2017).
- Nimmo, D. D., Alphey, L., Meredith, J. M., Eggleston, P. High efficiency site-specific genetic engineering of the mosquito genome. Insect Molecular Biology. 15 (2), 129-136 (2006).
- Kim, A., Pyykko, I. Size matters: Versatile use of PiggyBac transposons as a genetic manipulation tool. Molecular and Cellular Biochemistry. 354, 301-309 (2011).
- Thorpe, H. M., Smith, M. C. M. In vitro site-specific integration of bacteriophage DNA catalyzed by a recombinase of the resolvase/invertase family. Proceedings of the National Academy of Sciences of the United States of America. 95 (10), 5505-5510 (1998).
- Khaleel, T., Younger, E., Mcewan, A. R., Varghese, A. S., Smith, M. C. M. A phage protein that binds φC31 integrase to switch its directionality. Molecular Microbiology. 80 (6), 1450-1463 (2011).
- Farruggio, A. P., Chavez, C. L., Mikell, C. L., Calos, M. P. Efficient reversal of phiC31 integrase recombination in mammalian cells. Biotechnology Journal. 7 (11), 1332-1336 (2012).
- Venken, K. J. T., He, Y., Hoskins, R. A., Bellen, H. J. P[acman]: A BAC Transgenic Platform for Targeted Insertion of Large DNA Fragments in D. melanogaster. Science. 314 (5806), 1747-1751 (2006).
- Meredith, J. M., et al. Site-specific integration and expression of an anti-malarial gene in transgenic Anopheles gambiae significantly reduces Plasmodium infections. PLoS ONE. 6 (1), 14587 (2011).
- Meredith, J. M., Underhill, A., McArthur, C. C., Eggleston, P. Next-Generation Site-Directed Transgenesis in the Malaria Vector Mosquito Anopheles gambiae: Self-Docking Strains Expressing Germline-Specific phiC31 Integrase. PLoS ONE. 8 (3), 59264 (2013).
- Bernardini, F., et al. Site-specific genetic engineering of the Anopheles gambiae Y chromosome. Proceedings of the National Academy of Sciences of the United States of America. 111 (21), 7600-7605 (2014).
- Volohonsky, G., et al. Tools for Anopheles gambiae Transgenesis. G3. 5 (6), 1151-1163 (2015).
- Amenya, D. A., et al. Comparative fitness assessment of Anopheles stephensi transgenic lines receptive to site-specific integration. Insect Molecular Biology. 19 (2), 263-269 (2010).
- Isaacs, A. T., et al. Transgenic Anopheles stephensi coexpressing single-chain antibodies resist Plasmodium falciparum development. Proceedings of the National Academy of Sciences of the United States of America. 109 (28), 1922-1930 (2012).
- Pham, T. B., et al. Experimental population modification of the malaria vector mosquito, Anopheles stephensi. PLoS Genetics. 15 (12), 1008440 (2019).
- Hammond, A., et al. A CRISPR-Cas9 gene drive system targeting female reproduction in the malaria mosquito vector Anopheles gambiae. Nature Biotechnology. 34 (1), 78-83 (2015).
- Groth, A. C., Fish, M., Nusse, R., Calos, M. P. Construction of Transgenic Drosophila by Using the Site-Specific Integrase from Phage phiC31. Genetics. 166 (4), 1775-1782 (2004).
- Franz, A. W. E., et al. Comparison of transgene expression in Aedes aegypti generated by mariner Mos1 transposition and site-directed recombination. Insect Molecular Biology. 20 (5), 587-598 (2011).
- Labbé, G., Nimmo, D., Alphey, L. piggybac-and PhiC31-Mediated Genetic Transformation of the Asian Tiger Mosquito, Aedes albopictus (Skuse). PLoS Neglected Tropical Diseases. 4 (8), 788 (2010).
- Schetelig, M. F., Scolaric, F., Handler, A. M., Kittelmann, S., Gasperi, G., Wimmer, E. A. Site-specific recombination for the modification of transgenic strains of the Mediterranean fruit fly Ceratitis capitata. Proceedings of the National Academy of Sciences of the United States of America. 106 (43), 18171-18176 (2009).
- Yonemura, N., et al. phiC31-integrase-mediated, site-specific integration of transgenes in the silkworm, Bombyx mori (Lepidoptera: Bombycidae). Applied Entomology and Zoology. 43 (11), 997-1008 (2013).
- Bateman, J. R., Lee, A. M., Wu, C. T. Site-specific transformation of Drosophila via phiC31 integrase-mediated cassette exchange. Genetics. 173 (2), 769-777 (2006).
- Adolfi, A., Poulton, B., Anthousi, A., Macilwee, S., Ranson, H., Lycett, G. J. Functional genetic validation of key genes conferring insecticide resistance in the major African malaria vector, Anopheles gambiae. Proceedings of the National Academy of Sciences of the United States of America. 116 (51), 25764-25772 (2019).
- Haghighat-Khah, R. E., et al. Site-specific cassette exchange systems in the aedes aegypti mosquito and the Plutella xylostella moth. PLoS ONE. 10 (4), 0121097 (2015).
- Long, D., Lu, W., Zhang, Y., Bi, L., Xiang, Z., Zhao, A. An efficient strategy for producing a stable, replaceable, highly efficient transgene expression system in silkworm, Bombyx mori. Scientific Reports. 5 (1), 8802 (2015).
- Volohonsky, G., et al. Transgenic Expression of the Anti-parasitic Factor TEP1 in the Malaria Mosquito Anopheles gambiae. PLoS Pathogens. 13 (1), 1006113 (2017).
- Grigoraki, L., Grau-Bové, X., Yates, H. C., Lycett, G. J., Ranson, H. Isolation and transcriptomic analysis of anopheles gambiae oenocytes enables the delineation of hydrocarbon biosynthesis. eLife. 9, 58019 (2020).
- Kyrou, K., et al. A CRISPR-Cas9 gene drive targeting doublesex causes complete population suppression in caged Anopheles gambiae mosquitoes. Nature Biotechnology. 36 (11), 1062-1066 (2018).
- Berghammer, A. J., Klingler, M., Wimmer, E. A. A universal marker for transgenic insects. Nature. 402 (6760), 370-371 (1999).
- Ringrose, L. Transgenesis in Drosophila melanogaster. Methods in Molecular Biology. 561, 3-19 (2009).
- Dong, Y., Simões, M. L., Marois, E., Dimopoulos, G. CRISPR/Cas9 -mediated gene knockout of Anopheles gambiae FREP1 suppresses malaria parasite infection. PLoS Pathogens. 14 (3), 1006898 (2018).
- Lombardo, F., Lycett, G. J., Lanfrancotti, A., Coluzzi, M., Arcà, B. Analysis of apyrase 5′ upstream region validates improved Anopheles gambiae transformation technique. BMC research notes. 2, 24 (2009).
- Pondeville, E., et al. Efficient ΦC31 integrase-mediated site-specific germline transformation of Anopheles gambiae. Nature Protocols. 9 (7), 1698-1712 (2014).
- Lobo, N. F., Clayton, J. R., Fraser, M. J., Kafatos, F. C., Collins, F. H. High efficiency germ-line transformation of mosquitoes. Nature protocols. 1 (3), 1312-1317 (2006).
- Terenius, O., Juhn, J., James, A. A. Injection of An. stephensi embryos to generate malaria-resistant mosquitoes. Journal of Visualized Experiments. 5, 216 (2007).
- Lynd, A., et al. Insecticide resistance in Anopheles gambiae from the northern Democratic Republic of Congo, with extreme knockdown resistance (kdr) mutation frequencies revealed by a new diagnostic assay. Malaria Journal. 17 (1), 412 (2018).
- Marinotti, O., et al. Development of a population suppression strain of the human malaria vector mosquito, Anopheles stephensi. Malaria Journal. 12 (1), 142 (2013).
- Adolfi, A. In vivo functional genetic analysis of insecticide resistance in the malaria mosquito Anopheles gambiae. University of Liverpool. , (2017).
- Isaacs, A. T., Lynd, A., Donnelly, M. J. Insecticide-induced leg loss does not eliminate biting and reproduction in Anopheles gambiae mosquitoes. Scientific Reports. 7, 46674 (2017).
- Gantz, V. M., et al. Highly efficient Cas9-mediated gene drive for population modification of the malaria vector mosquito Anopheles stephensi. Proceedings of the National Academy of Sciences of the United States of America. 112 (49), 6736-6743 (2015).
- Li, M., Akbari, O. S., White, B. J. Highly efficient site-specific mutagenesis in malaria mosquitoes using CRISPR. G3: Genes, Genomes, Genetics. 8 (2), 653-658 (2018).
- Poulton, B. C., et al. Using the GAL4-UAS System for Functional Genetics in Anopheles gambiae. J. Vis. Exp. , (2021).

