DNA-Spannungssonden zur Kartierung der transienten Piconewton-Rezeptor-Kräfte durch Immunzellen
Summary
In dieser Arbeit wird ein detailliertes Protokoll für die Verwendung von DNA-basierten Spannungssonden beschrieben, um die von Immunzellen ausgeübten Rezeptorkräfte abzubilden. Dieser Ansatz kann Rezeptorkräfte >4,7 pN in Echtzeit abbilden und Kräfte über die Zeit integrieren.
Abstract
Mechanische Kräfte, die an der Verbindungsstelle zwischen zwei benachbarten Zellen und an der Verbindungsstelle zwischen Zellen und der extrazellulären Matrix übertragen werden, sind entscheidend für die Regulierung vieler Prozesse, die von der Entwicklung bis zur Immunologie reichen. Daher ist es von entscheidender Bedeutung, die Werkzeuge zu entwickeln, um diese Kräfte auf molekularer Ebene zu untersuchen. Unsere Gruppe entwickelte eine Reihe von molekularen Spannungssensoren, um die von Zellen erzeugten und auf bestimmte Liganden übertragenen Kräfte zu quantifizieren und zu visualisieren. Die empfindlichste Klasse von molekularen Spannungssensoren besteht aus Nukleinsäure-Stammschleifen-Haarnadeln. Diese Sensoren verwenden Fluorophor-Quencher-Paare, um die mechanische Dehnung und Entfaltung von DNA-Haarnadeln unter Krafteinwirkung zu melden. Eine Herausforderung bei DNA-Hairpin-Spannungssensoren besteht darin, dass sie reversibel sind, wobei die Hairpin-Spannung beim Beenden der Spannung schnell zurückgefaltet werden kann und somit transiente Kräfte schwer zu erfassen sind. In diesem Artikel beschreiben wir die Protokolle zur Herstellung von DNA-Spannungssensoren, die “verriegelt” und am erneuten Falten gehindert werden können, um das “Speichern” mechanischer Informationen zu ermöglichen. Dies ermöglicht die Aufzeichnung von hochtransienten Piconewton-Kräften, die anschließend durch die Zugabe komplementärer Nukleinsäuren, die die Sperre entfernen, “gelöscht” werden können. Diese Fähigkeit, zwischen Echtzeit-Spannungsmapping und mechanischer Informationsspeicherung umzuschalten, offenbart schwache, kurzlebige und weniger reichlich vorhandene Kräfte, die von T-Zellen üblicherweise als Teil ihrer Immunfunktionen eingesetzt werden.
Introduction
Immunzellen wehren sich gegen Krankheitserreger und Krebszellen, indem sie kontinuierlich die Oberflächen von Zielzellen nach Antigenen durchsuchen und deren Oberfläche abtasten 1,2. Die Antigenerkennung wird durch die Bindung zwischen dem T-Zell-Rezeptor (TCR) und dem Peptid-Major-Histokompatibilitätskomplex MHC (pMHC) eingeleitet, der auf der Oberfläche der Zielzellen exprimiert wird. Da die TCR-pMHC-Erkennung an der Verbindungsstelle zwischen zwei beweglichen Zellen erfolgt, steht sie seit langem im Verdacht, mechanische Kräfte zu erfahren. Darüber hinaus führte dies zum Mechanosensormodell der TCR-Aktivierung, das darauf hindeutet, dass TCR-Kräfte zu seiner Funktion beitragen 3,4. Um zu verstehen, wann, wo und wie mechanische Kräfte zur Funktion von T-Zellen beitragen, ist es unerlässlich, Werkzeuge zu entwickeln, um die von T-Zellen übertragenen molekularen Kräfte sichtbar zu machen. Traditionell werden Methoden wie Zugkraftmikroskopie (TFM) und Mikrosäulen-Arrays verwendet, um zelluläre Kräfte zu untersuchen 5,6. Die Kraftempfindlichkeit von TFM- und Mikrosäulen-Arrays liegt jedoch im Nanonewton (nN)-Bereich und reicht daher oft nicht aus, um die molekularen Piconewton (pN)-Kräfte zu untersuchen, die von Zellrezeptoren übertragenwerden 7. Um die Kraft und die räumliche Auflösung für die Detektion zu verbessern, leistete unser Labor Pionierarbeit bei der Entwicklung von molekularen Spannungssonden, die ursprünglich mit Polyethylenglykol (PEG)-Polymeren synthetisiert wurden7. Molekulare Spannungssonden bestehen aus einer ausziehbaren molekularen “Feder” (PEG, Protein, DNA), die von einem Fluorophor und Quencher flankiert wird und auf einer Oberfläche verankert ist. Kräfte, die auf den Endpunkt der Sonde ausgeübt werden, führen zu ihrer Verlängerung, trennen Fluorophor und Quencher und erzeugen so ein starkes Fluoreszenzsignal (Abbildung 1A)8,9,10.
In den letzten zehn Jahren haben wir eine Bibliothek verschiedener Klassen von molekularen Zugsonden mit Federelementen aus Nukleinsäuren11, Proteinen10 und Polymeren8 entwickelt. Unter diesen bieten die DNA-basierten Zugsonden das höchste Signal-Rausch-Verhältnis und die größte Kraftempfindlichkeit, die leicht von wenigen pN bis zu ~20 pN11 eingestellt werden kann. Wir haben diese Echtzeit-DNA-Spannungssonden verwendet, um die molekularen Kräfte zu untersuchen, die von vielen verschiedenen Zelltypen erzeugt werden, darunter Fibroblasten, Krebszellen, Blutplättchen und Immunzellen11,12,13. In diesem Manuskript werden Protokolle zur Synthese und Montage von DNA-Zugsonden auf einer Oberfläche beschrieben, um molekulare Rezeptorkräfte mit pN-Kraftauflösung unter Verwendung eines konventionellen Fluoreszenzmikroskops abzubilden. Während das derzeitige Verfahren chemische Modifikationen der Nukleinsäure umfasst, um den fluoreszierenden Reporter einzuführen (Abbildung 1B), ist es wichtig zu beachten, dass viele der Modifikations- und Aufreinigungsschritte an kundenspezifische DNA-Syntheseunternehmen ausgelagert werden können. Daher ist die Technologie der DNA-Spannungssonden einfach und für die breitere Gemeinschaft der Zellbiologie und Mechanobiologie zugänglich.
Kurz gesagt, um DNA-Spannungssensoren zusammenzubauen, wird eine DNA-Haarnadel mit einem fluoreszierenden Ligandenstrang auf einem Arm und einem Quencher-Ankerstrang auf dem anderen Arm hybridisiert und dann auf einem Glassubstrat immobilisiert (Abbildung 1C, Echtzeitspannung). In Abwesenheit einer mechanischen Kraft wird die Haarnadel geschlossen und somit die Fluoreszenz gelöscht. Wenn jedoch die ausgeübte mechanische Kraft größer als F1/2 ist (die Kraft im Gleichgewicht, die zu einer 50%igen Wahrscheinlichkeit der Entfaltung führt), schmilzt die Haarnadel mechanisch und es wird ein fluoreszierendes Signal erzeugt.
Aufbauend auf dem Echtzeit-DNA-Spannungssensor beschreiben wir auch Protokolle zur Kartierung akkumulierter Kräfte, was besonders nützlich ist, um Interaktionen zwischen Rezeptoren auf Immunzellen und ihrem natürlichen Liganden zu untersuchen. Dies liegt daran, dass Immunrezeptoren oft kurzlebige Bindungen aufweisen 3,14. Die akkumulierten Kräfte werden mit einem “verriegelnden” Strang abgebildet, der bevorzugt an offene DNA-Haarnadeln bindet und die Speicherung von Fluoreszenzsignalen ermöglicht, die mit mechanischen Zugereignissen verbunden sind (Abbildung 1C, verriegelte Spannung). Der Verriegelungsstrang ist so konzipiert, dass er eine kryptische Bindungsstelle bindet, die beim mechanisch induzierten Schmelzen der Haarnadel freigelegt wird, und die Haarnadel im offenen Zustand sperrt, indem er die Rückfaltung der Haarnadel blockiert, wodurch das Spannungssignal gespeichert und eine akkumulierte Spannungskarte erzeugt wird. Darüber hinaus ist der Locking-Strang mit einem Acht-Nukleotid-Zehengriff ausgelegt, der eine Zehengriff-vermittelte Strangverdrängungsreaktion mit seinem vollständigen Komplement, dem “entsperrenden” Strang, ermöglicht. Durch das Hinzufügen des Entriegelungsstrangs wird der gebundene Verriegelungsstrang vom Hairpin-Konstrukt abgestreift, wodurch das gespeicherte Spannungssignal gelöscht und der Hairpin wieder in den Echtzeitzustand zurückgesetzt wird.
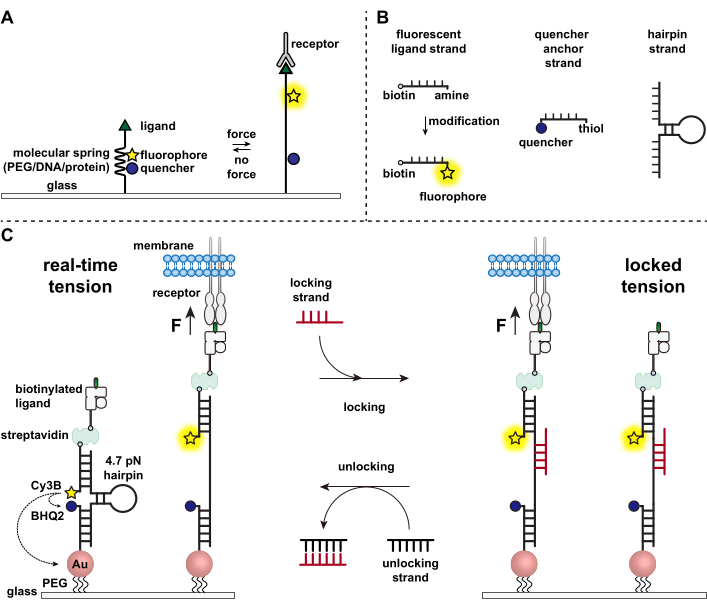
Abbildung 1: Schema der hochmodernen molekularen Spannungssonden. (A) Allgemeines Design einer Echtzeit-Molekularspannungssonde, (B) Stränge für das DNA-basierte Spannungssondenkonstrukt und (C) DNA-basierte Spannungssonden und deren Umschalten zwischen Echtzeitzustand und verriegeltem Zustand. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
Das Hauptprotokoll besteht aus vier Hauptabschnitten – Oligonukleotidpräparation, Oberflächenpräparation, Bildgebung und Datenanalyse. Dieses Protokoll wurde von unserem Labor und anderen erfolgreich in naiven und aktivierten OT-1 CD8+ T-Zellen, OT-II CD4+ Zellen sowie Hybridomen demonstriert und kann angewendet werden, um verschiedene Immunzellrezeptoren zu untersuchen, einschließlich des T-Zell-Rezeptors, des programmierten Zelltodrezeptors (PD1) und der Lymphozytenfunktions-assoziierten Antigen-1-Kräfte (LFA-1). OT-1 CD8+ naive T-Zellen werden in dieser Arbeit als Beispielzelllinie verwendet.
Protocol
Representative Results
Discussion
Mit den hier vorgestellten detaillierten Verfahren kann man DNA-Haarnadel-Spannungssondensubstrate herstellen, um die von Immunzellen produzierte Rezeptorspannung zu kartieren und zu quantifizieren. Wenn Zellen auf das Substrat der DNA-Haarnadel-Spannungssonde plattiert werden, landen, heften sie sich an und breiten sich aus, während die Rezeptoren die Liganden sowohl chemisch als auch mechanisch wahrnehmen, wobei letzteres von unseren Sonden erkannt wird. In einigen Fällen kann es jedoch vorkommen, dass sich die Zelle…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Diese Arbeit wurde durch die NIH Grants R01GM131099, NIH R01GM124472 und NSF CAREER 1350829 unterstützt. Wir danken der NIH Tetramer Facility für pMHC-Liganden. Diese Studie wurde zum Teil durch den Emory Comprehensive Glycomics Core unterstützt.
Materials
| 3-hydroxypicolinic acid (3-HPA) | Sigma | 56197 | maldi-TOF-MS matrix |
| mPEG-SC | Biochempeg | MF001023-2K | surface prep |
| (3-Aminopropyl)triethoxysilane | Acros | AC430941000 | surface prep |
| 10x Red blood cell lysis buffer | Biolegend | 00-4333-57 | buffer |
| 8.8 nm gold nanoparticles, tannic acid | Nanocomposix | customized order | surface prep |
| Atto647N NHS ester | Sigma | 18373-1MG-F | fluorophore, oligo prep |
| Attofluor Cell Chamber, for microscopy | Thermo Fisher Scientific | A7816 | imaging |
| BD Syringes only with Luer-Lok | BD bioscience | 309657 | cells |
| biotinylated anti-mouse CD3e | ebioscience | 13-0031-82 | antibody/ligand |
| Biotinylated pMHC ovalbumin (SIINFEKL) | NIH Tetramer Core Facility at Emory University | NA | antibody/ligand |
| bovine serum albumin | Sigma | 735078001 | block non-specific interactions |
| Cell strainers | Biologix | 15-1100 | cells |
| Coverslip Mini-Rack, teflon | Thermo Fisher Scientific | C14784 | surface prep |
| Cy3B NHS ester | GE Healthcare | PA63101 | fluorophore, oligo prep |
| Dulbecco's phosphate-buffered saline (DPBS) | Corning | 21-031-CM | buffer |
| ethanol | Sigma | 459836 | surface prep |
| Hank’s balanced salts (HBSS) | Sigma | H8264 | buffer |
| hydrogen peroxide | Sigma | H1009 | surface prep |
| LA-PEG-SC | Biochempeg | HE039023-3.4K | surface prep |
| Midi MACS (LS) startup kit | Miltenyi Biotec | 130-042-301 | cells |
| mouse CD8+ T cell isolation kit | Miltenyi Biotec | 130-104-075 | cells |
| Nanosep MF centrifugal devices | Pall laboratory | ODM02C35 | oligo prep |
| No. 2 round glass coverslips | VWR | 48382-085 | surface prep |
| NTA-SAM | Dojindo Molecular Technologies | N475-10 | surface prep |
| P2 gel | Bio-rad | 1504118 | oligo prep |
| sufuric acid | EMD Millipore Corporation | SX1244-6 | surface prep |
| Sulfo-NHS acetate | Thermo Fisher Scientific | 26777 | surface prep |
| Equipment | |||
| Agilent AdvanceBio Oligonucleotide C18 column, 4.6 x 150 mm, 2.7 μm | 653950-702 | oligonucleotide preparation | |
| Barnstead Nanopure water purifying system | Thermo Fisher | water | |
| CFI Apo 100× NA 1.49 objective | Nikon | Microscopy | |
| Cy5 cube | CHROMA | Microscopy | |
| evolve electron multiplying charge coupled device (EMCCD) | Photometrics | Microscopy | |
| High-performance liquid chromatography | Agilent 1100 | oligonucleotide preparation | |
| Intensilight epifluorescence source | Nikon | Microscopy | |
| Matrix-assisted laser desorption/ionization time-of-flight mass spectrometer (MALDI-TOF-MS) | Voyager STR | oligonucleotide preparation | |
| Nanodrop 2000 UV-Vis Spectrophotometer | Thermo Fisher | oligonucleotide preparation | |
| Nikon Eclipse Ti inverted microscope | Nikon | Microscopy | |
| Nikon Perfect Focus System | Nikon | Microscopy | |
| NIS Elements software | Nikon | Microscopy | |
| quad band TIRF 405/488/561/647 cube | CHROMA | Microscopy | |
| RICM cube | CHROMA | Microscopy | |
| TIRF launcher with 488 nm (50 mW), 561 nm (50 mW), and 640 nm | Coherent | Microscopy | |
| TRITC cube | CHROMA | Microscopy | |
| oligo name | 5' modification / 3' modification | sequence (5' to 3') | Use |
| 15mer amine locking strand | 5' modification: no modification 3' modification: /3AmMO/ |
AAA AAA CAT TTA TAC CCT ACC TA | locking real-time tension signal |
| 15mer Atto647N locking strand | 5' modification: Atto647N 3' modification: /3AmMO/ |
AAA AAA CAT TTA TAC CCT ACC TA | locking real-time tension signal |
| 15mer non-fluoresccent locking strand | 5' modification: no modification 3' modification: no modification |
A AAA AAC ATT TAT AC | locking real-time tension signal for quantitative analysis |
| 4.7 pN hairpin strand | 5' modification: no modification 3' modification: no modification |
GTGAAATACCGCACAGATGCGT TTGTATAAATGTTTTTTTCATTTAT ACTTTAAGAGCGCCACGTAGCC CAGC |
hairpin probe |
| amine ligand strand | 5' modification: /5AmMC6/ 3' modification: /3Bio/ |
CGCATCTGTGCG GTA TTT CAC TTT | hairpin probe |
| BHQ2 anchor strand | 5' modification: /5ThiolMC6-D/ 3' modification: /3BHQ_2/ |
TTTGCTGGGCTACGTGGCGCTCTT | hairpin probe |
| Cy3B ligand strand | 5' modification: Cy3B 3' modification: /3Bio/ |
CGCATCTGTGCG GTA TTT CAC TTT | hairpin probe |
| unlocking strand | 5' modification: no modification 3' modification: no modification |
TAG GTA GGG TAT AAA TGT TTT TTT C | unlocking accumulated tension signal |
References
- Dustin, M. L. T-cell activation through immunological synapses and kinapses. Immunological Reviews. 221 (1), 77-89 (2008).
- Spillane, K. M., Tolar, P. B cell antigen extraction is regulated by physical properties of antigen-presenting cells. Journal of Cell Biology. 216 (1), 217-230 (2017).
- Feng, Y., et al. Mechanosensing drives acuity of αβ T-cell recognition. Proceedings of the National Academy of Sciences. 114 (39), 8204-8213 (2017).
- Hong, J., et al. A TCR mechanotransduction signaling loop induces negative selection in the thymus. Nature Immunology. 19 (12), 1379-1390 (2018).
- Basu, R., et al. Cytotoxic T cells use mechanical force to potentiate target cell killing. Cell. 165 (1), 100-110 (2016).
- Bashour, K. T., et al. CD28 and CD3 have complementary roles in T-cell traction forces. Proceedings of the National Academy of Sciences. 111 (6), 2241-2246 (2014).
- Ma, V. P. Y., Salaita, K. DNA nanotechnology as an emerging tool to study mechanotransduction in living systems. Small. 15 (26), 1900961 (2019).
- Liu, Y., Yehl, K., Narui, Y., Salaita, K. Tension sensing nanoparticles for mechano-imaging at the living/nonliving interface. Journal of the American Chemical Society. 135 (14), 5320-5323 (2013).
- Glazier, R., et al. DNA mechanotechnology reveals that integrin receptors apply pN forces in podosomes on fluid substrates. Nature Communications. 10 (1), 1-13 (2019).
- Galior, K., Liu, Y., Yehl, K., Vivek, S., Salaita, K. Titin-based nanoparticle tension sensors map high-magnitude integrin forces within focal adhesions. Nano Letters. 16 (1), 341-348 (2016).
- Zhang, Y., Ge, C., Zhu, C., Salaita, K. DNA-based digital tension probes reveal integrin forces during early cell adhesion. Nature Communications. 5, 5167 (2014).
- Liu, Y., et al. DNA-based nanoparticle tension sensors reveal that T-cell receptors transmit defined pN forces to their antigens for enhanced fidelity. Proceedings of the National Academy of Sciences. 113 (20), 5610-5615 (2016).
- Zhang, Y., et al. Platelet integrins exhibit anisotropic mechanosensing and harness piconewton forces to mediate platelet aggregation. Proceedings of the National Academy of Sciences. 115 (2), 325-330 (2018).
- Huang, J., et al. The kinetics of two-dimensional TCR and pMHC interactions determine T-cell responsiveness. Nature. 464 (7290), 932-936 (2010).
- Ma, R., et al. DNA probes that store mechanical information reveal transient piconewton forces applied by T cells. Proceedings of the National Academy of Sciences. 116 (34), 16949-16954 (2019).
- Hui, E., et al. T cell costimulatory receptor CD28 is a primary target for PD-1-mediated inhibition. Science. 355 (6332), 1428-1433 (2017).
- Whitley, K. D., Comstock, M. J., Chemla, Y. R. Elasticity of the transition state for oligonucleotide hybridization. Nucleic Acids Research. 45 (2), 547-555 (2016).
- Brockman, J. M., et al. Live-cell super-resolved PAINT imaging of piconewton cellular traction forces. Nature Methods. 17 (10), 1018-1024 (2020).

