使用开源 smfBox 进行精确和准确的单分子 FRET 测量
Summary
本文提供了使用开源、廉价的 smfBox 对单个、自由扩散的生物分子进行完全校正的准确 FRET 测量的分步说明,从打开、通过对准和聚焦,再到数据收集和分析。
Abstract
smfBox是最近开发的一种具有成本效益的开源仪器,用于单分子Förster共振能量转移(smFRET),它使自由扩散生物分子的测量更容易获得。本概述包括使用此仪器测量双链DNA样品中精确FRET效率的分步方案,包括样品制备,仪器设置和校准,数据采集和完整分析程序的详细信息。所提出的方法包括如何确定精确FRET派生的距离测量所需的所有校正因素,建立在FRET社区最近的大量协作工作的基础上,旨在建立标准协议和分析方法。该协议易于适应一系列生物分子系统,为更广泛的科学界的smFRET民主化努力做出了贡献。
Introduction
单分子Förster共振能量转移(smFRET)是一种在单个分子水平上测量两种染料(供体和受体)之间的FRET效率的技术。FRET是由两种染料的重叠能谱引起的光物理过程:供体被特定波长的光激发,并将能量非辐射地传递给受体,导致受体发射。这种转移的效率与两种染料之间距离的六次方成反比,因此转移效率随距离而变化1。因此,这种FRET效率可用于确定染料附着在3-10nm范围内的分子2 的空间信息。这种尺度,以及FRET效率的变化对埃分子运动敏感的事实3,使得该技术非常适合研究有关生物分子的结构信息-如核酸和蛋白质-而没有集合平均的并发症4,5,6。虽然相对FRET效率的变化可用于监测生物分子相互作用和构象动力学,揭示关键的细胞过程,如蛋白质(未)折叠,转录以及DNA复制和修复,但绝对的FRET效率已用于确定生物分子结构测定的精确距离7,8,9,10,11,克服了其他一些结构方法所需的结晶或冷冻需求4,12。
smFRET实验通常采用两种形式,共聚焦或全内反射荧光(TIRF)显微镜。在这两种方法之间,生物分子的分子动力学通常可以在从皮克到毫秒(共聚焦,自由扩散分子)到毫秒到几小时(TIRF,表面固定分子)的时间尺度上进行研究。这是由于每种技术涉及不同的设置。在TIRF显微镜下,分子固定在载玻片表面并被倏逝波激发(图1A)。然而,这里的重点是共聚焦显微镜,因为这是smfBox的格式。在共聚焦显微镜中,分子不是固定的,而是通过共聚焦体积(〜1 fL)的布朗运动自由扩散,通过将激光束通过高数值孔径透镜聚焦到溶液内某个指定深度的点而形成(图1B)。产生的发射通过相同的孔径聚焦,并通过二向色镜过滤(图1C 为完整原理图)。然后通过针孔聚焦,以消除任何失焦光并进入雪崩光电二极管(APD)。当APD检测到光子时,它会输出一个TTL脉冲,其时序可以以高达皮秒的分辨率记录下来。这些自由扩散的分子在共聚焦体积附近的观察时间通常在毫秒级以内。
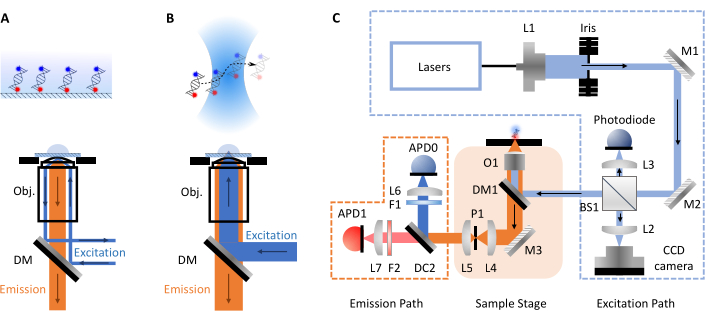
图1:显示显微镜原理和smfBox设置的示意图。 (A)全内反射荧光(TIRF)显微镜原理:激发光被引导到物镜(Obj.)的边缘,并在盖玻片 – 缓冲液界面处经历全内反射,产生指数衰减的消失场以激发表面附着的分子。(B)共聚焦显微镜:自由扩散的分子被聚焦到样品中的近衍射极限点激发。(C)该协议中使用的smfBox设置,显示所有关键组件:雪崩光电二极管(APD),分束器(BS),二向色镜(DM),滤光片(F),反射镜(M),物镜(O)和针孔(P)。 请点击此处查看此图的放大版本。
最近,smFRET技术结合了两种颜色激发,其中与供体和受体激发波长匹配的激光器交替5。这可以通过两种方式之一完成,第一种是通过在KHz时间尺度上调制连续波激光器,这被称为交替激光激发(ALEX)13,14。第二种方法在MHz时间尺度上交错快速脉冲;这是纳秒-ALEX15 或脉冲交错激励(PIE)16。在所有这些方法中,来自受体激光的信息导致所谓的化学计量学的计算,该化学计量学可以区分具有低FRET效率的分子和那些缺乏受体的分子(通过不完全标记或光漂白)。使用PIE/ns-ALEX还可以在单分子水平上获得荧光寿命,并且当与偏振光学器件结合使用时,可以测量各向异性。这种测量组合称为多参数荧光检测(MFD)9。
尽管smFRET具有许多优点,但由于商业仪器的高成本以及缺乏简单的自建替代品,它并没有在专业实验室之外广泛使用。低成本开源显微镜的发展趋势正在增长,最近出现了其他平台,包括Planktonscope17,OpenFlexure Microscope18,Flexiscope19,miCube20,liteTIRF21和Squid22。本文描述了使用smfBox的方案,smfBox是一种最近开发的具有成本效益的共聚焦设置,能够测量自由扩散的单分子上两种染料之间的FRET效率。详细的构建说明和所有必要的操作软件可在以下网址免费获得:https://craggslab.github.io/smfBox/ 23。smfBox的光学配置由从价格合理且易于访问的制造商处购买的现成组件组装而成,而显微镜主体(在标准共聚焦设置中负责大部分费用)已被定制的光密阳极氧化铝盒取代(允许在环境光条件下进行测量)。该盒子包含关键的光学元件,包括激发二向色性、物镜和针孔,以及机械激光互锁,使其能够作为I类激光产品安全运行(完整原理图见图1C)。smfBox使用ALEX来验证染料化学计量学并确定准确的FRET校正因子。它使用定制编写的开源软件(smOTTER)进行操作,该软件控制数据采集的各个方面,并以开源photon-HDF5格式24输出数据,与许多第三方分析工具兼容。smfBox以及采集和数据分析协议最近在一项多实验室盲研究中针对>20其他仪器(共聚焦和TIRF)进行了测试25。所获得的FRET效率与所有其他仪器非常一致,尽管smfBox的成本仅为商用设置价格的一小部分。
本文概述了一个分步方案,用于获取和分析使用 smfBox 自由扩散 DNA 双链体的准确、绝对 FRET 效率,从打开、通过对准和聚焦,一直到数据收集和分析。这里使用的样品是三种双工DNA(表现出高,中和低FRET效率,见 表1),它们在世界范围的盲研究中进行了评估25;然而,该方法适用于许多分子系统,包括蛋白质和其他核酸。希望如此详细的协议,以及已经存在的smfBox23构建说明,将有助于使这种强大的技术更容易被广泛的实验室所接受。
Protocol
Representative Results
Discussion
方案中最关键的步骤是显微镜的对准和将样品浓度调整到正确的稀释度。如果对准关闭,则可能没有足够的信号来识别突发和绘制直方图,如果样品之间发生不对准,则由于泄漏和检测/激发效率的变化,准确的FRET校正可能会失败。使用适当的浓度也很重要,浓度过高会产生重合的爆发,包含具有潜在不同FRET效率或标记化学计量的多个分子。浓度过低将导致爆发太少,无法进行可靠的数据分析。
此处描述的协议用于测量静态单个FRET物种的距离。如果样品在FRET效率直方图中具有多个峰,或者峰看起来很宽(动态物种可能会发生这种情况),则可能需要更多的脉冲才能将直方图拟合到相同的精度。对于两个分离良好的峰值,则需要大约两倍的数据,但如果总体略有重叠,则需要更多的数据。
如果两个群体在实验的时间尺度上相互转换,则可以潜在地确定系统的动力学和动力学。BVA27和2CDE28等测试可以证实中间爆发本质上是动态的,而包括dPDA29,30或H2MM31在内的分析可以确定相互转换的速率。用于BVA和2CDE的Jupyter笔记本可在FRETBursts26网站上找到,基于MATLab的软件PAM32可以运行BVA,2CDE和PDA分析。
共聚焦单分子FRET可以很容易地观察到比TIRF寿命短得多(~1 ms)的状态;然而,受扩散限制的短观察时间没有给出分子历史,因此不能像表面固定实验那样确定更长的停留时间或复杂的过渡网络。
由于该协议以非常低的浓度测量自由扩散的分子,因此在测量同一分子上的分子内距离时效果最佳。可以测量瞬态结合分子之间的分子间距离,前提是两个分子的Kd 足够低,使得配合物在实验所需的低工作浓度(〜100 pM)下以显着的数量存在。如果Kd 远高于此值,则只能看到单独标记的分子。这个问题可以通过使用微流体以高浓度将两种标记的组分混合在一起,然后在复合物解离之前快速稀释并流过物镜来克服33,34。
与集合技术相比,在单分子水平上测量FRET效率具有显着优势,因为它可以告知异质亚群,在集合实验中,异质亚群将被平均。此外,带有ALEX的单分子FRET可以获得精确的FRET效率,这可以转换为精确的距离。这样可以确定更详细的结构信息,而不是简单地探测相对距离变化。smfBox具有所有这些优点和功能,但可以比能够共聚焦smFRET23的同类商用显微镜在低得多的预算下构建。
smfBox代表了smFRET技术的进入门槛要低得多,使研究人员能够测量构象变化,以及蛋白质和核酸内部和之间的精确距离7,8,9,10,11,35。
Disclosures
The authors have nothing to disclose.
Acknowledgements
作者感谢以下资金来源:BBSRC(BB/T008032/1);EPSRC(B.A.的助学金)和MRC(A.R.-T.的学生奖学金)。
Materials
| Amino modified oligonucleotide | Eurogentec | N/A | May be ordered from various suppliers or synthesised; amino modification enables labeling with NHS-ester modified dyes |
| Avalanche photodiode (APD) | Excelitas | SPCM-AQRH-14 | Two APDs are required for the smfBox setup |
| Bovine Serum Albumin (BSA) | Merck | A2153 | System dependant; imaging buffer component (0.1 mg/mL in buffer) |
| Compact Laser Combiner | OMICRON | LightHUB-2 | 515 nm (80 mW) and 638 nm (100 mW) lasers |
| Coverglass | VWR | 630-2742 | Thickness: 0.17 ± 0.01 mm, LxW: 22×22 mm |
| Cy3B | Cytiva | PA63101 | 1 mg, PA63100 (5 mg), PA96106 (25 mg) |
| FRETBursts Python Package | N/A | N/A | Open-source python package for burst analysis of freely-diffusing single-molecule FRET data: https://fretbursts.readthedocs.io |
| Imaging Buffer | N/A | System dependant; 5 mM NaCl, 20 mM MgCl2, 5 mM Tris pH 7.5 and 0.1 mg/mL BSA | |
| Immersion Oil | Olympus | IMMOIL-F30CC | |
| Jupyter notebooks | Project Jupyter | N/A | Open-source web application to create and share documents that contain live code, equations, visualizations and text; data analysis notebooks for smfBox can be found in the SI |
| Lens Tissue | ThorLabs | MC-5 | MC-50E is same item in bulk |
| Magnesium Chloride | Merck | M2670 | System dependant; imaging buffer component (20 mM in buffer) |
| MilliQ/Ultrapure water | N/A | ||
| Nanopoistioner | Piezoconcept | FOC300 | Nanopositioner for accurate positioning of microscope objective |
| NHS-ester modified ATTO-550 | ATTO-TEC | AD 550-31 | 1 mg, AD 550-35 (5 mg) |
| NHS-ester modified ATTO-647N | ATTO-TEC | AD 647N-31 | 1 mg, AD 647N-35 (5 mg) |
| Objective lens | Olympus | N1480700 | Olympus objective series from orignal smfBox discontinued; replaced by N5702300 |
| OMICRON Control Center (OCC)- laser control center | OMICRON | N/A | v3.5.34 – OMICRON laser driver software |
| Press-To-Seal silicone isolator | Grace Bio-Labs | 664201 | 8-9 mm Diameter x 1.7 mm Depth |
| smOTTER | N/A | N/A | Open-source acquisition software for the Craggs Lab smfBox: https://github.com/craggslab/smOTTER |
| Sodium Chloride | Merck | S7653 | System dependant; imaging buffer component (5 mM in buffer) |
| Tris base | Merck | 93362 | System dependant; imaging buffer component (5 mM, pH 7.5 in buffer) |
| Type I ultrapure water | Merck | ZIQ7000T0 | Milli-Q® IQ 7000 Ultrapure Water System |
References
- Forster, T. Intermolecular energy migration and fluorescence. Annals of Physics. 437 (1-2), 55-75 (1948).
- Stryer, L., Haugland, R. P. Energy transfer: a spectroscopic ruler. Proceedings of the National Academy of Sciences. 58 (2), 719-726 (1967).
- Hohlbein, J., et al. Conformational landscapes of DNA polymerase I and mutator derivatives establish fidelity checkpoints for nucleotide insertion. Nature Communications. 4 (1), 2131 (2013).
- Lerner, E., et al. Toward dynamic structural biology: Two decades of single-molecule Förster resonance energy transfer. Science. 359 (6373), (2018).
- Hohlbein, J., Craggs, T. D., Cordes, T. Alternating-laser excitation: single-molecule FRET and beyond. Chemical Society Reviews. 43 (4), 1156-1171 (2014).
- Lerner, E., et al. The FRET-based structural dynamics challenge — community contributions to consistent and open science practices. arXiv. , (2020).
- Hellenkamp, B., Wortmann, P., Kandzia, F., Zacharias, M., Hugel, T. Multidomain structure and correlated dynamics determined by self-consistent FRET networks. Nature Methods. 14 (2), 174-180 (2017).
- Craggs, T. D., et al. Substrate conformational dynamics facilitate structure-specific recognition of gapped DNA by DNA polymerase. Nucleic Acids Research. 47 (20), 10788-10800 (2019).
- Tsytlonok, M., et al. Dynamic anticipation by Cdk2/Cyclin A-bound p27 mediates signal integration in cell cycle regulation. Nature Communications. 10 (1), 1676 (2019).
- Nagy, J., et al. Complete architecture of the archaeal RNA polymerase open complex from single-molecule FRET and NPS. Nature Communications. 6 (1), 6161 (2015).
- LeBlanc, S. J., et al. Coordinated protein and DNA conformational changes govern mismatch repair initiation by MutS. Nucleic Acids Research. 46 (20), 10782-10795 (2018).
- Segal, M., et al. High-throughput smFRET analysis of freely diffusing nucleic acid molecules and associated proteins. Methods. 169, 21-45 (2019).
- Kapanidis, A. N., et al. Fluorescence-aided molecule sorting: Analysis of structure and interactions by alternating-laser excitation of single molecules. Proceedings of the National Academy of Sciences. 101 (24), 8936-8941 (2004).
- Kapanidis, A. N., et al. Alternating-laser excitation of single molecules. Accounts of Chemical Research. 38 (7), 523-533 (2005).
- Müller, B. K., Zaychikov, E., Brauchle, C., Lamb, D. C. Pulsed interleaved excitation. Biophysical Journal. 89 (5), 3508-3522 (2005).
- Laurence, T. A., Kong, X., Jager, M., Weiss, S. Probing structural heterogeneities and fluctuations of nucleic acids and denatured proteins. Proceedings of the National Academy of Sciences of the United States of America. 102 (48), 17348-17353 (2005).
- Pollina, T., et al. PlanktonScope: Affordable modular imaging platform for citizen oceanography. bioRxiv. , 056978 (2020).
- Collins, J. T., et al. Robotic microscopy for everyone: the OpenFlexure microscope. Biomedical Optics Express. 11 (5), 2447-2460 (2020).
- Courtney, A., Alvey, L. M., Merces, G. O. T., Burke, N., Pickering, M. The Flexiscope: a low cost, flexible, convertible and modular microscope with automated scanning and micromanipulation. Royal Society Open Science. 7 (3), 191949 (2020).
- Martens, K. J. A., et al. Visualisation of dCas9 target search in vivo using an open-microscopy framework. Nature Communications. 10 (1), 3552 (2019).
- Auer, A., et al. Nanometer-scale multiplexed super-resolution imaging with an economic 3D-DNA-PAINT microscope. ChemPhysChem. 19 (22), 3024-3034 (2018).
- Li, H., et al. Squid: Simplifying quantitative imaging platform development and deployment. bioRxiv. , 424613 (2020).
- Ambrose, B., et al. The smfBox is an open-source platform for single-molecule FRET. Nature Communications. 11 (1), 5641 (2020).
- Ingargiola, A., Laurence, T., Boutelle, R., Weiss, S., Michalet, X. Photon-HDF5: An open file format for timestamp-based single-molecule fluorescence experiments. Biophysical Journal. 110 (1), 26-33 (2016).
- Hellenkamp, B., et al. Precision and accuracy of single-molecule FRET measurements-a multi-laboratory benchmark study. Nature Methods. 15 (9), 669-676 (2018).
- Ingargiola, A., Lerner, E., Chung, S., Weiss, S., Michalet, X. FRETBursts: An open source toolkit for analysis of freely-diffusing single-molecule FRET. PLOS One. 11 (8), 0160716 (2016).
- Torella, J. P., Holden, S. J., Santoso, Y., Hohlbein, J., Kapanidis, A. N. Identifying molecular dynamics in single-molecule FRET experiments with burst variance analysis. Biophysical Journal. 100 (6), 1568-1577 (2011).
- Tomov, T. E., et al. Disentangling subpopulations in single-molecule FRET and ALEX experiments with photon distribution analysis. Biophysical Journal. 102 (5), 1163-1173 (2012).
- Santoso, Y., Torella, J. P., Kapanidis, A. N. Characterizing single-molecule FRET dynamics with probability distribution analysis. ChemPhysChem. 11 (10), 2209-2219 (2010).
- Kalinin, S., Valeri, A., Antonik, M., Felekyan, S., Seidel, C. A. M. Detection of structural dynamics by FRET: A photon distribution and fluorescence lifetime analysis of systems with multiple states. The Journal of Physical Chemistry B. 114 (23), 7983-7995 (2010).
- Pirchi, M., et al. Photon-by-photon hidden Markov model analysis for microsecond single-molecule FRET kinetics. The Journal of Physical Chemistry B. 120 (51), 13065-13075 (2016).
- Schrimpf, W., Barth, A., Hendrix, J., Lamb, D. C. PAM: A framework for integrated analysis of imaging, single-molecule, and ensemble fluorescence data. Biophysical Journal. 114 (7), 1518-1528 (2018).
- Zijlstra, N., et al. Rapid microfluidic dilution for single-molecule spectroscopy of low-affinity biomolecular complexes. Angewandte Chemie International Edition. 56 (25), 7126-7129 (2017).
- Hellenkamp, B., Thurn, J., Stadlmeier, M., Hugel, T. Kinetics of transient protein complexes determined via diffusion-independent microfluidic mixing and fluorescence stoichiometry. The Journal of Physical Chemistry B. 122 (49), 11554-11560 (2018).
- Bennet, I. A., et al. Regional conformational flexibility couples substrate specificity and scissile phosphate diester selectivity in human flap endonuclease 1. Nucleic Acids Research. 46 (11), 5618-5633 (2018).

