Præcis og præcis enkeltmolekyle FRET-målinger ved hjælp af Open Source smfBox
Summary
Denne artikel indeholder trinvise instruktioner til at foretage fuldt korrigerede nøjagtige FRET-målinger på individuelle, frit diffuse biomolekyler ved hjælp af open source, billig smfBox, fra tænd, over justering og fokusering, til dataindsamling og -analyse.
Abstract
SmfBox er et nyligt udviklet omkostningseffektivt open source-instrument til enkeltmolekylet Förster Resonance Energy Transfer (smFRET), som gør målinger på frit spredende biomolekyler mere tilgængelige. Denne oversigt omfatter en trinvis protokol til brug af dette instrument til at foretage målinger af præcise FRET-effektivitetsgevinster i duplex-DNA-prøver, herunder oplysninger om prøveforberedelsen, instrumentopsætning og -justering, dataindsamling og komplette analyserutiner. Den fremlagte tilgang, som omfatter, hvordan man kan bestemme alle de korrektionsfaktorer, der er nødvendige for nøjagtige FRET-afledte afstandsmålinger, bygger på en lang række nylige samarbejdsarbejder i hele FRET-Fællesskabet, som har til formål at etablere standardprotokoller og analysetilgange. Denne protokol, som let kan tilpasses en række biomolekyllære systemer, bidrager til den voksende indsats for at demokratisere smFRET for det bredere videnskabelige samfund.
Introduction
Single-molekyle Förster resonans energioverførsel (smFRET) er en teknik, der måler FRET effektivitet mellem to farvestoffer-en donor og en acceptor-på niveau med de enkelte molekyler. FRET er en fotofysisk proces, der opstår som følge af det overlappende energispektre af to farvestoffer: Donoren er begejstret for lyset af en bestemt bølgelængde og overfører energi ikke-radiativt til acceptoren, hvilket resulterer i emission fra acceptoren. Effektiviteten af denne overførsel er omvendt proportional med den sjette effekt af afstanden mellem de to farvestoffer, så overførselseffektiviteten varierer med afstand1. Således kan denne FRET-effektivitet bruges til at bestemme rumlige oplysninger om det eller de molekyler, som farvestofferne er fastgjort til, inden for et interval på 3-10 nm. Denne skala, og det faktum, at ændringer i FRET effektivitet er følsomme over for Angstrom molekylære bevægelser3, gør teknikken velegnet til at undersøge strukturelle oplysninger om biomolekyler-såsom nukleinsyrer og proteiner-uden komplikationer af ensemble gennemsnit4,5,6. Mens ændringer i relative FRET effektivitetsgevinster kan bruges til at overvåge biomolekylær interaktioner og kropsbygningsdynamik, kaste lys på centrale cellulære processer såsom protein (un)foldning, transskription, og DNA replikation og reparation, absolut FRET effektivitet er blevet brugt til at bestemme præcise afstande for biomolekylær struktur bestemmelse7,8,9,10,11 , overvinde behovet for krystallisering eller frysning, som er nødvendig for nogle andre strukturelle metoder4,12.
smFRET-eksperimenter oftest har to former, konfocal eller total intern refleksion fluorescens (TIRF) mikroskopi. Mellem begge tilgange kan biomolekylernes molekylære dynamik typisk undersøges på tidshorisonter fra pico- til millisekunder (confocal, frit diffuse molekyler) op til millisekunder til timer (TIRF, overflade immobiliserede molekyler). Dette skyldes de forskellige opsætninger, der er involveret i hver teknik. I TIRF-mikroskopi immobiliseres molekyler på overfladen af et dias og ophidses af en evanescentbølge (Figur 1A). Her er fokus dog på konfokal mikroskopi, da dette er formatet af smfBox. I konfokal mikroskopi, molekyler er ikke immobiliseret og i stedet frit diffus via Brownian bevægelse gennem confocal volumen (~ 1 fL), dannet ved at fokusere en laserstråle gennem en høj numerisk blænde linse i et sted på nogle udpegede dybde i løsningen (Figur 1B). Den resulterende emission er fokuseret tilbage gennem den samme blænde og filtreret gennem en dichroic spejl (Figur 1C for fuld skematisk). Det er derefter fokuseret gennem et pinhole for at fjerne enhver out-of-fokus lys og på en lavine photodiode (APD). Når APD registrerer en foton, udsender den en TTL-puls, hvis timing kan registreres med op til picosecondopløsning. Observationstiden for disse frit diffuse molekyler i nærheden af det konfokale volumen er almindeligvis inden for rækkefølgen af millisekunder.
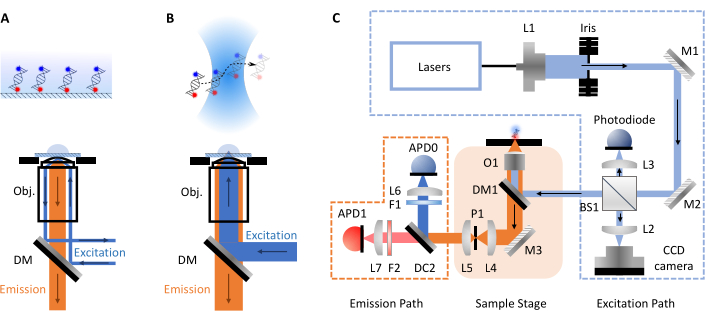
Figur 1: Skemaer, der viser principperne for mikroskopi og smfBox-opsætningen. (A) Total Internal Reflection Fluorescens (TIRF) Mikroskopiprincip: Excitationslys ledes ind i kanten af målet (Obj.) og gennemgår total intern refleksion ved coverslip-buffer-grænsefladen, der genererer et eksponentielt forfaldent evanescencefelt for at ophidse overfladeknyttede molekyler. (B) Konfokal mikroskopi: Frit diffuserende molekyler er begejstrede for en næsten diffraktion-begrænset stedet fokuseret på prøven. (C) Den smfBox-opsætning, der anvendes i denne protokol, og som viser alle nøglekomponenter: lavinefotodioder (APD), strålekløver (BS), dichroiske spejle (DM), filtre (F), spejle (M), mål (O) og pinhole (P). Klik her for at se en større version af dette tal.
For nylig, smFRET teknikker indarbejdet to farve excitation, hvor lasere matcher donor og acceptor excitation bølgelængder er vekslet5. Dette kan gøres på en af to måder, den første ved at modulere kontinuerlige bølge lasere på KHz tidsskala, som er kendt som skiftevis laser excitation (ALEX)13,14. Den anden metode blander hurtige impulser på MHz-tidsskalaen. dette er nanosekund-ALEX15 eller pulserende interleaved excitation (PIE)16. I alle disse tilgange fører oplysninger fra acceptorlaseren til beregning af den såkaldte stoichimetri, som kan skelne mellem molekyler med en lav FRET-effektivitet og dem, der mangler en acceptor (enten gennem ufuldstændig mærkning eller fotobleaching). Ved hjælp af PIE/ns-ALEX giver derudover adgang til fluorescerende levetid på enkeltmolekyleniveau, og anisotropier kan måles, når de kombineres med polariserende optik. Denne kombination af målinger kaldes multiparameter fluorescensdetektering (MFD)9.
På trods af de mange fordele ved smFRET er det ikke meget udbredt uden for specialiserede laboratorier på grund af de høje omkostninger ved kommercielle instrumenter og mangel på enkle, selvbyggede alternativer. En stigende tendens til udvikling af billige opensource mikroskopi finder sted, og andre platforme er for nylig dukket op, herunder Planktonscope17, OpenFlexure Microscope18, Flexiscope19, miCube20, liteTIRF21, og Squid22. Heri beskriver undersøgelsen protokollen for brug af smfBox, en nyligt udviklet omkostningseffektiv konfokal set-up, der er i stand til at måle FRET-effektiviteten mellem to farvestoffer på frit diffuse enkelte molekyler. Detaljerede byggeinstruktioner og al den nødvendige driftssoftware er frit tilgængelige på: https://craggslab.github.io/smfBox/ 23. SmfBoxens optiske arrangement samles fra lettilgængelige komponenter købt hos overkommelige og bredt tilgængelige producenter, mens mikroskophuset (ansvarlig for størstedelen af udgiften i et standardkonfokalt set-up) er blevet erstattet af en brugerdefineret lystæt anodiseret aluminiumskasse (hvilket gør det muligt at foretage målinger under omgivende lysforhold). Denne boks huser vigtige optiske komponenter, herunder excitation dichroic, mål, og pinhole, og en mekanisk laser interlock, muliggør sin sikker drift som en klasse I laser produkt (se figur 1C for en fuld skematisk). SmfBox bruger ALEX til at validere farvestof stoichimetri og til at bestemme nøjagtige FRET korrektion faktorer. Det drives ved hjælp af specialskrevet, open source-software (smOTTER), som styrer alle aspekter af dataindsamlingen og udsender dataene i open source photon-HDF5 format24, der er kompatibel med mange tredjepartsanalyseværktøjer. SmfBox og erhvervelses- og dataanalyseprotokollerne blev for nylig testet mod >20 andre instrumenter (både confocal og TIRF) i et multilaboratoriet blindstudie25. Fret-effektivitetsgevinsterne var i god overensstemmelse med alle de andre instrumenter, på trods af at smfBox kun kostede en brøkdel af prisen på kommercielt tilgængelige opsætninger.
Her er en trin-for-trin protokol skitseret for at erhverve og analysere nøjagtige, absolutte FRET-effektivitetsgevinster på frit spredeNDE DNA-duplex’er ved hjælp af smfBox, hele vejen fra tænd, over justering og fokusering til dataindsamling og analyse. De prøver, der anvendes her, er tre duplex-DNA’er (der udviser høj-, mellem- og lav-FRET-effektivitet, se tabel 1), som blev vurderet i det verdensomspændende blindstudie25; metoden kan dog tilpasses mange molekylære systemer, herunder proteiner og andre nukleinsyrer. Håbet er, at en sådan detaljeret protokol, sammen med de allerede eksisterende byggeinstruktioner til smfBox23, vil bidrage til at gøre denne kraftfulde teknik endnu mere tilgængelig for en bred vifte af laboratorier.
Protocol
Representative Results
Discussion
De mest kritiske trin i protokollen er justeringen af mikroskopet og justering af prøvekoncentrationen til den korrekte fortynding. Hvis justeringen er slukket, kan der være utilstrækkeligt signal til at identificere byger og plot histogrammer, og hvis forskydning opstår mellem prøverne derefter præcis FRET korrektion kan mislykkes på grund af ændringer i lækage og detektion / excitation effektivitetsgevinster. Brugen af en passende koncentration er også vigtig, for høj en koncentration vil give tilfældige udbrud, der indeholder flere molekyler med potentielt forskellige FRET-effektivitetsgevinster eller mærkning af stoichiometrier. For lav koncentration vil give for få byger til robust dataanalyse.
Den protokol, der er beskrevet her, er til måling af afstande i statiske enkelt FRET arter. Hvis prøven har mere end én top i FRET-effektivitets histogrammet, eller toppe forekommer brede (hvilket kan ske med dynamiske arter), kan der være behov for flere udbrud for at passe histogrammer til samme grad af præcision. For to velseparerede toppe vil der være behov for ca. dobbelt så mange data, men hvis populationerne overlapper lidt, er der behov for endnu flere data.
Hvis de to populationer interkonverterer på eksperimentets tidsskala, kan systemets dynamik og kinetika potentielt bestemmes. Test som BVA27 og 2CDE28 kan bekræfte, at de mellemliggende udbrud er dynamiske, mens analyser, herunder dPDA29, 30 eller H2MM31, kan bestemme interkonverteringsraterne. Jupyter notebooks til BVA og 2CDE er tilgængelige på FRETBursts26 hjemmeside, og MATLab baseret software PAM32 kan køre BVA, 2CDE, og PDA analyser.
Confocal enkeltmolekyle FRET kan nemt observere tilstande meget mere kortvarigt (~ 1 ms) end TIRF; men de korte observationstider, begrænset af diffusion, giver ingen molekylær historie, og kan derfor ikke bestemme længere opholdstider, eller komplekse overgangsnetværk på den måde, at overflade immobiliserede eksperimenter kan.
Da protokollen måler frit diffuserende molekyler ved en meget lav koncentration, fungerer den bedst, når man måler intramolekylære afstande på det samme molekyle. Intermolekylære afstande mellem forbigående bundne molekyler kan måles, forudsat at KD af de to molekyler er lav nok til, at komplekset eksisterer i en betydelig mængde ved den lave arbejdskoncentration, der kræves af eksperimentet (~ 100 pM). Hvis KD er meget højere end dette, så kun syngende mærket molekyler vil blive set. Dette problem kan løses ved at bruge mikrofluidics til at blande de to mærkede komponenter sammen i en høj koncentration og derefter hurtigt fortynde og flyde over målet, før komplekset dissocierer33,34.
Måling fret effektivitet på enkelt-molekyle niveau har en betydelig fordel i forhold til ensemble teknikker, som det informerer om heterogene subpopulationer, som i et ensemble eksperiment ville være gennemsnit. Desuden giver enkeltmolekylet FRET med ALEX adgang til nøjagtige FRET-effektivitetsgevinster, som kan konverteres til nøjagtige afstande. Dette gør det muligt at fastlægge mere detaljerede strukturelle oplysninger i stedet for blot at undersøge relative afstandsændringer. SmfBox bærer alle disse fordele og kapaciteter, men kan konstrueres på et meget lavere budget end sammenlignelige kommercielt tilgængelige mikroskoper i stand til confocal smFRET23.
SmfBox repræsenterer en meget lavere adgangsbarriere for smFRET-teknikker, der gør det muligt for forskere at måle kropslige ændringer og nøjagtige afstande inden for og mellem proteiner og nukleinsyrer7,8,9,10,11,35.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Forfatterne anerkender taknemmeligt følgende finansieringskilder: BBSRC (BB/T008032/1); EPSRC (Studentship til B.A.) og MRC (Studentship til A.R.-T.).
Materials
| Amino modified oligonucleotide | Eurogentec | N/A | May be ordered from various suppliers or synthesised; amino modification enables labeling with NHS-ester modified dyes |
| Avalanche photodiode (APD) | Excelitas | SPCM-AQRH-14 | Two APDs are required for the smfBox setup |
| Bovine Serum Albumin (BSA) | Merck | A2153 | System dependant; imaging buffer component (0.1 mg/mL in buffer) |
| Compact Laser Combiner | OMICRON | LightHUB-2 | 515 nm (80 mW) and 638 nm (100 mW) lasers |
| Coverglass | VWR | 630-2742 | Thickness: 0.17 ± 0.01 mm, LxW: 22×22 mm |
| Cy3B | Cytiva | PA63101 | 1 mg, PA63100 (5 mg), PA96106 (25 mg) |
| FRETBursts Python Package | N/A | N/A | Open-source python package for burst analysis of freely-diffusing single-molecule FRET data: https://fretbursts.readthedocs.io |
| Imaging Buffer | N/A | System dependant; 5 mM NaCl, 20 mM MgCl2, 5 mM Tris pH 7.5 and 0.1 mg/mL BSA | |
| Immersion Oil | Olympus | IMMOIL-F30CC | |
| Jupyter notebooks | Project Jupyter | N/A | Open-source web application to create and share documents that contain live code, equations, visualizations and text; data analysis notebooks for smfBox can be found in the SI |
| Lens Tissue | ThorLabs | MC-5 | MC-50E is same item in bulk |
| Magnesium Chloride | Merck | M2670 | System dependant; imaging buffer component (20 mM in buffer) |
| MilliQ/Ultrapure water | N/A | ||
| Nanopoistioner | Piezoconcept | FOC300 | Nanopositioner for accurate positioning of microscope objective |
| NHS-ester modified ATTO-550 | ATTO-TEC | AD 550-31 | 1 mg, AD 550-35 (5 mg) |
| NHS-ester modified ATTO-647N | ATTO-TEC | AD 647N-31 | 1 mg, AD 647N-35 (5 mg) |
| Objective lens | Olympus | N1480700 | Olympus objective series from orignal smfBox discontinued; replaced by N5702300 |
| OMICRON Control Center (OCC)- laser control center | OMICRON | N/A | v3.5.34 – OMICRON laser driver software |
| Press-To-Seal silicone isolator | Grace Bio-Labs | 664201 | 8-9 mm Diameter x 1.7 mm Depth |
| smOTTER | N/A | N/A | Open-source acquisition software for the Craggs Lab smfBox: https://github.com/craggslab/smOTTER |
| Sodium Chloride | Merck | S7653 | System dependant; imaging buffer component (5 mM in buffer) |
| Tris base | Merck | 93362 | System dependant; imaging buffer component (5 mM, pH 7.5 in buffer) |
| Type I ultrapure water | Merck | ZIQ7000T0 | Milli-Q® IQ 7000 Ultrapure Water System |
References
- Forster, T. Intermolecular energy migration and fluorescence. Annals of Physics. 437 (1-2), 55-75 (1948).
- Stryer, L., Haugland, R. P. Energy transfer: a spectroscopic ruler. Proceedings of the National Academy of Sciences. 58 (2), 719-726 (1967).
- Hohlbein, J., et al. Conformational landscapes of DNA polymerase I and mutator derivatives establish fidelity checkpoints for nucleotide insertion. Nature Communications. 4 (1), 2131 (2013).
- Lerner, E., et al. Toward dynamic structural biology: Two decades of single-molecule Förster resonance energy transfer. Science. 359 (6373), (2018).
- Hohlbein, J., Craggs, T. D., Cordes, T. Alternating-laser excitation: single-molecule FRET and beyond. Chemical Society Reviews. 43 (4), 1156-1171 (2014).
- Lerner, E., et al. The FRET-based structural dynamics challenge — community contributions to consistent and open science practices. arXiv. , (2020).
- Hellenkamp, B., Wortmann, P., Kandzia, F., Zacharias, M., Hugel, T. Multidomain structure and correlated dynamics determined by self-consistent FRET networks. Nature Methods. 14 (2), 174-180 (2017).
- Craggs, T. D., et al. Substrate conformational dynamics facilitate structure-specific recognition of gapped DNA by DNA polymerase. Nucleic Acids Research. 47 (20), 10788-10800 (2019).
- Tsytlonok, M., et al. Dynamic anticipation by Cdk2/Cyclin A-bound p27 mediates signal integration in cell cycle regulation. Nature Communications. 10 (1), 1676 (2019).
- Nagy, J., et al. Complete architecture of the archaeal RNA polymerase open complex from single-molecule FRET and NPS. Nature Communications. 6 (1), 6161 (2015).
- LeBlanc, S. J., et al. Coordinated protein and DNA conformational changes govern mismatch repair initiation by MutS. Nucleic Acids Research. 46 (20), 10782-10795 (2018).
- Segal, M., et al. High-throughput smFRET analysis of freely diffusing nucleic acid molecules and associated proteins. Methods. 169, 21-45 (2019).
- Kapanidis, A. N., et al. Fluorescence-aided molecule sorting: Analysis of structure and interactions by alternating-laser excitation of single molecules. Proceedings of the National Academy of Sciences. 101 (24), 8936-8941 (2004).
- Kapanidis, A. N., et al. Alternating-laser excitation of single molecules. Accounts of Chemical Research. 38 (7), 523-533 (2005).
- Müller, B. K., Zaychikov, E., Brauchle, C., Lamb, D. C. Pulsed interleaved excitation. Biophysical Journal. 89 (5), 3508-3522 (2005).
- Laurence, T. A., Kong, X., Jager, M., Weiss, S. Probing structural heterogeneities and fluctuations of nucleic acids and denatured proteins. Proceedings of the National Academy of Sciences of the United States of America. 102 (48), 17348-17353 (2005).
- Pollina, T., et al. PlanktonScope: Affordable modular imaging platform for citizen oceanography. bioRxiv. , 056978 (2020).
- Collins, J. T., et al. Robotic microscopy for everyone: the OpenFlexure microscope. Biomedical Optics Express. 11 (5), 2447-2460 (2020).
- Courtney, A., Alvey, L. M., Merces, G. O. T., Burke, N., Pickering, M. The Flexiscope: a low cost, flexible, convertible and modular microscope with automated scanning and micromanipulation. Royal Society Open Science. 7 (3), 191949 (2020).
- Martens, K. J. A., et al. Visualisation of dCas9 target search in vivo using an open-microscopy framework. Nature Communications. 10 (1), 3552 (2019).
- Auer, A., et al. Nanometer-scale multiplexed super-resolution imaging with an economic 3D-DNA-PAINT microscope. ChemPhysChem. 19 (22), 3024-3034 (2018).
- Li, H., et al. Squid: Simplifying quantitative imaging platform development and deployment. bioRxiv. , 424613 (2020).
- Ambrose, B., et al. The smfBox is an open-source platform for single-molecule FRET. Nature Communications. 11 (1), 5641 (2020).
- Ingargiola, A., Laurence, T., Boutelle, R., Weiss, S., Michalet, X. Photon-HDF5: An open file format for timestamp-based single-molecule fluorescence experiments. Biophysical Journal. 110 (1), 26-33 (2016).
- Hellenkamp, B., et al. Precision and accuracy of single-molecule FRET measurements-a multi-laboratory benchmark study. Nature Methods. 15 (9), 669-676 (2018).
- Ingargiola, A., Lerner, E., Chung, S., Weiss, S., Michalet, X. FRETBursts: An open source toolkit for analysis of freely-diffusing single-molecule FRET. PLOS One. 11 (8), 0160716 (2016).
- Torella, J. P., Holden, S. J., Santoso, Y., Hohlbein, J., Kapanidis, A. N. Identifying molecular dynamics in single-molecule FRET experiments with burst variance analysis. Biophysical Journal. 100 (6), 1568-1577 (2011).
- Tomov, T. E., et al. Disentangling subpopulations in single-molecule FRET and ALEX experiments with photon distribution analysis. Biophysical Journal. 102 (5), 1163-1173 (2012).
- Santoso, Y., Torella, J. P., Kapanidis, A. N. Characterizing single-molecule FRET dynamics with probability distribution analysis. ChemPhysChem. 11 (10), 2209-2219 (2010).
- Kalinin, S., Valeri, A., Antonik, M., Felekyan, S., Seidel, C. A. M. Detection of structural dynamics by FRET: A photon distribution and fluorescence lifetime analysis of systems with multiple states. The Journal of Physical Chemistry B. 114 (23), 7983-7995 (2010).
- Pirchi, M., et al. Photon-by-photon hidden Markov model analysis for microsecond single-molecule FRET kinetics. The Journal of Physical Chemistry B. 120 (51), 13065-13075 (2016).
- Schrimpf, W., Barth, A., Hendrix, J., Lamb, D. C. PAM: A framework for integrated analysis of imaging, single-molecule, and ensemble fluorescence data. Biophysical Journal. 114 (7), 1518-1528 (2018).
- Zijlstra, N., et al. Rapid microfluidic dilution for single-molecule spectroscopy of low-affinity biomolecular complexes. Angewandte Chemie International Edition. 56 (25), 7126-7129 (2017).
- Hellenkamp, B., Thurn, J., Stadlmeier, M., Hugel, T. Kinetics of transient protein complexes determined via diffusion-independent microfluidic mixing and fluorescence stoichiometry. The Journal of Physical Chemistry B. 122 (49), 11554-11560 (2018).
- Bennet, I. A., et al. Regional conformational flexibility couples substrate specificity and scissile phosphate diester selectivity in human flap endonuclease 1. Nucleic Acids Research. 46 (11), 5618-5633 (2018).

