ड्रोसोफिला ओसाइट में परमाणु प्रवासन
Summary
ड्रोसोफिलामें, ओसाइट न्यूक्लियस ऊजनजेलिस के दौरान माइक्रोट्यूबुल पर निर्भर प्रवास से गुजरता है। यहां, हम एक प्रोटोकॉल का वर्णन करते हैं जिसे अंडे के कक्षों पूर्व वीवोपर लाइव इमेजिंग करके माइग्रेशन का पालन करने के लिए विकसित किया गया था। हमारी प्रक्रिया कताई-डिस्क कॉन्फोकल माइक्रोस्कोपी का उपयोग करके बहु-स्थिति 3डी समय-चूक फिल्मों को प्राप्त करने के लिए 12 एच के लिए जीवित अंडे कक्षों का रखरखाव करती है।
Abstract
लाइव सेल इमेजिंग विशेष रूप से सेलुलर और आणविक तंत्र को समझने के लिए आवश्यक है जो ऑर्गेनेल आंदोलनों, साइटोस्केलेटन पुनर्व्यवस्थाओं, या कोशिकाओं के भीतर ध्रुवता पैटर्निंग को विनियमित करता है। ओसाइट न्यूक्लियस पोजिशनिंग का अध्ययन करते समय, इस प्रक्रिया की गतिशील घटनाओं को पकड़ने के लिए लाइव-इमेजिंग तकनीकें आवश्यक हैं। ड्रोसोफिला अंडा कक्ष एक बहुकोशिकीय संरचना है और इस घटना का अध्ययन करने के लिए एक उत्कृष्ट मॉडल प्रणाली है क्योंकि इसके बड़े आकार और कई आनुवंशिक उपकरणों की उपलब्धता है। ड्रोसोफिला मिड-ऊजीनेसिस के दौरान, नाभिक माइक्रोट्यूबुले-जनित बलों द्वारा मध्यस्थता की गई असममित स्थिति को अपनाने के लिए ओसाइट के भीतर एक केंद्रीय स्थिति से स्थानांतरित हो जाता है। भ्रूण और बाद में वयस्क मक्खी की ध्रुवता कुल्हाड़ियों को निर्धारित करने के लिए नाभिक का यह प्रवास और स्थिति आवश्यक है। इस माइग्रेशन की एक विशेषता यह है कि यह तीन आयामों (3 डी) में होता है, जिससे लाइव इमेजिंग की आवश्यकता होती है। इस प्रकार, परमाणु प्रवास को विनियमित करने वाले तंत्रों का अध्ययन करने के लिए, हमने विच्छेदित अंडे कक्षों को संस्कृति देने और कताई-डिस्क कॉन्फोकल माइक्रोस्कोपी का उपयोग करके समय-चूक अधिग्रहण द्वारा 12 घंटे के लिए लाइव इमेजिंग करने के लिए एक प्रोटोकॉल विकसित किया है । कुल मिलाकर, हमारी स्थितियां हमें लंबे समय तक ड्रोसोफिला अंडे के कक्षों को जीवित रखने की अनुमति देती हैं, जिससे परमाणु प्रवास को पूरा करने को 3 डी में बड़ी संख्या में नमूनों में कल्पना करने में सक्षम बनाया जा सके ।
Introduction
कई वर्षों से ड्रोसोफिला ओसाइट परमाणु प्रवास का अध्ययन करने के लिए एक आदर्श प्रणाली के रूप में उभरा है । ड्रोसोफिला ओसाइट एक बहुकोशिकीय संरचना में विकसित होता है जिसे अंडा कक्ष कहा जाता है। अंडे के कक्षों में 16 रोगाणु कोशिकाएं (15 नर्स कोशिकाएं और ओसाइट) शामिल हैं जो कूप दैहिक कोशिकाओं की एक महामारी परत से घिरा हुआ है। अंडा कक्ष विकास को 14 चरणों(चित्रा 1A)में विभाजित किया गया है, जिसके दौरान ओसाइट बढ़ेगा और भ्रूण के प्रारंभिक विकास के लिए आवश्यक भंडार जमा होगा। विकास के दौरान, माइक्रोट्यूबुल पुनर्गठन और मातृ निर्धारकों के असममित परिवहन पर, ऑसाइट एंटेरो-पृष्ठीय और डोरसो-वेंट्रल कुल्हाड़ियों के साथ ध्रुवित होता है। ये अक्ष भ्रूण के बाद की ध्रुवता कुल्हाड़ियों और इस ओसाइट1के निषेचन से उत्पन्न होने वाले वयस्क को निर्धारित करते हैं । ऊजीने के दौरान, नाभिक ओसाइट में असममित स्थिति को अपनाता है। चरण 6 में, नाभिक कोशिका में केंद्रित है। ओसाइट द्वारा प्राप्त होने वाली पीछे की कूप कोशिकाओं द्वारा उत्सर्जित सिग्नल की पहचान किए जाने पर, नाभिक चरण 7(चित्रा 1 बी)2,3में पूर्वकाल और पार्श्व प्लाज्मा झिल्ली के बीच चौराहे की ओर पलायन करता है। इस असममित स्थिति को डोरसो-वेंट्रल अक्ष के निर्धारण को प्रेरित करने की आवश्यकता होती है।
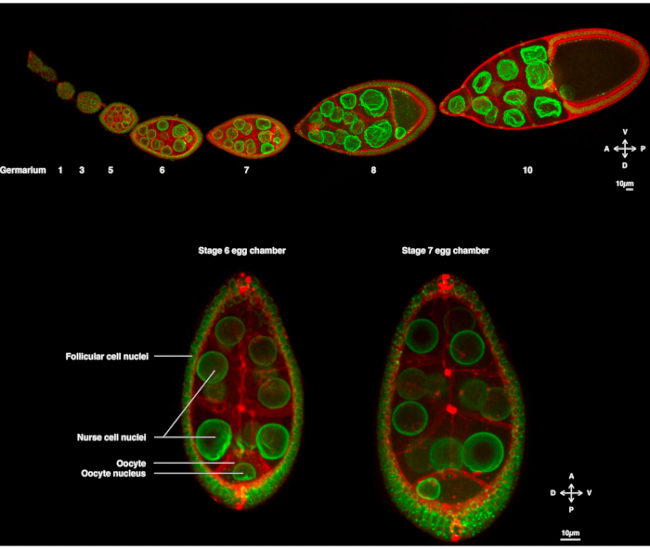
चित्रा 1: ड्रोसोफिला मेलनोगास्टर अंडे कक्ष। (ए)ट्रांसजेनिक मक्खियों से फिक्स्ड ओवेरियोल एफएसएस (2) केट-जीएफपी व्यक्त करते हैं जो परमाणु लिफाफे और यूबीआई-पीएच-आरएफपी को लेबल करता है जो प्लाज्मा झिल्ली को लेबल करता है। ओवेरिओल विभिन्न चरणों में अंडे के कक्षों के विकास से बना है। पूर्वकाल टिप (बाएं) पर रोगाणु के साथ पूर्वाचल धुरी के साथ परिपक्वता बढ़ जाती है जहां रोगाणु स्टेम सेल रहता है और पीछे की नोक पर पुराने चरण (दाएं)। (ख)ओजेनेसिस (बाएं) के चरण 6 पर डिस्क कॉन्फोकल माइक्रोस्कोपी कताई द्वारा जीवित अंडे के कक्ष का जेड-प्रक्षेपण, जिसमें नाभिक ओसाइट में केंद्रित होता है। नाभिक पूर्वकाल प्लाज्मा झिल्ली (ओसाइट और नर्स सेल के बीच) और पार्श्व प्लाज्मा झिल्ली (ओसाइट और कूप कोशिकाओं के बीच) के संपर्क में चरण 7 (दाएं) पर विषम स्थिति को अपनाने के लिए माइग्रेट करेगा। यह स्थिति पृष्ठीय पक्ष के निर्धारण को प्रेरित करेगी और इस प्रकार, अंडे के कक्ष की डोरसो-वेंट्रल धुरी। कृपया इस आंकड़े का एक बड़ा संस्करण देखने के लिए यहां क्लिक करें ।
कई दशकों से इस परमाणु प्रवास का अध्ययन इम्यूनोदाता द्वारा तय ऊतकों पर किया जाता रहा है । इस दृष्टिकोण ने यह प्रदर्शित करना संभव बना दिया है कि यह प्रक्रिया माइक्रोट्यूबल्स4,5के सघन नेटवर्क पर निर्भर करती है । हाल ही में, हमने कई घंटों के दौरान ओसाइट के लाइव इमेजिंग के साथ संगत स्थितियों की पेशकश करने वाला एक प्रोटोकॉल विकसित किया जिससे इस प्रक्रिया का गतिशील रूप से अध्ययन करना संभव होसके 6।
इसलिए, पहली बार, हम यह वर्णन करने में सक्षम रहे हैं कि नाभिक के प्रवास के दौरान तरजीही और विशिष्ट प्रक्षेप पथ हैं, एक पूर्वकाल प्लाज्मा झिल्ली (एपीएम) के साथ और दूसरा ओसाइट(चित्रा 2)के पार्श्व प्लाज्मा झिल्ली (एलपीएम) के साथ। ये नवीनतम परिणाम परमाणु प्रवासन जैसी गतिशील प्रक्रियाओं का अध्ययन करते समय लाइव-इमेजिंग प्रोटोकॉल के महत्व को रेखांकित करते हैं ।
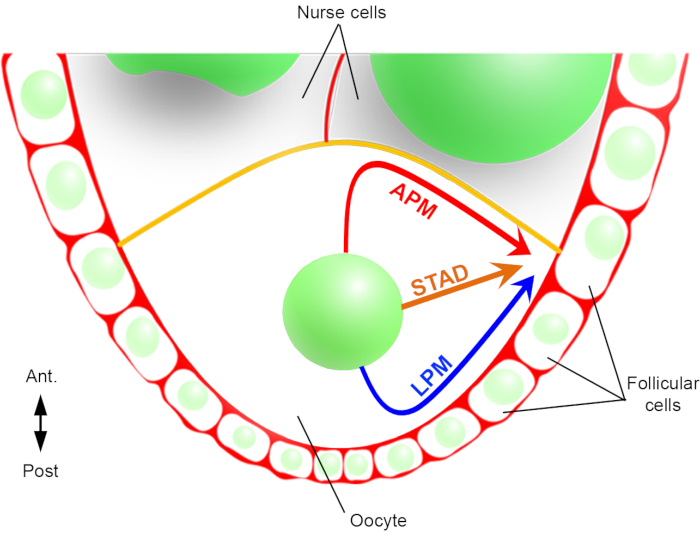
चित्रा 2:नाभिक के विभिन्न प्रवास पथों का योजनाबद्ध प्रतिनिधित्व। ऊजेनेसिस के चरण 6 में, ओसाइट एक केंद्रीय नाभिक के साथ एक बड़ी कोशिका है। इस स्तर पर, पूर्व-पीछे ध्रुवीयता धुरी कूप कोशिकाओं के संपर्क में ओसाइट के पीछे/पार्श्व प्लाज्मा झिल्ली के साथ सेट की जाती है और पूर्वकाल प्लाज्मा झिल्ली (पीले रंग में) नर्स कोशिकाओं2के संपर्क में है। हमने पहले बताया है कि नाभिक या तो पूर्वकाल प्लाज्मा झिल्ली (एपीएम) के साथ, पार्श्व प्लाज्मा झिल्ली (एलपीएम) के साथ, या साइटोप्लाज्म (एआरटीएडी, सीधे एंटेरो-पृष्ठीय प्रांतस्था)6के माध्यम से स्थानांतरित हो सकता है। कृपया इस आंकड़े का एक बड़ा संस्करण देखने के लिए यहां क्लिक करें ।
ओसाइट न्यूक्लियस माइग्रेशन लगभग 3 एच6की घटना है, और अब तक, वास्तविक माइग्रेशन की शुरुआत को ट्रिगर करने वाली घटना अज्ञात है। माइग्रेशन की शुरुआत में इस तंत्र का अध्ययन करने के लिए उपयोग किए जाने वाले प्रोटीन म्यूटेंट द्वारा भी देरी की जा सकती है। इन अज्ञात चर हमें लंबे समय तक (10-12 घंटे) से अधिक छवियों को प्राप्त करने के लिए प्रेरित किया । इसलिए यह सुनिश्चित करना जरूरी है कि ओसाइट्स जिंदा रहें । जैसे ही अंडा कक्ष विकसित होता है, यह एक गोलाकार से अण्डाकार आकार तक एंटेरो-पीछे की धुरी के साथ बढ़ जाता है। यह विस्तार कूप कोशिकाओं के घूर्णन से प्रेरित होता है, जो चरण 1 से चरण 8 तक होता है, लंबवत से एंटीरो-पीछे की धुरी7तक। इसके अलावा, स्पंदन संपत्ति के साथ मांसपेशियों की एक ट्यूबलर म्यान अंडे के कक्षों को घेरे हुए है। इसका शारीरिक कार्य विकासशील रोम को लगातार8की ओर धकेलना है । उनके विच्छेदन के बाद अंडे कक्षों के दोलनों को प्रेरित करने वाले आंदोलनों को सीमित करने के लिए, हमने ऊंचाई में 150 माइक्रोमीटर(चित्र 3 ए)को मापने वाला एक अवलोकन माइक्रो-चैंबर तैयार किया। यह ऊंचाई 10 और 11 चरणों में एक कूप के आकार से मामूली अधिक है । यह अंडे के कक्ष के घूर्णन को संरक्षित करते हुए नमूने के ऊर्ध्वाधर आंदोलनों को काफी सीमित करता है, जिसके परिणामस्वरूप कूप विकास में सीमित दोष होते हैं। हम तो एक कताई डिस्क कंफोकल माइक्रोस्कोप का उपयोग कर बहु स्थिति समय चूक अधिग्रहण द्वारा विच्छेदित अंडे कक्षों पर 12 घंटे के लिए लाइव इमेजिंग प्रदर्शन करते हैं । यहां हम चरणों 6 और 7 के बीच oocyte परमाणु प्रवास का अध्ययन करने के लिए हमारे प्रोटोकॉल का वर्णन ।
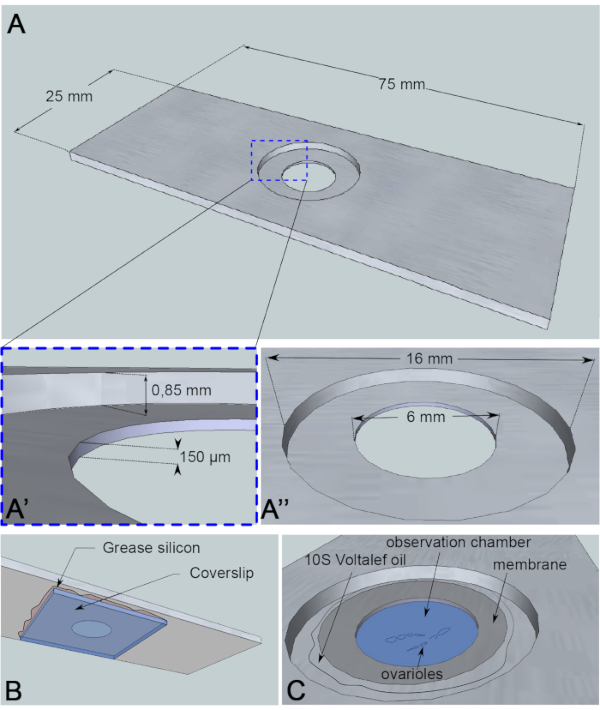
चित्रा 3:अवलोकन कक्ष का योजनाबद्ध प्रतिनिधित्व। (ए)(शीर्ष दृश्य) एल्यूमीनियम स्लाइड के सटीक आयामों को ऊंचाइयों (ए’) और स्लाइड के बीच में अच्छी तरह से ड्रिल किए गए परिधि (ए’) के साथ। (ख)(नीचे देखें) कुएं को अवरुद्ध करने वाला एक कवरस्लिप सिलिकॉन तेल के साथ स्लाइड करने के लिए सील किया जाता है । (ग)(टॉप व्यू) विच्छेदित ओवरियोल्स एक इमेजिंग माध्यम में विकसित होते हैं जो गैस पारमी योग्य झिल्ली से ढका होता है। झिल्ली को स्थिर करने के लिए हेलोकार्बन तेल का उपयोग किया जाता है। कृपया इस आंकड़े का एक बड़ा संस्करण देखने के लिए यहां क्लिक करें ।
परमाणु प्रवास का पालन करने और ओसाइट में प्रक्षेप पथ का सटीक आकलन करने के लिए, परमाणु लिफाफे और प्लाज्मा झिल्ली दोनों के लिए मार्कर की आवश्यकता है । इस उद्देश्य के साथ, दो ट्रांसजीन जिनका उच्च संकेत/शोर अनुपात है और लाइव इमेजिंग के दौरान फीका नहीं है, का चयन किया गया है । प्लाज्मा झिल्ली को लेबल करने के लिए, एक पी [यूबीआई-पीएच-आरएफपी] का उपयोग जो आरएफपी के लिए जुड़े मानव फॉस्फोलिपेज सी ∂1 (पीएलसी∂1) के प्लेक्ट्रिन होमोलॉजी (पीएच) डोमेन को एन्कोड करता है। यह पीएच डोमेन ओसाइट 9 की प्लाज्मा झिल्ली के साथ वितरित फॉस्फोनोसिटाइडपीआई (4,5)पी 2 से बांधता है। परमाणु लिफाफे के लिए, पी [पीपीटी-un1] Fs (2) केट-जीएफपी प्रोटीन-ट्रैप तनाव जहां जीएफपी को जीन एन्कोडिंग के भीतर डाला जाता है ड्रोसोफिला एस-इम्पोर्टिन एक सजातीय और एक गहन संकेत10प्रदर्शित करता है । युवा मक्खियों (1-2 दिन पुराने) को अंडाशय विच्छेदन से पहले शुष्क खमीर 24-48 घंटे वाली ताजा शीशियों में रखा जाता है।
इस लाइव इमेजिंग परख के लिए, एल्यूमीनियम का एक 1 मिमी मोटा टुकड़ा है, जो नमूने के लिए अट्रैक्टिव है, को माइक्रोस्कोपी स्लाइड के आयामों में काट दिया गया है। इसमें स्लाइड के केंद्र में 16 मिमी व्यास का छेद है जिसे 0.85 मिमी तक काउंटर किया गया है। इस काउंटरबोर में 150 माइक्रोन(चित्रा 3 ए)की गहराई के साथ एक अतिरिक्त 6 मिमी व्यास छेद है। एल्यूमीनियम कक्ष(चित्रा 3B)के तल पर एक कवरस्लिप सिलिकॉन तेल (नमूने के लिए निष्क्रिय) से चिपका हुआ है। नमूनों को मध्यम-भरे कुएं में रखने के बाद, ओ2/सीओ 2एक्सचेंज के लिए पार की गई एक झिल्ली को मध्यम पर रखाजाता है और हेलोकार्बन तेल(चित्रा 3सी)से घिरा हुआ है।
विच्छेदन के लिए, 0.05 x 0.02 मिमी के टिप आयाम के साथ स्टेनलेस स्टील संदंश का उपयोग करने की सिफारिश की जाती है, और ओवरियोल्स(चित्रा 4B,सी)के पृथक्करण के लिए 0.20 मिमी व्यास सुई। माइग्रेट करने वाले नाभिक को कैमरे से लैस कताई-डिस्क कॉन्फोकल उल्टे माइक्रोस्कोप सीएसयू-एक्स1 पर चित्रित किया जाता है। बहु-स्थिति छवियों को 24 डिग्री सेल्सियस पर हर 15 मिनट में समय-चूक द्वारा प्राप्त किया गया था। 15 मिनट के अंतराल में नमूनों के लिए फ्लोरोसेंट प्रोटीन और फोटोटॉक्सिकिटी के सीमित फोटोब्लैचिंग के साथ बहु-स्थिति अधिग्रहण करने की अनुमति मिलती है। इसके अलावा, एक छोटा अंतराल परमाणु प्रक्षेप पथ का पालन करने के लिए बहुत अधिक जानकारीपूर्ण डेटा प्रदान नहीं करेगा । फिल्मों को फिजी सॉफ्टवेयर11 के माध्यम से संसाधित और विश्लेषण किया जाता है।
Protocol
Representative Results
Discussion
अन्य प्रोटोकॉल ों में वर्णन किया गया है कि ड्रोसोफिला अंडे के कक्षों को लाइव-इमेजिंग परख12, 13के लिए तैयार और संस्कृति कैसे तैयार कियाजाए। इस प्रोटोकॉल की नवीनता एक खोखले एल्यू?…
Disclosures
The authors have nothing to disclose.
Acknowledgements
हम जीन-एंटोनी लेपसेंट और निकोलस टिसोट के बेहद आभारी हैं जिन्होंने मूल रूप से प्रोटोकॉल विकसित किया और हमारे साथ चित्र 3 के कुछ चित्रमय तत्वों को साझा किया। हम फैनी रोलैंड-गॉसेलिन का शुक्रिया अदा करते हैं जिन्होंने फिगर 4 की तस्वीरें लीं । हम अन्य प्रयोगशाला सदस्यों को भी सहायक चर्चाओं के लिए धन्यवाद देते हैं जिन्होंने इस तकनीक के सुधार में योगदान दिया और नथानिएल हेनेमैन ने अपनी टिप्पणियों के लिए इस पांडुलिपि को बेहतर बनाने में मदद की। हम इंस्टीट्यूट जैक्स मोनोड की इमागोसैन कोर सुविधा को स्वीकार करते हैं, फ्रांस-बायोइमेजिंग (एएनआर-10-आईएनबीएस-04) के सदस्य। Maëlys Loh फ्रांस के अनुसंधान मंत्रालय (MESRI) से पीएचडी फैलोशिप द्वारा समर्थित है । एंटोनी गुइशे और फ्रेड बर्नार्ड को एआरसी (ग्रांट PJA20181208148), एसोसिएशन डेस एंट्रेप्रिस कॉन्ट्रोवर्सी ले कैंसर (ग्रांट गेफ्लूक 2020 #221366) और IdEx Université de पेरिस (ANR-18-IDEX-0001) से उद्भव अनुदान द्वारा समर्थित किया गया था।
Materials
| Anesthetize CO2 pad | Dutscher | 789060 | Anesthetize flies |
| Coverslip (24×50 mm) | Knittel Glass | VD12450Y100A | Observation-chamber preparation |
| Forceps Dumont #5 | Carl Roth | K342.1 | Dissection |
| Stainless steel needles | Entosphinx | 20 | Dissection |
| Heat-inactivated fetal calf serum | SIGMA-ALDRICH | F7524 | Imaging medium |
| Insulin solution bovine pancreas | SIGMA-ALDRICH | 10516 – 5ml | Imaging medium |
| Penicilin/Streptomycin solution | SIGMA-ALDRICH | P0781 | Imaging medium |
| Permeable membrane | Leica | 11521746 | Observation-chamber preparation |
| Schneider Medium | Pan Biotech | P04-91500 | Imaging medium |
| Silicon grease | BECKMAN COULTER | 335148 | Observation-chamber preparation |
| Spinning disk confocal | Zeiss | CSU-X1 | Nuclear migration observation |
| Voltalef oil 10S | VWR | 24627 – 188 | Observation-chamber preparation |
References
- Merkle, J. A., Wittes, J., Schüpbach, T. Signaling between somatic follicle cells and the germline patterns the egg and embryo of Drosophila. Current Topics in Developmental Biology. 140, 55-86 (2020).
- Roth, S., Lynch, J. A. Symmetry breaking during drosophila oogenesis. Cold Spring Harbor Perspectives in Biology. 1 (2), 001891 (2009).
- Bernard, F., Lepesant, J. -. A., Guichet, A. Nucleus positioning within Drosophila egg chamber. Seminars in Cell and Developmental Biology. 82, 25-33 (2017).
- Koch, E. A., Spitzer, R. H. Multiple effects of colchicine on oogenesis in Drosophila: Induced sterility and switch of potential oocyte to nurse-cell developmental pathway. Cell and Tissue Research. 228 (1), 21-32 (1983).
- Januschke, J., et al. The centrosome-nucleus complex and microtubule organization in the Drosophila oocyte. Development. 133, 129-139 (2006).
- Tissot, N., et al. Distinct molecular cues ensure a robust microtubule-dependent nuclear positioning in the Drosophila oocyte. Nature Communications. 8, 15168 (2017).
- Cetera, M., Horne-Badovinac, S. Round and round gets you somewhere: collective cell migration and planar polarity in elongating Drosophila egg chambers. Current Opinion in Genetics & Development. 32, 10-15 (2015).
- Hudson, A. M., Petrella, L. N., Tanaka, A. J., Cooley, L. Mononuclear muscle cells in Drosophila ovaries revealed by GFP protein traps. Developmental Biology. 314, 329-340 (2008).
- Gervais, L., Claret, S., Januschke, J., Roth, S., Guichet, A. PIP5K-dependent production of PIP2 sustains microtubule organization to establish polarized transport in the Drosophila oocyte. Development. 135 (23), 3829-3838 (2008).
- Villányi, Z., Debec, A., Timinszky, G., Tirián, L., Szabad, J. Long persistence of importin- b explains extended survival of cells and zygotes that lack the encoding gene ‘ n Villa. Mechanisms of Development. 3-4 (125), 196-206 (2008).
- Schindelin, J., et al. Fiji: An open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- Prasad, M., Jang, A. C. C., Starz-Gaiano, M., Melani, M., Montell, D. J. A protocol for culturing drosophila melanogaster stage 9 egg chambers for live imaging. Nature Protocols. 2 (10), 2467-2473 (2007).
- Weil, T. T., Parton, R. M., Davis, I. Preparing individual Drosophila egg chambers for live imaging. Journal of Visualized Experiments: JoVE. (60), (2012).
- Chanet, S., Huynh, J. R. Collective cell sorting requires contractile cortical waves in germline cells. Current Biology. 30 (21), 4213-4226 (2020).
- Zhao, T., Graham, O. S., Raposo, A., St Johnston, D. Growing microtubules push the oocyte nucleus to polarize the drosophila dorsal-ventral axis. Science. 336 (6084), 999-1003 (2012).
- Legent, K., Tissot, N., Guichet, A. Chapter 7 Oogenesis using fixed and live imaging. Drosophila Oogenesis: Methods and Protocols. 1328, 99-112 (2015).

