En mikroplatemateranalyse med høy gjennomstrømning for kvantifisering av forbruk i Drosophila
Summary
Mikroplatemateranalysen tilbyr en økonomisk, høy gjennomstrømningsmetode for kvantifisering av flytende matforbruk i Drosophila. En 3D-trykt enhet forbinder en 96-brønns mikroplate der fluer er plassert til en 1536-brønns mikroplate hvorfra fluer bruker en fôringsløsning med sporstoff. Nedgangen i løsningsvolumet måles spektrofotometrisk.
Abstract
Kvantifisering av matinntaket i Drosophila brukes til å studere de genetiske og fysiologiske understøttelsene av forbruksrelaterte egenskaper, deres miljøfaktorer og de toksikologiske og farmakologiske effektene av mange stoffer. Få metoder som for tiden implementeres, er egnet til måling av høy gjennomstrømning. Microplate Feeder Assay (MFA) ble utviklet for å kvantifisere forbruket av flytende mat til individuelle fluer ved hjelp av absorbans. I denne analysen bruker fluer flytende mat medium fra utvalgte brønner av en 1536-brønns mikroplate. Ved å inkorporere et fortynnet sporstoff i det flytende matmediet og laste inn et kjent volum i hver brønn, reflekterer absorbansmålinger av brønnen som er oppnådd før og etter forbruk den resulterende volumendringen (dvs. forbruk av volum). For å muliggjøre høy gjennomstrømningsanalyse med denne metoden, ble en 3D-trykt kobling designet som gjør at fluer kan sorteres individuelt i 96-brønns mikroplater. Denne enheten orienterer nøyaktig 96- og 1536-brønns mikroplater for å gi hver fluetilgang til opptil 4 brønner til konsum, og muliggjør dermed kvantifisering av matpreferanser i tillegg til vanlig forbruk. Videre har enheten barrierestrimler som veksler mellom åpne og lukkede posisjoner for å tillate kontrollert inneslutning og frigjøring av en kolonne med prøver om gangen. Denne metoden muliggjør høye gjennomstrømningsmålinger av forbruk av vandige løsninger av mange fluer samtidig. Det har også potensial til å bli tilpasset andre insekter og å screene forbruk av næringsstoffer, giftstoffer eller legemidler.
Introduction
Drosophila melanogaster har sett bred bruk som en genetisk modellorganisme for å studere de biologiske understøttelsene av matinntak og egenskaper forbundet med forbruk1. Det anslås at 65% av menneskelige sykdomsfremkallende gener har funksjonelle homologer i fluer, med en betydelig andel av dem som uttrykkes i funksjonelt tilsvarende vev mellom fluer og mennesker2. Videre gjør D. melanogasters størrelse, kort intergenerasjonell tid, enkelt vedlikehold og genetisk tractability det til en attraktiv modell for studier på forbruk av næringsstoffer3,4 og toksikologiske og farmakologiske effekter av en rekke stoffer, inkludert insektmidler5, miljøgifter6, legemidler7og legemidler av misbruk8,9,10.
I mange tilfeller krever studiet av slike egenskaper presis kvantifisering av forbruket. Metoder for kvantifisering av forbruk er varierte og inkluderer CApillary FEeder (CAFE) analyse11, MAnual FEeding (MAFE) analyse12, Proboscis Extension Response (PER) analyse13, tracer fargestoffutvinning14,15, oligonukleotid tracer ekstraksjon16, og radio-isotope ekstraksjon5,17. Nyere innsats har fokusert på å forbedre gjennomstrømningen av disse analysene, som i Expresso-analysen18 eller det platebaserte Whole Animal Feeding FLat (WAFFL) -systemet19. Til tross for deres nytte, kan disse analysene være kompliserte, kostbare eller arbeidskrevende, noe som hindrer bruken i studier med høy gjennomstrømning.
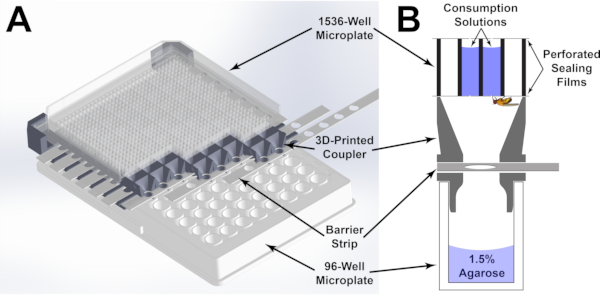
Figur 1: Komponenter i mikroplatemateranalysen (A) 3D-gjengivelse av den monterte mikroplatemateranalysen. Mikroplaten på 1536 brønner er orientert av den 3D-trykte koplingen slik at hver brønn på den nedre mikroplaten på 96 brønner har tilgang til fire brønner i den øvre mikroplaten på 1536 brønner. Tilgangen til brønnene kan styres ved å justere posisjonen til barrierestrimler som går gjennom koplingen. (B) En grafisk fremstilling av hver brønn i mikroplatemateranalysen. Forbruksløsninger beholdes i hver brønn ved hjelp av en tetningsfilm som har blitt perforert for å gi tilgang med fluen. Klikk her for å se en større versjon av denne figuren.
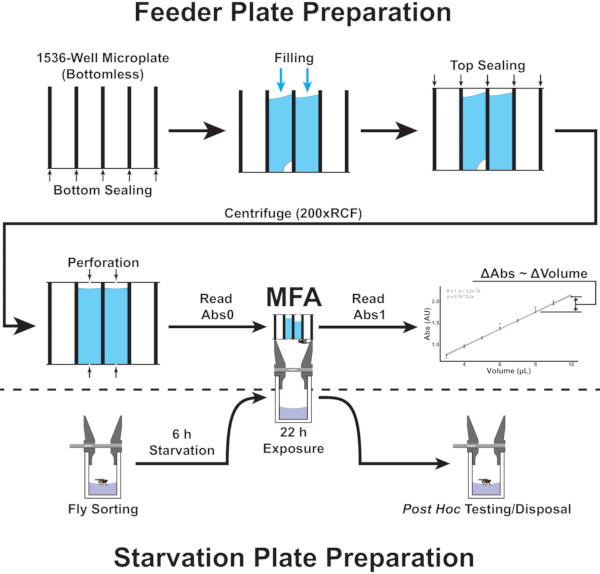
Figur 2: Oversikt over prosedyrene i mikroplatemateranalysen. Figuren viser et flytskjema som tilsvarer trinn 4.1-5.8 i protokollen. Klikk her for å se en større versjon av denne figuren.
For å overvinne disse hindringene, microplate feeder assay (MFA; Figur 1) ble utviklet. I denne analysen er fluer plassert individuelt i 96-brønns mikroplater. Hver mikroplate er koblet til en 1536-brønns mikroplate ved hjelp av en tilpasset, 3D-trykt enhet. Enheten orienterer nøyaktig de to platene slik at hver fly i sin respektive brønn på 96-brønnsplaten har tilgang til 4 brønner av 1536-brønns mikroplaten. Ved å bruke en bunnløs 1536-brønnsplate og tetningsfilmer, dispenseres løsninger i utvalgte brønner og perforeres med presise nåler med diameter på 0,25 mm for å gi tilgang til fluene. Kritisk, slik at forbruk direkte fra en mikroplate gir umiddelbare absorbansbaserte målinger ved hjelp av en mikroplateleser. Et fortynnet tracerfargestoff er innlemmet i forbruksmediet, og endringen i absorbans etter eksponering brukes til å bestemme volumet som forbrukes (figur 2 og figur 3). Siden væsken i hver brønn tilnærmer seg en kolonne med væske, vil volumetriske forskjeller manifestere seg som forskjeller i kolonnens høyde. (Figur 3A) I henhold til Øl-Lambert lov20:
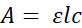
hvor A er absorbansen, ε er molarabsorpsjonskoeffisienten for den dempende analytten, l er den optiske banelengden, og c er konsentrasjonen av den dempende analytten. Således, med konstant molar absorpsjonskoeffisient og konsentrasjon, skyldes endringer i absorbans utelukkende endringer i den optiske lysbanen, det vil si væskenivået i en gitt brønn. Ved å måle absorbans før og etter eksponering reflekterer den proporsjonale endringen i absorbans den proporsjonale volumendringen (figur 3B).
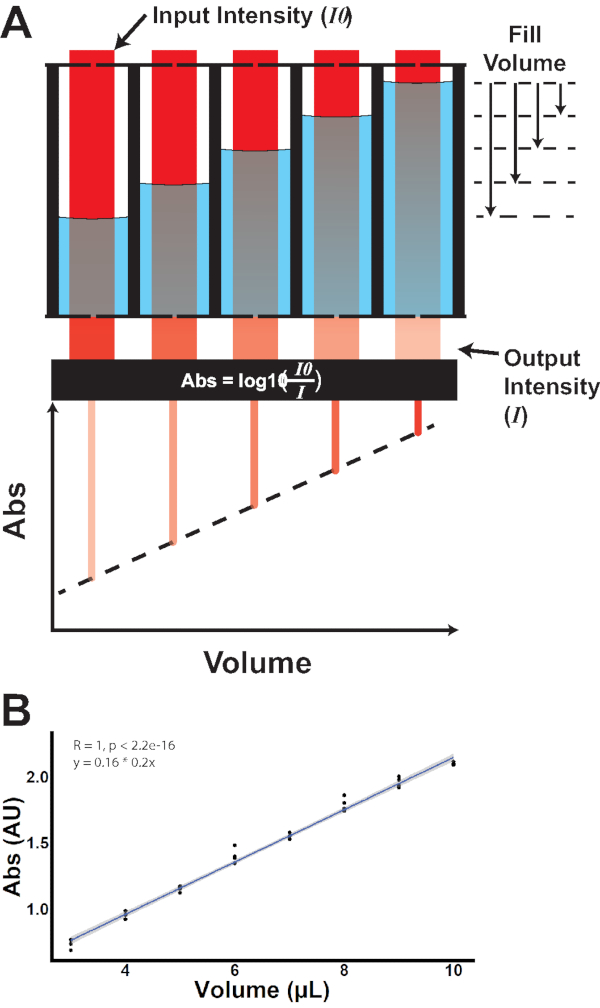
Figur 3: Absorbansbasert kvantifisering av brønnvolum. (A) Hendelseslys av kjent inngangsintensitet (I0) krysser hver brønn. Demping av lys ved ulike fyllvolumer gir forskjellige utgangsintensiteter (I), som viser en lineær sammenheng mellom volum og absorbans. (B) Empirisk måling av absorbans kontra volum. Klikk her for å se en større versjon av denne figuren.
Basert på volumendringen kan mengden av enhver inntatt forbindelse beregnes ut fra den kjente konsentrasjonen i fôringsløsningen. Delene som trengs for analysen er lave i kostnader og har en høy grad av gjenbrukbarhet, noe som reduserer de tilbakevendende kostnadene for analysen betydelig. Dermed tilbyr denne prosedyren en rimelig, høy gjennomstrømningsmetode for nøyaktig kvantifisering av forbruk.
Protocol
Representative Results
Discussion
Studien beskriver en ny protokoll for kvantifisering av forbruket i Drosophila: Microplate Feeder Assay (MFA). I denne analysen forbruker fluer fra forseglede brønner av en 1536-brønns mikroplate gjennom kontrollerte perforeringer (Figur 1, Figur 2; Tilleggsvideo S.1). Siden flytende mat farges og leveres via mikroplate, kan målinger av den optiske absorbansen av maten oppnås ved hjelp av et mikroplatespektrofotometer (figur 3). På denne måten bestemmes forbruket ved å sammenligne absorbansen før og etter forbruk, og deretter bruke denne andelen til det kjente volumet som ble dispensert før forbruk. Dette ble verifisert empirisk ved å måle absorbansen av forskjellige volumer av det fargede mediet (Figur 3B).
For å utvikle denne analysen var det nødvendig med en enhet som kunne utnytte den absorbansbaserte kvantifiseringen av forbruket. Testing av fluer i et mikroplateformat er tiltalende fordi det utfyller mikroplaten som brukes til å dispensere mat og gir fleksibilitet i å velge mellom flere plateformater (f.eks. 6-, 12-, 48- eller 96-brønnsformater) ved å justere koblingsgeometrien. Et 96-brønns mikroplateformat ble valgt for å tillate individuell fluekultur.
Den 3D-trykte enheten (figur 1) orienterer nøyaktig 1536-brønns materplaten med 96-brønns kulturplaten, noe som gir hver fluetilgang til opptil 4 brønner av materplaten til konsum. Videre, for å gi tilstrekkelig tid til å distribuere fluer inn i boligplaten og for å kontrollere analyseinitiering, inkluderer enheten toggling barrierestrimler som inneholder fluene i sine respektive brønner og forhindrer brudd. Filene som trengs for å anskaffe eller endre disse delene er gitt (Tilleggsfiler S.2–S.3), samt de nødvendige fabrikasjonsinstruksjonene for de aktuelle stykkene (Tilleggsfil S.4).
MFA gir en enkel høy gjennomstrømningsmetode som utfyller mer forseggjorte metoder for å overvåke Drosophila fôringsatferd18,21,22. MFA tilbyr flere fordeler i forhold til andre metoder som brukes til å kvantifisere matinntaket. Gjennomstrømningen økes ved å kvantifisere forbruket ved hjelp av en plateleser. Dette eliminerer manuelle målinger og hindrer manuell dataregistrering. Data er også egnet til programmatisk utvinning og behandling. I tillegg øker den høyere gjennomstrømningen det mulige antallet biologiske repliker, spesielt sammenlignet med felles materdesign, noe som øker kraften betydelig for å oppdage små forskjeller i forbruk. Ved hjelp av MFA kan en enkelt eksperimenter kvantifisere forbruket eller preferansen til over 500 fluer per nattkjøring av analysen. Ved overlappende serier av analysen kan over 2000 fluer testes i løpet av en 5-dagers periode. Til slutt er det langsiktige kostnadsbesparelser på grunn av gjenbrukbarheten av mikroplater og koblinger (Supplementary File S.5). Ved hjelp av MFA kan den estimerte kostnaden per analyse være så lav som $ 14.80, med en $ 127.60 forhåndskostnad for utstyret. Ved hjelp av den klassiske CApillary FEeder (CAFE)-analysen, som krever kostbare presisjonsmikrokapillærer, er den estimerte kostnaden per analyse for et sammenlignbart antall replikeringer $ 46,08. Selv om det er en forhåndsinvestering i å anskaffe nødvendig utstyr, kan reduksjonen i tilbakevendende kostnader føre til betydelige besparelser, spesielt i tilfeller der gjentatt testing utføres.
Som med alle analyser har MFA visse begrensninger. Hovedsakelig krever det tilgang til et mikroplatespektrofotometer som er i stand til å lese 1536-brønns mikroplater. I tillegg gjør avhengigheten av absorberingsmålinger for kvantifisering metoden utsatt for optisk interferens. Dette manifesterer seg som negative forbruksverdier for et lite delsett av prøver som er testet. Næringsstoffer, legemidler, legemidler eller giftstoffer av interesse må også være vannløselige for å være kompatible med analysen.
Til tross for begrensningene tilbyr denne metoden en høy gjennomstrømningsmetode for kvantifisering av forbruksatferd i Drosophila. Videre kan koblingsenheten enkelt endres for å akseptere mange plateformater, slik at den kan imøtekomme en rekke insektarter.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Dette arbeidet ble støttet av et stipend fra National Institute on Drug Abuse (U01 DA041613) til TFCM og RRHA.
Materials
| 0.25 mm Diameter Needers | Rave Scientific | RS-MN-52-001012 | |
| 0.45 µm Syringe Filters | Olympus Plastics | 25-245 | |
| 10 mL Disposable Syringe | EXELINT | 26200 | |
| Agarose | Fisher Scientific | BP1600 | |
| Barrier Strips (Laser Cut) | Ponoko | – | Material: clear PETG, 0.5mm thickness; Supplementary File: |
| Centrifuge 5810 R | Eppendorf | 22625501 | |
| Centrifuge Rotor A-4-62 with micro-titer plate buckets | Eppendorf | 22638041 | |
| FD&C Blue #1 | Spectrum Chemical Mfg Corp | FD110 | |
| Film Sealing Paddle | Fisher Scientific | 50-563-280 | |
| Flystuff Flypad | Genesee Scientific | #59-114 and #59-119 | CO2 Anesthesia: The Flypads come in two sizes, either of which is appropriate |
| Microplate Coupler (3D Printed) | Shapeways | – | Material: Multi Jet Fusion nylon (MJF PA12); Supplementary File: |
| Microplate Lids | Greiner Bio-One | 656170 | |
| Molecular Devices SpectraMax iD5 | Molecular Devices | – | Any microplate reader with 1536-well resolution will do. |
| Needle Probe Holder | Rave Scientific | RS-MN-52-001000 | |
| Polyester Sealing Film | Excel Scientific, Inc. | 100-SEAL-PLT | |
| Polystyrene 96-well microplates | Greiner Bio-One | 655101 | |
| Polystyrene, Bottomless, 15396-well microplates | Greiner Bio-One | 783000 | Made to Order; allow for adequate lead time when purchasing. |
| Rubber Bands | |||
| Sucrose | Sigma | S7903 | |
| Weather Stripping | 1/2" x 1/8" High Density Self Adhesive Neoprene Rubber | ||
| Yeast Extract | Fisher Scientific | BP1422 |
References
- Wong, R., Piper, M. D. W., Wertheim, B., Partridge, L. Quantification of food intake in Drosophila. PLoS ONE. 4 (6), (2009).
- Ugur, B., Chen, K., Bellen, H. J. Drosophila tools and assays for the study of human diseases. Disease Models & Mechanisms. 9 (3), 235-244 (2016).
- Spitaler, U., et al. Yeast species affects feeding and fitness of Drosophila suzukii adults. Journal of Pest Science. 93 (4), 1295-1309 (2020).
- Wang, Q. P., et al. PGC1α controls sucrose taste sensitization in Drosophila. Cell Reports. 31 (1), 107480 (2020).
- Valtierra-de-Luis, D., et al. Quantification of dose-mortality responses in adult Diptera: Validation using Ceratitis capitata and Drosophila suzukii responses to spinosad. PLoS ONE. 14 (2), 1-11 (2019).
- Williams, M. J., et al. Exposure to bisphenol A affects lipid metabolism in Drosophila melanogaster. Basic & Clinical Pharmacology & Toxicology. 114 (5), 414-420 (2014).
- Jajoo, A., Donlon, C., Shnayder, S., Levin, M., McVey, M. Sertraline induces DNA damage and cellular toxicity in Drosophila that can be ameliorated by antioxidants. Scientific Reports. 10 (1), 1-12 (2020).
- Fochler, S., et al. Genetics of alcohol consumption in Drosophila melanogaster. Genes, Brain and Behavior. 16 (7), 675-685 (2017).
- Highfill, C. A., Baker, B. M., Stevens, S. D., Anholt, R. R. H., Mackay, T. F. C. Genetics of cocaine and methamphetamine consumption and preference in Drosophila melanogaster. PLOS Genetics. 15 (5), 1007834 (2019).
- Keebaugh, E. S., Park, J. H., Su, C., Yamada, R., Ja, W. W. Nutrition Influences caffeine-mediated sleep loss in Drosophila. Sleep. 40 (11), (2017).
- Ja, W. W., et al. Prandiology of Drosophila and the CAFE assay. Proceedings of the National Academy of Sciences. 104 (20), 8253-8256 (2007).
- Qi, W., et al. A quantitative feeding assay in adult Drosophila reveals rapid modulation of food ingestion by its nutritional value. Molecular Brain. 8 (1), 87 (2015).
- Shiraiwa, T., Carlson, J. R. Proboscis extension response (PER) assay in Drosophila. Journal of Visualized Experiments: JoVE. (3), e193 (2007).
- Shell, B. C., et al. Measurement of solid food intake in Drosophila via consumption-excretion of a dye tracer. Scientific Reports. 8 (1), 1-13 (2018).
- Wu, Q., et al. Excreta quantification (EX-Q) for longitudinal measurements of food intake in Drosophila. iScience. 23 (1), 100776 (2020).
- Park, A., Tran, T., Atkinson, N. S. Monitoring food preference in Drosophila by oligonucleotide tagging. Proceedings of the National Academy of Sciences of the United States of America. 115 (36), 9020-9025 (2018).
- Deshpande, S. A., et al. Quantifying Drosophila food intake: Comparative analysis of current methodology. Nature Methods. 11 (5), 535-540 (2014).
- Yapici, N., Cohn, R., Schusterreiter, C., Ruta, V., Vosshall, L. B. A Taste circuit that regulates ingestion by integrating food and hunger signals. Cell. 165 (3), 715-729 (2016).
- Jaime, M. D. L. A., et al. The high-throughput WAFFL system for treating and monitoring individual Drosophila melanogaster adults. bioRxiv. , (2018).
- IUPAC. . Compendium of Chemical Terminology (The “Gold Book”). , (1997).
- Itskov, P. M., et al. Automated monitoring and quantitative analysis of feeding behaviour in Drosophila. Nature Communications. 5, 4560 (2014).
- Ro, J., Harvanek, Z. M., Pletcher, S. D. FLIC: high-throughput, continuous analysis of feeding behaviors in Drosophila. PLoS One. 9 (6), 101107 (2014).

