Deep-Tissue Three-Photon Fluorescence Microscopy in Intact Mouse and Zebrafish Brain
Summary
Drie-fotonenmicroscopie maakt fluorescentiebeeldvorming met hoog contrast mogelijk diep in levende biologische weefsels, zoals muizen- en zebravishersenen, met een hoge spatiotemporale resolutie.
Abstract
Multifotonenmicroscopietechnieken, zoals tweefotonenmicroscopie (2PM) en drie-fotonenmicroscopie (3PM), zijn krachtige hulpmiddelen voor deep-tissue in vivo beeldvorming met subcellulaire resolutie. 3PM heeft twee grote voordelen voor deep-tissue beeldvorming over 2PM die op grote schaal is gebruikt in biologielaboratoria: (i) langere dempingslengte in verstrooiende weefsels door gebruik te maken van ~ 1.300 nm of ~ 1.700 nm excitatielaser; ii) minder achtergrondfluorescentiegeneratie als gevolg van niet-lineaire excitatie van hogere orde. Als gevolg hiervan maakt 3PM structurele en functionele beeldvorming met hoog contrast diep in verstrooiende weefsels mogelijk, zoals intact muizenbrein van de corticale lagen naar de hippocampus en de volledige voorhersenen van volwassen zebravissen.
Tegenwoordig zijn laserbronnen die geschikt zijn voor 3PM commercieel beschikbaar, waardoor een bestaand twee-foton (2P) beeldvormingssysteem kan worden omgezet in een drie-foton (3P) systeem. Bovendien zijn er meerdere commerciële 3P-microscopen beschikbaar, waardoor deze techniek gemakkelijk beschikbaar is voor biologische onderzoekslaboratoria. Dit artikel toont de optimalisatie van een typische 3PM-opstelling, met name gericht op biologiegroepen die al een 2P-opstelling hebben, en demonstreert intravitale 3D-beeldvorming in intacte muizen- en volwassen zebravishersenen. Dit protocol omvat de volledige experimentele procedure van 3P-beeldvorming, inclusief microscoopuitlijning, prechirping van ~ 1.300 en ~ 1.700 nm laserpulsen, diervoorbereiding en intravitale 3P-fluorescentiebeeldvorming diep in volwassen zebravis- en muizenhersenen.
Introduction
In de biowetenschappen zijn multifotonenmicroscopie (MPM) -technieken, zoals 2PM en 3PM, krachtige hulpmiddelen geweest voor diepe in vivo beeldvorming met een hoge spatiotemporale resolutie en een hoog contrast in verstrooiende weefsels. Bovendien veroorzaken deze methoden minder fotobleaching in vergelijking met confocale microscopiemet één foton 1,2,3,4. 3PM is voordelig voor beeldvorming van dieper weefsel in vergelijking met 2PM vanwege twee belangrijke kenmerken: (i) het gebruik van excitatie met een langere golflengte (~ 1.300 nm of ~ 1.700 nm) vermindert weefselverstrooiing, en (ii) het excitatieproces van hogere orde (d.w.z. fluorescentiesignaal hangt af van de kubus van het excitatievermogen in 3PM in plaats van het kwadraat van het excitatievermogen in 2PM) dat de ongewenste achtergrondfluorescentie onderdrukt3 . Bijgevolg maakt 3PM beeldvorming met hoog contrast mogelijk op diepere gebieden in levende weefsels zoals de hippocampus in een intact volwassen muizenbrein 3,5,6,7,8,9,10,11 en de volledige voorhersenen van volwassen zebravissen12, inclusief Ca2+ activiteitsregistratie en veelkleurige waarnemingen. Bovendien zijn contrastrijke beelden verkregen met 3PM door de intacte schedels van muis en volwassen zebravis12,13.
Tegenwoordig zijn excitatielaserbronnen die geschikt zijn voor 3P-excitatie (3PE) bij ~ 1.300 en ~ 1.700 nm in de handel verkrijgbaar. Omdat het laserscansysteem in wezen hetzelfde is voor 2PM en 3PM, is het omzetten van een bestaande 2P-opstelling naar een 3P-opstelling mogelijk in biologielaboratoria met de installatie van een commercieel verkrijgbare laser voor 3PE. Het 3P-fluorescentiesignaal is afhankelijk van het laservermogen, de pulsduur, de laserherhalingsfrequentie en het numerieke diafragma (NA) van de objectieflens. Uitgaande van een diffractie-beperkte focus (d.w.z. het achterste diafragma van de objectieflens wordt overvuld door de excitatiebundel), beschrijft Eq (1) de tijdgemiddelde fluorescentiefotonenflux van het brandpuntsvolume als gevolg van 3PE.
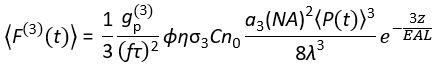 (1)
(1)
Waarbij f de laserherhalingssnelheid is, τ de duur van de laserpuls (volledige breedte bij maximaal de helft), φ de efficiëntie van de systeemverzameling is, η de fluorescentie-kwantumefficiëntie is, σ3 de 3P-absorptiedoorsnede is, C de fluorofoorconcentratie, n0 de reflecterende index van het monstermedium (bijv. Water), λ de excitatiegolflengte in vacuüm is, NA is het numerieke diafragma van de objectieflens, een3 is de ruimtelijke integratieconstante van het brandpuntsvolume, 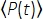 is de tijdgemiddelde excitatiefotonenflux (fotonen / s) onder de objectieflens, z is de bebeelde diepte en EAL is de effectieve dempingslengte14. Hier hebben we aangenomen dat de EAL (meestal > 100 μm) veel groter is dan de axiale resolutie van de microscoop (meestal < 10 μm). Bij paraxiale benadering is een3 gelijk aan 28,114. gp(3) is de3e-orde temporele coherentie van de excitatiebron, en gp(3) is respectievelijk 0,41 en 0,51 voor hyperbolisch-secant-kwadraatpulsen en gaussische pulsen. De opvangefficiëntie φ kan worden geschat door rekening te houden met de fluorescentieverzameling door de objectieflens, de transmissie van de objectieflens, de reflectiviteit van de dichroïsche spiegel, de transmissie van de filters en de detectie-efficiëntie van de detector (bijv. Fotomultiplicatorbuis of PMT). Omdat de 3P-fluorescentie-intensiteit sterk afhankelijk is van verschillende parameters, is optimalisatie van de 3P-opstelling vereist om de 3P-fluorescentiesignalen te maximaliseren.
is de tijdgemiddelde excitatiefotonenflux (fotonen / s) onder de objectieflens, z is de bebeelde diepte en EAL is de effectieve dempingslengte14. Hier hebben we aangenomen dat de EAL (meestal > 100 μm) veel groter is dan de axiale resolutie van de microscoop (meestal < 10 μm). Bij paraxiale benadering is een3 gelijk aan 28,114. gp(3) is de3e-orde temporele coherentie van de excitatiebron, en gp(3) is respectievelijk 0,41 en 0,51 voor hyperbolisch-secant-kwadraatpulsen en gaussische pulsen. De opvangefficiëntie φ kan worden geschat door rekening te houden met de fluorescentieverzameling door de objectieflens, de transmissie van de objectieflens, de reflectiviteit van de dichroïsche spiegel, de transmissie van de filters en de detectie-efficiëntie van de detector (bijv. Fotomultiplicatorbuis of PMT). Omdat de 3P-fluorescentie-intensiteit sterk afhankelijk is van verschillende parameters, is optimalisatie van de 3P-opstelling vereist om de 3P-fluorescentiesignalen te maximaliseren.
Dit protocol illustreert het optimalisatieproces van een typische 3P-opstelling, wat met name nuttig zal zijn voor biologielaboratoria die een 2P-opstelling hebben en van plan zijn om de mogelijkheden uit te breiden naar 3P-beeldvorming of om hun commerciële 3P-opstelling op optimale prestaties te houden. Dit video-artikel demonstreert ook deep-tissue 3P-beeldvorming in levende dierlijke hersenen. Het eerste deel behandelt de optimalisatie van een typische 3P-opstelling met een in de handel verkrijgbare laserbron en multifotonenmicroscoop. Het tweede en derde deel beschrijven respectievelijk zebravissen en muizenvoorbereiding voor 3PM van neuronale structuren en activiteiten. De craniotomiechirurgie bij muizen is eerder gemeld in protocoldocumentenen 15,16,17. Het vierde deel toont intravitale 3P-beeldvorming in zebravis- en muizenhersenen.
Protocol
Representative Results
Discussion
Dit protocol legt stapsgewijze procedures uit voor het instellen van 3P-beeldvorming met een commerciële microscoop en laserbron. In vergelijking met 2PM heeft 3PM een voordeel in toepassingen die optische toegang vereisen in de diepere gebieden, zoals in de hippocampus van de hersenen van de muis. Hoewel 3PM meestal wordt gebruikt in de neurowetenschappen, kan 3PM mogelijk worden toegepast in andere weefsels zoals lymfeklieren, botten en tumoren voor observatie van diep weefsel.
Het is belangrijk om te controleren of het beeldvormingssysteem dicht bij de opnameruislimiet presteert, wat ervoor zorgt dat de detectie- en data-acquisitie-elektronica verwaarloosbare ruis aan het beeld toevoegt na de PMT’s. De onzekerheid in het aantal gedetecteerde fotonen wordt fundamenteel beperkt door fotonopnameruis. Shot-noise beperkte prestaties kunnen worden bereikt in een typische multifotonenmicroscoop met behulp van een high-gain fotodetector (bijvoorbeeld een PMT). Fotonopnameruis volgt een Poisson statistische verdeling, waarbij de standaarddeviatie van de verdeling gelijk is aan de vierkantswortel van het gemiddelde van de verdeling. Als u de prestaties van de opnameruis wilt controleren, volgt u stap 1.14 in de protocolsectie.
Om lichte demping door H2O te voorkomen, is het gebruik van D2O voor onderdompeling nuttig, met name voor ~1.700 nm excitatie. Wanneer D2O wordt gebruikt, is het essentieel om D2O elke ~ 10 minuten te vernieuwen of een groot volume D2O te gebruiken om D2O / H2O-uitwisseling tijdens beeldvorming te voorkomen. Men kan ook de D2O afdichten van de kameromgeving3. Als een wd-objectieflens (long working distance) (bijv. WD bij 4 mm of langer) wordt gebruikt voor beeldvorming, kan de dikte van de dompelvloeistof groter zijn dan 2-3 mm. De toegenomen dikte maakt H2O absorptie niet-verwaarloosbaar, zelfs bij ~1.300 nm21. Daarom kan D2O zelfs nodig zijn voor 1.300 nm 3PM bij gebruik van een lange WD-objectieflens.
Aangezien de 3P-fluorescentie-intensiteit afhankelijk is van de kubus van de excitatiepulsenergie op de focus (Eq. (1)), is het instellen van het juiste laservermogen bijzonder belangrijk om adequate 3P-fluorescentiesignalen te verkrijgen en tegelijkertijd thermische en niet-lineaire schade in levende weefsels te voorkomen. Het gemiddelde laservermogen moet onder de thermische schadedrempel worden gehouden. In het muizenbrein, bijvoorbeeld, om thermische weefselschade te voorkomen, moet het gemiddelde vermogen op het hersenoppervlak van de muis op of onder ~ 100 mW worden gehouden voor ~ 1.300 nm excitatie op een diepte van 1 mm en met een gezichtsveld (FOV) van 230 μm x 230 μm21. Evenzo moet het gemiddelde vermogen op ~ 1.700 nm op of onder ~ 50 mW op ~ 1 mm diepte en een FOV van ~ 230 μm x 230 μm (niet-gepubliceerde gegevens) worden gehouden. Verder, om excitatieverzadiging en potentiële niet-lineaire schade te voorkomen, moet de excitatiepulsenergie op 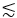 2 nJ en
2 nJ en 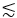 3 nJ worden gehouden voor ~ 1.300 nm en ~ 1.700 nm excitatie, respectievelijk30.
3 nJ worden gehouden voor ~ 1.300 nm en ~ 1.700 nm excitatie, respectievelijk30.
Door lichtabsorptie en verstrooiing in weefsels wordt de pulsenergie bij focus verzwakt tot 1/e (~37%) na penetratie van weefsels door 1 EAL. De EAL varieert in verschillende weefsels en met de excitatiegolflengten, bijvoorbeeld in de neocortex van het muizenbrein, is de EAL ~ 300 μm en ~ 400 μm bij ~ 1.300 nm en ~ 1.700 nm, respectievelijk 3,29 (figuur 5). Om dezelfde pulsenergie scherp te houden (bijv. 1 nJ/puls) op een diepte van n EHL’s, moet de oppervlaktepulsenergie daarom worden vermenigvuldigd met 1 nJ × en. Voor een snelle beeldvorming van structurele en functionele dynamica is een excitatielaser met een hoge herhalingsfrequentie (bij 1 MHz of hoger) wenselijk om een hoge frameratevan 5,6,7,10 te bereiken. De pulsenergiebehoefte en de gemiddelde laservermogenslimiet beperken echter de toepasselijke herhalingssnelheid.
Wanneer we bijvoorbeeld een matig diep gebied bij 4 EPL’s (d.w.z. ~ 1,2 mm in de muizencortex met 1.300 nm excitatie) in beeld brengen, is ~ 55 nJ / puls aan het oppervlak nodig om 1 nJ / puls scherp te houden. Wanneer de gemiddelde vermogensbeperking 100 mW is, kunnen we een laserherhalingssnelheid van ~ 2 MHz toepassen. Om echter dieper te fotograferen op een diepte van 7 EPL’s, is ~ 1.100 nJ / puls aan het oppervlak vereist om 1 nJ / puls scherp te houden. Ervan uitgaande dat het maximale gemiddelde vermogen 100 mW is om thermische schade te voorkomen, moet de laserherhalingssnelheid worden verlaagd tot 0,1 MHz om een 1.100 nJ / puls aan het oppervlak te bereiken. Tabel 1 geeft een overzicht van typische beeldvormingscondities in de hersenschors van muizen. Merk op dat de beelddiepten in tabel 1 ervan uitgaan dat de EAL uniform is in de gehele cortex van de muis.
Bovendien bestaat er vanwege de beperking van het laservermogen in deep-tissue 3PM een afweging tussen de framesnelheid en de grootte van de beeldpixel, wat vooral belangrijk is voor functionele beeldvorming zoals calciumbeeldvorming. De maximaal beschikbare laserherhalingssnelheid wordt op elke diepte bepaald op basis van de vereiste pulsenergie bij focus en het toepasselijke gemiddelde laservermogen zoals hierboven besproken, bijvoorbeeld 2 MHz op een diepte die overeenkomt met ~ 4 EHL’s met 1.300 nm excitatie. Over het algemeen vereist beeldvorming ten minste één puls per pixel. Dienovereenkomstig wordt de minimaal beschikbare pixelverblijftijd bepaald door de laserherhalingssnelheid, bijvoorbeeld 0,5 μs / pixel met 2 MHz excitatie.
Om de hoge ruimtelijke resolutie (~1 μm in lateraal) in 3P-beelden te behouden, is het ideaal om 1 pixel in te stellen op een oppervlakte van ~1 μm2, bijvoorbeeld 256 x 256 pixels voor een FOV van 250 x 250 μm2. Daarom, om snelle beeldvorming uit te voeren met een aanzienlijk grote FOV (bijv. 250 x 250 μm2 met 256 x 256 pixels), 0,5 MHz, 1 MHz en 2 MHz pulsherhalingsfrequenties geven theoretische maximale framesnelheden van respectievelijk ~ 7,6, ~ 15 en ~ 30 frames / s. Evenzo is de optimalisatie van de laserherhalingssnelheid essentieel, afhankelijk van de doeldiepte, scansnelheid en FOV, om voldoende pulsenergie toe te passen onder de thermische schadedrempel. Om de beeldvormingssnelheid te verhogen, kan een adaptieve excitatiebron worden gebruikt om alle excitatiepulsen op de neuronen (d.w.z. interessegebieden) te concentreren door laserpulsen op aanvraag aan de neuronen te leveren31.
3PM is voordelig in vergelijking met 2PM in diepe beeldvorming in levende weefsels en door sterk verstrooiende media zoals een schedel, botten en de witte stoflaag (d.w.z. de externe capsule) van de muizenhersenen. De langere EAL en de hogere orde niet-lineaire excitatie van 3PE komt ten goede aan deep-tissue imaging. Om bijvoorbeeld GCaMP6 in de muizenschors in beeld te brengen, is het 2P-fluorescentiesignaal met 920 nm excitatie hoger dan het 3P-fluorescentiesignaal met 1.300 nm excitatie in ondiepe gebieden bij 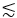 690 μm (d.w.z. ~ 2,3 EPL’s bij 1.300 nm)21. Vanwege de langere EAL bij 1.300 nm in vergelijking met 920 nm, geeft 3PE echter sterkere fluorescentie dan 2P-excitatie (2PE) op een diepte van ~ 690 μm en dieper21. Deze diepte wordt gedefinieerd als ‘signaalovergangsdiepte’, waarbij de fluorescentiesignaalsterkten van 2PE en 3PE identiek zijn met dezelfde herhalingsfrequentie en dezelfde maximaal toegestane gemiddelde vermogens21. De signaalovergangsdiepte is afhankelijk van de excitatiegolflengten voor 2PE en 3PE en de fluorofoor.
690 μm (d.w.z. ~ 2,3 EPL’s bij 1.300 nm)21. Vanwege de langere EAL bij 1.300 nm in vergelijking met 920 nm, geeft 3PE echter sterkere fluorescentie dan 2P-excitatie (2PE) op een diepte van ~ 690 μm en dieper21. Deze diepte wordt gedefinieerd als ‘signaalovergangsdiepte’, waarbij de fluorescentiesignaalsterkten van 2PE en 3PE identiek zijn met dezelfde herhalingsfrequentie en dezelfde maximaal toegestane gemiddelde vermogens21. De signaalovergangsdiepte is afhankelijk van de excitatiegolflengten voor 2PE en 3PE en de fluorofoor.
In de praktijk maakt 920 nm excitatie een hoger gemiddeld laservermogen mogelijk dan 1.300 nm excitatie door minder waterabsorptie. Het hogere gemiddelde vermogen van 2PE zou de signaalovergangsdiepte echter slechts met 0,9 EPL’sduwen 4. Bovendien, wanneer het monster dicht gelabeld is, heeft 3PE het extra voordeel van een veel hogere SBR. Daarom kan 3PM, zelfs voordat de crossover-lengte van het signaal wordt bereikt, beter zijn voor beeldvorming dan 2PM. Bijvoorbeeld, bij het afbeelden van de hersenen van de muis, die een volumefractie (d.w.z. labelingdichtheid) heeft van ~ 2%, 1.300 nm 3PM met 100 mW excitatievermogen presteert beter dan 920 nm 2PM met 200 mW excitatievermogen op een diepte van ~ 700 μm voor fluoresceïne.
3PM heeft ook een voordeel bij beeldvorming door een dunne maar sterk verstrooiende laag die de puntspreidingsfunctie van de excitatiestraal kan vervormen en een onscherpte-achtergrond kan genereren4. Bijvoorbeeld, door de intacte schedel van het muizenbrein lijden 2PM-beelden aan de onscherpte-achtergrond, zelfs op de ondiepe diepte van <100 μm van het hersenoppervlak13. Een vergelijkbare onscherpte-achtergrond werd waargenomen in 2PM met 1.280 nm excitatie door de witte stof in het muizenbrein32. Daarom, wanneer weefsels worden afgebeeld door troebele lagen, heeft 3PM de voorkeur boven 2PM voor beeldvorming met hoog contrast, ongeacht de labelingdichtheid.
We hebben onlangs een fantoom- en theoretische analyse van kralen gemeld waaruit blijkt dat de beelddieptelimiet van 3PM meer dan 8 EPL’s33 is; 8 EOL’s zijn gelijk aan ~3 mm met ~1.700 nm excitatie in de muizenschors. De momenteel beschikbare laser heeft echter niet genoeg pulsenergie om 8 EPL’s in het muizenbrein te bereiken. Verdere ontwikkeling van sterkere lasers zal de huidige beelddieptegrens van 15.00 uur verleggen.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Dit werk werd ondersteund door NSF DBI-1707312 Cornell NeuroNex Hub en NIH 1U01NS103516.
Materials
| 5% Povidone-iodine | Amazon | NDC 67818-155-32 | Aceptical cleaning of surgical areas |
| 70% Ethanol | Thermo Fisher Scientific | CAS 64-17-5 | Aceptical cleaning of surgical areas |
| Agarose | Sigma | A4718-256 | Preparing zebrafish chamber |
| Atropine | Cornell Veterinary Care | ||
| Bergamo II | Thorlabs | Multiphoton Imaging Microscope | |
| Bupivacaine | Cornell Veterinary Care | ||
| Dexamethasone | Cornell Veterinary Care | ||
| Donut shape glass (ID4.5, OD6.5) | Potomac Photonics | Cover glass used for craniotomy | |
| eye ointment (or topical ophthalmic ointment) | Puralube Vet Ointment | NDC 17033-211-38 | Used as a lubricant to prevent irritation or to relieve dryness of the eye during surgery and anesthesia |
| GaAsP Amplified PMT | Thorlabs | PMT2100 | PMT detector |
| Glucose | Cornell Veterinary Care | ||
| Glycopyrrolate | Cornell Veterinary Care | ||
| Heater (800 W) | Finnex | Aquarium heater for zebrafish water) | |
| Isoflurane USP 250 mL | Piramal | NDC 66794-0013-25 | For anesthesia of mice |
| Ketoprofen | Cornell Veterinary Care | ||
| Kimwipes | Kimtech | Laboratory tissue for preparing zebrafish | |
| Nanofil syringe (10 micrometer) with 36 G needle | WPI | NANOFIL + NF36BV | Syringe and needle for injection of pancuronium bromide |
| Optical Adhesive | Norland | NOA 68 | To stick round coverslip and donut shape glass together. |
| Pancuronium Bromide | Cornell Veterinary Care | ||
| Peristaltic Pump | Elemental Science | ESI MP2 | Water pump for zebrafish setup |
| Polyethylene tubing (I.D. 0.58 mm., O.D. 0.965 mm.) | Elemental Science | MP2 pump tubing | Tubing that goes in the mouth of the zebrafish |
| Round Cover Slip German Glass #1.5, 5 mm | Electron Microscopy Sciences | 7229605 | Cover glass used for craniotomy |
| Spirit-NOPA | Spectra Physics | Tunable Optical Parametric Amplifier | |
| SR400 | Stanford Research Systems | SR400 | Photon counter |
| Standard Photodiode Power Sensor | Thorlabs | S122C | Power detector |
| Sterilized phosphate buffered saline (PBS) | Millipore Sigma | SKU 806552-500ml | Used during mouse brain surgery |
| Surgical drape | Dynarex disposable towel drape | 4410 | For aceptical mouse surgery |
| Thin strip boxing wax | Corning Rubber Co., Inc. | Holding tubing in place in zebrafish chamber | |
| ThorImage | Thorlabs | Image acquisition software | |
| Tricaine (Ethyl-m-aminobenzoate methanesulfonate salt) | MP | 103106 | Zebrafish anesthesia and euthanasia |
| Tygon tubing (I.D. 1/16 in., O.D. 1/8 in.) | Tygon | Tubing for water flow for zebrafish preparation | |
| VaporGuard | VetEquip | 931401 | For recycling isoflurane |
| Vetbond tissue adhesive | 3M | 1469SB | To glue the glass window on the mouse skull, and to glue the laboratory tissue when preparing the fish. |
| XLPLN25XWMP2 | Olympus | Multiphoton Excitation Dedicated Objective |
References
- Denk, W., Strickler, J. H., Webb, W. W. Two-photon laser scanning fluorescence microscopy. Science. 248 (4951), 73-76 (1990).
- Helmchen, F., Denk, W. Deep tissue two-photon microscopy. Nature Methods. 2 (12), 932-940 (2005).
- Horton, N. G., et al. In vivo three-photon microscopy of subcortical structures within an intact mouse brain. Nature Photonics. 7 (3), 205-209 (2013).
- Wang, T., Xu, C. Three-photon neuronal imaging in deep mouse brain. Optica. 7 (8), 947-960 (2020).
- Ouzounov, D. G., et al. In vivo three-photon imaging of activity of GCaMP6-labeled neurons deep in intact mouse brain. Nature Methods. 14 (4), 388-390 (2017).
- Weisenburger, S., et al. Volumetric Ca2+ imaging in the mouse brain using hybrid multiplexed sculpted light microscopy. Cell. 177 (4), 1050-1066 (2019).
- Yildirim, M., Sugihara, H., So, P. T. C., Sur, M. Functional imaging of visual cortical layers and subplate in awake mice with optimized three-photon microscopy. Nature Communications. 10, 177 (2019).
- Takasaki, K., Abbasi-Asl, R., Waters, J. Superficial bound of the depth limit of two-photon imaging in mouse brain. eNeuro. 7 (1), (2020).
- Guesmi, K., et al. Dual-color deep-tissue three-photon microscopy with a multiband infrared laser. Light, Science & Applications. 7, 12 (2018).
- Hontani, Y., Xia, F., Xu, C. Multicolor three-photon fluorescence imaging with single-wavelength excitation deep in mouse brain. Science Advances. 7 (12), 3531 (2021).
- Liu, H., et al. In vivo deep-brain structural and hemodynamic multiphoton microscopy enabled by quantum dots. Nano Letters. 19 (8), 5260-5265 (2019).
- Chow, D. M., et al. Deep three-photon imaging of the brain in intact adult zebrafish. Nature Methods. 17 (6), 605-608 (2020).
- Wang, T., et al. Three-photon imaging of mouse brain structure and function through the intact skull. Nature Methods. 15 (10), 789-792 (2018).
- Xu, C., Webb, W. W. Multiphoton excitation of molecular fluorophores and nonlinear laser microscopy. Topics in Fluorescence Spectroscopy. 5. , 471-540 (2002).
- Mostany, R., Portera-Cailliau, C. A craniotomy surgery procedure for chronic brain imaging. Journal of Visualized Experiments: JoVE. (12), e680 (2008).
- Łukasiewicz, K., Robacha, M., Bożycki, &. #. 3. 2. 1. ;., Radwanska, K., Czajkowski, R. Simultaneous two-photon in vivo imaging of synaptic inputs and postsynaptic targets in the mouse retrosplenial cortex. Journal of Visualized Experiments: JoVE. (109), e53528 (2016).
- Kyweriga, M., Sun, J., Wang, S., Kline, R., Mohajerani, M. H. A large lateral craniotomy procedure for mesoscale wide-field optical imaging of brain activity. Journal of Visualized Experiments: JoVE. (123), e52642 (2017).
- Gordon, J. P., Martinez, O. E., Fork, R. L. Negative dispersion using pairs of prisms. Optics Letters. 9 (5), 150-152 (1984).
- Entenberg, D., et al. Setup and use of a two-laser multiphoton microscope for multichannel intravital fluorescence imaging. Nature Protocols. 6 (10), 1500-1520 (2011).
- Horton, N. G., Xu, C. Dispersion compensation in three-photon fluorescence microscopy at 1,700 nm. Biomedical Optics Express. 6 (4), 1392-1397 (2015).
- Wang, T., et al. Quantitative analysis of 1300-nm three-photon calcium imaging in the mouse brain. eLife. 9, 53205 (2020).
- Cheng, L. -. C., Horton, N. G., Wang, K., Chen, S. -. J., Xu, C. Measurements of multiphoton action cross sections for multiphoton microscopy. Biomedical Optics Express. 5 (10), 3427-3433 (2014).
- Huang, K. -. H., et al. A virtual reality system to analyze neural activity and behavior in adult zebrafish. Nature Methods. 17 (3), 343-351 (2020).
- Jacobson, G. A., Rupprecht, P., Friedrich, R. W. Experience-dependent plasticity of odor representations in the telencephalon of zebrafish. Current Biology. 28 (1), 1-14 (2018).
- Li, J., et al. Early development of functional spatial maps in the zebrafish olfactory bulb. Journal of Neuroscience. 25 (24), 5784-5795 (2005).
- Barbosa, J. S., et al. Live imaging of adult neural stem cell behavior in the intact and injured zebrafish brain. Science. 348 (6236), 789-793 (2015).
- Dray, N., et al. Large-scale live imaging of adult neural stem cells in their endogenous niche. Development. 142 (20), 3592-3600 (2015).
- Kobat, D., et al. Deep tissue multiphoton microscopy using longer wavelength excitation. Optics Express. 17 (16), 13354-13364 (2009).
- Wang, M., Wu, C., Sinefeld, D., Li, B., Xia, F., Xu, C. Comparing the effective attenuation lengths for long wavelength in vivo imaging of the mouse brain. Biomedical Optics Express. 9 (8), 3534-3543 (2018).
- Vogel, A., Noack, J., Hüttman, G., Paltauf, G. Mechanisms of femtosecond laser nanosurgery of cells and tissues. Applied Physics B. 81 (8), 1015-1047 (2005).
- Li, B., Wu, C., Wang, M., Charan, K., Xu, C. An adaptive excitation source for high-speed multiphoton microscopy. Nature Methods. 17 (2), 163-166 (2019).
- Kobat, D., Horton, N. G., Xu, C. In vivo two-photon microscopy to 1.6-mm depth in mouse cortex. Journal of Biomedical Optics. 16 (10), 106014 (2011).
- Akbari, N., Rebec, M. R., Xia, F., Xu, C. Imaging deeper than the transport mean free path with multiphoton microscopy. Biomedical Optics Express. 13, 452-463 (2022).

