纸基脚趾开关诊断开发和患者验证的设计到实施研究
Summary
获得分散、低成本和高容量的诊断方法,这些诊断方法可以部署到社区中进行分散检测,这对于应对全球卫生危机至关重要。本手稿描述了如何为可以使用便携式光学阅读器检测的病毒RNA序列构建基于纸张的诊断方法。
Abstract
获得可部署到社区进行测试的低负担分子诊断越来越重要,并对社会和经济稳定具有有意义的更广泛影响。近年来,出现了几种新的等温诊断模式,以满足对快速、低成本分子诊断的需求。我们通过开发和患者验证基于脚趾开关的诊断方法(包括蚊媒寨卡病毒和基孔肯雅病毒的诊断)为这项工作做出了贡献,这些诊断提供了与基于金标准逆转录定量聚合酶链反应(RT-qPCR)的测定相当的性能。这些诊断的开发和制造成本低廉,并且有可能为资源匮乏的环境提供诊断能力。在这里,该协议提供了开发基于开关的寨卡病毒检测检测方法所需的所有步骤。本文将引导读者完成逐步诊断开发过程。首先,寨卡病毒的基因组序列作为使用开源软件计算设计候选开关的输入。接下来,显示了用于使用合成RNA序列进行经验筛选和优化诊断灵敏度的传感器的组装。完成后,使用患者样本与RT-qPCR和专用光学读取器PLUM并行进行验证。这项工作为研究人员开发低成本的基于脚趾开关的传感器提供了技术路线图,用于人类健康,农业和环境监测。
Introduction
RT-qPCR由于其出色的灵敏度和特异性,一直是临床诊断的金标准技术。尽管该方法非常稳定,但依赖于昂贵的专用设备和试剂,这些设备和试剂需要温控分布和储存。这给全球高质量诊断的可及性带来了重大障碍,特别是在疾病暴发时期和设备齐全的实验室访问受限的地区1,2。这是在2015/2016年巴西寨卡病毒暴发期间观察到的。由于只有五个集中实验室可以提供RT-qPCR检测,因此产生了严重的瓶颈,限制了诊断的可及性。这对于受疫情影响更严重的城郊地区个人来说尤其具有挑战性3,4。为了改善对诊断的访问,该协议展示了一个已经开发的平台,该平台有可能在资源匮乏的环境中提供分散、低成本和高容量的诊断。作为其中的一部分,建立了一个诊断发现管道,将等温扩增和基于合成RNA开关的传感器与基于纸张的无细胞表达系统5,6耦合。
无细胞蛋白质合成(CFPS)系统,特别是基于大肠杆菌的无细胞系统,是一个有吸引力的平台,适用于从环境监测7,8到病原体诊断5,6,9,10,11,12的广泛生物传感应用.CFPS系统由转录和翻译所需的组件组成,与全细胞生物传感器相比具有显着优势。具体来说,传感不受细胞壁的限制,通常,它们是模块化设计的,生物安全的,价格低廉,并且可以冷冻干燥以供便携式使用。将基于基因回路的反应冷冻干燥到纸或纺织品等基质上的能力,使运输、室温下长期储存5,甚至可纳入可穿戴技术13。
先前的工作表明,无大肠杆菌细胞系统可用于检测多种分析物,例如汞等有毒金属、四环素7,14 等抗生素、干扰内分泌的化学物质 15,16、马尿酸 17 等生物标志物、病原体相关群体感应分子9,18 和可卡因 17 等非法物质以及羟基丁酸 γ (GHB)19.对于核酸的序列特异性检测,策略在很大程度上依赖于使用基于开关的生物传感器与等温扩增技术相结合。脚趾开关是合成的核糖调节剂(在文本的其余部分也称为“开关”),它包含一个发夹结构,通过隔离核糖体结合位点(RBS)和起始密码子来阻断下游翻译。在与它们的靶触发RNA相互作用时,发夹结构被解除,随后的报告开放阅读框的翻译被启用20。
等温扩增也可用作分子诊断21;然而,这些方法容易发生非特异性扩增,这会降低特异性,从而降低测试的准确性,使其低于RT-qPCR 22。在这里报告的工作中,基于开关的传感器上游的等温放大用于提供组合信号放大,从而能够对核酸(飞摩尔到阿托摩尔)进行临床相关的检测。这两种方法的配对还提供了两个序列特异性检查点,它们的组合可提供高水平的特异性。使用这种方法,以前的工作已经证明了对寨卡6,埃博拉5,诺如病毒10等病毒的检测,以及艰难梭菌23和抗生素耐药性伤寒12等致病菌的检测。最近,已经证明了用于SARS-CoV-2检测的无细胞脚趾开关,旨在为COVID-19大流行提供可访问的诊断11,12,13。
以下协议概述了用于寨卡病毒检测的无细胞、基于纸张的合成脚趾开关测定的开发和验证,从 计算机 生物传感器设计到组装和优化步骤,再到患者样本的现场验证。该方案从基于寨卡病毒RNA的RNA脚趾开关传感器和等温扩增引物 的计算机设计开始 。尽管存在许多等温扩增方法,但这里使用基于核酸序列的扩增(NASBA)来增加反应中存在的病毒RNA靶标的浓度,从而具有临床显着的灵敏度。实际上,等温扩增方法具有在恒定温度下运行的优点,无需对专用设备的需求,例如热循环仪,这些设备通常仅限于集中位置。
接下来,描述了通过重叠延伸PCR组装具有报告编码序列的合成脚趾开关传感器的过程,并使用合成RNA筛选合成脚趾开关传感器以在无细胞系统中获得最佳性能。对于这组寨卡病毒传感器,我们选择了编码β-半乳糖苷酶的 lacZ 基因,该酶能够切割比色底物氯酚红-β-D-吡喃半乳糖苷(CPRG),以产生黄色到紫色的颜色变化,可以通过眼睛或酶标器检测到。一旦确定了性能最佳的合成开关,就描述了使用合成RNA筛选引物以基于核酸序列等温扩增相应靶序列以找到提供最佳灵敏度的组的过程。
最后,诊断平台的性能在拉丁美洲进行了现场验证(图1)。为了确定临床诊断的准确性,使用来自患者的寨卡病毒样本进行基于纸张的无细胞测定;同时进行金标准RT-qPCR测定以进行比较。为了监测无比色细胞分析,我们可以在没有热循环仪的区域对结果进行现场定量。这里还介绍了手工组装的酶标仪,称为便携式,低成本,用户友好,多模式(PLUM;以下简称便携式酶标仪)24。便携式酶标仪最初是作为无细胞合成脚趾开关诊断的配套设备开发的,提供了一种以高通量方式孵育和读取结果的便捷方式,为用户提供基于计算机视觉的集成软件分析。
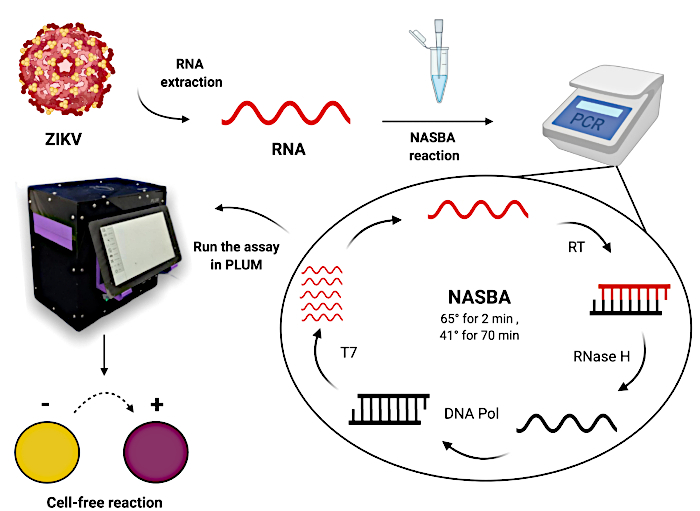
图 1:使用纸质无细胞脚趾开关反应测试患者样品的工作流程。 请点击此处查看此图的大图。
Protocol
Representative Results
Discussion
这里描述的组合纸基系统可以将临床相关的分子诊断,其性能在功能上可与RT-qPCR相媲美,达到需求点6。重要的是,对于远程设置,现场诊断的可用性可以将获得结果的时间从几天缩短到几小时。突出了这种方法的可编程性,所描述的管道可用于检测几乎任何病原体靶标。我们将分子工具与专用便携式酶标仪配对,该酶标仪结构紧凑且与电池操作(8-9 小时)兼容,并提供板载数据分析以支持分布式应用。在其他工作中,我们已经用268个患者样本验证了硬件和寨卡病毒诊断平台的组合,并与RT-qPCR并行,发现诊断准确率为98.5%24。总而言之,我们的目标是使该平台能够向研究人员转移技术,以便社区可以重新利用和改进该平台,以解决未满足的诊断需求。
计算机式脚趾开关设计过程已集成并自动化到可分为三个阶段的管道中。第一阶段生成一组脚趾开关设计,这些设计以一个核苷酸增量与靶序列杂交。第二阶段检查二级结构和脚趾开关的可用性,并消除带有帧内过早停止密码子的传感器。然后实施考虑多种因素(例如,脚趾开关的缺陷水平、脚趾开关可用性和目标部位可访问性)的评分功能,以根据总分选择顶部脚趾开关设计。在最后阶段,为顶部脚趾开关设计及其相应的目标触发器生成序列列表。应使用 NCBI/引物-BLAST25 筛选顶部传感器序列对人类转录组和密切相关的病毒基因组的特异性。在寨卡病毒基因组中筛选传感器靶位点以进行序列保存也是最佳实践,以确保传感器能够提供广泛而强大的检测。已经开发了多个版本的脚趾式开关设计软件,设计算法允许用户生成两个版本,即 A 系列 6 或 B 系列脚趾式开关6。在本文中,重点介绍了B系列脚趾开关设计。
在商业DNA合成之后,可以快速组装脚趾开关,然后通过对对应于靶基因组短区域(200-300 nt)的合成靶触发序列进行初始筛选来进行测试。为了筛选基于脚趾开关的传感器的性能,最好以RNA的形式添加靶序列。在本文中,概述了添加 体外 转录触发RNA所需的步骤。但是,如果可用,可以使用全长基因组模板,例如定量的病毒RNA提取物或商业合成RNA基因组或标准品。使用全长RNA基因组进行初始脚趾开关筛选是有益的,因为它可以告知其他因素(如RNA二级结构)是否会影响传感器性能。为了优化候选开关的开/关比,可以将脚趾开关DNA滴定到无细胞反应中。此步骤还可用于识别高性能的脚趾保持开关(折叠扩增或高 ON/OFF 比),并从下游表征步骤中省略泄漏的脚趾保持开关(在没有靶 RNA 的情况下的高信号)。
为了提高性能最佳的脚趾开关候选物的检测限,NASBA用于将靶标寨卡病毒RNA的临床相关浓度提高到可以通过脚趾开关检测到的水平6。筛选正向和反向引物组的不同组合,以确定最佳的NASBA引物和脚趾开关组合,以便在临床相关浓度下进行检测。一旦确定了理想的引物组和脚趾开关组合,该测定将进行临床验证。需要注意的是,脚趾开关和NASBA筛选阶段可能是劳动力和资源密集型的,因此测试开发最适合资源充足的研究地点。虽然我们还没有应用流程自动化,但这很可能会加速迭代设计、构建和测试周期32。幸运的是,从传感器设计和测试到部署的周转时间可能非常短(不到一周),这使得该策略非常适合时间紧迫的情况,例如流行病爆发6。
即使在开发出具有临床相关灵敏度的生物传感器之后,也存在需要解决的技术挑战。由于该协议涉及手动操作并且是一个多步骤程序,因此存在样品之间交叉污染的风险。我们尽最大努力通过仔细的实验室实践来降低这种风险。在最近对268个患者样本进行的临床试验中,我们没有遇到任何污染问题;然而,这是一个重要的考虑因素24.考虑到这一点,该协议仍然是实验室测定,需要熟练的用户掌握适当的分子生物学技术。部署的另一个考虑因素是从患者样本中分离RNA。在这里,我们描述了使用基于柱的核酸提取试剂盒进行RNA分离。然而,在其他工作中,我们已经展示了一种有效且简单的沸腾裂解方法(95°C2分钟)用于低负担的患者样品处理6。这种策略几乎消除了与RNA提取相关的成本,并避免了使用基于柱的核酸提取试剂盒,在资源匮乏的环境中或在危机期间(如COVID-19大流行)期间的供应链问题中,这可能会带来物流挑战33。
正如我们在 COVID-19 大流行期间所看到的那样,用于执行 RT-qPCR 的仪器本身可能成为瓶颈并限制患者获得检测的机会。这一因素在很大程度上也是财务因素,导致集中测试模式可以限制诊断访问。例如,在2015/2016年寨卡疫情期间,巴西只有五个国家参考实验室,这导致患者检测延迟。在不考虑规模经济的潜在好处的情况下,便携式酶标仪目前的商品成本为~500美元,即使考虑到劳动力和商业利润而增加五倍,仍然提供了一种负担得起的工具。相比之下,RT-qPCR 仪器的成本从 15,000 美元到 90,000 美元不等,34 美元不等。此外,拉丁美洲无细胞检测的每次检测费用约为5.48美元,而在寨卡病毒爆发时,巴西RT-qPCR的每次检测费用为~10-11美元36。除了设备成本外,便携式酶标仪占地面积小(20 cm3),自动分析, 数据 通过互联网上传到云端,并且可以使用电池供电。这些功能极大地扩展了可以部署测试的潜在设置,并同时扩大了可以服务的患者群体。
迄今为止,最常见的商用大肠杆菌CFPS平台是S30和PURE系统37;然而,改善低收入和中等收入国家获得诊断服务的一个关键考虑因素是这些试剂的国内供应有限。解决这一挑战的一个重要步骤是发展当地的CFPS生产。Federici实验室最近在开发一个非商业平台方面取得了重大进展,该平台在基于裂解物的无细胞系统中实施基于脚趾开关的传感器,寨卡病毒RNA14达到2.7 fM LOD。这一成就不仅允许试剂在使用国生产,避免进口关税和延误,而且劳动力成本也随着当地费率的调整,因此总体成本可以显着降低。在Federici小组概述的工作中,智利生产CFPS表达反应(5μL)的成本为6.9美分(美元)35,38,为实施基于裂解物的系统提供了双重激励(改善物流和成本)35,38。
将RT-qPCR可比检测放入分布式诊断网络可以带来比当前依赖于将样本运输到集中式RT-qPCR设施的做法的显着优势。在寨卡病例集中的城郊地区,患者与诊断机构之间的物理距离会减慢诊断速度,并增加结果无法在临床相关时间到达患者的风险。我们希望,这里介绍的工作能够有助于使研究界能够通过知识转让,为人类健康、农业和环境监测创造分散的生物技术和便携式硬件。
Disclosures
The authors have nothing to disclose.
Acknowledgements
作者感谢Green,Pardee和Pena实验室的所有成员,以及与本手稿中披露的工作有关的先前手稿的所有合著者。S.J.R.D.S.得到了巴西伯南布哥州科学技术基金会(FACEPE)赞助的博士奖学金的支持,参考编号IBPG-1321-2.12/18,目前由加拿大多伦多大学赞助的博士后奖学金支持。P.B.得到了多伦多大学药学院的William Knapp Buckley奖的支持。M.K.得到了多伦多大学精准医学计划(PRiME)的支持,内部奖学金编号PRMF2019-002。这项工作得到了加拿大研究主席计划(文件950-231075和950-233107),多伦多大学主要研究项目管理基金,CIHR基金会资助计划(201610FDN-375469)的K.P资金支持,并通过CIHR / IDRC团队资助向L.P,A.A.G.和K.P.提供的资金支持:加拿大 – 拉丁美洲/美洲 – 加勒比寨卡病毒计划(FRN: 149783),以及加拿大国际发展研究中心(拨款109434-001)通过加拿大2019年新型冠状病毒(COVID-19)快速研究资助机会向KP提供的资金。这项工作还得到了亚利桑那州生物医学研究委员会新研究者奖(ADHS16-162400),盖茨基金会(OPP1160667),NIH主任新创新奖(1DP2GM126892),NIH R21奖(1R21AI136571-01A1)和Alfred P. Sloan奖学金(FG-2017-9108)的资金支持。 图 1 是在 K.P. 的学术许可下与 Biorender.com 一起创建的。
Materials
| 384 well plate covers – aluminum | Sarstedt | 95.1995 | Used to cover the 384-well plates before they are inserted into the PLUM reader |
| 384 well plate covers – transparent | Sarstedt | 95.1994 | Used to cover the 384-well plates before they are inserted into the BioTek plate reader |
| 384 well plates | VWR | CA11006-180 | 2 mm paper-based diagnostics are placed into the wells of these plates for quantification |
| Agarose | BioShop Canada | AGA001.500 | Gel electrophoresis |
| BSA | BioShop Canada | ALB001.500 | Blocking agent for the Whatman filter paper |
| Cell free reactions | New England Biolabs | E6800L | PURExpress |
| CPRG | Roche | 10884308001 | Chlorophenol red-b-D-galactopyranoside |
| Disposable Sterile Biopsy Punches | Integra Miltex | 23233-31 | Used to create 2 mm paper discs that fit into a 384-well plate |
| DNAse I | Thermo Scientific | K2981 | Digests template DNA following incubation of the in vitro transcription reaction |
| DNAse I Kit | Thermo Scientific | 74104 | DNase I Kit For removing template DNA from IVT RNA |
| dNTPs | New England Biolabs | N0446S | Used for PCRs |
| electrophoresis system | Bio-Rad | 1704487 | Used to run the agarose gels |
| Gel imaging station | Bio-Rad | 1708265 | ChemiDoc XRS+ Imaging System |
| IVT kit | New England Biolabs | E2040S | Used for in vitro transcribing template (trigger) RNA for switch screening |
| Nanodrop One | Thermo Scientific | ND-ONE-W | Used for determining nucleic acid concentrations |
| NASBA kit | Life Sciences Advanced Technologies | NWK-1 | Isothermal amplification reaction components |
| Nuclease free H20 | invitrogen | 10977015 | Added to reaction mixes |
| PAGE electrophoresis system | Biorad | 1658001FC | Used to cast and run polyacrylamide gels |
| pCOLADuet-LacZ DNA | Addgene | 75006 | https://www.addgene.org/75006/ |
| Phusion polymerase/reactioin buffer | New England Biolabs | M0530L | Used for PCRs |
| Plate reader | BioTek | BioTek NEO2 | Multi Mode Plate Reader, Synergy Neo2 |
| Primers | Integrated DNA Technologies | Custom oligo synthesis | |
| Q5 polymerase/reaction buffer | New England Biolabs | M0491L | Used for PCRs |
| Qiagen PCR Puriifcation Kit | QIAGEN | 27106 | QIAprep Spin Miniprep Kit |
| RNA loading dye | New England Biolabs | B0363S | 2X RNA loading dye |
| RNA Purification Kit | QIAGEN | EN0521 | QIAamp Viral RNA extraction kit |
| RNase inhibitor | New England Biolabs | M0314S | Used to prevent contamination of RNases A, B, and C |
| RT-qPCR kit | QIAGEN | 208352 | QuantiNova Probe RT-PCR Kit |
| SYBR Gold | Invitrogen S11494 | S11494 | PAGE gel stain for nucleic acids |
| TAE Buffer | BioShop Canada | TAE222.4 | Gel electrophoresis buffer |
| Thermal Cycler | Applied Biosystems | 4484073 | Used for temperature cycling and incubating reactions |
| Whatman 42 filter paper | GE Healthcare | 1442-042 | Used to imbed molecular components for paper-based diagnostics |
References
- Urdea, M., et al. Requirements for high impact diagnostics in the developing world. Nature. 444, 73-79 (2006).
- Yager, P., Domingo, G. J., Gerdes, J. Point-of-care diagnostics for global health. Annual Review of Biomedical Engineering. 10, 107-144 (2008).
- Faria, N. R., et al. Mobile real-time surveillance of Zika virus in Brazil. Genome Medicine. 8 (1), 97 (2016).
- Faria, N. R., et al. Zika virus in the Americas: Early epidemiological and genetic findings. Science. 352 (6283), 345-349 (2016).
- Pardee, K., et al. Paper-based synthetic gene networks. Cell. 159 (4), 940-954 (2014).
- Pardee, K., et al. Rapid, low-cost detection of Zika virus using programmable biomolecular components. Cell. 165 (5), 1255-1266 (2016).
- Duyen, T. T. M., et al. Paper-based colorimetric biosensor for antibiotics inhibiting bacterial protein synthesis. Journal of Bioscience and Bioengineering. 123 (1), 96-100 (2017).
- Jung, J. K., et al. Cell-free biosensors for rapid detection of water contaminants. Nature Biotechnology. 38 (12), 1451-1459 (2020).
- Yang, Y. H., et al. Cell-free Escherichia coli-based system to screen for quorum-sensing molecules interacting with quorum receptor proteins of streptomyces coelicolor. Applied and Environmental Microbiology. 75 (19), 6367 (2009).
- Ma, D., Shen, L., Wu, K., Diehnelt, C. W., Green, A. A. Low-cost detection of norovirus using paper-based cell-free systems and synbody-based viral enrichment. Synthetic Biology. 3 (1), (2018).
- Park, S., Lee, J. W. Detection of coronaviruses using RNA toehold switch sensors. International Journal of Molecular Sciences. 22 (4), 1-13 (2021).
- Amalfitano, E., et al. A glucose meter interface for point-of-care gene circuit-based diagnostics. Nature Communications. 12 (1), 1-10 (2021).
- Nguyen, P. Q., et al. Wearable materials with embedded synthetic biology sensors for biomolecule detection. Nature Biotechnology. 39 (11), 1366-1374 (2021).
- Pellinen, T., Huovinen, T., Karp, M. A cell-free biosensor for the detection of transcriptional inducers using firefly luciferase as a reporter. Analytical Biochemistry. 330 (1), 52-57 (2004).
- Salehi, A. S. M., et al. Cell-free protein synthesis approach to biosensing hTRβ-specific endocrine disruptors. Analytical Chemistry. 89 (6), 3395-3401 (2017).
- Salehi, A. S. M., et al. Biosensing estrogenic endocrine disruptors in human blood and urine: A RAPID cell-free protein synthesis approach. Toxicology and Applied Pharmacology. 345, 19-25 (2018).
- Voyvodic, P. L., et al. Plug-and-play metabolic transducers expand the chemical detection space of cell-free biosensors. Nature Communications. 10 (1), 1-8 (2019).
- Yang, W. C., Patel, K. G., Wong, H. E., Swartz, J. R. Simplifying and streamlining Escherichia coli-based cell-free protein synthesis. Biotechnology Progress. 28 (2), 413-420 (2012).
- Gräwe, A., et al. A paper-based, cell-free biosensor system for the detection of heavy metals and date rape drugs. PLOS One. 14 (3), 0210940 (2019).
- Green, A. A., Silver, P. A., Collins, J. J., Yin, P. Toehold Switches: De-Novo-Designed Regulators of Gene Expression. Cell. 159 (4), 925-939 (2014).
- Craw, P., Balachandran, W. Isothermal nucleic acid amplification technologies for point-of-care diagnostics: a critical review. Lab on a Chip. 12 (14), 2469-2486 (2012).
- Zyrina, N. V., Antipova, V. N. Nonspecific Synthesis in the Reactions of Isothermal Nucleic Acid Amplification. Biochemistry (Moscow). 86 (7), 887-897 (2021).
- Takahashi, M. K., et al. A low-cost paper-based synthetic biology platform for analyzing gut microbiota and host biomarkers. Nature Communications. 9 (1), 1-12 (2018).
- Karlikow, M., et al. Field validation of the performance of paper-based tests for the detection of the Zika and chikungunya viruses in serum samples. Nature Biomedical Engineering. 6 (3), 246-256 (2022).
- Agarwala, R., et al. Database resources of the National Center for Biotechnology Information. Nucleic Acids Research. 44 (1), 7-19 (2016).
- . BLAST: Basic Local Alignment Search Tool Available from: https://blast.ncbi.nlm.nih.gov/Blast.cgi (2022)
- Deiman, B., Van Aarle, P., Sillekens, P. Characteristics and applications of nucleic acid sequence-based amplification (NASBA). Molecular Biotechnology. 20 (2), 163-179 (2002).
- Zadeh, J. N., Wolfe, B. R., Pierce, N. A. Nucleic acid sequence design via efficient ensemble defect optimization. Journal of Computational Chemistry. 32 (3), 439-452 (2011).
- JoVE Science Education Database. Basic Methods in Cellular and Molecular Biology. DNA Gel Electrophoresis. Journal of Visualized Experiments: JoVE. , (2021).
- Lanciotti, R. S., et al. Genetic and serologic properties of Zika virus associated with an epidemic, Yap State, Micronesia, 2007. Emerging Infectious Diseases. 14 (8), 1232 (2008).
- Walsh, D. I., et al. Standardizing automated DNA assembly: Best practices, metrics, and protocols using robots. SLAS Technology. 24 (3), 282 (2019).
- Silva, S. J. R., de Magalhães, J. J. F., de Pena, L. Simultaneous circulation of DENV, CHIKV, ZIKV and SARS-CoV-2 in Brazil: An inconvenient truth. One Health. 12, 100205 (2021).
- Kimura, S., Fujinaga, K., Sekiya, T. PCR machine. Tanpakushitsu kakusan koso. Protein, Nucleic Acid, Enzyme. 41 (5), 514-517 (1996).
- Arce, A., et al. Decentralizing cell-free RNA sensing with the use of low-cost cell extracts. Frontiers in Bioengineering and Biotechnology. 9, 727584 (2021).
- Silva, S. J. R., Pardee, K., Balasuriya, U. B. R., Pena, L. Development and validation of a one-step reverse transcription loop-mediated isothermal amplification (RT-LAMP) for rapid detection of ZIKV in patient samples from Brazil. Scientific Reports. 11 (1), 1-13 (2021).
- Shimizu, Y. Cell-free translation reconstituted with purified components. Nature Biotechnology. 19 (8), 751-755 (2001).
- Lavickova, B., Maerkl, S. J. A simple, robust, and low-cost method to produce the PURE cell-free system. ACS Synthetic Biology. 8 (2), 455-462 (2019).

