Аптамер на основе датчика для нехелатированной гадолиния (III)
Summary
The use of polydeoxynucleotide (44-mer aptamer) molecules for sensing unchelated gadolinium(III) ion in an aqueous solution is described. The presence of the ion is detected via an increase in the fluorescence emission of the sensor.
Abstract
A method for determining the presence of unchelated trivalent gadolinium ion (Gd3+) in aqueous solution is demonstrated. Gd3+ is often present in samples of gadolinium-based contrast agents as a result of incomplete reactions between the ligand and the ion, or as a dissociation product. Since the ion is toxic, its detection is of critical importance. Herein, the design and usage of an aptamer-based sensor (Gd-sensor) for Gd3+ are described. The sensor produces a fluorescence change in response to increasing concentrations of the ion, and has a limit of detection in the nanomolar range (~100 nM with a signal-to-noise ratio of 3). The assay may be run in an aqueous buffer at ambient pH (~7 – 7.4) in a 384-well microplate. The sensor is relatively unreactive toward other physiologically relevant metal ions such as sodium, potassium, and calcium ions, although it is not specific for Gd3+ over other trivalent lanthanides such as europium(III) and terbium(III). Nevertheless, the lanthanides are not commonly found in contrast agents or the biological systems, and the sensor may therefore be used to selectively determine unchelated Gd3+ in aqueous conditions.
Introduction
Возрастающее значение магнитно – резонансной томографии (МРТ) в клинической диагностике, которая ограничена присущей чувствительности метода, привело к быстрому росту исследований в области разработки новых гадолиния основе контрастных агентов (GBCAs) 1. GBCAs представляют собой молекулы, которые вводят для улучшения качества изображения, и они , как правило , имеют химическую структуру трехвалентного иона гадолиния (Gd 3+) координирован с полидентатным лигандом. Это комплексообразование имеет решающее значение как нехелатированной Gd 3+ является токсичным; он участвует в развитии нефрогенной системного фиброза у некоторых больных с почечной недостаточностью или недостаточностью 2. Следовательно, обнаружение водного свободного иона играет важную роль в обеспечении безопасности GBCAs. Присутствие нехелатированной Gd 3+ в растворах GBCA часто является результатом неполной реакции между лигандом и ионом, диссоциации комплекса или displacemenт других биологических катионов металлов 3.
Среди нескольких методов , используемых в настоящее время для определения присутствия Gd 3+, те , которые полагаются на хроматографии и / или спектрометрического ранга высшей точки зрения универсальности и применимости 4. Среди их сильные стороны являются высокая чувствительность и точность, возможность анализа различных матриц проб ( в том числе сыворотки человека 5, мочи и волос 6, 7 сточной воды, а также композиций , агентов контрастных 8), а также одновременного количественного определения нескольких 3+ комплексов Gd (листинг исследований до 2013 года описана в комплексном обзоре Telgmann и др.) 4. Единственным недостатком является то, что некоторые из этих методов требует контрольно- измерительные приборы (например, с индуктивно связанной плазмой масс – спектрометрии) 4 , что некоторые лаборатории не могут иметь доступ. В контексте нового открытия GBCA на исследования и доказательство правильности концепции уровней, арelatively более удобный, быстрый и экономически эффективный метод спектроскопического основе (например, УФ-Vis поглощения или флуоресценции), может служить ценным альтернативой. С помощью этих приложений в виду, флуоресцентный аптамеры на основе датчика для водного раствора Gd 3+ был разработан 9.
Аптамеров (Gd-аптамеров) представляет собой 44-щелочное долго одноцепочечной молекулой ДНК с определенной последовательностью оснований, выделенный в процессе систематического выделение лигандов экспоненциальным обогащением (SELEX) 9. Для адаптации аптамер в флуоресцентным датчиком, флуорофор присоединен к концу 5 'нити, которая затем гибридизуют с жаждоутоляющей нити (QS) через 13 дополнительных оснований (рисунок 1). QS помечен темной молекулой гасителя на 3'-конца. При отсутствии Gd 3+, датчик (Gd-сенсор), состоящий из соотношении 1: 2 моль Г.Д.-аптамеров и QS соответственно будут иметь минимальное излучение флуоресценции из – за тпередача энергии от о флуорофора к гасителя. Добавление водного раствора Gd 3+ сместит QS из Gd-аптамеров, что приводит к увеличению флуоресцентной эмиссии.
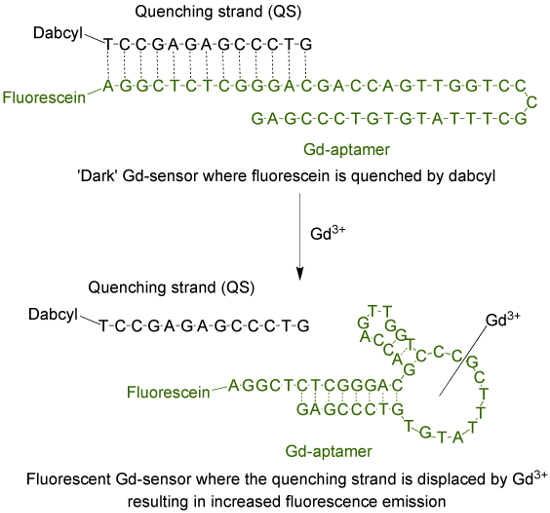
Рисунок 1. Датчик (Gd-сенсор) , который состоит из 44-основания длинной аптамеров (Gd-аптамеров) метили флуоресцеина (флуорофор) и 13-база длиной цепи закалки (QS) помеченным dabcyl (темный гасителя) , При отсутствии нехелатированной Gd 3+, флуоресценция датчика минимальна. С добавлением Gd 3+, смещение QS происходит и наблюдается увеличение эмиссии флуоресценции. Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этой фигуры.
Существует в настоящее время широко используется один спектроскопического основе метод обнаруженияИНГ водного Gd 3+. В этом анализе используют молекулу ксиленоловым апельсин, обнаруживающая сдвиг максимума длины волны поглощения от 433 до 573 нм при хелятации к иону 10. Отношение этих двух максимумов поглощения могут быть использованы для определения количества нехелатированной Gd 3+. Датчик аптамеров является альтернативой (также может быть комплементарной) к ксиленол оранжевого анализа, поскольку эти два метода имеют разные условия реакции (например, рН и состав буферных растворов, используемых), задачи селективностью, линейные диапазоны количественной оценки, а также методов обнаружения 9.
Protocol
Representative Results
Discussion
Использование аптамеров на основе Gd-сенсор, увеличение эмиссии флуоресценции, которая пропорциональна концентрации нехелатированной Gd 3+ наблюдается. Для того, чтобы свести к минимуму количество используемого образца, анализ может выполняться в микропланшет 384-луночного с общи?…
Divulgaciones
The authors have nothing to disclose.
Acknowledgements
We would like to gratefully acknowledge Dr. Milan N Stojanovic from Columbia University, New York, NY for valuable scientific input. This work is supported by funding from the California State University East Bay (CSUEB) and the CSUEB Faculty Support Grant-Individual Researcher. O.E., T.C., and A.L. were supported by the CSUEB Center for Student Research (CSR) Fellowship.
Materials
| Gd-aptamer | IDTDNA | Input sequence and fluorophore modification in the order form | A fluorophore with a different emission wavelength may be used. The aptamer may also be ordered from another company. |
| Quenching strand | IDTDNA | Input sequence and quencher modification in the order form | A different quencher for optimal energy transfer from the fluorophore may be used. The aptamer may also be ordered from another company. |
| Molecular biology grade water | No specific manufacturer, both DEPC or non-DEPC treated work equally well | ||
| Gadolinium(III) chloride anhydrous | Strem | 936416 | Toxic |
| HEPES | Fisher Scientific | BP310-500 | |
| Magnesium chloride anhydrous | MP Biomedicals | 0520984480 – 100 g | |
| Sodium Chloride | Acros Organics | 327300025 | |
| Potassium chloride | Fisher Scientific | P333-500 | |
| Sodium hydroxide, pellets | Fisher Scientific | BP359 | Corrosive |
| Hydrochloric acid | Fisher Scientific | SA49 | Toxic and corrosive |
| 384-well low flange black flat bottom polystyrene NBS plates | Corning | 3575 | Plates which are suitable for fluorescence reading are required. |
| Nalgene Rapid-Flow sterile disposable bottle top filter | Thermo Scientific | 5680020 | The bottle top is fitted with 0.2 micron PES membrane |
| Disposable sterile bottles 250 mL | Corning | 430281 | A larger or smaller bottle may be used |
| 1.5 mL microcentrifuge tubes | No specific manufacturer, as long as they are DNAse and RNAse-free | ||
| 0.2 mL PCR tubes | No specific manufacturer, as long as they are DNAse and RNAse-free | ||
| Micropipets | No specific manufacturer | ||
| Pipet tips (non filter) of appropriate sizes | No specific manufacturer, as long as they are DNAse and RNAse-free | ||
| Name of Equipment | |||
| Plate reader | Biotek Synergy H1 | Plate readers from other manufacturers would work equally well |
Referencias
- Shen, C., New, E. J. Promising strategies for Gd-based responsive magnetic resonance imaging contrast agents. Curr. Opin. Chem. Biol. 17 (2), 158-166 (2013).
- Cheong, B. Y. C., Muthupillai, R. Nephrogenic systemic fibrosis: a concise review for cardiologists. Tex. Heart Inst. J. 37 (5), 508-515 (2010).
- Hao, D., Ai, T., Goerner, F., Hu, X., Runge, V. M., Tweedle, M. MRI contrast agents: basic chemistry and safety. J Magn. Reson. Imaging. 36 (5), 1060-1071 (2012).
- Telgmann, L., Sperling, M., Karst, U. Determination of gadolinium-based MRI contrast agents in biological and environmental samples: a review. Anal. Chim. Acta. 764, 1-16 (2013).
- Frenzel, T., Lengsfeld, P., Schirmer, H., Hütter, J., Weinmann, H. -. J. Stability of gadolinium-based magnetic resonance imaging contrast agents in human serum at 37 degrees C. Invest. Radiol. 43 (12), 817-828 (2008).
- Loreti, V., Bettmer, J. Determination of the MRI contrast agent Gd-DTPA by SEC-ICP-MS. Anal. Bioanal. Chem. 379 (7), 1050-1054 (2004).
- Telgmann, L., et al. Speciation and isotope dilution analysis of gadolinium-based contrast agents in wastewater. Environ. Sci. Technol. 46 (21), 11929-11936 (2012).
- Cleveland, D., et al. Chromatographic methods for the quantification of free and chelated gadolinium species in MRI contrast agent formulations. Anal. Bioanal. Chem. 398 (7), 2987-2995 (2010).
- Edogun, O., Nguyen, N. H., Halim, M. Fluorescent single-stranded DNA-based assay for detecting unchelated gadolinium(III) ions in aqueous solution. Anal. Bioanal. Chem. 408 (15), 4121-4131 (2016).
- Barge, A., Cravotto, G., Gianolio, E., Fedeli, F. How to determine free Gd and free ligand in solution of Gd chelates. A technical note. Contrast Med. Mol. Imaging. 1 (5), 184-188 (2006).
- Johansson, M. K. Choosing reporter-quencher pairs for efficient quenching through formation of intramolecular dimers. Methods Mol. Biol. 335, 17-29 (2006).
- Sherry, A. D., Caravan, P., Lenkinski, R. E. A primer on gadolinium chemistry. J. Magn. Reson. Imaging. 30 (6), 1240-1248 (2009).
- Shakhverdov, T. A. A cross-relaxation mechanism of fluorescence quenching in complexes of lanthanide ions with organic ligands. Opt. Spectrosc. 95 (4), 571-580 (2003).
- Brittain, H. G. Submicrogram determination of lanthanides through quenching of calcein blue fluorescence. Anal. Chem. 59 (8), 1122-1125 (1987).

