تحديد الوضع الوظيفي للمسار القشري الشوكي في غضون أسبوع واحد من السكتة الدماغية
Summary
هذا البروتوكول هو لتقييم وظيفة الجهاز النخاعي في غضون 1 أسبوع من السكتة الدماغية. ويمكن استخدامه لاختيار المرضى وطبقاتهم في تجارب التدخلات المصممة لتحسين استعادة حركية الأطراف العلوية والنتائج وفي الممارسة السريرية للتنبؤ بالنتائج الوظيفية للطرف العلوي بعد 3 أشهر من السكتة الدماغية.
Abstract
يعني التغير الكبير بين الأفراد في استعادة وظيفة الطرف العلوي (UL) بعد السكتة الدماغية أنه من الصعب التنبؤ بإمكانية تعافي الفرد استنادًا إلى التقييمات السريرية وحدها. السلامة الوظيفية للمسار القشري الشوكي هو علامة بيولوجية تشخيصية هامة لاستعادة وظيفة UL ، خاصة بالنسبة لأولئك الذين يعانون من ضعف UL الأولي الشديد. تقدم هذه المقالة بروتوكولًا لتقييم وظيفة الجهاز الكورتيكفي النخاعي في غضون أسبوع واحد من السكتة الدماغية. يمكن استخدام هذا البروتوكول لاختيار المرضى وطبقاتهم في تجارب التدخلات المصممة لتحسين تعافي محرك UL والنتائج بعد السكتة الدماغية. البروتوكول يشكل أيضا جزءا من خوارزمية PREP2، الذي يتوقع وظيفة UL للمرضى الأفراد 3 أشهر بعد السكتة الدماغية. تجمع الخوارزمية بشكل تسلسلي بين تقييم قوة UL والعمر والتحفيز المغناطيسي عبر الجمجمة وشدة السكتة الدماغية ، في غضون أيام قليلة من السكتة الدماغية. يتم وصف فوائد استخدام PREP2 في الممارسة السريرية في مكان آخر. تركز هذه المقالة على استخدام تقييم قوة UL والتحفيز المغناطيسي عبر الجمجمة لتقييم وظيفة الجهاز النخاعي.
Introduction
عادة ما تضعف وظيفة الطرف العلوي بعد السكتة الدماغية ، واستعادة وظيفة UL مهم لاستعادة الاستقلال في أنشطة الحياة اليومية1. غالبًا ما تهدف تجارب إعادة تأهيل السكتة الدماغية إلى تحسين تعافي UL والنتائج بعد السكتة الدماغية. يتم إجراء معظم أبحاث إعادة تأهيل السكتة الدماغية مع المرضى في المرحلة المزمنة (> 6 أشهر بعد السكتة الدماغية) ، ومع ذلك فإن معظم إعادة التأهيل يحدث في وقت مبكر بعد السكتة الدماغية2،3. يجب إجراء المزيد من الأبحاث مع المرضى بعد السكتة الدماغية مباشرة لبناء قاعدة أدلة لممارسة إعادة التأهيل.
واحدة من أكبر التحديات عند إجراء البحوث بعد فترة وجيزة من السكتة الدماغية هو الكشف عن آثار التدخل على خلفية الانتعاش التي تحدث خلال الأسابيع والأشهر الأولى بعد السكتة الدماغية. يؤدي التباين الشديد في العرض السريري والانتعاش إلى خلق ضوضاء يمكن أن تحجب الآثار المفيدة للتدخلات. وعادة ما تكون مجموعات التدخل والمكافحة متوازنة على المقاييس السريرية للإعاقة العصبية الأولية. ومع ذلك ، فإن هذه التدابير غالبا ما تكون مؤشرات ضعيفة على قدرة المريض على الشفاء اللاحق ، ولا سيما أولئك الذين يعانون من ضعف أولي حاد4،5. وهذا يعني أنه يمكن مطابقة المجموعات للمقاييس السريرية الأساسية وعدم مطابقتها لإمكانات تعافيها، مما يجعل من الصعب التأكد من آثار التدخل. يمكن للعلامات الحيوية معالجة هذا التحدي من خلال تحديد إمكانات المريض الفردي لاستعادة المحرك ، بحيث يمكن مطابقة المجموعات بدقة وطبقات6،7،8. يمكن استخدام المؤشرات الحيوية أيضًا لاختيار المرضى الذين من المرجح أن يستجيبوا لآليات التدخل المعروفة أو المفترضة للعمل6.
السلامة الوظيفية للمسار القشري (CST) هو علامة حيوية رئيسية تتوقع استرداد وظيفة UL بعد السكتة الدماغية5،8،9،10،11،12. لجنة العلم والتكنولوجيا ينقل الناتج الحركي التنازلي من قشرة المحرك الأولية إلى الحبل الشوكي وضروري للتنسيق والتحكم الحركي غرامة. المرضى الذين يعانون من CST وظيفية بعد السكتة الدماغية هم أكثر عرضة لاستعادة القوة والتنسيق، والبراعة من المرضى دون. يمكن أن يكون التقييم السريري كافيًا للتأكد من أن CST تعمل في المرضى الذين يعانون من ضعف خفيف13،14،15. ومع ذلك ، فإن المرضى الذين يعانون من ضعف أولي أكثر شدة قد يكون أو لا يكون لديهم CST وظيفية ، وهناك حاجة إلى تقييم عصبي فسيولوجي باستخدام التحفيز المغناطيسي عبر الجمجمة (TMS)9،10،11،16،17.
TMS هو تقنية غير باضعة وغير مؤلمة التي يمكن استخدامها لاختبار وظيفة CST18. لفائف TMS يسلم التحفيز المغناطيسي على قشرة المحرك الأساسي الذي يولد كرة تنازلي في لجنة العلم والتكنولوجيا، مما يثير إمكانات المحرك أثار (MEP) في عضلات الطرف المقابل19. يشير وجود MEP في الذراع أو اليد (MEP+) إلى CST وظيفيويرتبط بإمكانية أكبر لاسترداد وظيفة UL. المرضى الذين هم MEP- هي الأكثر احتمالا أن يكون أسوأ الانتعاش UL، مع عدم عودة وظيفة اليد منسقة وبارعة4،6،9،12،16.
اختبار جميع المرضى الذين يعانون من TMS غير عملي وغير ضروري ، حيث أن أولئك الذين يعانون من ضعف أولي خفيف لديهم على الأرجح CST17وظيفية. لذلك ، هناك حاجة إلى نهج هرمي بحيث يتم استخدام TMS فقط للمرضى الذين يعانون من ضعف أولي أكثر شدة. تم تطوير خوارزمية PREP2 باستخدام مزيج من التدابير السريرية وTMS لتقييم وظيفة CST والتنبؤ بالنتيجة المحتملة UL في 3 أشهر بعد السكتة الدماغية(الشكل 1)17. PREP2 يبدأ في اليوم 3 poststroke عن طريق اختبار قوة اختطاف الكتف وتمديد الإصبع في الذراع paretic (درجة SAFE) ، وذلك باستخدام درجات مجلس البحوث الطبية. إذا كان مجموع هذه الدرجات هو 5 أو أكثر من أصل 10 ، فمن “الآمن” لنفترض أن المريض هو MEP +. ومن المتوقع أن يكون هؤلاء المرضى نتيجة جيدة أو ممتازة UL قبل 3 أشهر بعد السكتة الدماغية، اعتمادا على سنهم17. هؤلاء المرضى لا يحتاجون إلى TMS لتحديد حالة MEP ، وتقليل التكلفة والاختبارات غير الضرورية للمريض.
المرضى الذين يعانون من درجة آمنة أقل من 5 في اليوم 3 poststroke تتطلب TMS لتحديد النزاهة الوظيفية للجنة العلم والتكنولوجيا الخاصة بهم. إذا كان يمكن الحصول على MEP من شعاع يريفاليس الكاربي الباسط (ECR) أو العضلات البينية الظهرية الأولى (FDI) ، فإن المريض هو MEP + ومن المتوقع أن يستعيد التحكم الحركي الدقيق في اليد عن طريق 3 أشهر بعد السكتة الدماغية. ما يقرب من نصف المرضى الذين يعانون من درجة آمنة أقل من 5 في اليوم 3 بعد السكتة الدماغية هي MEP +. الأهم من ذلك، يمكن أن يكون المرضى درجة آمنة منخفضة مثل صفر وتكون MEP +. وهذا يوضح الحاجة إلى TMS في هذه المجموعة الفرعية من المرضى ، حيث لا يمكن للتقييم السريري وحده التمييز بين المرضى الذين يعانون من CST وظيفية وبدونها. المرضى الذين هم MEP- لديهم أضرار كبيرة CST. ومن المتوقع أن يكون هؤلاء المرضى نتيجة وظيفية محدودة أو ضعيفة UL اعتمادا على شدة السكتة الدماغية عموما، تقاس مع المعهد الوطني للصحة مقياس السكتة الدماغية (NIHSS)(الشكل 1)17. لا يُتوقع من هؤلاء المرضى في MEP استعادة التحكم المنسق والبراعة في الإصبع ويمكن تجميعهم معًا لأغراض البحث.
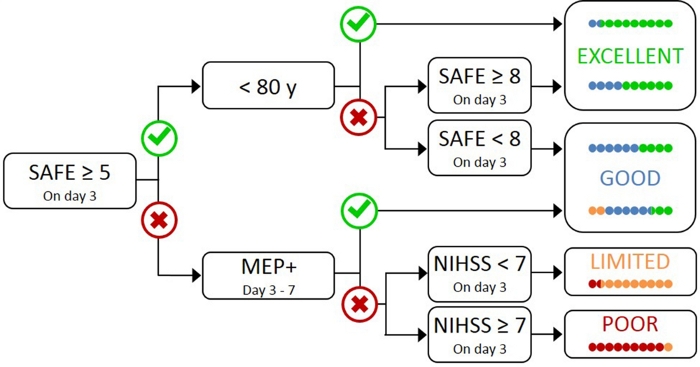
الشكل 1: خوارزمية PREP2. SAFE = اختطاف الكتف، درجة ملحق الإصبع، وهو مجموع درجات مجلس البحوث الطبية لكل من هذه الحركات من أصل 5، لمجموع نقاط SAFE من أصل 10. MEP + = يمكن الحصول على إمكانات Motor Evoked من شعاعي الكاربي الباسط (ECR) و / أو العضلات البينية الظهرية الأولى (FDI) للـ Bpii باستخدام التحفيز المغناطيسي عبر الجمجمة. NIHSS = المعاهد الوطنية لمقياس السكتة الدماغية الصحية. تتوقع الخوارزمية واحدة من أربع نتائج وظيفية محتملة UL في 3 أشهر بعد السكتة الدماغية. ترتبط كل فئة من فئات التنبؤ بتركيز إعادة التأهيل الذي يمكن استخدامه لتكييف العلاج UL2. تمثل النقاط الملونة، بشكل متناسب، دقة خوارزمية PREP2. النقاط هي اللون المرمزة على أساس فئة النتيجة حققت فعلا 3 أشهر بعد السكتة الدماغية (الأخضر = ممتاز; الأزرق = جيد; البرتقالي = محدود؛ الأحمر = الفقراء). الشكل المستنسخة من ستنير وآخرون17. يرجى الضغط هنا لعرض نسخة أكبر من هذا الرقم.
في الممارسة السريرية، PREP2 يتوقع واحدة من أربع فئات النتائج التي يمكن استخدامها لتكييف إعادة التأهيل للمرضى الأفراد ومساعدة المرضى والأسر على فهم ما يمكن أن نتوقع للشفاء UL بهم. حتى الآن ، PREP2 هو الوحيد التحقق الخارجي من صحة أداة التنبؤ UL التي تجمع بين التقييم السريري ومعلومات العلامات الحيوية في شجرة القرار17. بل هو أيضا أداة التنبؤ UL فقط مع البحوث على آثار التنفيذ في الممارسة السريرية20،21. تنبؤات PREP2 دقيقة لحوالي 75٪ من المرضى ، متفائلة للغاية بالنسبة لـ 17٪ ومتشائمة للغاية بالنسبة لـ 8٪ من المرضى في 3 أشهر بعد السكتة الدماغية17. الدقة هي الأعلى للمرضى MEP (دقيقة بالنسبة ل90٪ من المرضى MEP)، وتسليط الضوء على قيمة استخدام TMS لتحديد هؤلاء المرضى الذين يعانون من أضرار شديدة للمسارات الحركيةالتنازلية 17. PREP2 لا يزال صحيحا لحوالي 80٪ من المرضى في 2 سنوات بعد السكتة الدماغية22. وهذا يدعم استخدام PREP2 للتنبؤ UL نتائج المحرك الوظيفي في 3 أشهر وعلى المدى الطويل. معلومات حول تقديم تنبؤات PREP2 واستخدامها في الممارسة السريرية خارج نطاق هذه الأساليب ورقة، ولكن الموارد التفصيلية متوفرة على الانترنت23.
PREP2 يوفر للباحثين أداة لاختيار وطبقات المرضى للتجارب السريرية. وهذا يسمح للمرضى أن تكون مجمعة ليس فقط وفقا للخصائص السريرية خط الأساس، ولكن أيضا إمكاناتهم العصبية البيولوجية للانتعاش UL. على الرغم من الأدلة المتزايدة لاستخدام TMS كعلامة بيولوجية تشخيصية للشفاء UL، قد يكون عدم الإلمام ببروتوكولات TMS في إعدادات المستشفى مع مرضى السكتة الدماغية تحت الحاد عائقاً أمام استخدامه في البحوث. لذلك ، يهدف هذا البروتوكول إلى توضيح كيفية استخدام درجة SAFE و TMS لتقييم وظيفة CST في المرضى في إعداد المستشفى في وقت مبكر بعد السكتة الدماغية.
Protocol
Representative Results
Discussion
وظيفة CST التي تم تقييمها مع حالة MEP هي علامة بيولوجية تشخيصية رئيسية لتعافي UL والنتيجة بعد السكتة الدماغية. ما مجموعه 95 ٪ من المرضى الذين يعانون من CST وظيفية في 1 أسبوع بعد السكتة الدماغية تحقيق عمل البحوث اختبار الذراع (ARAT) درجة ما لا يقل عن 34 من أصل 57 من قبل 3 أشهر بعد17. على العكس ?…
Divulgaciones
The authors have nothing to disclose.
Acknowledgements
يشكر المؤلفان البروفيسور ونستون ببلو وهاري جوردان على مساهمتهما القيمة في هذا العمل. ومول هذا العمل مجلس البحوث الصحية في نيوزيلندا.
Materials
| alcohol/skin cleansing wipes | Reynard | alcohol prep pads | |
| electromyography electrodes | 3M | red dot electrodes | |
| Magstim TMS coil | Magstim | flat figure-8 coil | |
| razors | any | ||
| skin prep tape | 3M | red dot skin prep tape | |
| TMS stimulator | Magstim | Magstim 200 single pulse stimulator |
Referencias
- Veerbeek, J. M., Kwakkel, G., van Wegen, E. E., Ket, J. C., Heymans, M. W. Early prediction of outcome of activities of daily living after stroke: a systematic review. Stroke. 42 (5), 1482-1488 (2011).
- Lohse, K. R., Schaefer, S. Y., Raikes, A. C., Boyd, L. A., Lang, C. E. Asking New Questions with Old Data: The Centralized Open-Access Rehabilitation Database for Stroke. Frontiers in Neurology. 7, 153 (2016).
- Stinear, C., Ackerley, S., Byblow, W. Rehabilitation is initiated early after stroke, but most motor rehabilitation trials are not: a systematic review. Stroke. 44 (7), 2039-2045 (2013).
- Stinear, C. M. Prediction of recovery of motor function after stroke. Lancet Neurology. 9 (12), 1228-1232 (2010).
- Byblow, W. D., Stinear, C. M., Barber, P. A., Petoe, M. A., Ackerley, S. J. Proportional recovery after stroke depends on corticomotor integrity. Annals of Neurology. 78 (6), 848-859 (2015).
- Stinear, C. M. Prediction of motor recovery after stroke: advances in biomarkers. Lancet Neurology. 16 (10), 826-836 (2017).
- Kim, B., Winstein, C. Can Neurological Biomarkers of Brain Impairment Be Used to Predict Poststroke Motor Recovery? A Systematic Review. Neurorehabilitation and Neural Repair. 31 (1), 3-24 (2016).
- Boyd, L. A., et al. Biomarkers of stroke recovery: Consensus-based core recommendations from the Stroke Recovery and Rehabilitation Roundtable. International Journal of Stroke. 12 (5), 480-493 (2017).
- Escudero, J. V., Sancho, J., Bautista, D., Escudero, M., Lopez-Trigo, J. Prognostic value of motor evoked potential obtained by transcranial magnetic brain stimulation in motor function recovery in patients with acute ischemic stroke. Stroke. 29 (9), 1854-1859 (1998).
- Pennisi, G., et al. Absence of response to early transcranial magnetic stimulation in ischemic stroke patients: prognostic value for hand motor recovery. Stroke. 30 (12), 2666-2670 (1999).
- Rapisarda, G., Bastings, E., de Noordhout, A. M., Pennisi, G., Delwaide, P. J. Can motor recovery in stroke patients be predicted by early transcranial magnetic stimulation?. Stroke. 27 (12), 2191-2196 (1996).
- Bembenek, J. P., Kurczych, K., Karli Nski, M., Czlonkowska, A. The prognostic value of motor-evoked potentials in motor recovery and functional outcome after stroke – a systematic review of the literature. Functional Neurology. 27 (2), 79-84 (2012).
- Smania, N., et al. Active finger extension: a simple movement predicting recovery of arm function in patients with acute stroke. Stroke. 38 (3), 1088-1090 (2007).
- Nijland, R. H., van Wegen, E. E., Harmeling-van der Wel, B. C., Kwakkel, G. EPOS Investigators. Presence of finger extension and shoulder abduction within 72 hours after stroke predicts functional recovery: early prediction of functional outcome after stroke: the EPOS cohort study. Stroke. 41 (4), 745-750 (2010).
- Katrak, P., et al. Predicting upper limb recovery after stroke: the place of early shoulder and hand movement. Archives of Physical Medicine and Rehabilitation. 79 (7), 758-761 (1998).
- Stinear, C. M., Barber, P. A., Petoe, M., Anwar, S., Byblow, W. D. The PREP algorithm predicts potential for upper limb recovery after stroke. Brain. 135 (Pt 8), 2527-2535 (2012).
- Stinear, C. M., et al. PREP2: A biomarker-based algorithm for predicting upper limb function after stroke. Annals of Clinical and Translational Neurology. 4 (11), 811-820 (2017).
- Groppa, S., et al. A practical guide to diagnostic transcranial magnetic stimulation: report of an IFCN committee. Clinical Neurophysiology. 123 (5), 858-882 (2012).
- Barker, A. T., Jalinous, R., Freeston, I. L. Non-invasive magnetic stimulation of human motor cortex. Lancet. 1 (8437), 1106-1107 (1985).
- Stinear, C. M., Byblow, W. D., Ackerley, S. J., Barber, P. A., Smith, M. C. Predicting Recovery Potential for Individual Stroke Patients Increases Rehabilitation Efficiency. Stroke. 48 (4), 1011-1019 (2017).
- Connell, L. A., Smith, M. C., Byblow, W. D., Stinear, C. M. Implementing biomarkers to predict motor recovery after stroke. NeuroRehabilitation. 43 (1), 41-50 (2018).
- Smith, M. C., Ackerley, S. J., Barber, P. A., Byblow, W. D., Stinear, C. M. PREP2 Algorithm Predictions Are Correct at 2 Years Poststroke for Most Patients. Neurorehabilitation and Neural Repair. 33 (8), 635-642 (2019).
- Rossi, S., Hallett, M., Rossini, P. M., Pascual-Leone, A. Safety, ethical considerations, and application guidelines for the use of transcranial magnetic stimulation in clinical practice and research. Clinical Neurophysiology. 120 (12), 2008-2039 (2009).
- Talelli, P., Greenwood, R. J., Rothwell, J. C. Arm function after stroke: neurophysiological correlates and recovery mechanisms assessed by transcranial magnetic stimulation. Clinical Neurophysiology. 117 (8), 1641-1659 (2006).

