Nauwkeurige en nauwkeurige FRET-metingen met één molecuul uitvoeren met behulp van de Open-Source smfBox
Summary
Dit artikel biedt stapsgewijze instructies voor het uitvoeren van volledig gecorrigeerde nauwkeurige FRET-metingen op individuele, vrij verspreidende biomoleculen met behulp van de open-source, goedkope smfBox, van inschakelen, via uitlijning en scherpstellen, tot gegevensverzameling en -analyse.
Abstract
De smfBox is een recent ontwikkeld kosteneffectief, open-source instrument voor single-molecule Förster Resonance Energy Transfer (smFRET), dat metingen aan vrij diffunderende biomoleculen toegankelijker maakt. Dit overzicht bevat een stapsgewijs protocol voor het gebruik van dit instrument om metingen te doen van nauwkeurige FRET-efficiëntie in duplex DNA-monsters, inclusief details van de monstervoorbereiding, instrumentopstelling en -uitlijning, gegevensverzameling en volledige analyseroutines. De gepresenteerde aanpak, die omvat hoe alle correctiefactoren kunnen worden bepaald die nodig zijn voor nauwkeurige fret-afgeleide afstandsmetingen, bouwt voort op een groot aantal recente samenwerkingsverbanden in de FRET-gemeenschap, die gericht zijn op het vaststellen van standaardprotocollen en analysebenaderingen. Dit protocol, dat gemakkelijk kan worden aangepast aan een reeks biomoleculaire systemen, draagt bij aan de groeiende inspanningen om smFRET te democratiseren voor de bredere wetenschappelijke gemeenschap.
Introduction
Single-molecule Förster resonantie energieoverdracht (smFRET) is een techniek die de FRET-efficiëntie meet tussen twee kleurstoffen – een donor en een acceptor – op het niveau van individuele moleculen. FRET is een fotofysisch proces dat voortkomt uit de overlappende energiespectra van twee kleurstoffen: de donor wordt geëxciteerd door licht van een specifieke golflengte en draagt energie niet-stralingsmatig over aan de acceptor, wat resulteert in emissie van de acceptor. De efficiëntie van deze overdracht is omgekeerd evenredig met het zesde vermogen van de afstand tussen de twee kleurstoffen, dus de overdrachtsefficiëntie varieert met de afstand1. Deze FRET-efficiëntie kan dus worden gebruikt om ruimtelijke informatie te bepalen over het molecuul (en) 2 waaraan de kleurstoffen zijn bevestigd, binnen een bereik van 3-10 nm. Deze schaal, en het feit dat veranderingen in FRET-efficiëntie gevoelig zijn voor angstrom moleculaire bewegingen3, maakt de techniek zeer geschikt voor het onderzoeken van structurele informatie over biomoleculen – zoals nucleïnezuren en eiwitten – zonder de complicaties van ensemblegemiddelde4,5,6. Hoewel veranderingen in relatieve FRET-efficiëntie kunnen worden gebruikt om biomoleculaire interacties en conformatiedynamiek te monitoren en licht te werpen op belangrijke cellulaire processen zoals eiwit(on)vouwing, transcriptie en DNA-replicatie en -reparatie, zijn absolute FRET-efficiënties gebruikt om precieze afstanden te bepalen voor biomoleculaire structuurbepaling7,8,9,10,11 , het overwinnen van de noodzaak van kristallisatie of bevriezing zoals vereist is voor sommige andere structurele methoden4,12.
smFRET-experimenten nemen meestal twee vormen aan, confocale of totale interne reflectiefluorescentie (TIRF) microscopie. Tussen beide benaderingen kan de moleculaire dynamica van biomoleculen doorgaans worden onderzocht op tijdschalen van pico- tot milliseconde (confocale, vrij diffunderende moleculen) tot milliseconde tot uren (TIRF, oppervlakte geïmmobiliseerde moleculen). Dit komt door de verschillende opstellingen die bij elke techniek betrokken zijn. Bij TIRF-microscopie worden moleculen geïmmobiliseerd op het oppervlak van een dia en geëxciteerd door een evanescente golf (figuur 1A). Hier ligt de focus echter op confocale microscopie, omdat dit het formaat van de smfBox is. Bij confocale microscopie worden moleculen niet geïmmobiliseerd en diffunderen ze in plaats daarvan vrij via Brownse beweging door het confocale volume (~ 1 fL), gevormd door een laserstraal door een lens met een hoog numeriek diafragma te richten op een plek op een bepaalde diepte in de oplossing (figuur 1B). De resulterende emissie wordt teruggefocusseerd door hetzelfde diafragma en gefilterd door een dichroïsche spiegel (figuur 1C voor volledig schematisch). Het wordt vervolgens door een gaatje gericht om onscherp licht te verwijderen en op een lawinefotodiode (APD). Wanneer de APD een foton detecteert, geeft het een TTL-puls af, waarvan de timing kan worden opgenomen met een resolutie tot picoseconde. De waarnemingstijd van deze vrij diffurende moleculen in de nabijheid van het confocale volume ligt gewoonlijk binnen de orde van milliseconden.
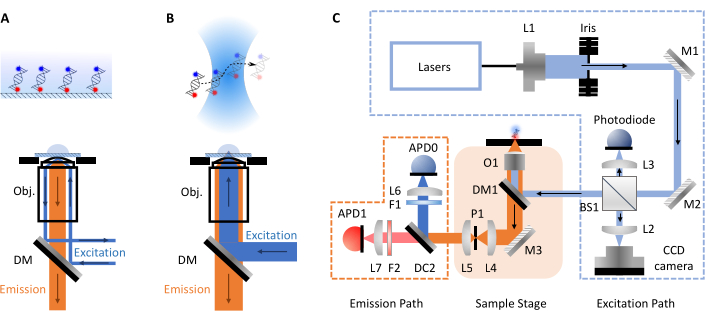
Figuur 1: Schema’s met principes van microscopie en de smfBox-opstelling. (A) Total Internal Reflection Fluorescence (TIRF) Microscopieprincipe: excitatielicht wordt gericht op de rand van het objectief (Obj.) en ondergaat totale interne reflectie op de coverslip-bufferinterface die een exponentieel rottend evanescence-veld genereert om aan het oppervlak gehechte moleculen te prikkelen. (B) Confocale microscopie: Vrij diffunderende moleculen worden geëxciteerd door een bijna diffractie-beperkte plek gericht in het monster. (C) De smfBox-opstelling die in dit protocol wordt gebruikt en toont alle belangrijke componenten: lawinefotodiodes (APD), beam splitter (BS), dichroïsche spiegels (DM), filters (F), spiegels (M), objectief (O) en pinhole (P). Klik hier om een grotere versie van deze figuur te bekijken.
Meer recent bevatten smFRET-technieken twee kleurexcitaties, waarbij lasers die overeenkomen met de donor- en acceptor-excitatiegolflengten worden afgewisseld5. Dit kan op twee manieren worden gedaan, de eerste door continue golflasers te moduleren op de KHz-tijdschaal, die bekend staat als alternating laser excitation (ALEX)13,14. De tweede methode interleaves snelle pulsen op de MHz-tijdschaal; dit is nanoseconde-ALEX15 of gepulseerde interleaved excitatie (PIE)16. Bij al deze benaderingen leidt informatie van de acceptorlaser tot berekening van de zogenaamde stoichiometrie, die onderscheid kan maken tussen moleculen met een lage FRET-efficiëntie en moleculen zonder acceptor (hetzij door onvolledige etikettering of fotobleaching). Het gebruik van PIE/ns-ALEX geeft bovendien toegang tot fluorescerende levensduur op het niveau van één molecuul, en anisotropieën kunnen worden gemeten in combinatie met polariserende optica. Deze combinatie van metingen staat bekend als multiparameter fluorescentiedetectie (MFD)9.
Ondanks de vele voordelen van smFRET, wordt het niet veel gebruikt buiten gespecialiseerde laboratoria vanwege de hoge kosten van commerciële instrumenten en een gebrek aan eenvoudige, zelfbouwalternatieven. Een groeiende trend naar de ontwikkeling van goedkope opensourcemicroscopie vindt plaats en andere platforms zijn onlangs ontstaan, waaronder Planktonscope17, OpenFlexure Microscope18, Flexiscope19, miCube20, liteTIRF21 en Squid22. Hierin beschrijft de studie het protocol voor het gebruik van de smfBox, een recent ontwikkelde kosteneffectieve confocale opstelling die in staat is om de FRET-efficiëntie tussen twee kleurstoffen op vrij diffunderende afzonderlijke moleculen te meten. Gedetailleerde bouwinstructies en alle benodigde operationele software zijn vrij beschikbaar op: https://craggslab.github.io/smfBox/ 23. De optische opstelling van de smfBox is samengesteld uit direct beschikbare componenten die zijn gekocht bij betaalbare en breed toegankelijke fabrikanten, terwijl de microscoopbehuizing (verantwoordelijk voor het grootste deel van de kosten in een standaard confocale opstelling) is vervangen door een aangepaste lichtdichte geanodiseerde aluminium doos (waardoor metingen kunnen worden uitgevoerd onder omgevingslichtomstandigheden). Deze doos bevat belangrijke optische componenten, waaronder de excitatie dichroïcum, objectief en pinhole, en een mechanische laservergrendeling, waardoor het veilig kan werken als een klasse I laserproduct (zie figuur 1C voor een volledig schema). De smfBox gebruikt ALEX om de kleurstof stoichiometrie te valideren en nauwkeurige FRET-correctiefactoren te bepalen. Het wordt bediend met behulp van op maat geschreven, open-source software (smOTTER), die alle aspecten van de gegevensverzameling controleert en de gegevens uitvoert in het open-source foton-HDF5-formaat24, compatibel met veel analysetools van derden. De smfBox en de acquisitie- en data-analyseprotocollen zijn onlangs getest tegen >20 andere instrumenten (zowel confocale als TIRF) in een blinde studie met meerdere laboratoria25. De verkregen FRET-efficiënties waren uitstekend in overeenstemming met alle andere instrumenten, ondanks dat de smfBox slechts een fractie van de prijs van commercieel verkrijgbare opstellingen kostte.
Hier wordt een stapsgewijs protocol geschetst voor het verwerven en analyseren van nauwkeurige, absolute FRET-efficiënties op vrij verspreidende DNA-duplexen met behulp van de smfBox, helemaal van inschakelen, via uitlijning en focus, tot gegevensverzameling en -analyse. De hier gebruikte monsters zijn drie duplex-DNA’s (met hoge, midden- en lage FRET-efficiënties, zie tabel 1) die werden beoordeeld in de wereldwijde blinde studie25; de methode is echter aanpasbaar aan vele moleculaire systemen, waaronder eiwitten en andere nucleïnezuren. De hoop is dat zo’n gedetailleerd protocol, samen met de reeds bestaande bouwinstructies voor de smfBox23, zal helpen om deze krachtige techniek nog toegankelijker te maken voor een breed scala aan laboratoria.
Protocol
Representative Results
Discussion
De meest kritische stappen in het protocol zijn de uitlijning van de microscoop en het aanpassen van de monsterconcentratie aan de juiste verdunning. Als de uitlijning is uitgeschakeld, is er mogelijk onvoldoende signaal om bursts te identificeren en histogrammen uit te zetten, en als er een verkeerde uitlijning optreedt tussen monsters, kan een nauwkeurige FRET-correctie mislukken als gevolg van veranderingen in lekkage en detectie / excitatie-efficiëntie. Het gebruik van een geschikte concentratie is ook belangrijk, een te hoge concentratie zal samenvallende uitbarstingen geven, die meerdere moleculen bevatten met potentieel verschillende FRET-efficiënties of stoichiometrieën labelen. Een te lage concentratie geeft te weinig bursts voor robuuste data-analyse.
Het hier beschreven protocol is voor het meten van afstanden in statische enkele FRET-soorten. Als het monster meer dan één piek in het FRET-efficiëntiehistogram heeft, of pieken breed lijken (wat kan gebeuren met dynamische soorten), dan kunnen meer uitbarstingen nodig zijn om histogrammen met dezelfde mate van precisie te passen. Voor twee goed gescheiden pieken is ongeveer twee keer zoveel data nodig, maar als de populaties elkaar iets overlappen dan zijn er nog meer data nodig.
Als de twee populaties interconverteren op de tijdschaal van het experiment, kunnen de dynamiek en kinetiek van het systeem mogelijk worden bepaald. Tests zoals BVA27 es 2CDE28 kunnen bevestigen dat de tussenliggende bursts dynamisch van aard zijn, terwijl analyses zoals dPDA29,30 of H2MM31 de snelheden van interconversie kunnen bepalen. Jupyter notebooks voor BVA en 2CDE zijn beschikbaar op de FRETBursts26 website, en de MATLab gebaseerde software PAM32 kan BVA, 2CDE en PDA analyses uitvoeren.
Confocale single-molecule FRET kan gemakkelijk toestanden waarnemen die veel korter leven (~ 1 ms) dan TIRF; de korte waarnemingstijden, beperkt door diffusie, geven echter geen moleculaire geschiedenis en kunnen dus geen langere verblijftijden of complexe overgangsnetwerken bepalen op de manier waarop oppervlakte-geïmmobiliseerde experimenten dat kunnen.
Omdat het protocol vrij diffunderende moleculen meet bij een zeer lage concentratie, werkt het het beste bij het meten van intramoleculaire afstanden op hetzelfde molecuul. Intermoleculaire afstanden tussen tijdelijk gebonden moleculen kunnen worden gemeten op voorwaarde dat de Kd van de twee moleculen laag genoeg is dat het complex in een significante hoeveelheid bestaat bij de lage werkconcentratie die vereist is voor het experiment (~ 100 pM). Als de Kd veel hoger is dan dit, dan zullen alleen afzonderlijk gelabelde moleculen worden gezien. Dit probleem kan worden opgelost door microfluïdica te gebruiken om de twee gelabelde componenten in een hoge concentratie samen te mengen en vervolgens snel te verdunnen en over het objectief te stromen voordat het complex dissocieert33,34.
Het meten van FRET-efficiëntie op het niveau van één molecuul heeft een aanzienlijk voordeel ten opzichte van ensembletechnieken, omdat het informeert over heterogene subpopulaties, die in een ensemble-experiment gemiddeld zouden zijn. Bovendien geeft single-molecule FRET met ALEX toegang tot nauwkeurige FRET-efficiënties, die kunnen worden omgezet in nauwkeurige afstanden. Dit maakt het mogelijk om meer gedetailleerde structurele informatie te bepalen in plaats van alleen relatieve afstandsveranderingen te onderzoeken. De smfBox heeft al deze voordelen en mogelijkheden, maar kan worden gebouwd met een veel lager budget dan vergelijkbare commercieel verkrijgbare microscopen die in staat zijn tot confocale smFRET23.
De smfBox vertegenwoordigt een veel lagere toetredingsdrempel voor smFRET-technieken, waardoor onderzoekers conformatieveranderingen en nauwkeurige afstanden binnen en tussen eiwitten en nucleïnezuren kunnen meten7,8,9,10,11,35.
Divulgaciones
The authors have nothing to disclose.
Acknowledgements
De auteurs erkennen dankbaar de volgende financieringsbronnen: BBSRC (BB/T008032/1); EPSRC (Studentship to B.A.) en MRC (Studentship to A.R.-T.).
Materials
| Amino modified oligonucleotide | Eurogentec | N/A | May be ordered from various suppliers or synthesised; amino modification enables labeling with NHS-ester modified dyes |
| Avalanche photodiode (APD) | Excelitas | SPCM-AQRH-14 | Two APDs are required for the smfBox setup |
| Bovine Serum Albumin (BSA) | Merck | A2153 | System dependant; imaging buffer component (0.1 mg/mL in buffer) |
| Compact Laser Combiner | OMICRON | LightHUB-2 | 515 nm (80 mW) and 638 nm (100 mW) lasers |
| Coverglass | VWR | 630-2742 | Thickness: 0.17 ± 0.01 mm, LxW: 22×22 mm |
| Cy3B | Cytiva | PA63101 | 1 mg, PA63100 (5 mg), PA96106 (25 mg) |
| FRETBursts Python Package | N/A | N/A | Open-source python package for burst analysis of freely-diffusing single-molecule FRET data: https://fretbursts.readthedocs.io |
| Imaging Buffer | N/A | System dependant; 5 mM NaCl, 20 mM MgCl2, 5 mM Tris pH 7.5 and 0.1 mg/mL BSA | |
| Immersion Oil | Olympus | IMMOIL-F30CC | |
| Jupyter notebooks | Project Jupyter | N/A | Open-source web application to create and share documents that contain live code, equations, visualizations and text; data analysis notebooks for smfBox can be found in the SI |
| Lens Tissue | ThorLabs | MC-5 | MC-50E is same item in bulk |
| Magnesium Chloride | Merck | M2670 | System dependant; imaging buffer component (20 mM in buffer) |
| MilliQ/Ultrapure water | N/A | ||
| Nanopoistioner | Piezoconcept | FOC300 | Nanopositioner for accurate positioning of microscope objective |
| NHS-ester modified ATTO-550 | ATTO-TEC | AD 550-31 | 1 mg, AD 550-35 (5 mg) |
| NHS-ester modified ATTO-647N | ATTO-TEC | AD 647N-31 | 1 mg, AD 647N-35 (5 mg) |
| Objective lens | Olympus | N1480700 | Olympus objective series from orignal smfBox discontinued; replaced by N5702300 |
| OMICRON Control Center (OCC)- laser control center | OMICRON | N/A | v3.5.34 – OMICRON laser driver software |
| Press-To-Seal silicone isolator | Grace Bio-Labs | 664201 | 8-9 mm Diameter x 1.7 mm Depth |
| smOTTER | N/A | N/A | Open-source acquisition software for the Craggs Lab smfBox: https://github.com/craggslab/smOTTER |
| Sodium Chloride | Merck | S7653 | System dependant; imaging buffer component (5 mM in buffer) |
| Tris base | Merck | 93362 | System dependant; imaging buffer component (5 mM, pH 7.5 in buffer) |
| Type I ultrapure water | Merck | ZIQ7000T0 | Milli-Q® IQ 7000 Ultrapure Water System |
Referencias
- Forster, T. Intermolecular energy migration and fluorescence. Annals of Physics. 437 (1-2), 55-75 (1948).
- Stryer, L., Haugland, R. P. Energy transfer: a spectroscopic ruler. Proceedings of the National Academy of Sciences. 58 (2), 719-726 (1967).
- Hohlbein, J., et al. Conformational landscapes of DNA polymerase I and mutator derivatives establish fidelity checkpoints for nucleotide insertion. Nature Communications. 4 (1), 2131 (2013).
- Lerner, E., et al. Toward dynamic structural biology: Two decades of single-molecule Förster resonance energy transfer. Science. 359 (6373), (2018).
- Hohlbein, J., Craggs, T. D., Cordes, T. Alternating-laser excitation: single-molecule FRET and beyond. Chemical Society Reviews. 43 (4), 1156-1171 (2014).
- Lerner, E., et al. The FRET-based structural dynamics challenge — community contributions to consistent and open science practices. arXiv. , (2020).
- Hellenkamp, B., Wortmann, P., Kandzia, F., Zacharias, M., Hugel, T. Multidomain structure and correlated dynamics determined by self-consistent FRET networks. Nature Methods. 14 (2), 174-180 (2017).
- Craggs, T. D., et al. Substrate conformational dynamics facilitate structure-specific recognition of gapped DNA by DNA polymerase. Nucleic Acids Research. 47 (20), 10788-10800 (2019).
- Tsytlonok, M., et al. Dynamic anticipation by Cdk2/Cyclin A-bound p27 mediates signal integration in cell cycle regulation. Nature Communications. 10 (1), 1676 (2019).
- Nagy, J., et al. Complete architecture of the archaeal RNA polymerase open complex from single-molecule FRET and NPS. Nature Communications. 6 (1), 6161 (2015).
- LeBlanc, S. J., et al. Coordinated protein and DNA conformational changes govern mismatch repair initiation by MutS. Nucleic Acids Research. 46 (20), 10782-10795 (2018).
- Segal, M., et al. High-throughput smFRET analysis of freely diffusing nucleic acid molecules and associated proteins. Methods. 169, 21-45 (2019).
- Kapanidis, A. N., et al. Fluorescence-aided molecule sorting: Analysis of structure and interactions by alternating-laser excitation of single molecules. Proceedings of the National Academy of Sciences. 101 (24), 8936-8941 (2004).
- Kapanidis, A. N., et al. Alternating-laser excitation of single molecules. Accounts of Chemical Research. 38 (7), 523-533 (2005).
- Müller, B. K., Zaychikov, E., Brauchle, C., Lamb, D. C. Pulsed interleaved excitation. Biophysical Journal. 89 (5), 3508-3522 (2005).
- Laurence, T. A., Kong, X., Jager, M., Weiss, S. Probing structural heterogeneities and fluctuations of nucleic acids and denatured proteins. Proceedings of the National Academy of Sciences of the United States of America. 102 (48), 17348-17353 (2005).
- Pollina, T., et al. PlanktonScope: Affordable modular imaging platform for citizen oceanography. bioRxiv. , 056978 (2020).
- Collins, J. T., et al. Robotic microscopy for everyone: the OpenFlexure microscope. Biomedical Optics Express. 11 (5), 2447-2460 (2020).
- Courtney, A., Alvey, L. M., Merces, G. O. T., Burke, N., Pickering, M. The Flexiscope: a low cost, flexible, convertible and modular microscope with automated scanning and micromanipulation. Royal Society Open Science. 7 (3), 191949 (2020).
- Martens, K. J. A., et al. Visualisation of dCas9 target search in vivo using an open-microscopy framework. Nature Communications. 10 (1), 3552 (2019).
- Auer, A., et al. Nanometer-scale multiplexed super-resolution imaging with an economic 3D-DNA-PAINT microscope. ChemPhysChem. 19 (22), 3024-3034 (2018).
- Li, H., et al. Squid: Simplifying quantitative imaging platform development and deployment. bioRxiv. , 424613 (2020).
- Ambrose, B., et al. The smfBox is an open-source platform for single-molecule FRET. Nature Communications. 11 (1), 5641 (2020).
- Ingargiola, A., Laurence, T., Boutelle, R., Weiss, S., Michalet, X. Photon-HDF5: An open file format for timestamp-based single-molecule fluorescence experiments. Biophysical Journal. 110 (1), 26-33 (2016).
- Hellenkamp, B., et al. Precision and accuracy of single-molecule FRET measurements-a multi-laboratory benchmark study. Nature Methods. 15 (9), 669-676 (2018).
- Ingargiola, A., Lerner, E., Chung, S., Weiss, S., Michalet, X. FRETBursts: An open source toolkit for analysis of freely-diffusing single-molecule FRET. PLOS One. 11 (8), 0160716 (2016).
- Torella, J. P., Holden, S. J., Santoso, Y., Hohlbein, J., Kapanidis, A. N. Identifying molecular dynamics in single-molecule FRET experiments with burst variance analysis. Biophysical Journal. 100 (6), 1568-1577 (2011).
- Tomov, T. E., et al. Disentangling subpopulations in single-molecule FRET and ALEX experiments with photon distribution analysis. Biophysical Journal. 102 (5), 1163-1173 (2012).
- Santoso, Y., Torella, J. P., Kapanidis, A. N. Characterizing single-molecule FRET dynamics with probability distribution analysis. ChemPhysChem. 11 (10), 2209-2219 (2010).
- Kalinin, S., Valeri, A., Antonik, M., Felekyan, S., Seidel, C. A. M. Detection of structural dynamics by FRET: A photon distribution and fluorescence lifetime analysis of systems with multiple states. The Journal of Physical Chemistry B. 114 (23), 7983-7995 (2010).
- Pirchi, M., et al. Photon-by-photon hidden Markov model analysis for microsecond single-molecule FRET kinetics. The Journal of Physical Chemistry B. 120 (51), 13065-13075 (2016).
- Schrimpf, W., Barth, A., Hendrix, J., Lamb, D. C. PAM: A framework for integrated analysis of imaging, single-molecule, and ensemble fluorescence data. Biophysical Journal. 114 (7), 1518-1528 (2018).
- Zijlstra, N., et al. Rapid microfluidic dilution for single-molecule spectroscopy of low-affinity biomolecular complexes. Angewandte Chemie International Edition. 56 (25), 7126-7129 (2017).
- Hellenkamp, B., Thurn, J., Stadlmeier, M., Hugel, T. Kinetics of transient protein complexes determined via diffusion-independent microfluidic mixing and fluorescence stoichiometry. The Journal of Physical Chemistry B. 122 (49), 11554-11560 (2018).
- Bennet, I. A., et al. Regional conformational flexibility couples substrate specificity and scissile phosphate diester selectivity in human flap endonuclease 1. Nucleic Acids Research. 46 (11), 5618-5633 (2018).

