Próxima Geração Sequencing para Detecção de acionável mutações em tumores sólidos e líquidos
Summary
This manuscript describes clinical protocols for two next-generation sequencing panels. One panel interrogates hematologic malignancies while the other panel targets genes commonly mutated in solid tumors. Molecular classification of driver mutations in human malignancies offers valuable prognostic and predictive information.
Abstract
As our understanding of the driver mutations necessary for initiation and progression of cancers improves, we gain critical information on how specific molecular profiles of a tumor may predict responsiveness to therapeutic agents or provide knowledge about prognosis. At our institution a tumor genotyping program was established as part of routine clinical care, screening both hematologic and solid tumors for a wide spectrum of mutations using two next-generation sequencing (NGS) panels: a custom, 33 gene hematological malignancies panel for use with peripheral blood and bone marrow, and a commercially produced solid tumor panel for use with formalin-fixed paraffin-embedded tissue that targets 47 genes commonly mutated in cancer. Our workflow includes a pathologist review of the biopsy to ensure there is adequate amount of tumor for the assay followed by customized DNA extraction is performed on the specimen. Quality control of the specimen includes steps for quantity, quality and integrity and only after the extracted DNA passes these metrics an amplicon library is generated and sequenced. The resulting data is analyzed through an in-house bioinformatics pipeline and the variants are reviewed and interpreted for pathogenicity. Here we provide a snapshot of the utility of each panel using two clinical cases to provide insight into how a well-designed NGS workflow can contribute to optimizing clinical outcomes.
Introduction
sequenciamento de próxima geração (NGS) de espécimes clínicos de oncologia tornou-se mais amplamente disponível ao longo dos últimos anos, como o crescimento pontos literatura científica para a importância de identificar as mudanças genéticas segmentáveis e marcadores moleculares preditivos / prognósticos. Painel multi-gene análises e estudos de sequenciamento exome inteiras em ambos os epiteliais 1,2 e hematológica 3 malignidades ter solidificado o conceito de heterogeneidade do tumor e evolução clonal como a doença progride e recaídas. Além disso, ao contrário de tecnologias concorrentes como a reação em cadeia da polimerase (PCR) ou seqüenciamento Sanger, NGS pode detectar a maioria das alterações genômicas em todos os genes do cancro clinicamente relevantes em um único ensaio 4.
O Centro de Diagnóstico personalizados inicialmente lançado com dois painéis clínicos NGS, um costume Painel hematológica (Heme-NGS Panel) e um off-the-shelf Cancer Panel para amostras FFPE (Solid-NGS painel) (veja <strong> Figura 1). Estes painéis cobrir regiões de interesse clinicamente relevantes ou altas dos genes selecionados; nem todos os genes ou exons são totalmente cobertos. Amplicões são gerados por hibridação sonda seguido por extensão e ligação. As regiões-alvo são ainda mais amplificada utilizando PCR com primers universais duplas-indexados, permitindo que até 96 amostras a reunir para o sequenciamento.
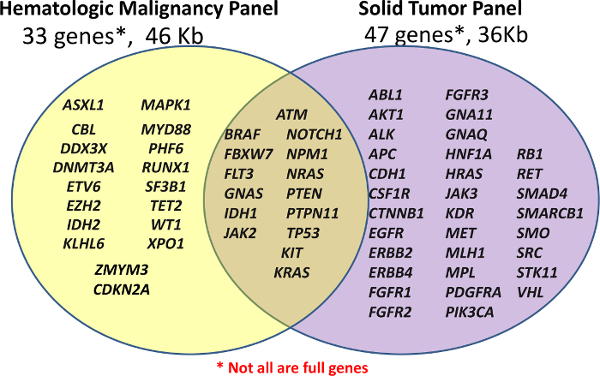
Figura 1:. Lista de Genes abordados nos painéis preparação Biblioteca é realizada usando o costume Painel hematológica (Painel Heme-NGS) de 33 genes ou o off-the-shelf Cancer Panel Amplicon (Solid-NGS) de 47 genes. Nem todos os genes ou exons são cobertos na totalidade, como alguns produtos de amplificação só pode cobrir certos hotspots. Por favor clique aqui para ver uma versão maior desta figura. </ A>
O conteúdo do painel de heme-NGS foi derivado de várias fontes, mas gira em torno de 16 genes mutados na leucemia mielóide aguda (LMA), previamente descrito como demonstrando um elevado nível de utilidade clínica 5. O Painel Solid-NGS é produzido comercialmente com as regiões-alvo com base em genes comumente mutado no cancro como relatado no Catálogo de somáticas Mutações em Câncer (COSMIC) do banco de dados 6.
Vários passos-chave caracterizar o fluxo de trabalho geral para NGS clínicos. Após o médico ordena o teste, um patologista determina a adequação do espécime após a análise da percentagem de tumor e volume da amostra. Em nossa instituição, exigimos pelo menos 10% do tumor devido à taxa de fundo de sequenciação de erro ( "ruído") da tecnologia e da eficiência da abordagem específica. Se o tecido é adequada para o teste, o ADN genómico é extraído. Este ADN é então sujeito a um controlo de qualidade múltipla (QC) etapas. Se o DNA passa QC, uma biblioteca de fragmento amplificado é gerado e sequenciado. Os dados resultantes são analisadas através de um gasoduto de bioinformática in-house. Após a análise bioinformática, as variantes são manualmente revisto e interpretado por patogenicidade antes da incorporação um relatório clínico. Abaixo descrevemos dois casos que passaram por esta rigorosa do fluxo de trabalho e, finalmente, levou a mudanças no manejo clínico.
Caso 1 – Leucemia Mielóide Aguda
A biópsia de medula óssea do doente A era de diagnóstico para a AML, sem maturação. Os estudos citogenéticos foram enviados sobre o espécime de medula óssea e demonstraram um cariótipo feminina normal. Houve 95% de blastos circulantes presentes, por isso, uma amostra de sangue periférico foi enviado para testes de diagnóstico personalizado no Painel de Heme-NGS.
A leucemia mielóide aguda (LMA) é uma doença maligna hematológica da linhagem mielóide de células brancas do sangue. a detecçãode mutações genéticas em AML tornou-se cada vez mais importante para o prognóstico e tratamento, com mutações genéticas recorrentes reconhecidos como importantes na patogênese e prognóstico 7. Mutações no NPM1 e CEBPA têm sido associados com um risco prognóstico favorável, enquanto duplicações em tandem internas (ITD) em FLT3 têm sido associados com um resultado menos favorável 8. Um crescente corpo de evidências suporta um papel patogênico para estas e outras mutações na AML 9.
Caso 2 – Lung Adenocarcinoma
A biópsia de uma massa supraclavicular esquerdo de paciente B demonstrou adenocarcinoma pulmonar. material de biópsia a partir da (FFPE) em massa do linfonodo embebidos em parafina e fixado em formalina foi enviada para o teste genómico (painel sólido-NGS) como rolos / cachos com tumores maiores do que 50%, para identificar se uma mutação estava presente para a intervenção terapêutica alvo.
Lung cancer é a principal causa de mortalidade relacionada com o cancro nos Estados Unidos e é dividido em tipos principais, cancro dois pulmão de não pequenas células (NSCLC) e cancro do pulmão de pequenas células (CPPC). NSCLC pode ser ainda definido como qualquer um adenocarcinoma ou carcinoma de células escamosas, com base na histologia da lesão. Adenocarcinoma pulmonar é o subtipo mais comum de câncer de pulmão, visto em ambos os fumantes e não-fumantes, e é a forma mais comum de câncer de pulmão em não-fumantes 10. Estudos moleculares de adenocarcinomas do pulmão foram identificadas mutações em vários oncogenes 11. As mutações driver mais comuns identificados em fumantes são mutações no KRAS e BRAF. As mutações mais comuns em não-fumantes são mutações em EGFR, e rearranjos envolvendo os genes ALK, RET e ROS1. Tumores pulmonares foram descritos com um exão 20 de inserção em grelha no gene de ErbB2 (HER2 / neu). A anormalidade mais comum no HER2 / neu é uma amplificação de neste locus no cancro da mama para os quais uma terapia-alvo está disponível (trastuzumab: um anticorpo monoclonal humanizado contra HER2 / neu). O HER2 / neu exão 20 de inserção que é observado em 2-4% de pulmão adenocarcimomas 12 demonstrou uma resposta parcial ao tratamento com combinação de HER2 / neu e inibidores de mTOR (neratinib e temsirolímus, respectivamente) 13.
Protocol
Representative Results
Discussion
Como os dois testes NGS descritos neste manuscrito são oferecidos clinicamente, a consideração prática mais importante é o controle de qualidade. Especificamente, perto consideração deve ser dada à qualidade e quantidade de DNA extraído. Isto é especialmente importante para as amostras FFPE que são muitas vezes altamente degradada com um rendimento de ADN variável. Um método de precipitação com isopropanol foi desenvolvido a fim de maximizar o rendimento de ADN a partir de amostras de FFPE como métodos baseados em colunas foram encontrados para levar, por vezes, a tosquia de ADN com volumes de eluição limitados. Portanto, a maior parte do tempo quando uma amostra produz muito baixa concentração ou é muito degradada para o ensaio, isto é provavelmente devido ao tamanho do tecido, o tipo ou a fixação e não o processo de extracção. Para amostras / da medula óssea do sangue, se houver uma falha de extracção, é geralmente devido a um hemodilute amostra a ser (ou seja, não tendo o número suficiente de células brancas do sangue ou tumores em que sorteio) ou quimio extirpadas.
. Nt "> Durante a validação, pontos de corte para a aceitação da qualidade e quantidade de DNA deve ser estabelecida A entrada recomendada de 100-250 ng é muitas vezes usado no ensaio; no entanto, se a qualidade do DNA é boa, em seguida, mais baixos valores de entrada pode ser bem sucedido. Além disso, se a qualidade do DNA é deficiente (ou seja, a quantidade de ADN amplificável é menos de 100-250 ng), em seguida, quantidades de entrada mais elevadas podem melhorar a qualidade dos resultados da sequenciação (uma vez que a quantidade de ADN amplificável irá alcançar a entrada recomendada) . Métricas para a qualidade e quantidade de DNA deve ser aplicado a cada amostra antes de avançar o DNA em preparação biblioteca. Essas amostras em uma "zona cinzenta" (ver Figura 2) deve ser executado a critério do diretor do laboratório ou pessoa designada. Atualmente o melhor forma de prever se o ADN não será um bom desempenho durante a sequenciação é a realização de um ensaio à base de qPCR que permite a quantificação e a qualidade de avaliação de ADN de entrada. Esta abordagem elimina a bioavailability de diferentes fragmentos de tamanho na amostra, através da amplificação de diferentes fragmentos de tamanho (por exemplo, 100 pb, 150 pb, 200 pb e 300 pb) e comparação de rendimento.Actualmente, a preparação da biblioteca envolve um grande número de etapas manuais que um passo em falso em um dos vários momentos pode causar a biblioteca para falhar ou ser de má qualidade. A análise gel microfluídico é o único passo QC para verificar um problema de biblioteca de preparação antes de seqüenciamento. Consequentemente, existem diversos passos críticos onde atenção adicional pode aumentar a probabilidade de uma reacção bem sucedida. É imperativo para garantir a amostra correcta e banco de oligonucleótidos são utilizadas para cada espécime. Garantir e devidamente gravação que cada amostra contém uma das 96 combinações únicas de pares de primers de PCR de dupla indexado reduz a chance de um mix de amostra para cima. Além disso, é importante para garantir a placa de filtro (FPU) drena correctamente; se não drenar adequadamente esta pode causar o exteetapa nsion-ligadura da preparação biblioteca para executar subótima e levar a qualidade dos dados de sequenciamento pobres. Após biblioteca QC, é crítico para assegurar que os grânulos estejam totalmente LNB1 ressuspensas e que a solução LNB1 / LNA1 é bem misturado antes de adicionar as amostras como a concentração desta mistura é usada para determinar a molaridade da biblioteca. Finalmente, se o passo de eluição do grânulo leva a uma quantidade sub-óptima de biblioteca eluindo fora dos grânulos que irá diminuir a densidade de agrupamento e, eventualmente, causar a biblioteca para obter a cobertura não significativo adequada. Por outro lado, um excesso da biblioteca vai levar a uma qualidade lê. Portanto, é importante ser consistente na etapa de normalização baseadas em esferas para assegurar o agrupamento óptima e agrupamento das bibliotecas no sequenciador.
Além disso a preparação da biblioteca, que é crítico para validar um oleoduto bioinformática que irá produzir as chamadas de mutações precisas, a partir dos arquivos fastq desmultiplexado em bruto. escolhendo umsolução personalizada pode ser demorado, pois há muitos alinhadores de código aberto e disponíveis comercialmente, os chamadores variantes, e pacotes de software NGS que seria preciso peneirar. algoritmos personalizados terá de ser concebido para obter estatísticas de desempenho essenciais, identificar mutações recorrentes únicas que escapado ferramentas de código mais abertos e determinar o status do número de cópias sobre cada um dos loci. Durante o processo de validação de um oleoduto bioinformática, é importante para determinar os pontos de corte reportados para as variantes que satisfazem ou excedem tanto uma profundidade mínima de cobertura depois da filtragem da qualidade (por exemplo, um mínimo de 250 leituras) e uma frequência de alelos mínimo (por exemplo, 4 %). Uma vez que este um ensaio baseado em amplicão multiplexados, é importante para determinar o comprimento médio mínimo da profundidade de cobertura (por exemplo, 1.000 vezes) que a biblioteca necessita para conseguir a ser capaz de obter o menor fragmento amplificado realizando a profundidade mínima de leituras. Além disso, a natureza multiplexada do ensaio faz Cause off efeitos alvo e estes "artefatos" terá de ser descoberto e totalmente controlados antes do lançamento. Outra limitação importante para o ensaio descrito é a necessidade de amostras para conter mais de 10% do tumor, a fim de atingir a frequência do alelo menos validado.
A detecção de frequência baixa, 1%, inserções FLT3 é evidência de que a análise manual é ainda desejável neste processo. Mesmo com um corte de 5% freqüência do alelo, algumas mutações importantes talvez não atendidas e, assim, a revisão manual será essencial para determinar estas variantes. Para FLT3-ITD, inspeção visual do exão 14 é realizada para todos os pacientes com LMA para garantir um nível baixo ou grande inserção / duplicação não passa despercebido. Além disso, HER2 exão 20 inserções que são vulgarmente próxima à sequência de iniciador, necessitar de intervenção manual. Apesar de ter um pipeline de bioinformática robusta, algumas variantes poderia passar despercebida, que é apenas a natureza de ter um corte durooff para a maioria das estatísticas mencionadas acima. bioinformática melhores seriam necessários para ajudar a aliviar este problema, assim como as metodologias de preparação e / ou sequenciamento melhor biblioteca, porque é mais vantajoso ter dados de qualidade a cortes ainda mais baixas que contêm menos artefatos e falsos positivos.
A detecção e a interpretação de frequências de alelos pode ser difícil devido à dificuldade na determinação de tumores e de polarização percentagem amplificação de algumas regiões do genoma. Além disso, as frequências de alelos mais de 50% pode ser detectada, como observado no caso 2. Isto é interpretado como uma perda de heterozigotia (LOH) evento, quer devido à perda do alelo normal, o que conduz ao aumento aparente de mutante lê, uma ganho do alelo mutante (por exemplo, 2 mutante e uma cópia normal) ou outros mecanismos. Estes mecanismos podem ser elucidadas pela utilização de matriz de hibridação comparativa genómico (aCGH 19) e / ou uma matriz de genotipagem de SNP. 20.
As metodologias de enriquecimento alvo atuais contam com procedimentos de dia inteiro de qualquer das técnicas de PCR multiplexados captura híbrida ineficiente ou que resultam na necessidade de uma maior cobertura sequenciamento de uma única amostra e mais off sequenciamento alvo lê. Aplicações adicionais para oncologia molecular NGS esperadas no futuro próximo, irá incluir mais fáceis métodos de preparação de bibliotecas que podem ser completamente automatizável e ser capaz de processar as amostras com quantidades muito pequenas de ADN de entrada (ou seja, menos de 1 ng), bem como amostras com altamente degradada ADN. Para enfrentar esses desafios, a maioria dos métodos será presumivelmente, baseado na PCR, quer ser uma abordagem de PCR de várias etapas ou uma abordagem PCR singleplex massivamente paralelo. Além disso, o código de barras molecular de produtos de amplificação individuais foi demonstrado reduzir drasticamente fundo sequenciação ruído e irá permitir o teste das amostras com menores proporções de células de tumor para obter frequências alélicas inferiores e avançar para capturar circulating células tumorais.
Detecção de mutações associadas à doença em amostras de cancro tem sido padrão de atendimento durante décadas. Historicamente, os genes foram frequentemente testadas sequencialmente, um gene / exão de cada vez, com a identificação de uma mutação que conduz ao fim da sequência de teste. O advento de NGS tem permitido uma abordagem menos tendencioso para sequenciar vários genes associados com muitos cancros em paralelo que conduzem à identificação de múltiplas mutações que estão associados com neoplasia. A utilidade clínica de NGS para a detecção de mutações somáticas no cancro é cada vez mais evidente. De fato, a análise baseada em NGS de amostras de tumor representa um novo paradigma que desafia os testes genéticos tradicional, único, mas a utilidade clínica é muito clara. Laboratórios clínicos têm hoje a oportunidade excitante para se casar com a validação do método cuidadoso e interpretação do teste com a aplicação desta poderosa tecnologia.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Os autores gostariam de agradecer a ajuda de Daniel selvagem para a leitura do manuscrito e assistência na produção.
Materials
| Genomic DNA ScreenTape | Agilent Technology | 5067-5365 | |
| Genomic DNA Reagents | Agilent Technology | 5067-5366 | |
| High Sensitivity D1000 ScreenTape | Agilent Technology | 5067-5584 | |
| High Sensitivity D1000 Reagents | Agilent Technology | 5067-5585 | |
| TapeStation 2200 | Agilent Technology | G2965A | |
| TapeStation Analysis Software | Agilent Technology | A.01.04 or higher | |
| 96-well Tube Storage Racks | Any Vendor | ||
| 15/50 ml Tube Rack | Any Vendor | ||
| 96-well Plate Rack | Any Vendor | ||
| Pipette, single-channel, 0.5–2.5 μL | Any Vendor | ||
| Pipette, single-channel, 1–10 μL | Any Vendor | ||
| Pipette, single-channel, 2–20 μL | Any Vendor | ||
| Pipette, single-channel, 10–100 μL | Any Vendor | ||
| Pipette, single-channel, 20–200 μL | Any Vendor | ||
| Pipette, single-channel, 100–1000 μL | Any Vendor | ||
| Serological Pipettor | Any Vendor | ||
| Vortexer | Any Vendor | ||
| Ice bucket | Any Vendor | ||
| Microcentrifuge (for tubes and strip tubes) | Any Vendor | ||
| Freezer, -20 °C | Any Vendor | ||
| 4 °C Refrigerator | Any Vendor | ||
| Water or Bead Bath | Any Vendor | ||
| Incubator (37 oC) | Any Vendor | ||
| Serological Pipettes, 1 mL | Any Vendor | ||
| Serological Pipettes, 5 mL | Any Vendor | ||
| Serological Pipettes, 10 mL | Any Vendor | ||
| Serological Pipettes, 25 mL | Any Vendor | ||
| Gloves | Any Vendor | ||
| Razor Blades/Scaples | Any Vendor | ||
| KimWipes | Any Vendor | ||
| 15 mL Conical Tube | Any Vendor | ||
| 50 mL Conical Tube | Any Vendor | ||
| Paper Towels | Any Vendor | ||
| 200 proof Ethanol | Any Vendor | Store in Flammable Cabinet | |
| 2-Propanol (Isopropanol) | Any Vendor | Store in Flammable Cabinet | |
| 25ml Reservoirs | Any Vendor | ||
| 10N NaOH | Any Vendor | ||
| Pipette, 8-channel, 1–10 μL | Any Vendor | ||
| Pipette, 8-channel, 10–100 μL | Any Vendor | ||
| Pipette, 8-channel, 20–300 μL | Any Vendor | ||
| Ice Bucket | Any Vendor | ||
| Water Squirt Bottle | Any Vendor | ||
| Alcohol Squirt Bottle | Any Vendor | ||
| Lens Cleaning Paper | Any Vendor | ||
| Plates, 96-well PCR, Semi-Skirted | Any Vendor | ||
| Tube strips, 8-well, 0.2 mL | Any Vendor | ||
| Agencourt AMPure XP Beads | Beckman Coulter | A63881 | |
| BioShake IQ or 3000-T elm | Bulldog Bio/Q.Instruments | 1808-0506/ 1808-0517 | |
| DropPlate96 S – LabChipDS | Caliper | 128876 | |
| DropPlate96 D – LabChipDS | Caliper | 132848 | |
| DropSense96 | Caliper (Trinean) | ||
| DropQuant Software | Caliper (Trinean) | ||
| Plate Sealing Film | Denville | B1212-5S | |
| Aluminum Seal Foil | Denville | B1212-6S | |
| Nuclease-Free, Pure Water System | EMD Millipore | ||
| 5424 centrifuge | Eppendorf | 22621408 | |
| 5804R centrifuge | Eppendorf | 22623508 | Both 15 ml tube and plate rotators, preferably a centrifuge that can go up to 2,500 x g. |
| Safe-Lock Tube 1.5 mL, Natural | Eppendorf | 22431021 | |
| 5 mL Tube, DNA LoBind Tube | Eppendorf | 30108310 | |
| 5430R Centrifuge | Eppendorf | 022620645 | Any plate rotator centrifuge will work |
| Hybex Microsample Incubator | Fisher Scientific | 1057-30-0 | |
| Hybex 0.2 mL Tube Block | Fisher Scientific | 1057-31-0 | |
| TruSeq Amplicon – Cancer Panel | Illumina | FC-130-1008 | 96 reactions |
| TruSeq Custom Amplicon | Illumina | PE-940-1011 | 96 reactions |
| TruSeq Custom Amplicon Index Kit | Illumina | FC-130-1003 | 96 Indices, 384 Samples |
| MiSeq Reagent Kit v3, 500 Cycles | Illumina | MS-102-3003 | |
| MiSeq Reagent Kit v2, 300 Cycles | Illumina | MS-102-2002 | |
| MiSeq Reagent Kit v2, 500 Cycles | Illumina | MS-102-2003 | |
| Experiment Manager | Illumina | 1.3 or higher | |
| MiSeq Reporter | Illumina | 2.0 or higher | |
| Sequencing Analysis Viewer | Illumina | 1.8 or higher | |
| TruSeq Index Plate Fixture and Collar Kit | Illumina | FC-130-1007 | |
| MiSeq v2 | Illumina | SY-410-1003 | |
| TruSeq Custom Amplicon Filter Plate | Illumina | FC-130-1006 | |
| Index Adapter Replacement Caps | Illumina | 11294657 | |
| Qubit 2.0 | Invitrogen | Q32866 | |
| Qubit 0.5 ml Tubes | Invitrogen | Q32856 | |
| Qubit dsDNA Broad Range Assay Kit | Invitrogen | Q32853 | |
| DynaMa6-96 Magnetic Stand, Side Skirted | Invitrogen | 120.27 | |
| GeneAmp PCR System 9700 (gold/silver block) | Life Technologies | N8050200 | |
| Gentra Puregene Blood Kit | Qiagen | 158489 | |
| Deparaffinization Solution (16ml) | Qiagen | 19093 | |
| Buffer ATL (4x50ml) | Qiagen | 939011 | |
| Protein Precipitation Solution (50 ml) | Qiagen | 158910 | |
| DNA Hydration Solution (100ml) | Qiagen | 158914 | |
| Glycogen Solution (500 μl) | Qiagen | 158930 | |
| Qiagen Proteinase K | Qiagen | 19133 | |
| Rnase (5ml) | Qiagen | 158924 | |
| Nuclease-Free Water (10 x 50 ml) | Qiagen | 129114 | |
| Pestles | USA Scientific | 1415-5390 | |
| TipOne RPT 10 ul elongated filter pipet tips in sterilized racks, 10 racks of 96 tips (960 tips). | USA Scientific | 1180-3810 | |
| TipOne RPT 100 ul natural, beveled filter pipet tips in sterilized racks, 10 racks of 96 tips (960 tips) | USA Scientific | 1180-1840 | |
| TipOne RPT 200 μl natural, beveled filter pipet tips in racks, sterilized racks, 10 racks of 96 tips (960 tips) | USA Scientific | 1180-8810 | |
| TipOne RPT 20 μl natural, beveled filter pipet tips in racks, sterilized racks, 10 racks of 96 tips (960 tips) | USA Scientific | 1180-1810 | |
| TipOne RPT 1000 μl natural, graduated XL filter pipet tips in | USA Scientific | 1182-1830 |
References
- Gerlinger, M., et al. Intratumor heterogeneity and branched evolution revealed by multiregion sequencing. N Engl J Med. 366 (10), 883-892 (2012).
- Campbell, P. J., et al. The patterns and dynamics of genomic instability in metastatic pancreatic cancer. Nature. 467 (7319), 1109-1113 (2010).
- Ding, L., et al. Clonal evolution in relapsed acute myeloid leukaemia revealed by whole-genome sequencing. Nature. 481 (7382), 506-509 (2012).
- Frampton, G. M., et al. Development and validation of a clinical cancer genomic profiling test based on massively parallel DNA sequencing. Nature Biotechnol. 31 (11), 1023-1031 (2013).
- Patel, J. P., et al. Prognostic relevance of integrated genetic profiling in acute myeloid leukemia. N Engl J Med. 366 (12), 1079-1089 (2012).
- Forbes, S. A., et al. COSMIC (the Catalogue of Somatic Mutations in Cancer ): a resource to investigate acquired mutations in human cancer. Nucleic Acids Res. 38 (Database Issue), 652-657 (2010).
- Shih, A. H., Abdel-wahab, O., Patel, J. P., Levine, R. L. The role of mutations in epigenetic regulators in myeloid malignancies. Nat Rev Cancer. 12 (9), 599-612 (2012).
- Liersch, R., Müller-Tidow, C., Berdel, W. E., Krug, U. Prognostic factors for acute myeloid leukaemia in adults – biological significance and clinical use. Br J Haematol. 165 (1), 17-38 (2014).
- Bacher, U., Schnittger, S., Haferlach, T. Molecular genetics in acute myeloid leukemia. Curr Opin Oncol. 22 (6), 646-655 (2010).
- Subramanian, J., Govindan, R. Lung cancer in "Never-smokers": a unique entity. Oncology (Williston Park). 24 (1), 29-35 (2010).
- Sakashita, S., Sakashita, M., Tsao, M. S. Genes and pathology of non-small cell lung carcinoma. Semin Oncol. 41 (1), 28-39 (2014).
- Arcila, M. E., Chaft, J. E., Nafa, K. Prevalence clinicopathologic associations, and molecular spectrum of ERBB2 (HER2) tyrosine kinase mutations in lung adenocarcinomas. Clin Cancer Res. 18 (18), (2012).
- Gandhi, L., et al. Phase I study of neratinib in combination with temsirolimus in patients with human epidermal growth factor receptor 2-dependent and other solid tumors. J Clin Oncol. 32 (2), 68-75 (2014).
- Sheikhha, M. H., Awan, A., Tobal, K., Liu Yin, J. A. Prognostic significance of FLT3 ITD and D835 mutations in AML patients. Hematol J. 4 (1), 41-46 (2003).
- Mazières, J., et al. Lung cancer that harbors an HER2 mutation epidemiologic characteristics and therapeutic perspectives. J Clin Oncol. 31 (16), 1-8 (2014).
- Robinson, J. T., et al. Integrative Genomics Viewer. Nat Biotechnol. 29 (1), 495-500 (2011).
- Forbes, S. A., et al. COSMIC: exploring the world’s knowledge of somatic mutations in human cancer. Nucleic Acids Res. 43 (Database issue), D805-D811 (2014).
- Daber, R., Sukhadia, S., Morrissette, J. J. Understanding the limitations of next generation sequencing informatics, an approach to clinical pipeline validation using artificial data sets. Cancer Genetics. 206 (12), 441-448 (2013).
- Haraksingh, R. R., et al. Genome-Wide Mapping of Copy Number Variation in Humans: Comparative Analysis of High Resolution Array Platforms. PLoS ONE. 6 (11), e27859 (2011).
- de Leeuw, N., et al. SNP Array Analysis in Constitutional and Cancer Genome Diagnostics – Copy Number Variants, Genotyping and Quality Control. Cytogenet Genome Res. 135 (3-4), 212-221 (2011).

