Nästa generations sekvense för detektion av vilken talan Mutationer i fast och flytande tumörer
Summary
This manuscript describes clinical protocols for two next-generation sequencing panels. One panel interrogates hematologic malignancies while the other panel targets genes commonly mutated in solid tumors. Molecular classification of driver mutations in human malignancies offers valuable prognostic and predictive information.
Abstract
As our understanding of the driver mutations necessary for initiation and progression of cancers improves, we gain critical information on how specific molecular profiles of a tumor may predict responsiveness to therapeutic agents or provide knowledge about prognosis. At our institution a tumor genotyping program was established as part of routine clinical care, screening both hematologic and solid tumors for a wide spectrum of mutations using two next-generation sequencing (NGS) panels: a custom, 33 gene hematological malignancies panel for use with peripheral blood and bone marrow, and a commercially produced solid tumor panel for use with formalin-fixed paraffin-embedded tissue that targets 47 genes commonly mutated in cancer. Our workflow includes a pathologist review of the biopsy to ensure there is adequate amount of tumor for the assay followed by customized DNA extraction is performed on the specimen. Quality control of the specimen includes steps for quantity, quality and integrity and only after the extracted DNA passes these metrics an amplicon library is generated and sequenced. The resulting data is analyzed through an in-house bioinformatics pipeline and the variants are reviewed and interpreted for pathogenicity. Here we provide a snapshot of the utility of each panel using two clinical cases to provide insight into how a well-designed NGS workflow can contribute to optimizing clinical outcomes.
Introduction
Nästa generations sekvensering (NGS) of Clinical Oncology prover har blivit mer allmänt tillgängliga under de senaste åren som växande vetenskaplig litteratur pekar på vikten av att identifiera inriktnings genetiska förändringar och prediktiva / prognostiska molekylära markörer. Multi-gen panelen analyserar och hela exome sekvense studier i både epitelceller 1,2 och hematologiska maligniteter 3 har stelnat begreppet tumör heterogenitet och klonal utveckling som sjukdomen fortskrider och återfall. Dessutom, till skillnad från konkurrerande tekniker såsom polymerase chain reaction (PCR) eller Sanger-sekvensering, kan NGS identifiera de flesta genomiska förändringar i alla kliniskt relevanta cancergener i en enda analys 4.
Centrum för personlig diagnostik ursprungligen lanserades med två kliniska NGS paneler, en anpassad Hematologisk Panel (Heme-NGS Panelen) och en off-the-shelf Cancer Panel för FFPE prover (Solid-NGS Panel) (se <strong> Figur 1). Dessa paneler täcker kliniskt relevanta eller höga räntor regioner i utvalda gener; inte alla gener eller exoner är helt täckta. Amplikoner genereras av probhybridisering följt av förlängning och ligering. De riktade regioner förstärks ytterligare med hjälp av PCR med Universal Dubbel-indexerade primers, vilket gör att upp till 96 prover som skall samlas för sekvensering.
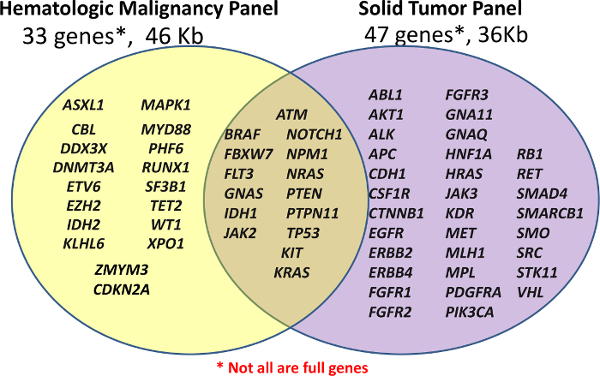
Figur 1:. Förteckning över gener som omfattas av paneler Bibliotek förberedelse utförs med hjälp av antingen anpassade Hematologisk Panel (Heme-NGS panel) av 33 gener eller off-the-shelf Amplicon Cancer Panel (Solid-NGS) av 47 gener. Inte alla av de gener eller exoner täcks fullt ut, eftersom vissa amplikoner kan bara täcka vissa hotspots. Klicka här för att se en större version av denna siffra. </ A>
Innehållet för Heme-NGS Panel härrör från flera källor, men kretsar kring 16 gener muterade i akut myeloisk leukemi (AML) som tidigare beskrivits som visar en hög nivå av klinisk användbarhet 5. Solid-NGS Panel tillverkas kommersiellt med de riktade regioner baserade på vanliga muterade gener i cancer som redovisas i katalogen av somatiska mutationer i cancer (COSMIC) databas 6.
Flera viktiga steg karakterisera den totala arbetsflödet för kliniska NGS. Efter läkaren beställer testet bestämmer en patolog lämplighet provet efter analys för tumör procent och provvolym. I vår institution, kräver vi åtminstone 10% tumör på grund av bakgrundssekvense felprocenten ( "brus") av den teknik och effektivitet målinriktad strategi. Om vävnaden är tillräcklig för testning, är genomiskt DNA extraheras. Detta DNA utsätts därefter för kvalitetskontroll multipla (QC) steg. Om DNA passerar QC är en amplikon library genereras och sekvenserades. Den resulterande data analyseras genom ett internt bioinformatik pipeline. Efter bioinformatik analys, är varianter manuellt granskas och tolkas för patogenicitet före införlivande i en klinisk rapport. Nedan beskriver vi två fall som gick igenom denna rigorösa arbetsflöde och slutligen ledde till förändringar i klinisk behandling.
Fall 1 – akut myeloisk leukemi
En benmärgsbiopsi från patient A var diagnostisk för AML, utan mognad. Cytogenetiska studier sändes på benmärgs provet och visade en normal kvinnlig karyotyp. Det fanns 95% cirkulerande blast närvarande, så en perifert blodprov skickades för personlig diagnostiska tester på Heme-NGS Panelen.
Akut myeloisk leukemi (AML) är en hematologisk malignitet av myeloid härkomst av vita blodkroppar. detekteringenav genmutationer i AML har blivit allt viktigare för prognos och behandling, med återkommande genmutationer anses vara viktiga i patogenesen och prognos 7. Mutationer i NPM1 och CEBPA har förknippats med en gynnsam prognostisk risk medan interna tandemdubbleringar (ITD) i FLT3 har förknippats med en mindre positivt resultat 8. En växande mängd bevis stöder en patogen roll för dessa och andra mutationer i AML 9.
Fall 2 – lungadenokarcinom
En biopsi av en vänster supraklavikulära massa från patient B visade lung adenocarcinom. Biopsimaterial från formalinfixerade paraffininbäddade (FFPE) lymfkörtel massa sändes för genomisk test (Solid-NGS Panel) som rullar / lockar med mer än 50% tumör, för att avgöra om en mutation var närvarande för riktad terapeutisk intervention.
Lung Cancer är den främsta orsaken till cancerrelaterad dödlighet i USA och är uppdelad i två huvudtyper, icke-småcellig lungcancer (NSCLC) och småcellig lungcancer (SCLC). NSCLC kan vidare definieras som antingen adenokarcinom eller skivepitelkarcinom, baserat på histologi av lesionen. Lungadenokarcinom är den vanligaste subtypen av lungcancer, sett i både rökare och icke-rökare, och är den vanligaste formen av lungcancer för icke-rökare 10. Molekylära studier av lung adenocarcinom har identifierat mutation i flera onkogener 11. De vanligaste förare mutationer som identifierats hos rökare är mutationer i KRAS och BRAF. De vanligaste mutationer i icke-rökare är mutationer i EGFR, och omarrangemang som omfattar generna ALK, RET och ROS1. Lungtumörer har beskrivits med en i-ram exon 20 insättning i genen ErbB2 (HER2 / neu). Den vanligaste abnormitet i HER2 / neu är en förstärkning av detta lokus i bröstcancer som en målinriktad terapi är tillgänglig (trastuzumab: en humaniserad monoklonal antikropp mot HER2 / neu). HER2 / neu exon 20 insättning som observeras i 2-4% av lung adenocarcimomas 12 har visat partiell respons på kombinationsbehandling med HER2 / neu och mTOR-hämmare (neratinib och temsirolimus, respektive) 13.
Protocol
Representative Results
Discussion
Eftersom de två NGS tester som beskrivs i detta manuskript erbjuds kliniskt, är den viktigaste praktiska övervägande kvalitetskontroll. Specifikt måste nära hänsyn tas till kvaliteten och kvantiteten av extraherat DNA. Detta är särskilt viktigt för FFPE prover som ofta starkt nedbrutet med variabel DNA avkastning. En isopropanolutfällning metod utvecklades för att maximera DNA utbyte från FFPE prover såsom kolonnbaserade metoder befanns ibland leda till DNA-klippning med begränsade elueringsvolymer. Därför är de flesta av den tid då ett prov ger alltför låg koncentration eller är alltför förstörd för analysen, är det mest troligt på grund av vävnads storlek, typ, eller fixering och inte utvinningsprocessen. För blod / benmärgsprover, om det finns ett utdrag fel, är det oftast på grund av att ett prov är hemodilute (dvs inte har tillräckligt antal vita blod eller tumörceller i det oavgjort) eller cellgifter avlägsnas.
. Nt "> Under validering, bör inrättas cutoffs för acceptans av DNA-kvalitet och kvantitet Den rekommenderade ingång 100-250 ng används ofta i analysen, men om DNA-kvaliteten är bra, då lägre ingångs mängder kan vara framgångsrik. Dessutom, om DNA-kvaliteten är dålig (dvs., är mängden av amplifierbara DNA mindre än 100 till 250 ng) då högre mängder ingångs kan förbättra kvaliteten på sekvenseringsresultaten (eftersom mängden amplifierbara DNA kommer att nå den rekommenderade ingång) . Metrics för DNA-kvalitet och kvantitet bör tillämpas på varje prov innan avancera DNA i biblioteket förberedelse. Dessa prover i en "gråzon" (se figur 2) ska köras vid bedömning av laboratoriechefen eller utsedd. för närvarande det bästa sätt att förutsäga om DNA inte kommer att fungera väl under sekvensering är att utföra en qPCR baserad analys som gör det möjligt för kvantifiering och kvalitetsbedömning av ingångs DNA. Detta tillvägagångssätt behandlar bioavailabbilitet av olika stora fragment i provet, genom amplifiering av olika stora fragment (t.ex. 100 bp, 150 bp, 200 bp och 300 bp) och jämförelser utbyte.För närvarande, bibliotek förberedelse innebär ett stort antal manuella steg där en felsteg på en av flera tidpunkter kan orsaka biblioteket för att antingen misslyckas eller vara av dålig kvalitet. Den mikroflödes gelanalys är den enda QC steg för att kontrollera ett bibliotek prep fråga innan sekvensering. Följaktligen finns det flera viktiga steg där extra mindfulness kan öka sannolikheten för en framgångsrik reaktion. Det är absolut nödvändigt för att garantera den korrekta provet och oligonukleotid pool användes för varje prov. Säkerställa och korrekt inspelning att varje prov innehåller en av 96 unika kombinationer av dubbla index PCR primerpar minskar risken för ett prov blandning upp. Dessutom är det viktigt att se till filterplattan (FPU) dränerar korrekt; om den inte dränera lämpligt detta kan orsaka att Technsion-ligeringssteget av biblioteket förberedelse för att utföra suboptimalt och leda till dålig kvalitet sekvenseringsdata. Efter biblioteks QC, är det viktigt att se till att de LNB1 pärlorna fullständigt återsuspenderas och att LNB1 / LNA1 lösningen blandas väl innan den läggs till proverna som koncentrationen av denna blandning används för att bestämma molariteten av biblioteket. Slutligen, om pärlan elueringssteget leder till en suboptimal mängd bibliotek eluering av pärlorna det kommer att minska klusterdensitet och möjligen orsaka biblioteket för att inte få tillräcklig genomsnittlig täckning. Omvänt kommer ett överskott av bibliotek leda till sämre kvalitet läser. Därför är det viktigt att vara konsekvent i pärlan baserade normalisering steg för att säkerställa en optimal sammanslagning och klustring av biblioteken på sequencer.
Förutom bibliotek förberedelse, är det viktigt att validera en bioinformatik pipeline som kommer att ge korrekta mutations samtal från den råa, de-multiplexering fastq filer. Att välja enanpassad lösning kan vara tidskrävande eftersom det finns många open source och kommersiellt tillgängliga Skenorna, variant ringer och NGS programpaket som man skulle behöva gå igenom. Anpassade algoritmer måste vara utformade för att extrahera viktiga resultatstatistik, identifiera unika återkommande mutationer som gäckat mest open source-verktyg, och bestämma antalet kopior status över varje loci. Under valideringsprocessen av en bioinformatik pipeline, är det viktigt att fastställa de rapporterings cutoffs för varianter som uppfyller eller överträffar både ett djup på minst täckning efter kvalitet filtrering (t.ex. minst 250 läsningar) och en minimi allel frekvens (t.ex. 4 %). Eftersom detta är en multiplex amplikon-baserad analys, är det viktigt att bestämma den minsta medeldjup av täckning (t.ex. 1,000x) att biblioteket måste uppnå för att kunna få den utförande amplikon lägsta till minsta djup läser. Dessutom den multiplexerade analysens natur gör cause av mål effekter och dessa "artefakter" måste upptäckas och helt kontrollerats innan lansering. En annan viktig begränsning till den beskrivna analysen är ett behov av prover för att innehålla mer än 10% tumör i syfte att uppnå den validerade minimi allelfrekvensen.
Detekteringen av låg frekvens, 1%, FLT3 infogningar finns bevis för att manuell granskning fortfarande är önskvärt i denna process. Även med en allel frekvens cut-off på 5%, några viktiga mutationer kanske missade och därmed manuell granskning kommer att vara avgörande för att fastställa dessa varianter. För FLT3-ITD är visuell inspektion av exon 14 utfördes för alla AML-patienter för att säkerställa en låg nivå eller stor insättning / dubbel inte gå obemärkt förbi. Dessutom HER2 exon 20 insättningar som är allmänt intill primersekvensen behöver manuellt ingripande. Trots att en robust bioinformatik rörledning, kan vissa varianter gå förbises vilket är precis den typ av har en hård snittoff för de flesta statistik som nämns ovan. Bättre bioinformatik skulle behövas för att lindra detta problem, liksom bättre biblioteks beredning och / eller sekvensering metoder, eftersom det är mer fördelaktigt att ha data av god kvalitet vid ännu lägre cutoffs som innehåller färre artefakter och falska positiva.
Detektering och tolkning av allelfrekvenser kan vara svårt på grund av svårigheten i tumör procentuell bestämning och amplifiering förspänningen hos vissa regioner av genomet. Dessutom kan allelfrekvenser över 50% detekteras, såsom observeras i fallet 2. Detta tolkas som en förlust av heterozygositet (LOH) händelse, antingen på grund av förlust av den normala allelen, vilket leder till den uppenbara ökningen av mutant läser, en förstärkningen för den mutanta allelen (t.ex., 2-mutant och en normal kopia) eller andra mekanismer. Dessa mekanismer kan belysas genom utnyttjande array jämförande genomisk hybridisering (aCGH 19) och / eller en SNP genotyping array. 20.
De nuvarande mål anrikningsmetoder förlitar sig på heldags förfaranden för antingen ineffektiva hybrid capture eller multiplexerade PCR-tekniker som resulterar i att det behövs mer sekvense täckning av ett enda prov och mer utanför mål sekvense läser. Ytterligare applikationer för NGS molekylär onkologi förväntas inom en snar framtid kommer att omfatta lättare biblioteksframställningsmetoder som kan vara helt automatiserade och kunna bearbeta prover med mycket små mängder av input-DNA (dvs mindre än 1 ng) samt prover med mycket försämras DNA. För att möta dessa utmaningar, kommer de flesta metoder förmodligen vara PCR-baserad, antingen är en flerstegs PCR strategi eller ett massivt parallella singleplex PCR strategi. Dessutom har molekylstreckkodning av individuella amplikoner visats dramatiskt minska bakgrundssekvense buller och kommer att möjliggöra testning av prover med lägre proportioner av tumörceller för att uppnå lägre allelfrekvensema och gå mot fånga circulating tumörceller.
Detektion av sjukdomsassocierade mutationer i cancerprover har varit standardbehandling för årtionden. Historiskt sett gener ofta testas sekventiellt, en gen / exon i taget, med identifiering av en mutation som leder till slutet av testsekvens. Tillkomsten av NGS har möjliggjort en mindre partisk inställning till sekvense flera gener associerade med många cancerformer parallellt leder till identifiering av flera mutationer som är förknippade med neoplasi. Den kliniska användbarheten av NGS för detektion av somatiska mutationer vid cancer är allt tydligare. I själva verket, NGS baserad analys av tumörprover representerar ett nytt paradigm som utmanar traditionell, enkel gentestning, men den kliniska nyttan är mycket tydlig. Kliniska laboratorier idag har spännande möjlighet att gifta noggrann metodvalidering och testa tolkning med tillämpningen av denna kraftfulla teknik.
Divulgations
The authors have nothing to disclose.
Acknowledgements
Författarna vill tacka för den hjälp av Daniel Wild för läsning av manuskriptet och hjälp i produktionen.
Materials
| Genomic DNA ScreenTape | Agilent Technology | 5067-5365 | |
| Genomic DNA Reagents | Agilent Technology | 5067-5366 | |
| High Sensitivity D1000 ScreenTape | Agilent Technology | 5067-5584 | |
| High Sensitivity D1000 Reagents | Agilent Technology | 5067-5585 | |
| TapeStation 2200 | Agilent Technology | G2965A | |
| TapeStation Analysis Software | Agilent Technology | A.01.04 or higher | |
| 96-well Tube Storage Racks | Any Vendor | ||
| 15/50 ml Tube Rack | Any Vendor | ||
| 96-well Plate Rack | Any Vendor | ||
| Pipette, single-channel, 0.5–2.5 μL | Any Vendor | ||
| Pipette, single-channel, 1–10 μL | Any Vendor | ||
| Pipette, single-channel, 2–20 μL | Any Vendor | ||
| Pipette, single-channel, 10–100 μL | Any Vendor | ||
| Pipette, single-channel, 20–200 μL | Any Vendor | ||
| Pipette, single-channel, 100–1000 μL | Any Vendor | ||
| Serological Pipettor | Any Vendor | ||
| Vortexer | Any Vendor | ||
| Ice bucket | Any Vendor | ||
| Microcentrifuge (for tubes and strip tubes) | Any Vendor | ||
| Freezer, -20 °C | Any Vendor | ||
| 4 °C Refrigerator | Any Vendor | ||
| Water or Bead Bath | Any Vendor | ||
| Incubator (37 oC) | Any Vendor | ||
| Serological Pipettes, 1 mL | Any Vendor | ||
| Serological Pipettes, 5 mL | Any Vendor | ||
| Serological Pipettes, 10 mL | Any Vendor | ||
| Serological Pipettes, 25 mL | Any Vendor | ||
| Gloves | Any Vendor | ||
| Razor Blades/Scaples | Any Vendor | ||
| KimWipes | Any Vendor | ||
| 15 mL Conical Tube | Any Vendor | ||
| 50 mL Conical Tube | Any Vendor | ||
| Paper Towels | Any Vendor | ||
| 200 proof Ethanol | Any Vendor | Store in Flammable Cabinet | |
| 2-Propanol (Isopropanol) | Any Vendor | Store in Flammable Cabinet | |
| 25ml Reservoirs | Any Vendor | ||
| 10N NaOH | Any Vendor | ||
| Pipette, 8-channel, 1–10 μL | Any Vendor | ||
| Pipette, 8-channel, 10–100 μL | Any Vendor | ||
| Pipette, 8-channel, 20–300 μL | Any Vendor | ||
| Ice Bucket | Any Vendor | ||
| Water Squirt Bottle | Any Vendor | ||
| Alcohol Squirt Bottle | Any Vendor | ||
| Lens Cleaning Paper | Any Vendor | ||
| Plates, 96-well PCR, Semi-Skirted | Any Vendor | ||
| Tube strips, 8-well, 0.2 mL | Any Vendor | ||
| Agencourt AMPure XP Beads | Beckman Coulter | A63881 | |
| BioShake IQ or 3000-T elm | Bulldog Bio/Q.Instruments | 1808-0506/ 1808-0517 | |
| DropPlate96 S – LabChipDS | Caliper | 128876 | |
| DropPlate96 D – LabChipDS | Caliper | 132848 | |
| DropSense96 | Caliper (Trinean) | ||
| DropQuant Software | Caliper (Trinean) | ||
| Plate Sealing Film | Denville | B1212-5S | |
| Aluminum Seal Foil | Denville | B1212-6S | |
| Nuclease-Free, Pure Water System | EMD Millipore | ||
| 5424 centrifuge | Eppendorf | 22621408 | |
| 5804R centrifuge | Eppendorf | 22623508 | Both 15 ml tube and plate rotators, preferably a centrifuge that can go up to 2,500 x g. |
| Safe-Lock Tube 1.5 mL, Natural | Eppendorf | 22431021 | |
| 5 mL Tube, DNA LoBind Tube | Eppendorf | 30108310 | |
| 5430R Centrifuge | Eppendorf | 022620645 | Any plate rotator centrifuge will work |
| Hybex Microsample Incubator | Fisher Scientific | 1057-30-0 | |
| Hybex 0.2 mL Tube Block | Fisher Scientific | 1057-31-0 | |
| TruSeq Amplicon – Cancer Panel | Illumina | FC-130-1008 | 96 reactions |
| TruSeq Custom Amplicon | Illumina | PE-940-1011 | 96 reactions |
| TruSeq Custom Amplicon Index Kit | Illumina | FC-130-1003 | 96 Indices, 384 Samples |
| MiSeq Reagent Kit v3, 500 Cycles | Illumina | MS-102-3003 | |
| MiSeq Reagent Kit v2, 300 Cycles | Illumina | MS-102-2002 | |
| MiSeq Reagent Kit v2, 500 Cycles | Illumina | MS-102-2003 | |
| Experiment Manager | Illumina | 1.3 or higher | |
| MiSeq Reporter | Illumina | 2.0 or higher | |
| Sequencing Analysis Viewer | Illumina | 1.8 or higher | |
| TruSeq Index Plate Fixture and Collar Kit | Illumina | FC-130-1007 | |
| MiSeq v2 | Illumina | SY-410-1003 | |
| TruSeq Custom Amplicon Filter Plate | Illumina | FC-130-1006 | |
| Index Adapter Replacement Caps | Illumina | 11294657 | |
| Qubit 2.0 | Invitrogen | Q32866 | |
| Qubit 0.5 ml Tubes | Invitrogen | Q32856 | |
| Qubit dsDNA Broad Range Assay Kit | Invitrogen | Q32853 | |
| DynaMa6-96 Magnetic Stand, Side Skirted | Invitrogen | 120.27 | |
| GeneAmp PCR System 9700 (gold/silver block) | Life Technologies | N8050200 | |
| Gentra Puregene Blood Kit | Qiagen | 158489 | |
| Deparaffinization Solution (16ml) | Qiagen | 19093 | |
| Buffer ATL (4x50ml) | Qiagen | 939011 | |
| Protein Precipitation Solution (50 ml) | Qiagen | 158910 | |
| DNA Hydration Solution (100ml) | Qiagen | 158914 | |
| Glycogen Solution (500 μl) | Qiagen | 158930 | |
| Qiagen Proteinase K | Qiagen | 19133 | |
| Rnase (5ml) | Qiagen | 158924 | |
| Nuclease-Free Water (10 x 50 ml) | Qiagen | 129114 | |
| Pestles | USA Scientific | 1415-5390 | |
| TipOne RPT 10 ul elongated filter pipet tips in sterilized racks, 10 racks of 96 tips (960 tips). | USA Scientific | 1180-3810 | |
| TipOne RPT 100 ul natural, beveled filter pipet tips in sterilized racks, 10 racks of 96 tips (960 tips) | USA Scientific | 1180-1840 | |
| TipOne RPT 200 μl natural, beveled filter pipet tips in racks, sterilized racks, 10 racks of 96 tips (960 tips) | USA Scientific | 1180-8810 | |
| TipOne RPT 20 μl natural, beveled filter pipet tips in racks, sterilized racks, 10 racks of 96 tips (960 tips) | USA Scientific | 1180-1810 | |
| TipOne RPT 1000 μl natural, graduated XL filter pipet tips in | USA Scientific | 1182-1830 |
References
- Gerlinger, M., et al. Intratumor heterogeneity and branched evolution revealed by multiregion sequencing. N Engl J Med. 366 (10), 883-892 (2012).
- Campbell, P. J., et al. The patterns and dynamics of genomic instability in metastatic pancreatic cancer. Nature. 467 (7319), 1109-1113 (2010).
- Ding, L., et al. Clonal evolution in relapsed acute myeloid leukaemia revealed by whole-genome sequencing. Nature. 481 (7382), 506-509 (2012).
- Frampton, G. M., et al. Development and validation of a clinical cancer genomic profiling test based on massively parallel DNA sequencing. Nature Biotechnol. 31 (11), 1023-1031 (2013).
- Patel, J. P., et al. Prognostic relevance of integrated genetic profiling in acute myeloid leukemia. N Engl J Med. 366 (12), 1079-1089 (2012).
- Forbes, S. A., et al. COSMIC (the Catalogue of Somatic Mutations in Cancer ): a resource to investigate acquired mutations in human cancer. Nucleic Acids Res. 38 (Database Issue), 652-657 (2010).
- Shih, A. H., Abdel-wahab, O., Patel, J. P., Levine, R. L. The role of mutations in epigenetic regulators in myeloid malignancies. Nat Rev Cancer. 12 (9), 599-612 (2012).
- Liersch, R., Müller-Tidow, C., Berdel, W. E., Krug, U. Prognostic factors for acute myeloid leukaemia in adults – biological significance and clinical use. Br J Haematol. 165 (1), 17-38 (2014).
- Bacher, U., Schnittger, S., Haferlach, T. Molecular genetics in acute myeloid leukemia. Curr Opin Oncol. 22 (6), 646-655 (2010).
- Subramanian, J., Govindan, R. Lung cancer in "Never-smokers": a unique entity. Oncology (Williston Park). 24 (1), 29-35 (2010).
- Sakashita, S., Sakashita, M., Tsao, M. S. Genes and pathology of non-small cell lung carcinoma. Semin Oncol. 41 (1), 28-39 (2014).
- Arcila, M. E., Chaft, J. E., Nafa, K. Prevalence clinicopathologic associations, and molecular spectrum of ERBB2 (HER2) tyrosine kinase mutations in lung adenocarcinomas. Clin Cancer Res. 18 (18), (2012).
- Gandhi, L., et al. Phase I study of neratinib in combination with temsirolimus in patients with human epidermal growth factor receptor 2-dependent and other solid tumors. J Clin Oncol. 32 (2), 68-75 (2014).
- Sheikhha, M. H., Awan, A., Tobal, K., Liu Yin, J. A. Prognostic significance of FLT3 ITD and D835 mutations in AML patients. Hematol J. 4 (1), 41-46 (2003).
- Mazières, J., et al. Lung cancer that harbors an HER2 mutation epidemiologic characteristics and therapeutic perspectives. J Clin Oncol. 31 (16), 1-8 (2014).
- Robinson, J. T., et al. Integrative Genomics Viewer. Nat Biotechnol. 29 (1), 495-500 (2011).
- Forbes, S. A., et al. COSMIC: exploring the world’s knowledge of somatic mutations in human cancer. Nucleic Acids Res. 43 (Database issue), D805-D811 (2014).
- Daber, R., Sukhadia, S., Morrissette, J. J. Understanding the limitations of next generation sequencing informatics, an approach to clinical pipeline validation using artificial data sets. Cancer Genetics. 206 (12), 441-448 (2013).
- Haraksingh, R. R., et al. Genome-Wide Mapping of Copy Number Variation in Humans: Comparative Analysis of High Resolution Array Platforms. PLoS ONE. 6 (11), e27859 (2011).
- de Leeuw, N., et al. SNP Array Analysis in Constitutional and Cancer Genome Diagnostics – Copy Number Variants, Genotyping and Quality Control. Cytogenet Genome Res. 135 (3-4), 212-221 (2011).

