Análise qPCRTag - A High Throughput, PCR em Tempo Real Ensaio para Sc2.0 Genotipagem
Summary
Designer chromosomes of the Synthetic Yeast Genome project, Sc2.0, can be distinguished from their native counterparts using a PCR-based genotyping assay called PCRTagging, which has a presence/absence endpoint. Here we describe a high-throughput real time PCR detection method for PCRTag genotyping.
Abstract
O Projeto Genoma fermento sintético (Sc2.0) pretende construir 16 grife cromossomas de levedura e combiná-los em uma única célula de levedura. Até à data, um cromossoma sintético, synIII 1, e um braço cromossoma sintético, synIXR 2, foram construídos e a sua função in vivo validado na ausência dos cromossomas de tipo selvagem correspondentes. Uma importante característica do modelo de cromossomas Sc2.0 é a introdução de PCRTags, que são sequências curtas, re-codificada dentro de quadros de leitura abertos (ORFs) que permitem a diferenciação dos cromossomas sintéticos dos seus homólogos de tipo selvagem. PCRTag iniciadores emparelham selectivamente, quer cromossomas de tipo selvagem ou sintéticos e a presença / ausência de cada tipo de ADN pode ser testada usando um ensaio de PCR simples. A leitura do ensaio padrão PCRTag é avaliar a presença / ausência de produtos de amplificação por electroforese em gel de agarose. No entanto, com uma densidade PCRTag amplicão média de um por 1,5 kb e agenome tamanho de ~ 12 Mb, o genoma Sc2.0 concluído irá codificar cerca de 8.000 PCRTags. Para melhorar o rendimento, temos desenvolvido um ensaio de detecção baseado em PCR em tempo real para PCRTag genotipagem que chamamos análise qPCRTag. O fluxo de trabalho especifica 500 nl reações em uma placa com múltiplas cavidades 1536, o que nos permite testar até 768 PCRTags com dois pares de primers tipo sintéticos e selvagens em um único experimento.
Introduction
Sc2.0, ou o Projeto Genoma fermento sintético ( www.syntheticyeast.org ), fixou o objetivo de projetar e construir um genoma eucariota inteiramente sintético. Usando a seqüência do genoma altamente curadoria de Saccharomyces cerevisiae 3 como ponto de partida, cada um dos cromossomos lineares dezesseis foi re-projetado para atender um conjunto de princípios de design que especificam a manutenção da aptidão de células, melhorando a estabilidade do genoma, e aumentando a flexibilidade genética. Por exemplo, elementos desestabilizadores, tais como repetições são excluídos de cromossomos Sc2.0. Todos os casos de codões de paragem TAG são re-codificada para TAA para "libertar-se 'um codão na estirpe final para a introdução de um aminoácido não geneticamente codificados. Além disso, um sistema de evolução induzível, precipitação, habilitado pelo sistema Cre-lox, permite a capacidade sem precedentes para gerar genomas derivativos com novas estruturas 4.
<p class="Jove_content"> Outro grande elemento de design no genoma Sc2.0 é a introdução de PCRTags, que servem como marcas d'água de ADN para permitir o rastreamento de DNA tipo sintético e selvagem. PCRTags são segmentos curtos, re-codificado em ORF nos cromossomos sintéticos; enquanto as sequências PCRTag diferem ao nível do ADN entre os cromossomas de tipo selvagem e sintéticos, as proteínas codificadas são idênticas em sequência de aminoácidos e assim, presumivelmente, a função. PCRTag sequências são especificamente concebidas como locais de ligação de iniciadores para facilitar a amplificação selectiva (Figura 1A). PCRTag desenho é efectuada utilizando o algoritmo 'mais diferente' em GeneDesign 5,6, dando origem a sequências sintéticas recodificados que são tipicamente ~ 60% diferente do que as sequências nativas (mínimo 33%) com temperaturas de fusão entre 58 ° C e 60 ° C e amplicão comprimentos entre 200-500 pares de bases 2. A recodificação não é permitida dentro do primeiro 100 pb de cada ORF, uma vez que estas regiões são conhecidas portêm preferências especiais em termos de uso de códon 7. Juntas, essas regras de design favorecer alto desempenho de quase todos os PCRTags sob um único conjunto de condições de PCR em que pares de primers tipo PCRTag sintéticos e selvagens exclusivamente ligam e amplificar DNA sintético e nativo, respectivamente (Figura 1B).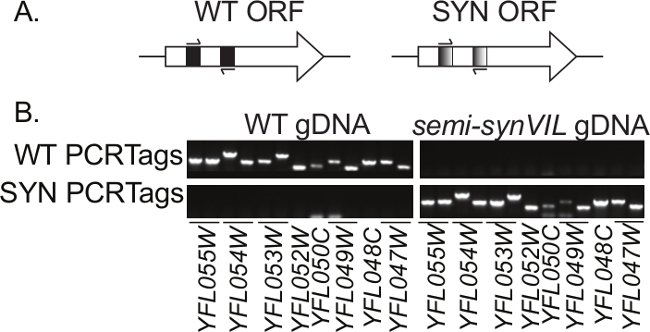
Figura 1:. PCRTag esquema (A) PCRTags são sequências dentro de quadros de leitura aberta (ORF) de genes nos cromossomas Sc2.0 recodificados. (B) sintético (SYN) e do tipo selvagem (WT) iniciadores PCRTag vincular exclusivamente e amplificar DNA genómico tipo sintético e selvagem (gDNA), respectivamente. Mostrado aqui é uma análise de um segmento de ~ 30 kb do braço esquerdo do cromossomo seis, testando treze pares de primers PCRTag usando tanto WT ou semi-synVIL2 gDNA como modelo. Em muitos casos, uma única ORF codifica mais do que um PCRTag. Presença / ausência de amplicões PCRTag é avaliada através de electroforese em gel de agarose. Amplicons PCRTag variam em tamanho de 200 pb e 500 pb. As espécies que migram mais rapidamente na parte inferior dos painéis são dimeros de iniciadores.
Análise PCRTag tem provado ser uma ferramenta importante para o conjunto de cromossomos Sc2.0. Numa experiência típica de 30-50 kb de ADN sintético, codificando 20-30 PCRTags, é transformado em células de levedura para substituir o tipo selvagem correspondente ADN 1,2,8. Análise PCRTag é então utilizado para identificar transformantes que codificam PCRTags tipo sintético, mas não selvagem abrangendo esse segmento de DNA, ou os chamados "vencedores". Geralmente é necessário testar vários transformantes para identificar "vencedores", de modo a produtividade e custo da análise PCRTag são considerações importantes. Actualmente dois cromossomas Sc2.0 foram concluídos (synIII 1 e synIXR 2), representando menos de 10% do genoma Sc2.0, altHough mais de metade dos cromossomas restantes estão actualmente em fase de síntese e montagem. A escala de análise PCRTag necessário para este projeto está rapidamente superando a capacidade de executar géis e marcar manualmente a presença de DNA sintético e ausência de DNA tipo selvagem.
Para melhorar o rendimento do ensaio PCRTag temos desenvolvido um trabalho utilizando PCR em tempo real para contornar a utilização de electroforese em gel de agarose. O fluxo de trabalho faz uso de um distribuidor de líquido para distribuir grandes quantidades de qPCR mastermix em cada poço de uma placa com múltiplas cavidades 1536, um distribuidor de líquido em nanoescala acústico para transferir ADN molde e iniciadores, e um termociclador 1536 qPCR, permitindo-nos para miniaturizar reacções a 500 nl maximizar o rendimento. Além disso análise pode ser automatizado. Este tipo de protocolo de genotipagem de alto rendimento deve ser generalizado a qualquer projecto requer uma análise de vários clones em loci múltiplos.
Protocol
Representative Results
Discussion
Incorporação de detecção em tempo real PCR para o ensaio de genotipagem PCRTag é um desenvolvimento importante para o projeto Sc2.0 pois permite significativamente maior taxa de transferência. O fluxo de trabalho anterior especificada 2,5 ul reações em 384 placas de PCR, 1,5 horas de tempo de execução ciclismo térmica, eletroforese em gel de agarose, e de anotação manual da gel.
O fluxo de trabalho apresentado aqui, chamada de análise qPCRTag, supera vários dos principais pontos de estrangulamento. Primeiro, uma corrida qPCRTag condensa 4 x 384 placas de poços em um único experimento que pode ser processado, do início ao fim (placa configurar mais tempo de execução), em cerca de uma hora. É importante notar que o custo de reagente por poço para análise qPCRTag está a par com a abordagem baseada em gel de agarose rendimento mais baixo. No entanto, por electroforese em gel de contornar e anotação manual, o fluxo de trabalho qPCRTag proporciona economias substanciais em tempo e mão de obra, que são as principais vantagens. É importante ressaltar o fluxo de trabalho é qPCRTag entirely compatível com a automatização.
Uma preocupação importante com a utilização de detecção em tempo real, como a saída do ensaio PCRTag é a taxa de falsos positivos e falsos negativos. Uma vez que os iniciadores PCRTag não foram originalmente concebidas para utilização em PCR em tempo real, espera-se que nem todos os pares de iniciadores será adequado para utilização com esta saída. Para este fim, é importante para a função e validar a especificidade de todos os pares de iniciadores PCRTag para excluir o subconjunto que não funcionam no ensaio com base em tempo real na frente. Por exemplo, cromossoma 3 PCRTag falsos positivos e negativos são a-e-grande reprodutível na dados de PCR em tempo real (Figuras 2 e 3) e estes podem ser excluídos de análises posteriores. Além disso, os pares de iniciadores conhecidos para falhar (avaliada por electroforese em gel e mostrado nas Figuras S6 e S7 de Annaluru et ai. 1) também podem ser excluídas. Isto é facilmente conseguido simplesmente excluding os pares de primers com defeito ao configurar o protocolo de transferência acústica.
Como a maioria dos ensaios de alto rendimento, temos a intenção de usar a detecção de PCRTag tempo real como uma tela principal para identificar transformantes que merecem uma validação adicional a jusante. Posteriormente, o padrão-ouro para o rastreio secundário permanecerá análise PCRTag com eletroforese em gel como a leitura. Além da aplicação da análise PCRTag para Sc2.0, combinando sistemas de manuseio de líquido nanoescala state-of-the-art com alta taxa de transferência de tecnologia PCR em tempo real permite a análise rápida e automatizada e tem potencial para impactar muitos campos. Por exemplo, este fluxo de trabalho pode ser aplicado a alta biblioteca throughput screening, diagnóstico de doenças infecciosas, análise microbiome, e genoma de edição de ponta se aproxima de tentar modificar loci múltiplos simultaneamente.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Este trabalho foi apoiado em parte pelo National Science Foundation Grant MCB-0718846 e Defesa Agência de Projetos de Pesquisa Avançada de contrato N66001-12-C-4020 (para JDB). LAM foi financiado por uma bolsa de pós-doutorado de Ciências Naturais e do Conselho de Investigação do Canadá Engenharia. A publicação deste artigo é patrocinado pela Roche.
Materials
| Yeast gDNA prep | |||
| yeast gDNA | custom | custom | template for real time PCR |
| Acid-washed glass beads (0.5mm) | Sigma | G8772 | yeast cell lysis |
| Ultrapure Phenol:Chloroform:Isoamyl Alcohol (25:24:1, v/v) | Invitrogen | 15593-031 | yeast cell lysis |
| 5432 Mixer | Eppendorf | 5432 | yeast cell lysis |
| Microcentrifuge 5417R | Eppendorf | 22621807 | yeast cell lysis |
| Qubit 3.0 Fluorometer | Life Technologies | Q33216 | gDNA quantification |
| Qubit dsDNA BR Assay Kit | Life Technologies | Q32850 | gDNA quantification |
| Labcyte 384PP plate | Labcyte | P-05525 | gDNA source plate |
| DNA Green Mastermix prep and dispensing | |||
| LightCycler 1536 DNA Green | Roche | 5573092001 | real time PCR mastermix |
| 1.5mL Microfuge Tube Holder | ARI | EST BD060314-1 | microfuge tube holder for deck of Cobra |
| LightCycler 1536 Multiwell Plate | Roche | 5358639001 | |
| Cobra liquid handling system | Art Robbins Instruments | 630-1000-10 | dispense qPCR master mix into 1536 plate |
| PCR Plate Spinner | VWR | 89184-608 | cenrifugation of 1536 plate |
| Template and primer dispensing | |||
| PCRTag primers | IDT | custom | premixed forward and reverse, [50uM] each |
| TempPlate pierceable sealing foil, sterile | USA Scientific | 2923-0110 | temporary seal for PCRTag primer plates |
| Labcyte LDV 384 well plate | Labcyte | LP-0200 | pre-mixed primer source plate |
| Echo 550 Liquid Handler | Labcyte | transfer 2.5nL drops of primer and template DNA into 1536 plate | |
| Plateloc Thermal Microplate Sealer | Agilent | G5402-90001 | heat seal for 1536 plate prior to LC1536 run |
| Clear Permanent Seal | Agilent | 24212-001 | optically clear heat seal for LC1536 multiwell plate |
| PlateLoc Roche/LightCycler 1536 Plate Stage | Agilent | G5402-20008 | can substitute ~2mm thick washers |
| Sorvall Legend XTR | Thermo Scientfic | 75-004-521 | centrifuge heat sealed 1536 plate |
| Industrial Air Compressor | Jun Air | 1795011 | to run the Echo and Heat Sealer |
| Real Time PCR | |||
| LightCycler 1536 | Roche | requires 220V outlet |
Riferimenti
- Annaluru, N., et al. Total synthesis of a functional designer eukaryotic chromosome. Science. 344 (6179), 55-58 (2014).
- Dymond, J. S., et al. Synthetic chromosome arms function in yeast and generate phenotypic diversity by design. Nature. 477 (7365), 471-476 (2011).
- Goffeau, A., et al. Life with 6000 genes. Science. 274 (5287), 546-547 (1996).
- Dymond, J., Boeke, J. The Saccharomyces cerevisiae SCRaMbLE system and genome minimization. Bioeng Bugs. 3 (3), 168-171 (2012).
- Richardson, S. M., Nunley, P. W., Yarrington, R. M., Boeke, J. D., Bader, J. S. GeneDesign 3.0 is an updated synthetic biology toolkit. Nucleic Acids Res. 38 (8), 2603-2606 (2010).
- Richardson, S. M., Liu, S., Boeke, J. D., Bader, J. S. Design-A-Gene with GeneDesign. Methods Mol Biol. 852, 235-247 (2012).
- Lajoie, M. J., et al. Probing the limits of genetic recoding in essential genes. Science. 342 (6156), 361-363 (2013).
- Jovicevic, D., Blount, B. A., Ellis, T. Total synthesis of a eukaryotic chromosome: Redesigning and SCRaMbLE-ing yeast. Bioessays. 36 (9), 855-860 (2014).
- Dymond, J. S. Preparation of genomic DNA from Saccharomyces cerevisiae. Methods Enzymol. 529, 153-160 (2013).
- Brachmann, C. B., et al. Designer deletion strains derived from Saccharomyces cerevisiae S288C: a useful set of strains and plasmids for PCR-mediated gene disruption and other applications. Yeast. 14 (2), 115-132 (1998).

