Analyse qPCRTag - un débit élevé, PCR temps réel pour Sc2.0 Génotypage
Summary
Designer chromosomes of the Synthetic Yeast Genome project, Sc2.0, can be distinguished from their native counterparts using a PCR-based genotyping assay called PCRTagging, which has a presence/absence endpoint. Here we describe a high-throughput real time PCR detection method for PCRTag genotyping.
Abstract
Le projet de génome de la levure synthétique (Sc2.0) vise à construire 16 concepteur chromosomes de levure et les combiner en une cellule de levure seule. A ce jour, un chromosome synthétique, synIII 1, et un bras de chromosome synthétique, synIXR 2, ont été construits et leur fonction in vivo validé en l'absence des chromosomes de type sauvage correspondantes. Une importante caractéristique de conception de chromosomes Sc2.0 est l'introduction de PCRTags, qui sont courtes, recodé séquences au sein des cadres de lecture ouverts (ORF) qui permettent la différenciation des chromosomes synthétiques de leurs homologues de type sauvage. PCRTag amorces hybrident sélectivement soit à des chromosomes de type sauvage ou de synthèse et la présence / absence de chaque type d'ADN peuvent être testés en utilisant un dosage PCR simple. La lecture de la norme d'essai est d'évaluer PCRTag présence / absence d'amplicons par électrophorèse sur gel d'agarose. Cependant, avec une densité de PCRTag amplicon une moyenne de 1,5 kb et par agenome taille de ~ 12 Mo, le génome de Sc2.0 complété va encoder environ 8.000 PCRTags. Pour améliorer le débit, nous avons développé un test de détection basé sur la PCR en temps réel pour le génotypage PCRTag que nous appelons analyse qPCRTag. Le flux de travail spécifie 500 réactions nl dans une plaque multipuits 1536, ce qui nous permet de tester jusqu'à 768 PCRTags avec les deux paires synthétiques et sauvages de type amorce dans une seule expérience.
Introduction
Sc2.0, ou le projet de génome de la levure synthétique ( www.syntheticyeast.org ), a fixé l'objectif de concevoir et de construire un génome eucaryote entièrement synthétique. Utilisation de la séquence du génome hautement organisée de Saccharomyces cerevisiae 3 comme point de départ, chacun des chromosomes linéaires seize a été re-conçu pour répondre à un ensemble de principes de conception qui spécifient maintien de la forme des cellules, l'amélioration de la stabilité du génome, et accroître la flexibilité génétique. Par exemple, des éléments de déstabilisation tels que les répétitions sont supprimés de chromosomes Sc2.0. Toutes les instances de codons stop TAG sont re-codés pour TAA à 'libérer' un codon dans la souche finale pour l'introduction d'un acide aminé non génétiquement codé. En outre, un système d'évolution inductible, Scramble, permis par le système Cre-lox, permet une capacité sans précédent de générer des génomes dérivés avec 4 nouvelles structures.
<p class="Jove_content"> Un autre élément de conception majeur dans le génome de Sc2.0 est l'introduction de PCRTags, qui servent de filigranes ADN pour permettre le suivi de l'ADN de type synthétique et sauvage. PCRTags sont courts segments de re-codées dans les ORF sur les chromosomes synthétiques; tandis que les séquences PCRTag diffèrent au niveau de l'ADN entre les chromosomes de type sauvage et synthétiques, les protéines codées sont identiques à la séquence d'acides aminés et, par conséquent, probablement, de la fonction. PCRTag séquences sont spécifiquement conçus comme des sites de liaison d'amorces pour faciliter l'amplification sélective (Figure 1A). PCRTag conception est effectuée en utilisant l'algorithme "le plus différent» dans GeneDesign 5,6, donnant recodé séquences synthétiques qui sont typiquement ~ 60% différente de celle des séquences natives (minimum 33%) avec des températures de fusion entre 58 ° C et 60 ° C et amplicon longueurs entre 200-500 paires de base 2. Recodage est interdit dans le premier 100 pb de chaque ORF, que ces régions sont connues pouravoir des préférences particulières en termes d'utilisation de codon 7. Ensemble, ces règles de conception favorisent haute performance de presque tous PCRTags sous un seul ensemble de conditions de PCR lequel paires d'amorces de type PCRTag synthétiques et sauvages se lient exclusivement et amplifier l'ADN synthétique et native, respectivement (figure 1B).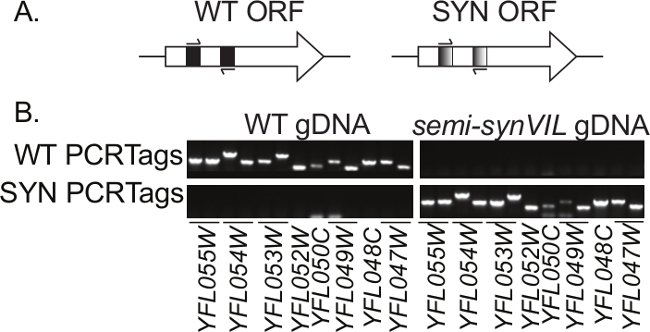
Figure 1:. PCRTag schématique (A) PCRTags sont séquences à l'intérieur des cadres de lecture ouverts (ORF) des gènes sur les chromosomes Sc2.0 recodées. (B) synthétique (SYN) et de type sauvage (WT) amorces PCRTag lient exclusivement et amplifient l'ADN génomique de type synthétique et sauvage (ADNg), respectivement. On voit ici une analyse d'un segment du bras gauche du chromosome six ~ 30 kb, tester treize PCRTag paires d'amorces utilisant soit WT ou semi-synVIL2 gDNA comme modèle. Dans de nombreux cas, une seule ORF code plus d'un PCRTag. Présence / absence d'amplicons PCRTag est évaluée par électrophorèse sur gel d'agarose. Amplicons PCRTag varient en taille de 200 pb à 500 pb. Les espèces migrant plus vite dans le bas des panneaux sont des dimères d'amorces.
PCRTag analyse a prouvé être un outil important dans l'assemblage de chromosomes Sc2.0. Dans une expérience typique de 30 à 50 kb de l'ADN synthétique, codant pour 20 à 30 PCRTags, est transformé dans des cellules de levure pour remplacer le type sauvage correspondant ADN 1,2,8. PCRTag analyse est ensuite utilisée pour identifier les transformants qui codent synthétiques mais pas sauvage PCRTags de type couvrant ce segment d'ADN, ou soi-disant «gagnants». Il est généralement nécessaire de tester plusieurs transformants d'identifier les «gagnants», de sorte débit et le coût de l'analyse PCRTag sont des considérations importantes. Actuellement deux chromosomes Sc2.0 ont été réalisées (une synIII et synIXR 2), ce qui représente moins de 10% du génome de Sc2.0, altHough plus de la moitié des chromosomes restants sont actuellement en cours de synthèse et l'assemblage. L'échelle d'analyse PCRTag requis pour ce projet est plus rapide que rapide la possibilité d'exécuter manuellement les gels et marquer la présence de l'ADN synthétique et l'absence d'ADN de type sauvage.
Pour améliorer le débit de l'essai PCRTag nous avons développé un flux de travail en utilisant la PCR en temps réel pour contourner l'utilisation d'une électrophorèse sur gel d'agarose. Le workflow permet l'utilisation d'un distributeur de liquide en vrac à distribuer qPCR mastermix dans chaque puits d'une plaque multipuits 1536, un distributeur de liquide acoustique échelle nanométrique pour transférer l'ADN de matrice et des amorces, et un cycleur thermique 1536 qPCR, ce qui nous permet de miniaturiser les réactions à 500 nl et maximiser le débit. En outre l'analyse peut être automatisée. Ce type de haut débit protocole de génotypage devrait être généralisables à tout projet nécessitant l'analyse de nombreux clones à des loci multiples.
Protocol
Representative Results
Discussion
Incorporation de détection de PCR en temps réel dans le test de génotypage PCRTag est un développement important pour le projet Sc2.0 car elle permet un débit nettement plus élevé. Le workflow précédente spécifié 2,5 réactions ul dans des plaques de 384 puits PCR, 1,5 heures de temps d'exécution de cyclage thermique, électrophorèse sur gel d'agarose, et d'annotation manuelle du gel.
Le flux de travail présenté ici, appelée analyse qPCRTag, surmonte plusieurs principaux goulets d'étranglement. Tout d'abord, une course de qPCRTag condense 4 x 384 plaques ainsi dans une expérience unique qui peut être traitée, début à la fin (plaque mis en place, plus le temps de fonctionner), en une heure environ. Il est important de noter que le coût de réactif par puits pour l'analyse qPCRTag est à égalité avec l'approche inférieure à base de gel agarose-débit. Cependant, en contournant électrophorèse sur gel et annotation manuelle, le workflow qPCRTag offre des économies substantielles de temps et de travail, qui sont les principaux avantages. Surtout le flux de travail est en qPCRTagtièrement compatible avec l'automatisation.
Une préoccupation majeure avec l'utilisation de la détection réelle de temps que la sortie de l'essai PCRTag est le taux de faux positifs et de faux négatifs. Depuis les amorces PCRTag ont pas été initialement conçus pour une utilisation dans la PCR en temps réel, il est prévu que tous les couples d'amorces seront appropriées pour une utilisation avec cette sortie. A cette fin, il est important de valider la fonction et la spécificité de toutes les paires d'amorces PCRTag à exclure le sous-ensemble qui ne fonctionne pas dans le dosage réel basé sur le temps à l'avant. Par exemple, chromosome 3 PCRTag faux positifs et négatifs sont des sous-grand-et reproductible dans la PCR en temps réel des données (figures 2 et 3) et ceux-ci peuvent être exclues d'autres analyses. En outre, les paires d'amorces connues à l'échec (évalués par électrophorèse sur gel et présentés dans les figures S6 et S7 de Annaluru et al. 1) peuvent également être exclus. Ceci est facilement accompli simplement excluding les paires d'amorces défectueux lors de la mise en place du protocole de transfert acoustique.
Comme la plupart des analyses à haut débit, nous avons l'intention d'utiliser la détection de PCRTag en temps réel comme un écran primaire pour identifier les transformants qui méritent une validation supplémentaire en aval. Par la suite, l'étalon-or pour le dépistage secondaire restera analyse PCRTag avec électrophorèse sur gel que la lecture. Au-delà de l'application de l'analyse PCRTag pour Sc2.0, combinant des systèmes de manipulation des liquides à l'échelle nanométrique état-of-the-art avec la technologie haut débit de PCR en temps réel permet une analyse rapide et automatisé et a le potentiel d'avoir un impact de nombreux domaines. Par exemple, ce flux de travail pourrait être appliquée à de dépistage grande capacité de la bibliothèque, le diagnostic des maladies infectieuses, l'analyse sur le microbiome, et pointe édition du génome approches tentant de modifier loci multiples simultanément.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Ce travail a été financé en partie par la National Science Foundation Grant MCB-0718846 et de la Défense Advanced Research Projects Agency contrat N66001-12-C-4020 (à JDB). LAM a été financé par une bourse de recherche postdoctorale du Conseil de recherches en génie du Canada en sciences naturelles et. Publication de cet article est sponsorisé par Roche.
Materials
| Yeast gDNA prep | |||
| yeast gDNA | custom | custom | template for real time PCR |
| Acid-washed glass beads (0.5mm) | Sigma | G8772 | yeast cell lysis |
| Ultrapure Phenol:Chloroform:Isoamyl Alcohol (25:24:1, v/v) | Invitrogen | 15593-031 | yeast cell lysis |
| 5432 Mixer | Eppendorf | 5432 | yeast cell lysis |
| Microcentrifuge 5417R | Eppendorf | 22621807 | yeast cell lysis |
| Qubit 3.0 Fluorometer | Life Technologies | Q33216 | gDNA quantification |
| Qubit dsDNA BR Assay Kit | Life Technologies | Q32850 | gDNA quantification |
| Labcyte 384PP plate | Labcyte | P-05525 | gDNA source plate |
| DNA Green Mastermix prep and dispensing | |||
| LightCycler 1536 DNA Green | Roche | 5573092001 | real time PCR mastermix |
| 1.5mL Microfuge Tube Holder | ARI | EST BD060314-1 | microfuge tube holder for deck of Cobra |
| LightCycler 1536 Multiwell Plate | Roche | 5358639001 | |
| Cobra liquid handling system | Art Robbins Instruments | 630-1000-10 | dispense qPCR master mix into 1536 plate |
| PCR Plate Spinner | VWR | 89184-608 | cenrifugation of 1536 plate |
| Template and primer dispensing | |||
| PCRTag primers | IDT | custom | premixed forward and reverse, [50uM] each |
| TempPlate pierceable sealing foil, sterile | USA Scientific | 2923-0110 | temporary seal for PCRTag primer plates |
| Labcyte LDV 384 well plate | Labcyte | LP-0200 | pre-mixed primer source plate |
| Echo 550 Liquid Handler | Labcyte | transfer 2.5nL drops of primer and template DNA into 1536 plate | |
| Plateloc Thermal Microplate Sealer | Agilent | G5402-90001 | heat seal for 1536 plate prior to LC1536 run |
| Clear Permanent Seal | Agilent | 24212-001 | optically clear heat seal for LC1536 multiwell plate |
| PlateLoc Roche/LightCycler 1536 Plate Stage | Agilent | G5402-20008 | can substitute ~2mm thick washers |
| Sorvall Legend XTR | Thermo Scientfic | 75-004-521 | centrifuge heat sealed 1536 plate |
| Industrial Air Compressor | Jun Air | 1795011 | to run the Echo and Heat Sealer |
| Real Time PCR | |||
| LightCycler 1536 | Roche | requires 220V outlet |
Riferimenti
- Annaluru, N., et al. Total synthesis of a functional designer eukaryotic chromosome. Science. 344 (6179), 55-58 (2014).
- Dymond, J. S., et al. Synthetic chromosome arms function in yeast and generate phenotypic diversity by design. Nature. 477 (7365), 471-476 (2011).
- Goffeau, A., et al. Life with 6000 genes. Science. 274 (5287), 546-547 (1996).
- Dymond, J., Boeke, J. The Saccharomyces cerevisiae SCRaMbLE system and genome minimization. Bioeng Bugs. 3 (3), 168-171 (2012).
- Richardson, S. M., Nunley, P. W., Yarrington, R. M., Boeke, J. D., Bader, J. S. GeneDesign 3.0 is an updated synthetic biology toolkit. Nucleic Acids Res. 38 (8), 2603-2606 (2010).
- Richardson, S. M., Liu, S., Boeke, J. D., Bader, J. S. Design-A-Gene with GeneDesign. Methods Mol Biol. 852, 235-247 (2012).
- Lajoie, M. J., et al. Probing the limits of genetic recoding in essential genes. Science. 342 (6156), 361-363 (2013).
- Jovicevic, D., Blount, B. A., Ellis, T. Total synthesis of a eukaryotic chromosome: Redesigning and SCRaMbLE-ing yeast. Bioessays. 36 (9), 855-860 (2014).
- Dymond, J. S. Preparation of genomic DNA from Saccharomyces cerevisiae. Methods Enzymol. 529, 153-160 (2013).
- Brachmann, C. B., et al. Designer deletion strains derived from Saccharomyces cerevisiae S288C: a useful set of strains and plasmids for PCR-mediated gene disruption and other applications. Yeast. 14 (2), 115-132 (1998).

