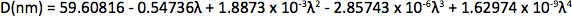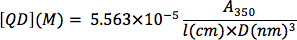Compact Quantum Dots voor Single-molecule Imaging
Summary
We beschrijven de bereiding van colloïdale quantum dots met minimale hydrodynamische grootte voor single-molecule fluorescentie beeldvorming. Vergeleken met conventionele quantum dots, deze nanodeeltjes zijn vergelijkbaar in grootte met globulaire eiwitten en zijn geoptimaliseerd voor single-molecule helderheid, stabiliteit tegen afbraak en resistentie tegen specifieke binding aan eiwitten en cellen.
Abstract
Single-molecule beeldvorming is een belangrijk instrument voor het begrijpen van de mechanismen van biomoleculaire functie en voor het visualiseren van de ruimtelijke en temporele heterogeniteit van moleculaire gedrag dat cellulaire biologie 1 tot 4 ten grondslag liggen. Om een afzonderlijk beeld molecuul van belang, is het meestal geconjugeerd aan een fluorescerend label (kleurstof, eiwit, kraal, of quantum dot) en waargenomen met epifluorescentie of totale interne reflectiefluorescentie (TIRF) microscopie. Terwijl kleurstoffen en fluorescerende eiwitten zijn de steunpilaar van de fluorescentie beeldvorming voor tientallen jaren, hun fluorescentie is niet stabiel onder hoge foton flux die nodig zijn om individuele moleculen te observeren, waardoor slechts een paar seconden van observatie voordat volledig verlies van signaal. Latex kralen en kleurstof gemerkte korrels een verbeterde signaal stabiliteit, maar ten koste van grotere hydrodynamische grootte drastisch, wat nadelig kan veranderen de verspreiding en het gedrag van de moleculen onder studie.
ntent "> Quantum dots (QD's) bieden een evenwicht tussen deze twee problematische regimes. Deze nanodeeltjes zijn samengesteld uit halfgeleidende materialen en kunnen worden gemanipuleerd met een hydrodynamisch compacte afmetingen met een uitzonderlijke weerstand tegen fotodegradatie 5. Aldus in de afgelopen jaren QDs zijn geweest bij zodat op lange termijn observatie van complexe macromoleculaire gedrag op de single molecule-niveau. Maar deze deeltjes hebben nog steeds is gebleken dat een verminderde diffusie vertonen in drukke moleculaire omgevingen, zoals de mobiele cytoplasma en de neuronale synaptische spleet, waar hun maten zijn nog steeds te groot 4,6 , 7.Onlangs hebben wij de engineering van de kernen en oppervlaktecoatings van QDs voor minimale hydrodynamische grootte, terwijl de afweging van offsets aan colloïdale stabiliteit, fotostabiliteit, helderheid en niet-specifieke binding dat het nut van compacte QDs hebben gehinderd in het verleden 8,9. Het doel van dit artikel is aan te tonende synthese, modificatie en karakterisering van deze geoptimaliseerde nanokristallen, bestaande uit een gelegeerd Hg x Cd 1-x Se kern bekleed met een isolerende Cd y Zn 1-y S shell, verder bekleed met een multidentaat ligand polymeer gemodificeerd met korte polyethyleenglycol ( PEG) ketens (figuur 1). Vergeleken met conventionele CdSe nanokristallen, Hg x Cd 1-x Se legeringen bieden meer kwantumopbrengsten van fluorescentie, fluorescentie bij rode en nabij-infrarode golflengten verbeterde signaal-ruisverhouding in cellen en excitatie bij niet-cytotoxische zichtbare golflengten. Multidentaat polymeer coatings binden aan het oppervlak nanokristallen in een gesloten vlakke conformatie om hydrodynamische grootte minimaliseren en PEG neutraliseert de oppervlaktelading om niet-specifieke binding minimaliseren cellen en biomoleculen. Het eindresultaat is een helder fluorescerende nanokristallen met emissie tussen 550 tot 800 nm en een totale hydrodynamische afmeting in de buurt 12 nm. Dit is in de same groottebereik zoveel oplosbare globulaire eiwitten in cellen en aanzienlijk kleiner dan conventionele PEGylated QDs (25-35 nm).
Protocol
Representative Results
Discussion
Vergeleken met conventionele CdSe quantum dots, kan ternaire legering Hg x Cd 1-x Se nanokristallen worden afgestemd in grootte en fluorescentie golflengte onafhankelijk van elkaar. De grootte wordt eerst geselecteerd tijdens de synthese van CdSe nanokristallen kernen en de fluorescentie golflengte wordt gekozen in een secundaire kwik kationuitwisselingsstap, die niet wezenlijk veranderen de nanokristallen maat 9. Het is belangrijk om de gezuiverde Hg x Cd 1-x Se na…
Disclosures
The authors have nothing to disclose.
Acknowledgements
De auteurs willen graag Dr Hong Yi danken aan de Emory University Geïntegreerde Microscopy Core voor elektronenmicroscopie beeldvorming. Dit werk werd gesponsord door NIH subsidie (PN2EY018244, R01 CA108468, U54CA119338, en 1K99CA154006-01).
Materials
| Name of the reagent | Company | Catalogue number | Comments (optional) |
| Selenium | Sigma-Aldrich | 229865 | |
| Tri-n-octylphosphine | Strem | 15-6655 | 97% pure, unstable in air |
| Cadmium oxide | Sigma-Aldrich | 202894 | Highly toxic: use caution |
| Tetradecylphosphonic acid | PCI Synthesis | 4671-75-4 | |
| Octadecene | Alfa Aesar | L11004 | Technical grade |
| Hexadecylamine | Sigma-Aldrich | H7408 | |
| Diphenylphosphine | Sigma-Aldrich | 252964 | Pyrophoric |
| Mercury acetate | Sigma-Aldrich | 456012 | Highly toxic: use caution |
| 1-Octanethiol | Sigma-Aldrich | 471836 | Strong odor |
| Oleic acid | Sigma-Aldrich | W281506 | |
| Zinc acetate | Alfa Aesar | 35792 | |
| Cadmium acetate hydrate | Sigma-Aldrich | 229490 | Highly toxic: use caution |
| Oleylamine | Fisher Scientific | AC12954 | Unstable in air |
| Sulfur | Sigma-Aldrich | 344621 | |
| Trioctylphosphine oxide | Strem | 15-6661 | 99% |
| Pyridine | VWR | EM-PX2012-6 | Anhydrous |
| Thioglycerol | Sigma-Aldrich | M1753 | Strong odor |
| Triethylamine | Sigma-Aldrich | 471283 | Anhydrous |
| Dialysis tubing | Spectrum Labs | 131342 | 20 kDa cutoff |
| Centrifugal filter | Millipore | UFC801024 | 10 kDa cutoff |
| Monoamino-PEG | Rapp Polymere | 12 750-2 | 750 Da |
| DMTMM, 4-(4,6-Dimethoxy-1,3,5-triazin-2-yl)-4-methylmorpholinium chloride hydrate | Alfa Aesar | H26333 | |
| AKTAprime Plus Chromatography System | GE HealthCare | ||
| Superose 6 10/300 GL chromatography column | GE HealthCare | 17-5172-01 | |
| Agarose, OmniPur | VWR | EM-2120 | |
Appendix Synthesis of mercury octanethiolate: Slowly add a methanol solution of mercury acetate (1 eq.) to a stirring solution of 1-octanethiol (3 eq.) and potassium hydroxide (3 eq.) in methanol at room temperature. Isolate the mercury(II) octanethiolate precipitate via filtration, wash two times with methanol and once with ether, and then dry under vacuum. Synthesis of multidentate polymer: Dissolve polyacrylic acid (1 g, 1,773 Da) in 25 ml dimethylformamide (DMF) in a 150 ml three-necked flask and bubble with argon for 30 min. Add an anhydrous solution of cysteamine (374 mg, 4.87 mmol) in 10 ml DMF. At room temperature with vigorous stirring, slowly add anhydrous diisopropylcarbodiimide (DIC, 736 mg, 5.83 mmol) over 30 min, followed by triethylamine (170 μl, 1.22 mmol), and allow the reaction to proceed for 72 hr at 60 °C. Add mercaptoethanol (501 mg, 6.41 mmol) to quench the reaction, and stir for 2 hr at room temperature. Remove DMF via rotary evaporation and isolate the polymer with the addition of a 2:1 mixture of ice-cold acetone:chloroform, followed by centrifugation. Dissolve the polymer in ~5 ml anhydrous DMF, filter, precipitate again with diethyl ether, and repeat. Dry the product under vacuum and store under argon. Determination of CdSe core diameter: From the UV-Vis absorption spectrum determine the wavelength of the first exciton peak (λ, in nm), which is the longest-wavelength peak (e.g. roughly 498 nm for CdSe in Figure 2a), and use the sizing curve of Mulvaney and coworkers 12:
Determination of CdSe nanocrystal concentration: From a background-subtracted UV-Vis spectrum of an optically clear solution of CdSe nanocrystals, determine the absorption at 350 nm wavelength. Serial dilutions can be used to determine if the optical absorption is within the linear range of Beer’s Law. The nanocrystal concentration (QD, in M) can be determined by plugging in the nanocrystal diameter (D, in nm), the optical absorption value (A3sa), and the cuvette path length (l, in cm) into the following equation from the empirical correlation of Bawendi and coworkers 13:
|
References
- Toprak, E., Selvin, P. R. New fluorescent tools for watching nanometer-scale conformational changes of single molecules. Annu. Rev. Biophys. Biomol. Struct. 36, 349-369 (2007).
- Joo, C., Balci, H., Ishitsuka, Y., Buranachai, C., Ha, T. J. Advances in single molecule fluorescence methods for molecular biology. Annu. Rev. Biochem. 77, 51-76 (2008).
- Pinaud, F., Clarke, S., Sittner, A., Dahan, M. Probing cellular events, one quantum dot at a time. Nat. Method. 7, 275-285 (2010).
- Smith, A. M., Wen, M. M., Nie, S. M. Imaging dynamic cellular events with quantum dots. Biochemist. 32, 12-17 (2010).
- Smith, A. M., Duan, H. W., Mohs, A. M., Nie, S. M. Bioconjugated quantum dots for in vivo molecular and cellular imaging. Adv. Drug Deliv. Rev. 60, 1226-1240 (2008).
- Smith, A. M., Nie, S. M. Next-generation quantum dots. Nature Biotech. 27, 732-733 (2009).
- Groc, L., Lafourcade, M., Heine, M., Renner, M., Racine, V., Sibarita, J. -. B., Lounis, B., Choquet, D., Cognet, L. Single trafficking of neurotransmitter receptor: comparison between single-molecule/quantum dot strategies. J. Neurosci. 27, 12433-12437 (2007).
- Smith, A. M., Nie, S. M. Minimizing the hydrodynamic size of quantum dots with multifunctional multidentate polymer ligands. J. Am. Chem. Soc. 130, 11278-11279 (2008).
- Smith, A. M., Nie, S. M. Bright and compact alloyed quantum dots with broadly tunable near-infrared absorption and fluorescence spectra through mercury cation exchange. J. Am. Chem. Soc. 133, 24-26 (2011).
- Shriver, D. F., Drezdzon, M. A. . The Manipulation of Air-Sensitive Compounds. , (1986).
- Errington, R. J. . Advanced Practical Inorganic and Metalorganic Chemistry. , (1997).
- Jasieniak, J., Smith, L., van Embden, J., Mulvaney, P., Califano, M. Re-examination of the size-dependent absorption properties of CdSe quantum dots. J. Phys. Chem. C. 113, 19468-19474 (2009).
- Leatherdale, C. A., Woo, W. K., Mikulec, F. V., Bawendi, M. G. On the absorption cross section of CdSe nanocrystal quantum dots. J. Phys. Chem. B. 106, 7619-7622 (2002).
- Smith, A. M., Mohs, A. M., Nie, S. M. Tuning the optical and electronic properties of colloidal nanocrystals by lattice strain. Nature Nanotech. 4, 56-63 (2009).
- Demas, J. N., Crosby, G. A. The measurement of photoluminescence quantum yields. A review. J. Phys. Chem. 75, 991-1024 (1971).
- Van Embden, J., Jasieniak, J., Mulvaney, P. Mapping the optical properties of CdSe/CdS heterostructure nanocrystals: the effects of core size and shell thickness. J. Am. Chem. Soc. 131, 14299-14309 (2009).
- Smith, A. M., Duan, H. W., Rhyner, M. N., Ruan, G., Nie, S. M. A systematic examination of surface coatings on the optical and chemical properties of semiconductor quantum dots. Phys. Chem. Chem. Phys. 8, 3895-3903 (2006).
- Zhang, X., Mohandessi, S., Miller, L. W., Snee, P. T. Efficient functionalization of aqueous CdSe/ZnS nanocrystals using small-molecule chemical activators. Chem. Comm. 47, 3532-3534 (2011).
- Bucio, L., Souza, V., Albores, A., Sierra, A., Chavez, E., Carabez, A., Guiterrez-Ruiz, M. C. Cadmium and mercury toxicity in a human fetal hepatic cell line (WRL-68 cells). Toxicol. 102, 285-299 (1995).
- Han, S. G., Castranova, V., Vallyathan, V. J. Comparative cytotoxicity of cadmium and mercury in a human bronchial epithelial cell line (BEAS-2B) and its role in oxidative stress and induction of heat shock protein 70. J. Toxicol. Environ. Health Part A. 70, 852-860 (2007).
- Strubelt, O., Kremer, J., Tilse, A., Keogh, J., Pentz, R. J. Comparative studies on the toxicity of mercury, cadmium, and copper toward the isolated perfused rat liver. J. Toxicol. Environ. Health Part A. 47, 267-283 (1996).