Bir Klinik öncesi Hasta Türetilmiş Tümör Roman Anti-Kanser Tedaviler Soruşturma Xenograftlarında Modeli Geliştirilmesi ve Bakımı
Summary
deri altı klinik öncesi modelde hasta kaynaklı tümörler kullanarak yeni tedavilerin, öngörü biyomarker keşif ve ilaca dirençli yolların etkinliğini incelemek için mükemmel bir yoldur. Bu model, ilaç geliştirme sürecinde, klinik araştırma önce birçok yeni anti-kanser terapisi kaderini belirlemede önemlidir.
Abstract
Patient derived tumor xenograft (PDTX) models provide a necessary platform in facilitating anti-cancer drug development prior to human trials. Human tumor pieces are injected subcutaneously into athymic nude mice (immunocompromised, T cell deficient) to create a bank of tumors and subsequently are passaged into different generations of mice in order to maintain these tumors from patients. Importantly, cellular heterogeneity of the original tumor is closely emulated in this model, which provides a more clinically relevant model for evaluation of drug efficacy studies (single agent and combination), biomarker analysis, resistant pathways and cancer stem cell biology. Some limitations of the PDTX model include the replacement of the human stroma with mouse stroma after the first generation in mice, inability to investigate treatment effects on metastasis due to the subcutaneous injections of the tumors, and the lack of evaluation of immunotherapies due to the use of immunocompromised mice. However, even with these limitations, the PDTX model provides a powerful preclinical platform in the drug discovery process.
Introduction
Kolorektal kanser (KRK) Amerika Birleşik Devletleri'nde kanser ölümlerinin önemli bir katkıda bulunmaktadır. 2015 yılında, 49.700 ölüm 1 ile ÇHS tahmini 132.700 yeni vaka vardı. lokalize hastalığı olan hastalarda prognoz mükemmel olmasına rağmen, ilerlemiş hastalığı olan hastalarda yeni tedavilerin geliştirilmesinde bu önemli bir öncelik haline kötü sonuçlar var. bakım kemoterapötik rejimleri ve bu hastalığa karşı konuşlandırılmış yeni biyolojik standart olmasına rağmen, genel sağkalım sadece bir artan bir artış olmuştur. Buna göre, bu hastalıkta tümör büyümesini kolaylaştırmak katılan sürücü yollarının anlaşılmasında önemli bir çaba var. Kanser Genom Atlas ağ en son sayıda ana CRC bozukluğunun karıştığı ve bunlar yolları belirlemiştir: WNT, fosfoinositid 3-kinaz (PI3K), RAS, dönüştürücü büyüme faktörü-β (TGF-β) ve TP53 2. Birlikte, araştırmalar ot nitelendirdiCRC büyümeyi güçlendirir onun yollar önemli ölçüde bu hasta popülasyonunda 3-5 sağkalımı iyileştirmeyi amaçlayan yeni tedavilerin gelişimini başlatmıştır. Onkoloji ilaç geliştirilmesinde kullanılması klinik öncesi modellerde, bu yeni bileşiklerin klinik aktivite tahmin bu süreçte temel olmuştur.
Çeşitli klinik öncesi modellerde ilaç geliştirme sürecinde kullanılmıştır. Preklinik transgenik hayvan modelleri ve hücre hatları büyük ölçüde insan tümörlerinin karmaşıklığını yansıtacak şekilde yetersizlik, yeni onkoloji tedavilerin klinik etkinliğini belirlemede başarısız olmuştur ölümsüzleştirdi göz önüne alındığında, hasta kaynaklı tümör xenograft (PDTX) modelleri kurulmuştur. Bu modelin en büyük avantajı, tümör heterojen bozulmadan kalır ve yakından menşeli hastanın tümör 6-9 moleküler özelliklerini ve klonalite yansıtır olmasıdır. PDTX modelleri, in vivo bir harikalarını sağlamakpreklinik bir platform yeni ajanlar, ilaç direnci yolları, kombinasyonel stratejileri ve kanser kök hücre biyolojisi 10 incelemek için.
PDTX işleminin genel bir bakış, Şekil 1 'de gösterilmiştir. Bu klinik başlar onların aşırı tümör dokusunun bir kısmı, bu araştırma için kullanılan izin vermek için hasta rızası. Sonraki, ameliyatta tümörün bir parça bir patolog tarafından hasılat ve araştırma personeline taşınacak ortama koydu. Bunun hemen ardından, tümör bölümü, küçük parçalar halinde kesilmiş ve deri altından bağışıklık yetersizliği olan farelere transplante edilir. Tümör büyüdükçe sonra, tümör 10 muhafaza edilmesi amacıyla farelerin farklı kuşaklar içine geçirilerek edilir. Tipik haliyle, F3 nesil sonra tümör yeni bileşikler ve / veya kombinasyonel tedaviler değerlendirilir tedavi çalışmaya genişletilebilir. Kullanan Next Gen Dizi (exome Seq, RNA Seq ve SNP dizi) potansiyel öngörü biyolojik belirteçler keşfetmek vardırBelirli bir tedaviden fayda görebilecek hastaların seçiminde yardımcı ed.
1) tek ajan olarak veya kombinasyon halinde yeni tedavilerin etkinliğini değerlendirmek ve 2) öncesinde klinik araştırma duyarlılık veya direnç tahmin biyobelirteçlerini tespit: PDTX modelleri kullanarak kapsayıcı hedefleri şunlardır. Bu yazıda, bir CRC PDTX bankanın başlatılması ve bakım metodoloji sağlamak ve ilaç geliştirme keşfi bu modelin avantajları ve sınırlamaları sağlamaktadır.
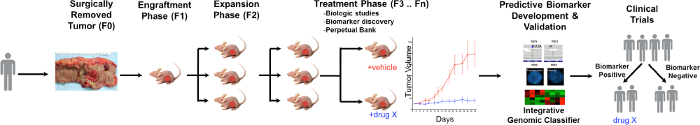
CRC PDTX Modeli Protokolü Şekil 1. Genel. Hasta edilen tümör cerrahisi alınan hemen deri altından atimik çıplak farelere enjekte edilir. Tümör büyüdükçe kez sonraki nesillere genişletilir ve sonuçta tedavi çalışmaları için genişletilir. Tedavi RESPOnses değerlendirilir ve tahmini biyomarkerlar. Hasta seçiminde yardımcı olabilir belirlenmiştir , bu rakamın büyük halini görmek için lütfen buraya tıklayınız.
Protocol
Representative Results
Discussion
PDTX ilaç keşif platformu yeni bileşiklerin klinik etkinliğini öngörmede güvenilmez diğer preklinik modellerin eksiklikleri gelişmiş bir model sunuyor. Önemli olarak, bu modelde, tümörler, biyolojik olarak kararlı, metastatik potansiyelini korumak ve kuşaktan içindeki ilaç tepki gösterirler. Bu modelde, hastanın türevli tümörler, atimik çıplak farelere enjekte geçişli ve daha sonra tedavi değerlendirmesinde kullanılır. içeren başarılı bir PDTX banka için birkaç kritik adımlar vardır:…
Disclosures
The authors have nothing to disclose.
Acknowledgements
This work was supported by grant 1R01CA152303-01.
Materials
| RPMI or DMEM | Corning | 10-040-CV | |
| Penicillin-Streptomycin | Corning | 30-002-CI | |
| Non-essential Amino Acids | Corning | 25-025-CI | |
| Fetal Bovine Serum | Corning | 35-010-CV | Thaw in -4 °C, then activate for 30 minutes at 60 °C water bath |
| CPT blood tube | BD vacutainer | 362761 | |
| Microcentrifuge tube | Surelock | A-7002 | |
| Phospate-Buffered Saline | Corning | 21-040-CV | |
| Cyrogenic vials | Cyroking | C0732901 | |
| Plastic tumor cutting dish | Trueline | TR4001 | |
| Scissors | Roboz | RS-5881 | |
| Forceps | Roboz | RS-5135 | |
| Matrigel (gelatinous protein mixture) | Corning | 354234 | Store at -20 or -80 °C, then thaw on ice, do not leave at room temperature |
| 10% Formalin cups | Protocol | 032-059 | |
| Liquid Nitrogen Dewar Storage | Thermolyne | CY50900 | |
| Portable liquid nitrogen dewar | Nalgene | 4150-2000 | |
| Dimethyl Sulfoxide | Fischer | 67-68-5 | |
| Freezing container: Mr Frosty | Nalgene | 5100-0001 | |
| Isopropyl Alcohol | Decon | 64-17-5 | |
| Trocars | Innovative Research of America | MP-182 | |
| Anesthesia machine | Patterson Veterinary | none | |
| Anesthesia box | Patterson Veterinary | none | |
| Isoflurane | Vet one | 1038005 | |
| F-Air Canister | Bickford Omnicon | 80120 | |
| Meloxicam | Vet one | 5182-90C | |
| Calipers | Fowler | 54-100-167 | |
| Weight scale | Ohaus | Scout Pro SP601 |
References
- Siegel, R. L., Miller, K. D., Jemal, A. Cancer statistics. 2015. CA Cancer J Clin. 65 (1), 5-29 (2015).
- . Comprehensive molecular characterization of human colon and rectal cancer. Nature. 487 (7407), 330-337 (2012).
- Arcaroli, J. J., et al. Tumours with elevated levels of the Notch and Wnt pathways exhibit efficacy to PF-03084014, a gamma-secretase inhibitor, in a preclinical colorectal explant model. Br J Cancer. 109 (3), 667-675 (2013).
- Hubbard, J., Grothey, A. Antiangiogenesis agents in colorectal cancer. Curr Opin Oncol. 22 (4), 374-380 (2010).
- van Es, J. H., et al. Notch/gamma-secretase inhibition turns proliferative cells in intestinal crypts and adenomas into goblet cells. Nature. 435 (7044), 959-963 (2005).
- Cassidy, J. W., Caldas, C., Bruna, A. Maintaining Tumor Heterogeneity in Patient-Derived Tumor Xenografts. Cancer Res. 75 (15), 2963-2968 (2015).
- Jin, K., et al. Patient-derived human tumour tissue xenografts in immunodeficient mice: a systematic review. Clin Transl Oncol. 12 (7), 473-480 (2010).
- Julien, S., et al. Characterization of a large panel of patient-derived tumor xenografts representing the clinical heterogeneity of human colorectal cancer. Clin Cancer Res. 18 (19), 5314-5328 (2012).
- Siolas, D., Hannon, G. J. Patient-derived tumor xenografts: transforming clinical samples into mouse models. Cancer Res. 73 (17), 5315-5319 (2013).
- Tentler, J. J., et al. Patient-derived tumour xenografts as models for oncology drug development. Nat Rev Clin Oncol. 9 (6), 338-350 (2012).
- Carson, F. L. . Histotechnology: A Self-Assessment Workbook. , (1996).
- Arcaroli, J. J., et al. Common PIK3CA mutants and a novel 3′ UTR mutation are associated with increased sensitivity to saracatinib. Clin Cancer Res. 18 (9), 2704-2714 (2012).
- Arcaroli, J. J., et al. A NOTCH1 gene copy number gain is a prognostic indicator of worse survival and a predictive biomarker to a Notch1 targeting antibody in colorectal cancer. Int J Cancer. 138 (1), 195-205 (2016).
- Arcaroli, J. J., et al. Gene array and fluorescence in situ hybridization biomarkers of activity of saracatinib (AZD0530), a Src inhibitor, in a preclinical model of colorectal cancer. Clin Cancer Res. 16 (16), 4165-4177 (2010).
- Lieu, C. H., et al. Antitumor activity of a potent MEK inhibitor, TAK-733, against colorectal cancer cell lines and patient derived xenografts. Oncotarget. 6 (33), 34561-34572 (2015).
- Pitts, T. M., et al. Association of the epithelial-to-mesenchymal transition phenotype with responsiveness to the p21-activated kinase inhibitor, PF-3758309, in colon cancer models. Front Pharmacol. 4, 35 (2013).
- Song, E. K., et al. Potent antitumor activity of cabozantinib, a c-MET and VEGFR2 inhibitor, in a colorectal cancer patient-derived tumor explant model. Int J Cancer. 136 (8), 1967-1975 (2015).
- Tentler, J. J., et al. Identification of predictive markers of response to the MEK1/2 inhibitor selumetinib (AZD6244) in K-ras-mutated colorectal cancer. Mol Cancer Ther. 9 (12), 3351-3362 (2010).
- Bardelli, A., et al. Amplification of the MET receptor drives resistance to anti-EGFR therapies in colorectal cancer. Cancer Discov. 3 (6), 658-673 (2013).
- Bertotti, A., et al. A molecularly annotated platform of patient-derived xenografts (“xenopatients”) identifies HER2 as an effective therapeutic target in cetuximab-resistant colorectal cancer. Cancer Discov. 1 (6), 508-523 (2011).
- Davis, S. L., et al. Combined inhibition of MEK and Aurora A kinase in KRAS/PIK3CA double-mutant colorectal cancer models. Front Pharmacol. 6, 120 (2015).
- Morelli, M. P., et al. Preclinical activity of the rational combination of selumetinib (AZD6244) in combination with vorinostat in KRAS-mutant colorectal cancer models. Clin Cancer Res. 18 (4), 1051-1062 (2012).
- Pitts, T. M., et al. Dual pharmacological targeting of the MAP kinase and PI3K/mTOR pathway in preclinical models of colorectal cancer. PLoS One. 9 (11), e113037 (2014).
- Spreafico, A., et al. Rational combination of a MEK inhibitor, selumetinib, and the Wnt/calcium pathway modulator, cyclosporin A, in preclinical models of colorectal cancer. Clin Cancer Res. 19 (15), 4149-4162 (2013).
- Arcaroli, J. J., et al. ALDH+ tumor-initiating cells exhibiting gain in NOTCH1 gene copy number have enhanced regrowth sensitivity to a gamma-secretase inhibitor and irinotecan in colorectal cancer. Mol Oncol. 6 (3), 370-381 (2012).
- Hoey, T., et al. DLL4 blockade inhibits tumor growth and reduces tumor-initiating cell frequency. Cell Stem Cell. 5 (2), 168-177 (2009).
- Ikebuchi, F., et al. Dissociation of c-Met phosphotyrosine sites in human cells in response to mouse hepatocyte growth factor but not human hepatocyte growth factor: the possible roles of different amino acids in different species. Cell Biochem Funct. 31 (4), 298-304 (2013).
- Zhang, Y. W., et al. Enhanced growth of human met-expressing xenografts in a new strain of immunocompromised mice transgenic for human hepatocyte growth factor/scatter factor. Oncogene. 24 (1), 101-106 (2005).

