通过微透析 实现 高通量蛋白质结晶
Summary
所提出的协议描述了一种使用96孔高通量透析板筛选蛋白质结晶条件和晶体生长的简单方法。透析管用于微晶的大规模生长也用于连续晶体学和MicroED应用。
Abstract
在分子水平上了解蛋白质等大分子的结构-功能关系对于生物医学和现代药物发现至关重要。迄今为止,X射线晶体学仍然是以原子分辨率求解三维蛋白质结构的最成功方法。随着连续晶体学的最新进展,无论是使用X射线自由电子激光器(XFEL)还是同步加速器光源,蛋白质晶体学已经发展到下一个前沿领域,其中获取时间分辨数据的能力为室温下生物分子的行为提供了重要的机理见解。该协议描述了一种简单的高通量(HTP)工作流程,用于通过使用96孔透析板筛选结晶条件。这些板遵循生物分子筛选协会(SBS)标准,可以使用任何标准结晶实验室轻松设置。一旦确定了最佳条件,就可以使用透析器生产大量晶体(数百个微晶)。为了验证这种方法的稳健性和多功能性,结晶了四种不同的蛋白质,包括两种膜蛋白。
Introduction
在上个世纪,X射线晶体学在阐明和理解生物大分子的结构 – 功能范式方面至关重要。迄今为止,它仍然是阐明许多独特不同蛋白质的原子分辨率结构的最成功方法之一,这些蛋白质对于细胞生物化学,医学和早期药物发现的基本理解至关重要1,2。然而,蛋白质结晶仍然是研究许多蛋白质靶标的瓶颈,特别是膜蛋白和大蛋白质复合物3。因此,由于采用劳动密集型的试错法,蛋白质结晶几乎总是被认为是一门艺术4,5,6。
沉淀剂通常以高浓度添加到蛋白质溶液中,以形成有序、规则和重复的蛋白质分子晶格排列,称为晶体。在有利的条件下,如温度、pH、浓度和沉淀剂,最终形成过饱和溶液,然后晶体成核并生长7,8。尽管结晶试验设置取得了许多进展,主要是随着高通量机器人系统的开发和现成的“稀疏基质”筛选的可用性,但多年来蛋白质结晶的一般方法基本保持不变。常见的实验性蛋白质结晶技术包括蒸汽扩散(悬挂液滴和坐滴)9,微批量(油下)10,11,自由界面扩散(微流体装置)12和透析(使用按钮和其他技术)13,14,15。然而,还存在其他更专业的设置,例如用于结晶膜蛋白16,17的中间相方法。虽然沉积在蛋白质数据库中的大多数X射线蛋白质结构到目前为止已经通过气相扩散方法6,18的结晶来解决,但其他方法,例如通过透析结晶,似乎没有得到充分利用,可能是由于与其实验设置相关的实际方面。
透析结晶仅依赖于溶质(沉淀剂、离子、添加剂和缓冲液)通过半透膜的缓慢扩散,同时防止蛋白质分子循环。这样,蛋白质溶液慢慢进入平衡状态,沉淀剂达到结晶所需的浓度。系统的动力学取决于温度、沉淀剂浓度和纤维素膜分子量截止值 (MWCO)19。迄今为止,最流行的透析结晶装置是使用由透明丙烯酸板制成的微透析按钮。它们通常浸入含有结晶沉淀剂溶液的储液器(主要使用蒸汽扩散悬挂滴板)中。然而,这种低通量方法还需要特定的组装来密封放置在纽扣室上方的透析膜内的蛋白质溶液,如图 1所示。此外,滞留在透析膜和蛋白质溶液之间的气泡是损害晶体生长的常见问题。该方法的另一个限制是样品要求,与蒸汽扩散方法相比,需要更高的浓度和体积来适应透析按钮。因此,使用微透析按钮进行结晶被认为是一种没有吸引力的方法,特别是对于膜蛋白等难以识别的靶标,其纯化率低得令人沮丧。最近,已经开发了微流体装置以促进通过透析15实现蛋白质结晶。这些芯片还被设计为具有高X射线透明度和低背景,允许芯片在室温下用于 原位 数据收集,从而消除了收获和低温冷却晶体的不便。尽管取得了这些进步,但这种方法的通量仍然非常低且成本高昂。
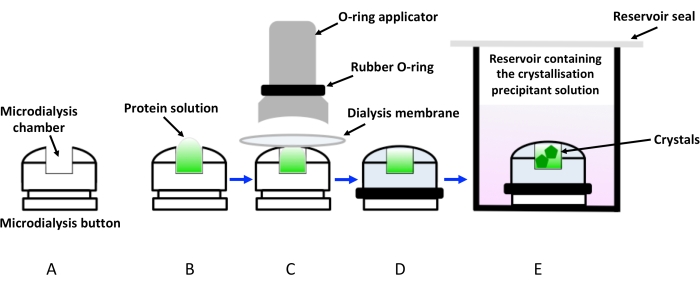
图1:使用透析按钮透析结晶的示意图 。 (A)结晶透析按钮的示意图。(B)将蛋白质溶液加入微透析纽室。(C)在通过涂抹器 施加的 橡胶圈(O形圈)的帮助下将透析膜固定在微透析按钮上。(D)透析按钮准备浸入含有结晶溶液(透析溶液)的储液器中,如(E)所示。装有浸入式透析按钮的小瓶必须密封以避免蒸发。 请点击此处查看此图的大图。
在这里,提出了一个简单的方案,用于使用96孔高通量透析板筛选蛋白质结晶条件和晶体生长。这些一次性板的设计用途类似于蒸汽扩散结晶板(移液器然后密封),如图 2所示。这些板可容纳多达 3.2 μL 的蛋白质和 350 μL 的透析液。每个孔都有一个单独的再生纤维素膜,以防止孔之间的交叉污染。设置大约需要 10 分钟才能完成,除了所有标准结晶实验室中都可以找到的设备外,不需要任何专业设备。四种不同的蛋白质,包括两种膜蛋白,用于证明和验证该方法作为高通量(HTP)蛋白质晶体学的有效方法。
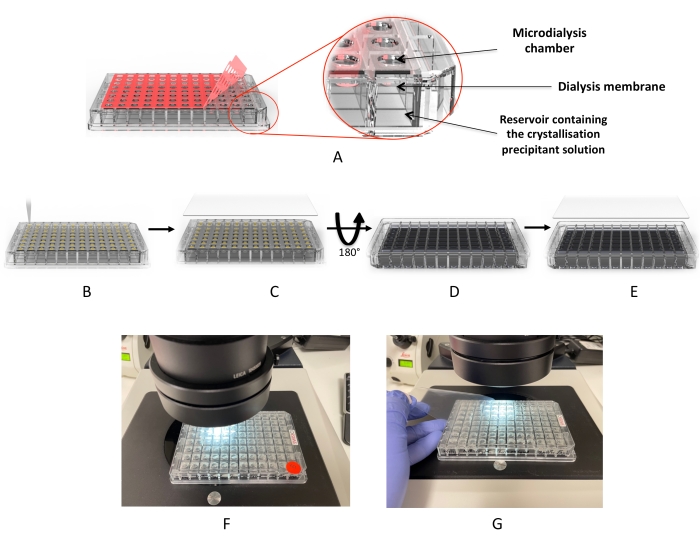
图2:使用微透析板的结晶工作流程。 (A)去除红色粘合剂“覆盖膜”。(B)将蛋白质液滴分配到每个滴孔中。(C)孔被紫外线“覆盖膜”覆盖。(D)将板倒置,加入透析液(或结晶筛)。(E)将板密封并孵育。(法,八)液滴的显微镜检查。 请点击此处查看此图的大图。
使用0.5 mL透析管(图3)证明了这种通过透析方案结晶的使用,用于大规模(数百至数千次)微晶生产,适用于最先进的数据收集方法,例如XFEL设施20,21,22,23,24和同步加速器25,26,27的连续晶体学,以及MicroED 28、29、30 方法。
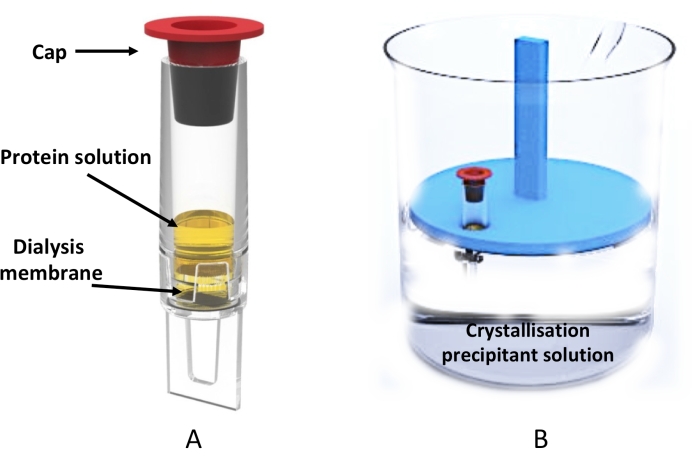
图 3:使用透析管的大规模微透析结晶。 (A) 0.5 mL 透析管的示意图。(B)装有结晶溶液的烧杯和装有透析管的浮动管架的侧视图。请点击此处查看此图的大图。
Protocol
Representative Results
Discussion
目前,透析结晶是最未充分利用的结晶方法,即由于现有方法(例如带按钮的微透析)的低通量和繁琐的性质。在这里,一个简单但强大的方案遵循HTP工作流程,通过市售的微透析板和透析管透析蛋白质晶体生长。根据目标蛋白的不同,手术中使用的微量透析板和透析管可以选择具有 3、5、10 或 30 kDa MWCO 的透析膜。该方案可以在任何标准结晶设施中轻松设置,并且具有适用于可溶性和膜蛋白的巨大优势。然而,在该协议期间未测试蛋白质 – 蛋白质和蛋白质 – 核酸复合物。
与任何透析结晶方法一样,蛋白质样品和透析溶液之间的体积比至关重要。在该协议中,建议样品和透析溶液之间的比例为1:100,但由于微透析板允许最大容量为350μL透析溶液,因此可以探索这些比例以获得晶体命中。在设置结晶板时,在所提出的方案中使用1-2μL蛋白质的体积。这是为了确保使用手动多通道移液器准确设置液滴。通过使用电动移液器(多通道或重复分液移液器)或HTP液体分液机器人,可以准确地滴低体积,从而降低所需的蛋白质量。此外,由于微透析板所需的透析缓冲液体积相对较低(与其他常规透析方法相反),因此可以(无需大量使用资源)探索大型化学空间,不仅使用市售的结晶筛,还使用优化筛(围绕初始结晶命中条件设计)。
所介绍的HTP程序的一个关键步骤是及时将小体积蛋白质(每个条件0.50-3.2μL)施加到透析板上,以限制脱水和样品损失。通过使用多通道移液器、重复分液移液器或机器人结晶系统,可以轻松缓解这种情况。板在20°C下的孵育时间长,例如超过2周,可能导致蛋白质液滴脱水或最近形成的晶体损坏。将透析板保存在加湿室或可密封袋内可以减轻这种影响。此外,建议使用无菌材料和技术以避免细菌生长。
如引言所述,最近,随着对了解疾病机制、蛋白质-配体结合相互作用和蛋白质-蛋白质相互作用的蛋白质结构动力学的需求增加,蛋白质 X 射线晶体学领域通过开发新的和现有的结晶技术、现代晶体样品输送方法、新一代 X 射线源以及用于数据采集和处理的新复杂方法而发生了革命性的变化36,37,38.因此,室温连续微晶体学的出现,无论是使用XFEL还是同步加速器光源进行,已成为结构生物学中的重要工具,特别是在膜蛋白领域39。然而,需要数千个微晶体才能产生足够的数据来形成稳健的结构解决方案,这不是一件容易的事(至少通过传统的结晶方法)。这里描述的透析结晶方法可以生产大量的微晶。一旦通过使用微透析板确定了生产微晶(1-10 μm)的结晶条件,就可以使用0.5 mL透析器装置生产大量高密度微晶(图5)。这些晶体非常适合使用固定目标或液体射流样品输送系统27,40进行数据收集。通过这种方法获得的晶体也适用于MicroED应用。然而,这些可能需要铣削到适合此特定应用的尺寸和厚度,因为电子与晶体的相互作用比X射线光子41强得多。
总之,这里描述的透析结晶方法增加了蛋白质结晶结构测定的不断发展策略,并扩大了可用于确定以前其他传统方法无法成功的新型蛋白质靶标的努力范围。
Disclosures
The authors have nothing to disclose.
Acknowledgements
我们感谢英国商业、能源和工业战略部 (BEIS) 的资助。我们感谢国家物理实验室的Alex R. Jones和Mike Shaw对手稿的反馈。
Materials
| 0.2 mL tubes | Thermo Scientific | AB0620 | For aliquoting protein solutions. |
| 0.2 µm syringe filter | Sartorius | 17823———-K | Surfactant-free cellulose acetate filters. For filtering dialysis solutions. |
| 0.22 µm membrane filters | Millipore | GSTF04700 | Membrane filters for filtering large volumes of buffers |
| 12-channel, variable 0.5 – 10 µL Research plus pipette | Eppendorf | 3125000028 | For dispensing protein drops onto the Diaplate. |
| 12-channel, variable 30 – 300 µL Eppendorf Research plus pipette | Eppendorf | 3125000060 | For dispensing dialysis solutions on the Diaplate reservoirs. |
| 20 mL syringe | Fisherbrand | 15889152 | For use with syringe filters. |
| 96 well 2.2 mL deep-well plates | Thermo Scientific | AB0788 | Polypropylene deep-well storage plates; for preparing screens using the Hamilton Microlab STARlet. |
| Centrifuge 5425 | Eppendorf | 5405000565 | With rotor FA-24×2 with a maximum g-force of 21,300 x g. |
| Diacon dialyser | SWISSCI | W72010 | Dialyzer tubes with a regenerated cellulose membrane with a molecular weight cut-off of 10 kDa. Ideal for protein solutions of up to 0.5 mL. |
| Diaplate 96-well plate | SWISSCI | W82010 | Microdialysis plate. The Diaplate consists of two sides with a regenerated cellulose membrane in-between with a molecular weight cut-off of 10 kDa. |
| Falcon 50 mL High Clarity PP Centrifuge Tube | Corning | 352070 | For holding dialysis solutions. |
| Floating rack | SWISSCI | n/a | Included in the Diacon kit |
| Floor-standing vibration-free incubator | Molecular Dimensions | MD5-01 | 400 L temperature-controlled incubator set to 20 °C. |
| Leica M205 C stereo microscope | Leica | Planapo 1.0x objective, 7.8x – 160x zoom range with DMC 4500 camera | |
| Lysozyme from chicken egg white | Sigma Aldrich | 62971 | Lyophilized protein |
| Memgold2 | Molecular Dimensions | MD1-64 | Sparse-matrix screen |
| Microlab STARlet | Hamilton | n/a | Liquid handler system. |
| Reservoir cover film | SWISSCI | n/a | Included in the Diaplate kit |
| Reusable bottle top filter | Thermo Scientific | DS0320-5045 | For fitering large volumes of buffers, for use with 0.22 µm membrane filters |
| Sealing paddle | SWISSCI | n/a | Included in the Diaplate kit |
| Thaumatin from Thaumatococcus daniellii | Sigma Aldrich | T7638 | Lyophilized protein |
| UV cover film | SWISSCI | n/a | Included in the Diaplate kit |
References
- Brooks-Bartlett, J. C., Garman, E. F. The nobel science: One hundred years of crystallography. Interdisciplinary Science Reviews. 40 (3), 244-264 (2015).
- Maveyraud, L., Mourey, L. Protein X-ray crystallography and drug discovery. Molecules. 25 (5), (2020).
- Kwan, T. O. C., Axford, D., Moraes, I. Membrane protein crystallography in the era of modern structural biology. Biochemical Society Transactions. 48 (6), 2505-2524 (2020).
- Birch, J., et al. The fine art of integral membrane protein crystallisation. Methods. 147, 150-162 (2018).
- Gorrec, F., Löwe, J. Automated protocols for macromolecular crystallization at the MRC laboratory of molecular biology. Journal of Visualized Experiments. 131 (131), (2018).
- Govada, L., Chayen, N. E. Choosing the method of crystallization to obtain optimal results. Crystals. 9 (2), 106 (2019).
- Chayen, N. E. Turning protein crystallisation from an art into science. Current Opinion in Structural Biology. 14 (5), 577-583 (2004).
- McPherson, A., Gavira, J. A. Introduction to protein crystallization. Acta Crystallographica Section F: Structural Biology Communications. 70 (1), 2-20 (2014).
- Gulbis, J. Protein crystallography: methods and protocols. Crystallography Reviews. 24 (2), 136-143 (2018).
- D’Arcy, A., Bergfors, T., Cowan-Jacob, S. W., Marsh, M. Microseed matrix screening for optimization in protein crystallization: What have we learned. Acta Crystallographica Section:F Structural Biology Communications. 70 (9), 1117-1126 (2014).
- Shaw Stewart, ., D, P., Kolek, S. A., Briggs, R. A., Chayen, N. E., Baldock, P. F. Random microseeding: a theoretical and practical exploration of seed stability and seeding techniques for successful protein crystallization. Crystal Growth & Design. 11 (8), 3432-3441 (2011).
- Junius, N., et al. A microfluidic device for both on-chip dialysis protein crystallization and in situ X-ray diffraction. Lab on a Chip. 20 (2), 296-310 (2020).
- Junius, N., Vahdatahar, E., Oksanen, E., Ferrer, J. L., Budayova-Spano, M. Optimization of crystallization of biological macromolecules using dialysis combined with temperature control. Journal of Applied Crystallography. 53 (3), 686-698 (2020).
- Vahdatahar, E., Junius, N., Budayova-Spano, M. Optimization of crystal growth for neutron macromolecular crystallography. Journal of Visualized Experiments. 169, (2021).
- Jaho, S., et al. Crystallization of proteins on chip by microdialysis for in situ X-ray diffraction studies. Journal of Visualized Experiments. 170, (2021).
- Liu, W., Cherezov, V. Crystallization of membrane proteins in lipidic mesophases. Journal of Visualized Experiments. 49, 2501 (2011).
- Ujwal, R., Abramson, J. High-throughput crystallization of membrane proteins using the lipidic bicelle method. Journal of Visualized Experiments. 59, (2012).
- Parker, J. L., Newstead, S. Membrane protein crystallisation: Current trends and future perspectives. Advances in Experimental Medicine and Biology. 922. , 61-72 (2016).
- Apostolopoulou, V., Junius, N., Sear, R. P., Budayova-Spano, M. Mixing salts and polyethylene glycol into protein solutions: The effects of diffusion across semi-permeable membranes and of convection. Crystal Growth & Design. 20 (6), 3927-3936 (2020).
- Neutze, R., Wouts, R., Vander Spoel, D., Weckert, E., Hajdu, J. Potential for biomolecular imaging with femtosecond X-ray pulses. Nature. 406 (6797), 752-757 (2000).
- Chapman, H. N., et al. Femtosecond X-ray protein nanocrystallography. Nature. 470 (7332), 73-78 (2011).
- Mizohata, E., Nakane, T., Fukuda, Y., Nango, E., Iwata, S. Serial femtosecond crystallography at the SACLA: breakthrough to dynamic structural biology. Biophysical Reviews. 10 (2), 209-218 (2018).
- Nogly, P., et al. Lipidic cubic phase serial millisecond crystallography using synchrotron radiation. IUCrJ. 2 (2), 168-176 (2015).
- Johansson, L. C., et al. XFEL structures of the human MT2 melatonin receptor reveal the basis of subtype selectivity. Nature. 569 (7755), 289-292 (2019).
- Owen, R. L., et al. Low-dose fixed-target serial synchrotron crystallography. Acta Crystallographica Section D: Structural Biology. 73 (4), 373-378 (2017).
- Weinert, T., et al. Serial millisecond crystallography for routine room-temperature structure determination at synchrotrons. Nature communications. 8 (1), 542 (2017).
- Axford, D., et al. Two states of a light-sensitive membrane protein captured at room temperature using thin-film sample mounts. Acta Crystallographica Section D: Structural Biology. 78 (1), 52-58 (2022).
- Nannenga, B. L., Gonen, T. The cryo-EM method microcrystal electron diffraction (MicroED). Nature Methods. 16 (5), 369-379 (2019).
- Nguyen, C., Gonen, T. Beyond protein structure determination with MicroED. Current Opinion in Structural Biology. 64, 51-58 (2020).
- Mu, X., Gillman, C., Nguyen, C., Gonen, T. An overview of microcrystal electron diffraction (MicroED). Annual Review of Biochemistry. 90, 431-450 (2021).
- Kwan, T. O. C., et al. Selection of biophysical methods for characterisation of membrane proteins. International Journal of Molecular Sciences. 22 (10), 2605 (2019).
- Pos, K. M., Purification Diederichs, K. crystallization and preliminary diffraction studies of AcrB, an inner-membrane multi-drug efflux protein. Acta Crystallographica Section D: Biological Crystallography. 58 (10), 1865-1867 (2002).
- Guan, L., Mirza, O., Verner, G., Iwata, S., Kaback, H. R. Structural determination of wild-type lactose permease. Proceedings of the National Academy of Sciences. 104 (39), 15294-15298 (2007).
- Kwan, T. O. C., Reis, R., Moraes, I. In situ measurements of polypeptide samples by dynamic light scattering: membrane proteins, a case study. Methods in Molecular Biology. , 189-202 (2021).
- Seddon, A. M., Curnow, P., Booth, P. J. Membrane proteins, lipids and detergents: not just a soap opera. Biochimica et Biophysica Acta (BBA)-Biomembranes. (1-2), 105-117 (2004).
- Wickstrand, C., et al. A tool for visualizing protein motions in time-resolved crystallography. Structural Dynamics. 7 (2), 024701 (2020).
- Orville, A. M. Recent results in time resolved serial femtosecond crystallography at XFELs. Current Opinion in Structural Biology. 65, 193-208 (2020).
- Schulz, E. C., Yorke, B. A., Pearson, A. R., Mehrabi, P. Best practices for time-resolved serial synchrotron crystallography. Acta Crystallographica Section D: Structural Biology. 78 (1), 14-29 (2022).
- Neutze, R., Brändén, G., Schertler, G. F. Membrane protein structural biology using X-ray free eletron lasers. Current Opinion in Structural Biology. 33, 115-125 (2015).
- Wierstall, U. Liquid sample delivery techniques for serial femtosecond crystallography. Philosophical Transactions of the Royal Society B: Biological Sciences. 369 (1647), 20130337 (2014).
- Shi, D., Nannenga, B. L., Iadanza, M. G., Gonen, T. Three-dimensional electron crystallography of protein microcrystals. eLife. 2, 01345 (2013).

