Primer para imunohistoquímica em tecido criosseccionada cérebro de um rato: Exemplo de coloração para Microglia e Neurônios
Summary
This introductory level protocol describes the reagents, equipment, and techniques required to complete immunohistochemical staining of rodent brains, using markers for microglia and neuronal elements as an example.
Abstract
A imuno-histoquímica é uma técnica amplamente utilizada para detectar a presença, localização e abundância relativa de antigénios in situ. Este protocolo nível introdutório descreve os reagentes, equipamentos e técnicas necessárias para concluir coloração imuno-histoquímica de tecido cerebral dos roedores, utilizando marcadores para microglia e elementos neuronais como um exemplo. Especificamente, este documento é um protocolo passo-a-passo para visualização fluorescente de microglia e neurônios via imunohistoquímica para Iba1 e pan-neuronal, respectivamente. Fluorescência-marcação dupla é particularmente útil para a localização de várias proteínas dentro da mesma amostra, proporcionando a oportunidade de observar com precisão interacções entre tipos de células, receptores, ligandos, e / ou a matriz extracelular em relação um ao outro, bem como co-proteína localização dentro de uma única célula. Ao contrário de outras técnicas de visualização, a intensidade da coloração imuno-histoquímica de fluorescência pode diminuir emas semanas a meses após a coloração, a menos que sejam tomadas precauções apropriadas. Apesar desta limitação, em muitas aplicações de rotulagem de fluorescência dupla é preferida em relação às alternativas tais como tetracloridrato de 3,3'-diaminobenzidina (DAB) ou fosfatase alcalina (AP), como fluorescência é mais eficaz do tempo e permite a diferenciação mais precisa entre dois ou mais marcadores. A discussão inclui dicas de solução de problemas e conselhos para promover o sucesso.
Introduction
A imuno-histoquímica é um processo para a detecção de antigénios (por exemplo, proteínas) em secções de tecido utilizando anticorpos primários que se ligam especificamente aos antigénios de interesse. A imuno-histoquímica foi lançada pela JR Marrack em 1934, quando ele determinou que os anticorpos poderiam localizar antígenos com grande especificidade 1. A partir de 1942, alguns dos primeiros estudos in vitro, utilizando anticorpos fluorescentes para visualizar imuno-histoquímica, foram publicadas 2,3, após o que o primeiro estudo in vivo histoquímica foi publicado em 4. Durante a década de 1960, três décadas após o início dos métodos imuno-histoquímica, os anticorpos conjugados com enzimas começou a ser usado como reagentes secundários. Estes métodos foram simultaneamente e independentemente desenvolvido na França e os EUA 5,6. Hoje, uma grande variedade de anticorpos oferece infinitas possibilidades para estudos de imunohistoquímica 7.
"> O objetivo geral desta correspondência é fornecer uma breve introdução sobre coloração imuno-histoquímica, não pretende ser uma análise abrangente e exaustiva desta técnica No método descrito, técnicas de imunohistoquímica para dois antígenos são apresentados (marcadores para microglia e. neurónios) para a coloração de paraformaldeído perfundido, sacarose crioprotegidos, criosseccionada cérebro de rato. coloração imuno-histoquímica começa com o bloqueio de ligação para reduzir a coloração de fundo não específica de antigénio. Em seguida, a incubação com anticorpo primário permite a ligação a um antigénio específico no tecido. Após o anticorpo primário, outro anticorpo, denominado anticorpo secundário, é aplicado para ligar o anticorpo primário a um sinal de visualização conjugado 8. O anticorpo secundário tem como alvo a imunoglobulina G (IgG) de domínio específico para as espécies em que o anticorpo primário foi levantadas. O anticorpo secundário amplifica o sinal do anticorpo primário, uma vez as regiões Fab de tque se ligam ao anticorpo secundário múltiplos locais no domínio de IgG do anticorpo primário. Enzimas ou moléculas fluorescentes conjugados com as regiões C F do anticorpo secundário permitir a visualização. Por exemplo, um anticorpo primário de coelho anti-Iba1 é uma molécula de IgG de coelho específico para Iba1. Quando burro anti-IgG de coelho é aplicado como anticorpo secundário, ele irá reconhecer e ligar-se a várias regiões do anticorpo anti-IgG de coelho Iba1 (ver Figura 1). O anticorpo de burro pode ser visualizado através de vários métodos. Esta correspondência se concentra na detecção de um fluoroforo conjugado com o anticorpo secundário, o qual reconhece o anticorpo primário, para a visualização por microscopia fluorescente. Em imuno fluorescente, um corante nuclear tal como Hoechst DAPI ou pode ser usado para visualizar todos os núcleos.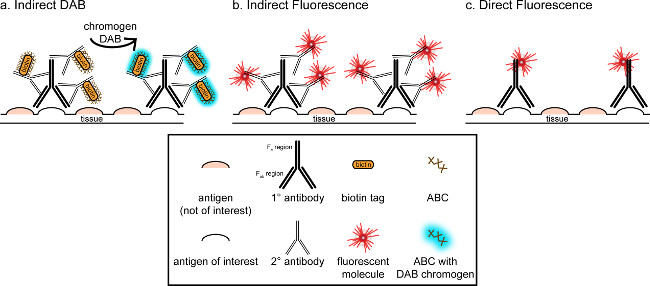
Figura 1: SchEmatic de representação directa vs. indirecta técnicas de marcação de anticorpos. Os anticorpos ligam-se ao antigénio de interesse e podem ser amplificados por anticorpos secundários dirigidos contra as espécies de os anticorpos primários. Esta técnica pode ser realizada utilizando complexo de avidina-biotina (ABC) para a amplificação e para a visualização DAB (A), ou um anticorpo secundário fluorescente directamente conjugado (B). Alternativamente, os anticorpos primários podem ser directamente conjugado com muitas marcas diferentes, incluindo biotina ou um fluoróforo (C). Por favor clique aqui para ver uma versão maior desta figura.
Um método alternativo para a visualização de coloração imuno-histoquímica utiliza 3,3'-diaminobenzidina (DAB; ver Figuras 1 e 2). Isso é diferente de fluorescência usando um biotinilado ouperoxidase de rábano (HRP) conjugado com anticorpo secundário, o qual fornece uma enzima para converter DAB a um precipitado que é visível sob microscopia de campo claro. Nos casos em que um único antígeno é de interesse ou coloração é necessário para ser duradouro, DAB pode ser mais apropriado do que a coloração fluorescente. No entanto, a coloração DAB não é bem adequada para a diferenciação entre vários marcadores, especialmente se dois antigénios nucleares são de interesse. Para obter informações sobre materiais DAB e modificações do protocolo, consultar Tabela 1. Em alternativa, cloreto de nitro azul de tetrazólio / 5-bromo-4-cloro-3-indolil fosfato (NBT / BCIP) pode ser usado para visualizar uma fosfatase alcalina (AP) secundário conjugado anticorpo.
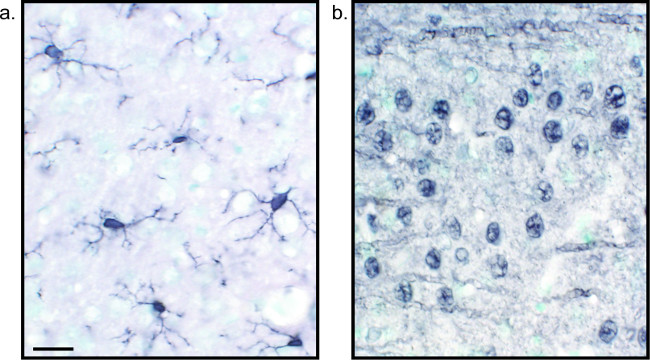
Figura 2:. Imagens representativas de cortes de tecido cerebral de níquel reforçada DAB individuais marcado Rato Rato cérebro ifficções que são rotulados com DAB-níquel reforçada para Iba1 (A) e pan-neuronal (B) permitir a análise de longa duração da microglia ou neurônios sozinho. Barra de escala de 20 um. Por favor clique aqui para ver uma versão maior desta figura.
Deve-se considerar a abundância estimado do antigénio de interesse dentro do tecido a ser analisado. Os métodos indirectos (como descrito acima) são úteis para alvos com baixa abundância. Quando o antigénio de interesse é em grande abundância, métodos directos podem ser aplicados. Os métodos directos envolvem um anticorpo primário que é conjugado directamente a um sinal de visualização, e, portanto, não é necessária qualquer anticorpo secundário. Este método simplifica o processo de coloração, mas elimina a amplificação alcançado por métodos indirectos. Usando um anticorpo primário conjugado directamente elimina também a reactividade cruzada de anticorpos secundáriosquando a rotulagem dupla.
Esta comunicação detalha o protocolo para a rotulagem de casal com Iba1 e Pan-neuronais (detalhes na Tabela 1). Iba1 manchas microglia em muitos estados de ativação, incluindo ramificados, hiper-ramificado, ativado, amebóides, ea vara. Manchas Pan-neuronais neuronal axônios, dendritos, e Soma. Desde Iba1 manchas mais microglia e metas Pan-neuronais do neurônio, esta combinação de manchas é útil na obtenção de um amplo entendimento das interações microglia-neurônio.
Em suma, a coloração imuno-histoquímica conta com a seleção cuidadosa de anticorpos. Como a questão de pesquisa se torna mais específica, os anticorpos produzidos contra antígenos alternativas pode ser desejado. Para atingir um estado de ativação microglial específico, pode-se optar pelo uso de anticorpos CD45 ou CD68, ao invés de Iba1. Além disso, ao trabalhar com camundongos, F4 / 80 pode obter os resultados necessários. Da mesma forma, os elementos neuronais pode ser dirigida especificamente com anticorpos razada contra o núcleo, sinapse (pré ou pós), axônio, e crescimento cone. Além disso, há outros marcadores que distinguem a idade do neurónio (duas vezes Cotrin, NeuN), e a regeneração neuronal (GAP-43).
Protocol
Representative Results
Discussion
O objectivo global desta comunicação era introduzir procedimentos de imuno-histoquímica para o leitor. Para isso, o exemplo da rotulagem de casal com Iba1 e antígenos Pan-neuronais para observar microglia e neurônios em paraformaldeído perfusão, foi utilizado sacarose cérebro crioprotegidos, rato criosseccionada.
Esta técnica pode ser adaptado para servir finalidades infinitas. Uma matriz de antigénios diferentes numa variedade de tipos de tecidos tais como, mas não limitado para …
Declarações
The authors have nothing to disclose.
Acknowledgements
The authors would like to thank Mr. Ryan Hart and Mr. Arriz Lucas for their invaluable feedback on this communication. This work was supported by NIH NINDS R01 NS065052 and Phoenix Children’s Hospital Mission Support Funds.
Materials
| Name of Material/ Equipment | Company | Catalog Number | Comments/Description |
| Fisherbrand Superfrost Plus Glass Slides | Fisher Scientific | 22-034-979 | Used for tissue mounting (1.2.2) |
| Oven | Thermo Scientific | 51028112 | Used for tissue drying (2.1.1) |
| Mini Pap pen | Life Technologies | 00-8877 | Used in step 2.2.2 |
| Andwin Scientific Tissue-tek Slide Staining Dish | Fisher Scientific | 22-149-429 | Used for all washes during staining (2.2), as well as the Hoechst step (2.2.8) |
| Kimwipes | Fisher Scientific | 06-666-A | Used for drying slides (2.2) |
| Black Staining Box | Ted Pella | 21050 | Used for blocking and staining steps (2.2) |
| Normal Donkey Serum | Fisher Scientific | 50-413-253 | Used for block and antibody incubation (2.2) |
| Mouse α-Pan-neuronal | Millipore | MAB2300 | Used for primary antibody (2.2.4) |
| Rabbit α-Iba1 | Wako Chemical | 019-19741 | Used for primary antibody (2.2.4) |
| Donkey α-Rabbit 594 | Jackson ImmunoResearch | 711-585-152 | Used for secondary antibody (2.2.6) |
| Donkey α-mouse 488 | Jackson ImmunoResearch | 715-545-150 | Used for secondary antibody (2.2.6) |
| Caterer's foil | Any | N/A | Used in steps 1.2.2 and 2.3.2 |
| Fluoromount-G | Southern Biotech | 0100-01 | Used for coverslipping (2.2.8) |
| Coverslips | Fisher Scientific | 12544E | Used for coverslipping (2.2.8) |
| Clear Nail Polish | Any | N/A | Used for coverslipping (2.2.8) |
| Axio Observer.Z1 and LSM 710 (laser scanning, confocal) | Carl Zeiss | N/A | Used for imaging (3) |
| Axioskop A2 | Carl Zeiss | N/A | Used for imaging (3) |
| CitriSolv | FisherScientific | For DAB protocol | |
| ABC | Vector Laboratories | PK-6100 | For DAB protocol |
| DAB Peroxidase kit | Vector Laboratories | SK-4100 | For DAB protocol |
| Biotinylated horse α-rabbit IgG | Vector Laboratories | BA-1100 | For DAB protocol |
| Biotinylated horse α-mouse IgG | Vector Laboratories | BA-2001 | For DAB protocol |
| 30% Hydrogen Peroxide | FisherScientific | H325-500 | For DAB protocol |
| Wheaton slide racks and staining dishes | TedPella | 21043 | For DAB protocol |
| Masterflex perfusion pump and tubing | Cole-Parmer | Used for perfusion (1.1.1 and 1.1.2) | |
| Andwin scientific tissue-tek CRYO-OCT compound (case of 12) | Fisher Scientific | 14-373-65 | Used for tissue freezing (1.2.1) |
| Thermometer (-50 to 50 C) | Fisher Scientific | 15-059-228 | Used for tissue freezing (1.2.1) |
| Cryostat | Leica | CM3500S | Used for tissue sectioning (1.2.2) |
| Staining Dish, Plastic with 2 Lids | Grale Scientific | 353 | For antigen retrival |
| 20 Place Staining Rack, Slides Horizontal | Grale Scientific | 354 | For antigen retrival |
| Microwave | Any | N/A | For antigen retrival |
Referências
- Marrack, J. R. Chemistry of antigens and antibodies. Nature. 134, 468-469 (1934).
- Coons, A. H., Creech, H. J., Jones, R. N., Berliner, E. The demonstration of pneumococcal antigen in tissues by the use of fluorescent antibody. J Immunol. 45, 159-170 (1942).
- Marshall, J. M. Localization of adrenocorticotropic hormone by histochemical and immunochemical methods. The Journal of experimental medicine. 94, 21-30 (1951).
- Mellors, R. C. Histochemical demonstration of the in vivo localization of antibodies: antigenic components of the kidney and the pathogenesis of glomerulonephritis. The journal of histochemistry and cytochemistry : official journal of the Histochemistry Society. 3, 284-289 (1955).
- Nakane, P. K., Pierce, G. B. Enzyme-labeled antibodies: preparation and application for the localization of antigens. The journal of histochemistry and cytochemistry : official journal of the Histochemistry Society. 14, 929-931 (1966).
- Avrameas, S., Uriel, J. Method of antigen and antibody labelling with enzymes and its immunodiffusion application. Comptes rendus hebdomadaires des seances de l’Academie des sciences. Serie D: Sciences naturelles. 262, 2543-2545 (1966).
- Cuello, A. C. . Immunohistochemistry. , (1983).
- Junqueira, L. C. U., Mescher, A. L. . Junqueira’s basic histology : text and atlas. , (2013).
- Gage, G. J., Kipke, D. R., Shain, W. Whole animal perfusion fixation for rodents. Journal of visualized experiments : JoVE. , (2012).
- Christensen, N. K., Winther, L., Kumar, G. L., Rudbeck, L. . Education Guide: Immunohistochemical (IHC) staining methods. , 103-108 (2009).
- Wang, G., Achim, C. L., Hamilton, R. L., Wiley, C. A., Soontornniyomkij, V. Tyramide signal amplification method in multiple-label immunofluorescence confocal microscopy). Methods. 18, 459-464 (1999).
- Feldengut, S., Del Tredici, K., Braak, H. Paraffin sections of 70-100 mum: a novel technique and its benefits for studying the nervous system. Journal of neuroscience methods. 215, 241-244 (2013).

