Modelagem e Simulações de Olfativo Drug Delivery com controles passivo e ativo do nasal inalados Farmacêuticas Aerossóis
Summary
This manuscript reviews the modeling and simulations of different protocols to deliver medications to the olfactory region in image-based nasal airway models. Multiple software modules are used to develop the anatomically accurate nose model, generate computational mesh, simulate nasal airflows, and predict particle deposition at the olfactory region.
Abstract
Há muitas vantagens da entrega directa nose-to-cérebro droga no tratamento de desordens neurológicas. No entanto, a sua aplicação é limitada pela eficiência extremamente baixa de entrega (<1%) à mucosa olfactiva que se liga directamente ao cérebro. É crucial para desenvolver novas técnicas para entregar medicamentos neurológicos de forma mais eficaz para a região olfactiva. O objetivo deste estudo é desenvolver uma plataforma numérica para simular e melhorar a entrega da droga olfativa intranasal. Um método de imagem de CFD acoplado foi apresentado que sintetizado o desenvolvimento baseado em imagem modelo, engrenagem qualidade, simulação de fluidos, e rastreamento de partículas magnéticas. Com este método, o desempenho de três protocolos de entrega intranasal foram numericamente avaliada e comparada. Influências de manobras de respiração, disposição ímã, intensidade do campo magnético, posição de liberação de drogas e de tamanho de partículas sobre a dose olfativo também foram numericamente estudada.
A partir da ssimulacoes, descobrimos que a dosagem olfativa clinicamente significativa (até 45%) eram possíveis, usando a combinação de layout de ímã e liberação da droga seletiva. Uma entrega 64 vezes de mais elevado de dosagem foi previsto, no caso com a orientação magnetophoretic em comparação com o caso sem ele. No entanto, a orientação precisa de aerossóis por via nasal inalados para a região olfactiva continua sendo um desafio devido à natureza instável da magnetoforese, bem como a alta sensibilidade da dosagem olfativa para-paciente, um dispositivo, e fatores relacionados à partícula.
Introduction
Drogas entregues à região olfactiva pode contornar a barreira sangue-cérebro-barreira e directamente entrar no cérebro, que conduz a uma absorção eficiente e rápido início de acção dos fármacos de 1,2. No entanto, os dispositivos nasais convencionais, tais como bombas e sprays nasais entregar doses extremamente baixas para a região olfactiva (<1%) por meio da via nasal 3,4. É principalmente devido à estrutura complicada do nariz humano que é composto de, passagens estreitas convolutos (Figura 1). A região olfactiva locates acima do meato superior, em que apenas uma fracção muito pequena de ar inalado pode atingir 5,6. Além disso, dispositivos de inalação convencionais dependem de forças aerodinâmicas para transportar agentes terapêuticos para a área de alvo 7. Não há mais controle sobre os movimentos das partículas após a sua libertação. Portanto, o transporte e deposição destas partículas predominantemente dependem de suas velocidades iniciais e posições de lançamento. Devidopara a passagem nasal complicada, bem como a falta de controlo de partículas, a maioria das partículas de fármaco estão presos no nariz anterior e não pode atingir a região olfactiva 8.
Embora existam muitas opções de dispositivos nasais, os que foram concebidos especificamente para a entrega olfativa alvo têm sido raramente relatada 7,9. Uma exceção é Hoekman e Ho 10 que desenvolveu um dispositivo de entrega olfativa preferencial e demonstraram níveis mais elevados córtex-a-sangue de drogas em ratos em vez de usar uma gota nariz. No entanto, escalando os resultados de deposição em ratos para os seres humanos não é simples, considerando as enormes diferenças anatômicas e fisiológicas entre estas duas espécies 11. existem muitas limitações quando se utiliza versões adaptadas de dispositivos nasais padrão para entregas olfativos. Um revés principal é que apenas uma muito pequena porção de medicamentos podem ser entregues para a mucosa olfactiva, através do qual os medicamentos podem entrar nocérebro. Modelação numérica previu que menos de 0,5% de nanopartículas por administração intranasal pode depositar na região olfactiva 3,5. A taxa de deposição é ainda mais baixa (0,007%) para as partículas micrométricas 12. A fim de fazer a entrega do nariz-para-cérebro clinicamente viável, a velocidade de deposição olfactiva tem de ser significativamente melhorado.
Existem várias abordagens possíveis para melhorar a entrega olfativo. Uma abordagem é a ideia inalador inteligente proposto por Kleinstreuer et al. 13, quando as partículas depositam em uma região são principalmente a partir de uma área específica na entrada, é possível fornecer as partículas para o local alvo, libertando-os apenas de certas áreas na entrada . A técnica de entrega inteligente foi mostrado para gerar uma entrega pulmonar muito mais eficiente do que os métodos convencionais. 13,14 Supõe-se que esta ideia inteligente entrega também pode ser aplicada na entrega da droga para intranasal idosagens mprove à mucosa olfactiva. Pela liberação de partículas em posições diferentes na abertura narina e de diferentes profundidades no interior da cavidade nasal, melhorou a eficiência de entrega olfativos e redução do desperdício de drogas no nariz anterior são possíveis.
Outro método possível é a de controlar activamente o movimento das partículas no interior da cavidade nasal, utilizando uma variedade de forças de campo, tais como a força eléctrica ou magnética. De comando eléctrico de partículas carregadas tem sido sugerido para a entrega de droga voltado para o nariz humano e pulmões 15-17. Xi et al. 18 numericamente testado o desempenho de orientação elétrica de partículas carregadas e previu melhorou significativamente doses olfativos. De modo semelhante, a orientação de partículas de droga ferromagnéticos com um campo magnético apropriado, também tem o potencial para atingir partículas para a mucosa olfactiva. Comportamentos de agentes inalados, se ferromagnético, pode ser alterado através da imposição de forças magnéticas apropriadas <sup> 19. Dames et al. 20 demonstrou que é prático para segmentar partículas ferromagnéticas para áreas específicas em pulmões de ratinho. Ao embalar agentes terapêuticos com nanopartículas de óxido de ferro superparamagnético, a deposição de um pulmão de um rato sob a influência de um campo magnético forte foi significativamente aumentada em comparação com o outro pulmão 20.
As partículas foram assumidos como sendo esférico e variou de 150 nm a 30 um de diâmetro. A equação governante é 21:
(1) 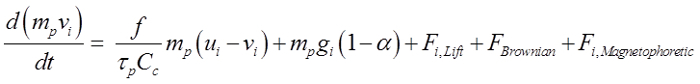
A equação acima descreve o movimento de uma partícula governado por força de arrasto, força gravitacional, Saffman elevador vigor 22, força browniano de nanopartículas e força magnetophoretic se colocado em um campo magnético. Aqui, v i é a velocidade da partícula, u i é a velocidade de fluxo, p é τo tempo de resposta das partículas, C c é o factor de correcção Cunningham, e α é a taxa de densidade de ar / partículas. Para orientar eficazmente os fármacos administrados por via intranasal à região olfactiva, é necessário que as forças aplicadas magnetophoretic a superar a inércia das partículas e força gravitacional. Neste estudo, um composto de 20% maghemite (γ-Fe 2 O 3, 4,9 g / cm 3) e 80% de agente activo foi assumido, o qual se obter uma densidade de aproximadamente 1,78 g / cm3 e uma permeabilidade relativa de 50. a selecção de γ-Fe 2 o 3 era devido ao seu baixo citotóxico. Ferro (3+) iões são amplamente encontradas no corpo humano e uma concentração de iões ligeiramente mais elevado não vai causar efeitos secundários significativos 23.
Protocol
Representative Results
Discussion
Um método de imagem de CFD acoplado foi apresentado neste estudo, que incorporou o desenvolvimento baseado em imagem modelo, engrenagem qualidade, simulação de fluxo de ar, e rastreamento de partículas magnéticas. Vários módulos de software foram implementadas para este fim, que incluiu funções de segmentação de imagens médicas, reconstrução / engrenagem de modelos das vias aéreas anatomicamente precisos, e simulações de fluxo de partículas. Usando este método numérico, desempenhos de três protocolo…
Declarações
The authors have nothing to disclose.
Acknowledgements
Este estudo foi financiado pela Central Michigan University Innovative Research Grant P421071 e Early Career Grant P622911.
Materials
| MIMICS 13 | Materialise Inc, Ann Arbor, MI | MR image segmentation | |
| Gambit | ANSYS Inc, Canonsburg, PA | Model development | |
| ANSYS ICEMCFD | ANSYS Inc, Canonsburg, PA | Meshing | |
| ANSYS Fluent | ANSYS Inc, Canonsburg, PA | Fluid and particle simulation | |
| COMSOL Multiphsics | COMSOL Inc, Burlington, MA | Magnetic particle tracing |
Referências
- Mistry, A., Stolnik, S., Illum, L. Nanoparticles for direct nose-to-brain delivery of drugs. Int. J. Pharm. 379 (1), 146-157 (2009).
- Alam, S., et al. Development and evaluation of thymoquinone-encapsulated chitosan nanoparticles for nose-to-brain targeting: a pharmacoscintigraphic study. Int. J. Nanomedicine. 7 (11), 5705-5718 (2012).
- Shi, H., Kleinstreuer, C., Zhang, Z. Laminar airflow and nanoparticle or vapor deposition in a human nasal cavity model. J. Biomech. Eng. 128 (5), 697-706 (2006).
- Si, X., Xi, J., Kim, J., Zhou, Y., Zhong, H. Modeling of release position and ventilation effects on olfactory aerosol drug delivery. Respir. Physiol. Neurobiol. 186 (1), 22-32 (2013).
- Si, X., Xi, J., Kim, J. Effect of laryngopharyngeal anatomy on expiratory airflow and submicrometer particle deposition in human extrathoracic airways. Open J. Fluid D. 3 (4), 286-301 (2013).
- Xi, J., Longest, P. W. Numerical predictions of submicrometer aerosol deposition in the nasal cavity using a novel drift flux approach. Int. J. Heat Mass Transfer. 51 (23), 5562-5577 (2008).
- Illum, L. Nasal drug delivery: new developments and strategies. Drug Discov. Today. 7 (23), 1184-1189 (2002).
- El Taoum, K. K., Xi, J., Kim, J. W., Berlinski, A. In vitro evaluation of aerosols delivered via the nasal route. Respir. Care. 60 (7), 1015-1025 (2015).
- Misra, A., Kher, G. Drug delivery systems from nose to brain. Curr. Pharm. Biotechnol. 13 (12), 2355-2379 (2012).
- Hoekman, J. D., Ho, R. J. Y. Effects of Localized Hydrophilic Mannitol and Hydrophobic Nelfinavir Administration Targeted to Olfactory Epithelium on Brain Distribution. Aaps Pharmscitech. 12 (2), 534-543 (2011).
- Corley, R. A., et al. Comparative Computational Modeling of Airflows and Vapor Dosimetry in the Respiratory Tracts of Rat, Monkey, and Human. Toxicol. Sci. 128 (2), 500-516 (2012).
- Shi, H., Kleinstreuer, C., Zhang, Z. Modeling of inertial particle transport and deposition in human nasal cavities with wall roughness. J. Aerosol Sci. 38 (4), 398-419 (2007).
- Kleinstreuer, C., Zhang, Z., Donohue, J. F. Targeted drug-aerosol delivery in human respiratory system. Annu. Rev. Biomed. Eng. 10 (4), 195-220 (2008).
- Kleinstreuer, C., Zhang, Z., Li, Z., Roberts, W. L., Rojas, C. A new methodology for targeting drug-aerosols in the human respiratory system. Int. J. Heat Mass Transfer. 51 (23), 5578-5589 (2008).
- Wilson, I. B. The deposition of charged particles in tubes, with reference to the retention of therapeutic aerosols in the human lung. J. Colloid Sci. 2 (2), 271-276 (1947).
- Wong, J., Chan, H. -. K., Kwok, P. C. L. Electrostatics in pharmaceutical aerosols for inhalation. Ther Deliv. 4 (8), 981-1002 (2013).
- Bailey, A. G. The inhalation and deposition of charged particles within the human lung. Journal of Electrostatics. 42 (1), 25-32 (1997).
- Xi, J., Si, X. A., Gaide, R. Electrophoretic particle guidance significantly enhances olfactory drug delivery: a feasibility study. PLoS ONE. 9 (1), e86593 (2014).
- Martin, A., Finlay, W. Alignment of magnetite-loaded high aspect ratio aerosol drug particles with magnetic fields. Aerosol Sci. Technol. 42 (4), 295-298 (2008).
- Dames, P., et al. Targeted delivery of magnetic aerosol droplets to the lung. Nature Nanotechnology. 2 (8), 495-499 (2007).
- Xi, J., Longest, P. W. Transport and deposition of micro-aerosols in realistic and simplified models of the oral airway. Ann. Biomed. Eng. 35 (4), 560-581 (2007).
- Longest, P. W., Xi, J. Effectiveness of direct Lagrangian tracking models for simulating nanoparticle deposition in the upper airways. Aerosol Sci. Technol. 41 (4), 380-397 (2007).
- Xi, J., Zhang, Z., Si, X. A., Yang, J., Deng, W. Optimization of magnetophoretic-guided drug delivery to the olfactory region in a human nose model. Biomech. Model. Mechanobiol. In. , (2015).
- Longest, P. W., Hindle, M., Das Choudhuri, S., Xi, J. X. Comparison of ambient and spray aerosol deposition in a standard induction port and more realistic mouth-throat geometry. J. Aerosol Sci. 39 (7), 572-591 (2008).
- Xi, J., et al. Design and Testing of Electric-Guided Delivery of Charged Particles to the Olfactory Region: Experimental and Numerical Studies. Curr. Drug Deliv. 13 (9), 1-15 (2015).
- Zhou, Y., Guo, M., Xi, J., Irshad, H., Cheng, Y. -. S. Nasal deposition in infants and children. Journal of aerosol medicine and pulmonary drug delivery. 27 (2), 110-116 (2014).
- Xi, J., Yuan, J. E., Si, X. A., Hasbany, J. Numerical optimization of targeted delivery of charged nanoparticles to the ostiomeatal complex for treatment of rhinosinusitis. Int. J. Nanomedicine. 10 (7), 4847-4861 (2015).

