Genizden İnhale İlaç Aerosollerin Pasif ve Aktif Kontroller ile Modelleme ve Koku Drug Delivery Simülasyonlar
Summary
This manuscript reviews the modeling and simulations of different protocols to deliver medications to the olfactory region in image-based nasal airway models. Multiple software modules are used to develop the anatomically accurate nose model, generate computational mesh, simulate nasal airflows, and predict particle deposition at the olfactory region.
Abstract
nörolojik hastalıkların tedavisinde doğrudan burun için-beyin ilaç uygulama pek çok avantajı vardır. Bununla birlikte, uygulama, doğrudan beyin bağlayan koku mukozaya son derece düşük uygulama randımanına (<% 1) ile sınırlıdır. Koku bölgeye daha etkin nörolojik ilaçlar sunmak için yeni teknikler geliştirmeye büyük önem taşımaktadır. Bu çalışmanın amacı simüle ve burun koku ilaç sunumunun iyileştirilmesi için sayısal bir platform geliştirmektir. Bir birleştiğinde görüntü CFD yöntemi görüntü tabanlı model geliştirme, kalite hasırlar, sıvı simülasyon ve manyetik parçacık izleme sentezlenmiş olduğu sunuldu. Bu yöntemde, üç burun içi verme protokolleri Performans sayısal değerlendirildi ve karşılaştırıldı. solunum manevraları, mıknatıs düzeni, manyetik alan şiddeti, ilaç salım konum ve koku dozaj üzerine parçacık boyutu Etkileri da sayısal olarak incelenmiştir.
simulations, biz (% 45 kadar) klinik olarak önemli koku dozaj mıknatıs düzeni ve seçici ilaç salım kombinasyonunu kullanarak mümkün olduğunu bulmuşlardır. doz 64 kat daha yüksek teslim olmadan duruma kıyasla magnetophoretic rehberlik durumunda tahmin edilmiştir. Bununla birlikte, koku bölgeye nazal inhaler aerosollerin hassas bir şekilde kılavuzlanması sayesinde magnetophoresis kararsız doğası, hem de koku hastaya dozajın, aygıttır, ve parçacık ile ilgili faktörler, yüksek hassasiyet zor olmaya devam etmektedir.
Introduction
İlaçların 1,2 etkin bir alımı ve hızlı hareket başlangıcı yol açan, kan-beyin bariyerini aşmak ve doğrudan beyin girebilirsiniz koku bölgeye teslim ilaçlar. Bununla birlikte, bu burun pompaları ve sprey gibi geleneksel nazal cihazlar nazal yol 3,4 ile koku bölgeye (<% 1), son derece düşük dozlar sağlamaktadır. Bu öncelikli olarak, dar, dolambaçlı geçiş yolları (Şekil 1) oluşan insan burnu karmaşık yapısının bir sonucudur. Koku bölge solunan havanın sadece çok küçük bir bölümü 5,6 ulaşabilir üstün meatus, yukarıda bulur. Ayrıca, geleneksel inhalasyon cihazları hedef alan 7 terapötik ajanlar taşımak için aerodinamik kuvvetler bağlıdır. onların serbest bırakıldıktan sonra parçacıkların hareketleri üzerinde daha fazla kontrol yoktur. Bu nedenle, bu parçacıkların, ve çökelme ağırlıklı olarak, başlangıç hızları ve salma konumları bağlıdır. gerekenkıvrık geniz yanı sıra parçacık kontrol eksikliği, ilaç partiküllerinin çoğunluğu ön burun içinde sıkışıp kalırlar ve koku bölgesini 8 ulaşamaz.
Burun cihazların birçok seçenek varken, bu özel olarak tasarlanmış hedeflenen koku teslimat için nadiren 7,9 olarak bildirilmiştir. Bunun tek istisnası, bir koku tercihli dağıtım cihazı geliştirmiş ve burun damlası ile karşı farelerde yüksek korteks-to-kan ilaç seviyeleri göstermiştir Hoekman Ho 10'dur. Bununla birlikte, insanlar için sıçanlarda çöktürmesi ölçekleme bu iki tür 11 arasındaki büyük anatomik ve fizyolojik farklılıklar dikkate alındığında, kolay değildir. koku teslimatlar için standart burun cihazların uyarlanmış sürümlerini kullanırken birçok sınırlamalar vardır. Bir birincil gerileme ilaçların sadece çok küçük bir kısmı ilaçlar girebilir oradan koku mukoza, teslim edilebilmesidirbeyin. Sayısal modelleme burundan uygulanan nanopartiküllerin az% 0.5 koku bölge 3,5 olarak yatırabilirsiniz öngördü. Biriktirme hızı mikrometre parçacıklarının 12 (0.007%) daha düşüktür. burun için-beyin dağıtım klinik olarak mümkün hale getirmek için, koku bırakma oranı önemli ölçüde iyileştirilmelidir.
koku sunumunun iyileştirilmesi için birkaç olası yaklaşımlar vardır mevcuttur. Bir yaklaşım bir bölgede yatırma parçacıklar çoğunlukla girişinde belirli bir bölgeden olduğundan Kleinstreuer ve ark., 13 önerdiği akıllı inhaler fikir, girişteki bazı alanlarda sadece onları serbest bırakarak hedef siteye parçacıklar teslim etmek mümkündür . Akıllı uygulama tekniği, geleneksel yöntemlere göre çok daha verimli bir akciğer teslim oluşturmak için gösterilmiştir. 13,14 akıllı dağıtım düşüncesi, i intranazal ilaç uygulama uygulanabilir varsayılmaktadırkoku mukozaya mprove dozlar. burun açılışında ve burun boşluğu içinde farklı derinliklerde farklı pozisyonlara parçacıklar bırakarak, koku teslim verimlilikleri ve ön burun azaltılmış ilaç atık mümkündür düzeldi.
Başka bir olası yöntem, aktif elektrikli ya da manyetik kuvvet gibi alan kuvvetlerinin çeşitli kullanarak burun boşluğu içindeki parçacık hareketini kontrol etmektir. Yüklü parçacıkların elektrik kontrol insan burun ve akciğerlerin 15-17 hedeflenmiş ilaç iletimi için önerilmiştir. Xi ve ark., 18 sayısal yüklü parçacıkların elektrik rehberlik performansı test edilmiş ve anlamlı koku doz geliştirilmiş öngördü. Benzer bir şekilde, uygun bir manyetik alan ile ferromanyetik ilaç parçacıklarının kılavuzlama da koku mukozaya parçacıklar hedef potansiyeline sahiptir. inhalasyon ajanlarının Davranışları, ferromanyetik eğer uygun manyetik kuvvetleri koyarak değiştirilebilir <sup> 19. Dames ve ark., 20 fare akciğerlerindeki belirli alanlara ferromanyetik parçacıklar hedef uygulama olduğunu göstermiştir. Süperparamanyetik demir oksit nanopartiküller ile terapötik ajanlar ambalaj ile, güçlü bir manyetik alanın etkisi altında bir fare tek akciğer birikim önemli ölçüde diğer akciğer 20 göre artış oldu.
Parçacıkların küresel olduğu kabul çapında ve 150 nm um ile 30 arasında değişmekteydi. Yöneten denklem 21'dir:
(1) 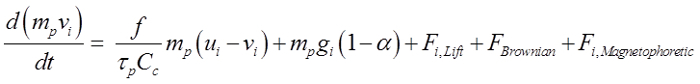
Yukarıdaki denklem bir manyetik alana yerleştirilir eğer sürtünme kuvveti, yerçekimi kuvveti, Saffman kaldırma kuvveti 22 nanopartiküller için Brownian kuvvet ve magnetophoretic kuvvet tarafından yönetilen bir parçacığın hareketini açıklar. Burada, v i parçacık hızı, u i τ p akış hızı olduğunuparçacık tepki süresi, C c Cunningham düzeltme faktörü, ve α hava / parçacık yoğunluğu oranıdır. etkili bir koku bölgeye intranazal yoldan ilaç kılavuz için, uygulanan magnetophoretic kuvvetler partikül atalet ve çekim kuvveti hem de üstesinden gelmek için gereklidir. Bu çalışmada,% 20 maghemit bir bileşik (γ-Fe 2 O 3, 4.9 g / cm3) ile, yaklaşık 1.78 g / cm3 arasında bir yoğunluğa ve 50 bir görece geçirgenliği elde aktif madde varsayılmıştır% 80. γ-Fe 2 O 3 seçim düşük sitotoksik nedeniyle oldu. Demir (3+) iyonları yaygın insan vücudunda bulunan ve biraz daha yüksek bir iyon konsantrasyonu önemli yan etkilere 23 neden olmaz.
Protocol
Representative Results
Discussion
Bir birleştiğinde görüntü CFD yöntemi görüntü tabanlı model geliştirme, kalite hasırlar, hava akımı simülasyon ve manyetik parçacık izleme dahil bu çalışmada sunuldu. Birden fazla yazılım modülleri tıbbi görüntülerin, yeniden / anatomik doğru havayolu modelleri bölümleme ve akış-parçacık simülasyonları segmentasyonu fonksiyonlarını içeren bu amaçla, uygulanmıştır. Bu sayısal yöntem kullanılarak, üç burun içi verme protokolleri performansları test edildi ve karşılaştı…
Declarações
The authors have nothing to disclose.
Acknowledgements
Bu çalışma Central Michigan Üniversitesi Yenilikçi Araştırma Bursu P421071 ve Erken Kariyer Hibe P622911 tarafından finanse edildi.
Materials
| MIMICS 13 | Materialise Inc, Ann Arbor, MI | MR image segmentation | |
| Gambit | ANSYS Inc, Canonsburg, PA | Model development | |
| ANSYS ICEMCFD | ANSYS Inc, Canonsburg, PA | Meshing | |
| ANSYS Fluent | ANSYS Inc, Canonsburg, PA | Fluid and particle simulation | |
| COMSOL Multiphsics | COMSOL Inc, Burlington, MA | Magnetic particle tracing |
Referências
- Mistry, A., Stolnik, S., Illum, L. Nanoparticles for direct nose-to-brain delivery of drugs. Int. J. Pharm. 379 (1), 146-157 (2009).
- Alam, S., et al. Development and evaluation of thymoquinone-encapsulated chitosan nanoparticles for nose-to-brain targeting: a pharmacoscintigraphic study. Int. J. Nanomedicine. 7 (11), 5705-5718 (2012).
- Shi, H., Kleinstreuer, C., Zhang, Z. Laminar airflow and nanoparticle or vapor deposition in a human nasal cavity model. J. Biomech. Eng. 128 (5), 697-706 (2006).
- Si, X., Xi, J., Kim, J., Zhou, Y., Zhong, H. Modeling of release position and ventilation effects on olfactory aerosol drug delivery. Respir. Physiol. Neurobiol. 186 (1), 22-32 (2013).
- Si, X., Xi, J., Kim, J. Effect of laryngopharyngeal anatomy on expiratory airflow and submicrometer particle deposition in human extrathoracic airways. Open J. Fluid D. 3 (4), 286-301 (2013).
- Xi, J., Longest, P. W. Numerical predictions of submicrometer aerosol deposition in the nasal cavity using a novel drift flux approach. Int. J. Heat Mass Transfer. 51 (23), 5562-5577 (2008).
- Illum, L. Nasal drug delivery: new developments and strategies. Drug Discov. Today. 7 (23), 1184-1189 (2002).
- El Taoum, K. K., Xi, J., Kim, J. W., Berlinski, A. In vitro evaluation of aerosols delivered via the nasal route. Respir. Care. 60 (7), 1015-1025 (2015).
- Misra, A., Kher, G. Drug delivery systems from nose to brain. Curr. Pharm. Biotechnol. 13 (12), 2355-2379 (2012).
- Hoekman, J. D., Ho, R. J. Y. Effects of Localized Hydrophilic Mannitol and Hydrophobic Nelfinavir Administration Targeted to Olfactory Epithelium on Brain Distribution. Aaps Pharmscitech. 12 (2), 534-543 (2011).
- Corley, R. A., et al. Comparative Computational Modeling of Airflows and Vapor Dosimetry in the Respiratory Tracts of Rat, Monkey, and Human. Toxicol. Sci. 128 (2), 500-516 (2012).
- Shi, H., Kleinstreuer, C., Zhang, Z. Modeling of inertial particle transport and deposition in human nasal cavities with wall roughness. J. Aerosol Sci. 38 (4), 398-419 (2007).
- Kleinstreuer, C., Zhang, Z., Donohue, J. F. Targeted drug-aerosol delivery in human respiratory system. Annu. Rev. Biomed. Eng. 10 (4), 195-220 (2008).
- Kleinstreuer, C., Zhang, Z., Li, Z., Roberts, W. L., Rojas, C. A new methodology for targeting drug-aerosols in the human respiratory system. Int. J. Heat Mass Transfer. 51 (23), 5578-5589 (2008).
- Wilson, I. B. The deposition of charged particles in tubes, with reference to the retention of therapeutic aerosols in the human lung. J. Colloid Sci. 2 (2), 271-276 (1947).
- Wong, J., Chan, H. -. K., Kwok, P. C. L. Electrostatics in pharmaceutical aerosols for inhalation. Ther Deliv. 4 (8), 981-1002 (2013).
- Bailey, A. G. The inhalation and deposition of charged particles within the human lung. Journal of Electrostatics. 42 (1), 25-32 (1997).
- Xi, J., Si, X. A., Gaide, R. Electrophoretic particle guidance significantly enhances olfactory drug delivery: a feasibility study. PLoS ONE. 9 (1), e86593 (2014).
- Martin, A., Finlay, W. Alignment of magnetite-loaded high aspect ratio aerosol drug particles with magnetic fields. Aerosol Sci. Technol. 42 (4), 295-298 (2008).
- Dames, P., et al. Targeted delivery of magnetic aerosol droplets to the lung. Nature Nanotechnology. 2 (8), 495-499 (2007).
- Xi, J., Longest, P. W. Transport and deposition of micro-aerosols in realistic and simplified models of the oral airway. Ann. Biomed. Eng. 35 (4), 560-581 (2007).
- Longest, P. W., Xi, J. Effectiveness of direct Lagrangian tracking models for simulating nanoparticle deposition in the upper airways. Aerosol Sci. Technol. 41 (4), 380-397 (2007).
- Xi, J., Zhang, Z., Si, X. A., Yang, J., Deng, W. Optimization of magnetophoretic-guided drug delivery to the olfactory region in a human nose model. Biomech. Model. Mechanobiol. In. , (2015).
- Longest, P. W., Hindle, M., Das Choudhuri, S., Xi, J. X. Comparison of ambient and spray aerosol deposition in a standard induction port and more realistic mouth-throat geometry. J. Aerosol Sci. 39 (7), 572-591 (2008).
- Xi, J., et al. Design and Testing of Electric-Guided Delivery of Charged Particles to the Olfactory Region: Experimental and Numerical Studies. Curr. Drug Deliv. 13 (9), 1-15 (2015).
- Zhou, Y., Guo, M., Xi, J., Irshad, H., Cheng, Y. -. S. Nasal deposition in infants and children. Journal of aerosol medicine and pulmonary drug delivery. 27 (2), 110-116 (2014).
- Xi, J., Yuan, J. E., Si, X. A., Hasbany, J. Numerical optimization of targeted delivery of charged nanoparticles to the ostiomeatal complex for treatment of rhinosinusitis. Int. J. Nanomedicine. 10 (7), 4847-4861 (2015).

