13.12:
효소
13.12:
효소
살아있는 유기체 안쪽에서는, 효소는 세포 대사에 관련되었던 많은 생화확적인 반응을 위한 촉매 역할을 합니다. 효소의 역할은 기판으로 복합체를 형성하여 생화학 반응의 활성화 에너지를 감소시키는 것입니다. 활성화 에너지의 낮추는 생화확적인 반응의 비율에 있는 증가를 선호합니다.
효소 결핍은 종종 생명을 위협하는 질병으로 이어질 수 있습니다. 예를 들어, 효소 G6PD(포도당-6-인산염 탈수소효소)의 결핍을 초래하는 유전적 이상은 NADPH를 세포에 공급하는 대사 경로에 악영향을 미친다.
이 신진 대사 통로에 있는 중단은 헤모글로빈 같이 그밖 효소 및 단백질에 손상을 일으키는 원인이 되는 적혈구에 있는 글루타티온을 감소시킬 수 있습니다. 헤모글로빈의 과도한 대사는 빌리루빈 수준을 형성하여 황달로 이어지며, 이는 심각해질 수 있는 조건입니다. 따라서 G6PD 결핍으로 고통받는 사람들은 글루타티온 결핍적혈구에 손상을 일으킬 수있는 화학 물질을 함유 한 특정 식품과 의약품을 피해야합니다.
효소 기능 및 구조
효소는 수행하는 특정 기능에 따라 다른 클래스로 그룹화됩니다. 예를 들어, 옥시도레덕타스는 레독스 반응에 관여하는 반면, 편입은 기능성 그룹의 전달을 촉매한다. ATP 가수분해와의 결합 형성에는 리구아제가 필요하며, 가수분해 반응과 이중 결합 형성은 각각 하이드로라제와 리아아즈에 의해 촉매처리됩니다. 이소머라제 효소는 일반적으로 이소성 화 반응을 촉매합니다.
효소는 일반적으로 활성 사이트를 소유. 이들은 효소 기판 복합체 또는 반응 중간체를 형성하기 위하여 특정 기질 (reactant 분자)에 결합하는 효소를 선호하는 변형을 가진 분자에 특정 지구입니다.
잠금 및 키 모델과 유도된 맞춤 모델인 두 모델이 활성 사이트의 작동을 설명하려고 시도합니다(그림 1). 가장 단순한 잠금 및 키 가설은 기판의 활성 부위와 분자 모양이 상호 보완적이라는 것을 시사합니다(그림 1a). 한편, 유도-맞춤 가설은 효소 분자가 기판과의 결합을 수용하기 위해 유연하고 모양을 변경한다는 것을 시사한다(도 1b).
그러나, 잠금 및 키 모델과 유도된 핏 모델 모두 효소가 특정 기판과만 결합할 수 있고 특정 반응만 촉매할 수 있다는 사실을 고려한다.
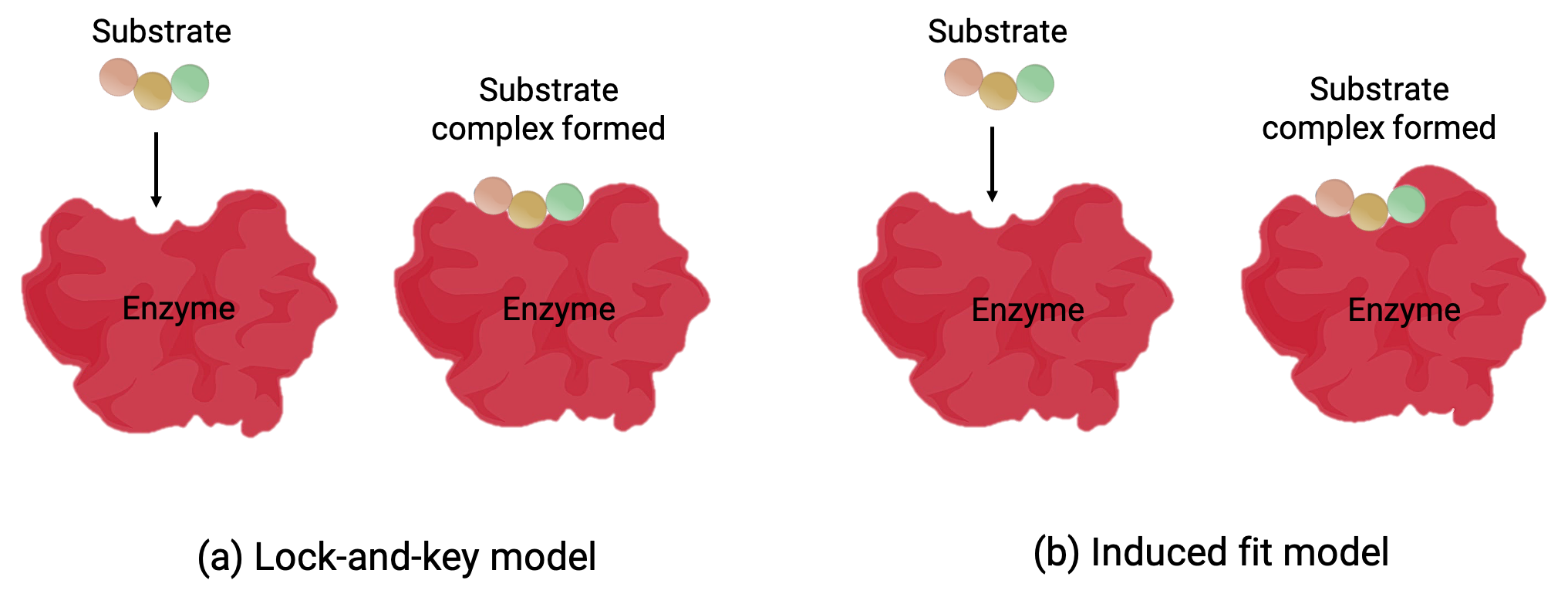
도 1 (a) 잠금 및 키 모델에 따르면 효소의 활성 부위의 모양은 기판에 딱 맞습니다. (b) 유도된 핏 모델에 따르면, 활성 부위는 다소 유연하며 기판과 결합하기 위해 모양을 변경할 수 있다.
효소 억제제
효소의 활성은 효소 억제 과정에 의해 중단될 수 있다. 효소 억제의 몇몇 일반적인 모형이 있습니다.
경쟁 억제 하는 동안, 분자 (자연 또는 합성) 기판 이외의 효소의 활성 사이트에 직접 결합. 기판에 대한 억제제의 구조적 및 화학적 유사성은 활성 부위에 대한 결합을 용이하게 한다. 이러한 경쟁 억제제는 따라서 기판과 경쟁하여 효소에 결합하지 못하게합니다. 대부분의 경우 기판 농도가 증가하면 경쟁 억제의 영향을 억제할 수 있습니다.
비 경쟁 억제에서, 분자 (천연 또는 합성) 알로스터에 결합 (다른) 효소의 영역, 그것의 활성 부위와 다른. 억제제 결합은 효소의 활성 부위에 형성 변화를 일으켜 효소의 반응을 촉매하는 효소의 능력이 감소합니다. 경쟁 억제와는 달리, 기판 농도의 증가는 비경쟁 억제의 억제 효과를 완화하지 않습니다.
이 텍스트의 일부는 Openstax, 화학 2e, 섹션 12.7: 촉매에서 채택됩니다.
