السريع خطوة واحدة الأنزيمية توليف وجميع المائيه تنقية طرهالوز النظائر
Summary
Trehalose analogues are emerging as important molecules for bio(techno)logical and biomedical applications. We describe an optimized protocol for enzymatically synthesizing and purifying trehalose analogues that is simple, efficient, fast, and environmentally friendly. Its application to the rapid production and administration of a probe for the detection of mycobacteria is demonstrated.
Abstract
معدلة كيميائيا إصدارات طرهالوز، أو نظائرها طرهالوز، لها تطبيقات في علم الأحياء والتكنولوجيا الحيوية، وعلم الأدوية، وغيرها من المجالات. على سبيل المثال، استخدمت نظائرها طرهالوز تحمل علامات كشف للكشف عن المتفطرة السلية، ويمكن أن تكون لها تطبيقات مثل الدرن وكلاء التصوير التشخيصي. كما يجري متابعة الإصدارات مستقرة هيدروليكيا من طرهالوز نظرا لقدرتها على استخدام مثل المحليات غير السعرات الحرارية وكلاء والسلامة البيولوجية. وعلى الرغم من جاذبية هذا الصنف من المركبات لمختلف التطبيقات، لا تزال إمكاناتها التي لم تتحقق نظرا لعدم وجود مسار قوي لإنتاجها. هنا، ونحن التقرير بروتوكول مفصلة لخطوة واحدة التوليف biocatalytic السريع والفعال للنظائرها طرهالوز أن يتجاوز المشاكل المرتبطة التركيب الكيميائي. من خلال الاستفادة من انزيم بالحرارة طرهالوز سينسيز (TreT) من مستحرة متقلبة القضيم، يمكن نظائرها طرهالوز يكون generatإد في خطوة واحدة من نظائرها الجلوكوز والجلوكوز يوريدين ثنائي فسفات في ارتفاع العائد (إلى تحويل الكمي) في 15-60 دقيقة. بروتوكول تنقية غير الكروماتوغرافي بسيط وسريع، والذي يتألف من غسيل الكلى تدور والتبادل الأيوني، ويمكن أن يحقق العديد من نظائرها طرهالوز التركيز المعروفة في محلول مائي في اقل من 45 دقيقة. في الحالات التي لا يزال غير المتفاعل الجلوكوز التناظرية، وتنقية الكروماتوغرافي من الناتج التناظرية طرهالوز لا يمكن أن يؤديها. وعموما، فإن هذا الأسلوب "الخضراء" منصة biocatalytic لتوليف المعجل وتنقية نظائرها طرهالوز تتسم بالكفاءة ويمكن الوصول إليها من غير الكيميائيين. لتجسد تطبيق هذه الطريقة، نحن تصف بروتوكول لتركيب، كل المائية تنقية، وإدارة المستندة إلى طرهالوز انقر الكيمياء التحقيق إلى المتفطرات، والتي استغرق أقل من 1 ساعة وتمكين الكشف عن مضان من المتفطرات. في المستقبل، ونحن نتصور أن من بين أوراسكوم تليكوم القابضةإيه التطبيقات، ويمكن تطبيق هذا البروتوكول إلى التوليف السريع لتحقيقات على أساس طرهالوز لتشخيص السل. على سبيل المثال، لم تدم طويلا نظائرها المعدلة النويدات المشعة طرهالوز (على سبيل المثال، 18 طرهالوز F معدلة) يمكن استخدامها لطرائق التصوير السريرية المتقدمة مثل التصوير المقطعي الطبقي-انبعاث البوزيترون (PET-CT).
Introduction
طرهالوز هو ديساكهارايد متناظرة غير الحد تتكون من اثنين من الأنصاف الجلوكوز التي انضم اليهم 1،1-α، السندات α غليكوزيدية (الشكل 1A). في حين طرهالوز غائب من البشر والثدييات الأخرى، وجدت عادة في البكتيريا والفطريات والنباتات واللافقاريات 1. الدور الأساسي للطرهالوز في معظم الكائنات الحية هو حماية ضد الضغوط البيئية، مثل جفاف 1. وبالإضافة إلى ذلك، بعض مسببات الأمراض البشرية تتطلب طرهالوز لالفوعة، بما في ذلك السل المتفطرة المسببة للمرض السل، الذي يستخدم طرهالوز كوسيط من الحيوي خلية مغلف وبوصفها لبنة لبناء السكرية المناعية 2.
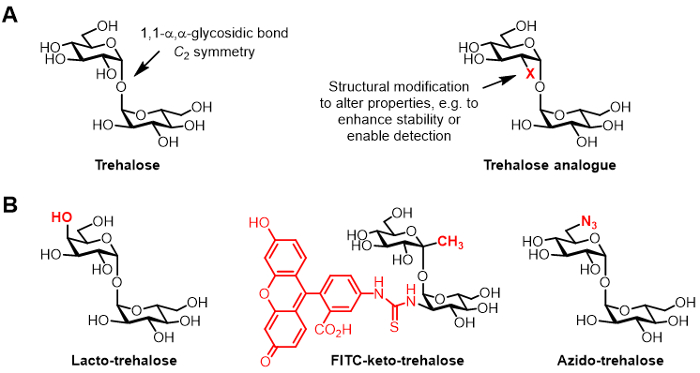
الشكل 1: طرهالوز ونظائرها طرهالوز. (A) هياكل من طرهالوز الطبيعي والتناظرية طرهالوز غير طبيعي، حيث X هو تعديل الهيكلي. (ب) أمثلة على نظائرها طرهالوز عنها في الأدبيات التي لها تطبيقات محتملة في biopreservation وbioimaging.
بسبب بنية فريدة من نوعها، والوظائف الفسيولوجية، وضعت طرهالوز اهتماما كبيرا للاستخدام في الحيوية (تكنو) منطقي والتطبيقات الطبية الحيوية 3. خصائص وقائية من طرهالوز لوحظ في nature- على سبيل المثال، القدرة ضرب بها للمساعدة في الحفاظ على الحياة في النباتات "القيامة" التي خضعت الجفاف الشديد 4 -have حفز الاستخدام الواسع النطاق في تطبيقات biopreservation. وقد استخدم طرهالوز للحفاظ على مجموعة واسعة من العينات البيولوجية، مثل الأحماض النووية والبروتينات والخلايا، والأنسجة 3. على سبيل المثال، يتم استخدام طرهالوز كمادة مضافة للاستقرار في عدد من المستحضرات الصيدلانية رقبعة هي على السوق، بما في ذلك العديد من الأجسام المضادة وحيدة النسيلة المضادة للسرطان 3. كذلك، يتم استخدام طرهالوز كمادة للتحلية في صناعة الأغذية، ويستخدم على نطاق واسع للحفاظ المنتج في كل من الصناعات الغذائية ومستحضرات التجميل. اعتماد طرهالوز لهذه الأنواع من التطبيقات التجارية كان محدودا في البداية بسبب عدم القدرة على الحصول على كميات كبيرة من طرهالوز النقي من مصادر طبيعية أو من خلال التوليف. ومع ذلك، تم مؤخرا بتطوير عملية الأنزيمية كفاءة لإنتاج الاقتصادي للطرهالوز من النشا، والتي حفزت استخدام التجاري الواسع 5.
كيميائيا تعديل مشتقات طرهالوز، المشار إليها هنا باسم نظائرها طرهالوز، اكتسبت اهتماما متزايدا لمختلف التطبيقات (هيكل عام هو مبين في الشكل 1A، أمثلة محددة من نظائرها طرهالوز هو مبين في الشكل 1B) 6. على سبيل المثال، شركة لاكتو-طرهالوز هو التناظرية طرهالوز مع واحدة من وحدات الجلوكوز في استبدال اللبن، وبالتالي مجموعتها الهيدروكسيل 4-موقف ديها تكوين فراغي مقلوب. شركة لاكتو-طرهالوز لديه نفس الخصائص استقرار كما طرهالوز لكن مقاوم للتحلل بفعل الإنزيمات في الأمعاء، مما يجعلها جذابة باعتباره غير السعرات الحرارية الغذائية المضافة 6 و 7.
مصلحتنا المجموعة في نظائرها طرهالوز يتعلق في المقام الأول إلى قيمتها بوصفها تحقيقات ومثبطات المتفطرة محددة. وضعت مجموعة باري وديفيس-كيتو طرهالوز التماثلية فلوريسئين مترافق، واسمه FITC-كيتو-طرهالوز، التي كانت تظهر لتسمية عملية الأيض جدار الخلية الحية من مرض السل م، مما كشف عن طريق مضان المجهر 8. تطوير المختبر Bertozzi أصغر azido-طرهالوز (TreAz) نظائرها التي يمكن تسمية عملية الأيض في جدار الخلية وتكون ديت لاحقاECTED باستخدام النقر كيمياء وتحليل مضان 9. وتشير هذه التطورات إلى إمكانية استخدام المجسات على أساس طرهالوز وكلاء التصوير التشخيصي لمرض السل. كما تم متابعة نظائرها طرهالوز باسم مثبطات م. السل بسبب قدرتها على تعطيل مسارات في البكتيريا التي لا غنى عنها لبقاء والفوعة 10 و 11 و 12.
وحتى الآن، فإن العقبة الرئيسية أمام تطوير نظائرها طرهالوز ل(تكنو) تطبيقات المنطقية والطبية الحيوية هي عدم وجود طرق الاصطناعية فعالة. وهما الطرق التقليدية لإنتاج نظائر طرهالوز تعتمد على التركيب الكيميائي (الشكل 2). ويتضمن أحد المسارات desymmetrization / تعديل طرهالوز الطبيعي، في حين ينطوي على الآخر بدءا من اللبنات أحادي السكاريد functionalized بشكل صحيح وأداء بالغليكوزيل الكيميائية لواقامة 1،1-α، السندات α غليكوزيدية. تلك الأساليب التي تم مؤخرا مناقشتها في مقالات المراجعة 13، 14، قد أثبتت فائدتها لإنجاز تركيب متعددة الخطوات كميات صغيرة من المنتجات الطبيعية التي تحتوي على طرهالوز المعقدة، مثل شحم سلفاتي-1 من السل م 15. ومع ذلك، كلا النهجين غير فعالة بشكل عام، تستغرق وقتا طويلا، لا يمكن الوصول إليها لغير الكيميائيين، وبالإضافة إلى ذلك، لا تعتبر أن تكون صديقة للبيئة. وبالتالي، لتجميع أنواع معينة من نظائرها طرهالوز، هذه الاستراتيجيات ليست مثالية.
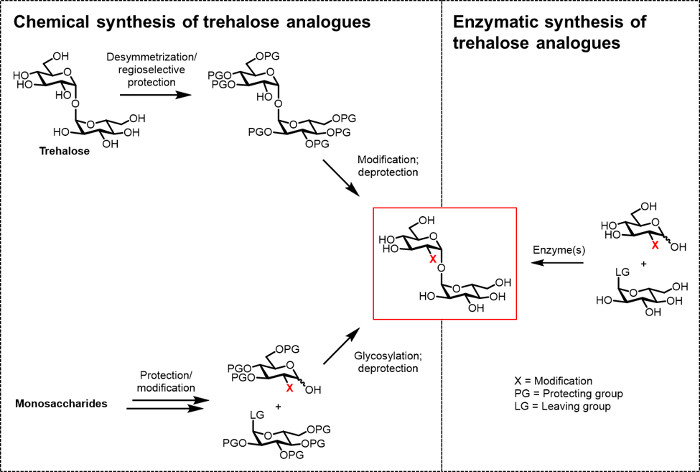
الشكل 2: النهج لتركيب طرهالوز التناظرية. نهج الكيميائية لتركيب طرهالوز التناظرية، كما هو موضح على اليسار، واستخدام إجراءات متعددة الخطوات التي تنطوي على بروتيك الصعبةخطوات نشوئها / deprotection، desymmetrization، و / أو بالغليكوزيل. التوليف الأنزيمية، كما هو موضح على اليمين، يستخدم إنزيم (ق) لتحويل stereoselectively بسيطة، ركائز غير المحمية إلى طرهالوز نظائرها في محلول مائي. بروتوكول الأنزيمية ذكرت هنا يستخدم إنزيم طرهالوز سينسيز (TreT) لتحويل نظائرها الجلوكوز وUDP الجلوكوز إلى نظائرها طرهالوز في خطوة واحدة. الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.
سيكون طريقا biocatalytic فعالة لنظائرها طرهالوز تسهيل الإنتاج، والتقييم، وتطبيق هذه الفئة الواعدة من الجزيئات. في حين أن عملية الأنزيمية التجارية لإنتاج طرهالوز 5 ليست قابلة للتكيف مع توليف نظائرها لأنه يستخدم النشا باعتبارها الركيزة، وهناك مسار آخر السكروزالطرق في الطبيعة التي يمكن استغلالها لتخليق التناظرية طرهالوز. ومع ذلك، والبحث في هذا المجال، الذي استعرض مؤخرا 6، كان محدودا. استخدم تقرير واحد طريقة مستوحاة من الإشريكية القولونية طرهالوز التخليق الحيوى الطريق للوصول إلى التماثلية الفلورية طرهالوز واحد من المقابلة الفلوري الجلوكوز. ومع ذلك، فإن هذا النهج يتطلب نظاما ثلاثة الانزيم الذي الكفاءة وعمومية 8 محدودة. وثمة نهج آخر أنه قد تم استكشافها هو استخدام فسفوريلاز طرهالوز (TREP) في الاتجاه المعاكس، من حيث المبدأ يسمح للتوليف خطوة واحدة من نظائرها طرهالوز من نظائرها الجلوكوز وسكر 1-فوسفات 6 و 16 و 17. على الرغم من أن هذا النهج قد وعد في المستقبل، على حد سواء قلب والاحتفاظ TrePs لديها حاليا عيوب لتخليق التناظرية. على سبيل المثال، TrePs عكس ديك بة باهظهجزيء nsive المانحة (β-D-الجلوكوز 1-الفوسفات) وTrePs الاحتفاظ لديها ضعف عائدات التعبير انزيم / الاستقرار ومحدود الاختلاط الركيزة. وستكون هناك حاجة تحسينات كبيرة (على سبيل المثال، عن طريق الهندسة انزيم) قبل تركيب التناظرية بوساطة TREP-هو عملي.
في الوقت الحاضر، فإن النهج الأكثر عملية لتركيب الأنزيمية من نظائرها طرهالوز هو استخدام طرهالوز سينسيز (TreT) الإنزيم الذي يحول الجلوكوز ويوريدين ثنائي الفوسفات (UDP) -glucose إلى طرهالوز في خطوة واحدة 6. بلغنا مؤخرا استخدام مستحرة متقلبة القضيم TreT-انزيم بالحرارة وأحادي الاتجاه 18 -to تجميع نظائرها طرهالوز من نظائرها الجلوكوز وUDP الجلوكوز (الشكل 3) 19. هذا الانزيم يعمل فقط في اتجاه الاصطناعية ويتجنب مشكلة تدهور طرهالوز وجدت في نظام TREP. هذه خطوة واحدة رد فعل قد يزيد عدد الجياعد أن تكتمل في 1 ساعة، وتم الوصول إلى مجموعة واسعة من نظائرها طرهالوز في ارتفاع العائد (إلى> 99٪ وفقا لما يحدده عالية الأداء اللوني السائل (HPLC)) من ركائز الجلوكوز التناظرية المتاحة بسهولة (انظر الجدول 1 في ممثل النتائج الجزء).
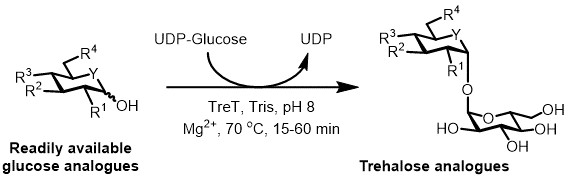
الشكل (3): تحفيز TreT التوليف خطوة واحدة من نظائرها طرهالوز. الانزيم TreT من القضيم T. يمكن أن تنضم stereoselectively نظائرها الجلوكوز المتاحة بسهولة وعن UDP الجلوكوز لتشكيل نظائرها طرهالوز في خطوة واحدة. R 1 -R 4 = متغير التعديل الهيكلي، على سبيل المثال azido-، fluoro-، ديوكسي، thio-، كيميائي فراغي، أو التعديلات النظائر. Y = متجانسة المتغيرة، على سبيل المثال الأكسجين أو الكبريت أو متجانسة المسمى isotopically.
هنا، ونحن نقدم الإعلانبروتوكول etailed لعملية التوليف TreT، بما في ذلك التعبير وتنقية TreT من كولاي، إلى أقصى حد TreT ظروف التفاعل، وتحسين طريقة تنقية التي نفذت تماما في المرحلة المائية. يتيح هذا البروتوكول تعديل التوليف المناسب والفعال وتنقية نظائرها طرهالوز متنوعة على نطاق شبه إعدادي (10-100 ملغ). نحن أيضا لشرح استخدام هذا البروتوكول لإعداد وإدارة التحقيق القائم على طرهالوز إلى المتفطرات في أقل من 1 ساعة، والتي مكنت من الكشف عن مضان السريع للخلايا المتفطرات.
Protocol
Representative Results
Discussion
نظائرها طرهالوز لديها القدرة على التأثير في مختلف المجالات، من الحفاظ على المواد الغذائية والأدوية لتشخيص وعلاج الالتهابات الجرثومية 6. طرق التركيب الكيميائي متعددة الخطوات الموجودة هي مفيدة لإنتاج نظائر طرهالوز معقدة مع مواقع متعددة من التعديل (على <e…
Disclosures
The authors have nothing to disclose.
Acknowledgements
This work was funded by a grant from the National Institutes of Health (R15 AI117670) to B.M.S and P.J.W, as well as a Cottrell College Scholar Award from the Research Corporation (20185) to P.J.W. L.M.M. was supported by a Provost’s Fellowship from CMU.
Materials
| LB agar | Research Products International | L24021 | |
| Ampicillin sodium salt | Sigma Aldrich | A9518 | |
| Luria broth | Research Products International | L24045 | |
| Terrific Broth | Research Products International | T15050 | |
| L-(+)-Arabinose | Sigma Aldrich | A3256 | |
| Phosphate-buffered Saline | GE Healthcare | SH30256 | |
| Imidazole | Sigma Aldrich | I5513 | |
| Sodium chloride | BDH | BDH9286 | |
| Sodium phosphate, | Fisher Scientific | S374 | |
| monobasic | |||
| Syringe filter, 0.45 µm | Fisher Scientific | 09719D | |
| Protease Inhibitor mini-tablets, EDTA-free | Thermo Scientific | 88666 | |
| HisTrap HP nickel affinity column, 5 mL | GE Healthcare | 17-5248-02 | |
| TRIS base ultrapure | Research Products International | T60040 | |
| Dialysis tubing, MWCO 12–14,000 | Fisher Scientific | 21-152-16 | |
| Glucose analogues | CarboSynth, | Examples of vendors that offer numerous glucose analogues | |
| Sigma Aldrich, | |||
| Santa Cruz Biotechnology, American Radiolabeled Chemicals | |||
| 6-Azido-6-deoxy glucopyranose (6-GlcAz) | CarboSynth | MA02620 | |
| UDP-Glucose | abcam Biochemicals | ab120384 | |
| Magnesium chloride hexahydrate | Fisher Scientific | M33 | |
| Amicon Ultra-15 centrifugal filter unit | EMD Millipore | UFC901008 | |
| Bio-Rex RG 501-X8 mixed-bed ion-exchange resin | Bio-Rad | 444-9999 | |
| Extra-Fine Bio-Gel P2 media | Bio-Rad | 150-4118 | |
| Glass-backed silica gel thin-layer chromatography plates | EMD Millipore | 1056280001 | |
| n-Butanol | Fisher Scientific | A399 | |
| Ethanol | Fisher Scientific | S25310A | |
| Sulfuric acid | Fisher Scientific | A300 | |
| Acetonitrile | EMD Millipore | AX0145 | |
| Deuterium oxide, 99.8% | Acros Organics | 351430075 | |
| Aminopropyl HPLC column | Sigma Aldrich | 58338 | |
| Bovine serum albumin | Sigma Aldrich | 5470 | |
| Para-formaldehyde | Ted Pella | 18505 | |
| Alkyne-488 | Sigma Aldrich | 761621 | |
| Sodium ascorbate | Sigma Aldrich | A7631 | |
| Tris[(1-benzyl-1H-1,2,3-triazol-4-yl)methyl]amine (TBTA) | Click Chemistry Tools | 1061 | |
| tert-Butanol | Sigma Aldrich | 360538 | |
| Dimethylsulfoxide | Sigma Aldrich | W387520 | |
| Copper(II) sulfate | Sigma Aldrich | C1297 | |
| Fluoromount-G mounting medium | Southern Biotechnology | 10001 |
References
- Elbein, A. D., Pan, Y. T., Pastuszak, I., Carroll, D. New insights on trehalose: a multifunctional molecule. Glycobiology. 13, 17-27 (2003).
- Tournu, H., Fiori, A., Van Dijck, P. Relevance of trehalose in pathogenicity: some general rules, yet many exceptions. PLoS Pathog. 9, 1003447 (2013).
- Ohtake, S., Wang, Y. J. Trehalose: Current use and future applications. J. Pharm. Sci. 100, 2020-2053 (2011).
- Adams, R. P., Kendall, E., Kartha, K. K. Comparison of free sugars in growing and desiccated plants of Selaginella lepidophylla. Biochem. Syst. Ecol. 18, 107-110 (1990).
- Kubota, M., Ohnishi, M. . Glycoenzymes. , (2000).
- Walmagh, M., Zhao, R., Desmet, T. Trehalose analogues: latest insights in properties and biocatalytic production. Int. J. Mol. Sci. 16, 13729-13745 (2015).
- Kim, H. -. M., Chang, Y. -. K., Ryu, S. -. I., Moon, S. -. G., Lee, S. -. B. Enzymatic synthesis of a galactose-containing trehalose analogue disaccharide by Pyrococcus horikoshii trehalose-synthesizing glycosyltransferase: Inhibitory effects on several disaccharidase activities. J. Mol. Catal. B: Enzym. 49, 98-103 (2007).
- Backus, K. M., et al. Uptake of unnatural trehalose analogs as a reporter for Mycobacterium tuberculosis. Nat. Chem. Biol. 7, 228-235 (2011).
- Swarts, B. M., et al. Probing the mycobacterial trehalome with bioorthogonal chemistry. J. Am. Chem. Soc. 134, 16123-16126 (2012).
- Rose, J. D., et al. Synthesis and biological evaluation of trehalose analogs as potential inhibitors of mycobacterial cell wall biosynthesis. Carbohydr. Res. 337, 105-120 (2002).
- Wang, J., et al. Synthesis of trehalose-based compounds and their inhibitory activities against Mycobacterium smegmatis. Bioorg. Med. Chem. 12, 6397-6413 (2004).
- Gobec, S., et al. Design, synthesis, biochemical evaluation and antimycobacterial action of phosphonate inhibitors of antigen 85C, a crucial enzyme involved in biosynthesis of the mycobacterial cell wall. Eur. J. Med. Chem. 42, 54-63 (2007).
- Sarpe, V. A., Kulkarni, S. S. Regioselective protection and functionalization of trehalose. Trends in Carbohydr. Res. 5, 8-33 (2013).
- Chaube, M. A., Kulkarni, S. S. Stereoselective construction of 1,1-alpha,alpha-glycosidic bonds. Trends in Carbohydr. Res. 4, 1-19 (2013).
- Leigh, C. D., Bertozzi, C. R. Synthetic studies toward Mycobacterium tuberculosis sulfolipid-I. J. Org. Chem. 73, 1008-1017 (2008).
- Chaen, H., et al. Efficient enzymatic synthesis of disaccharide, alpha-D-galactosyl-alpha-D-glucoside, by trehalose phosphorylase from Thermoanaerobacter brockii. J. Appl. Glycosci. 48, 135-137 (2001).
- Vander Borght, J., Soetaert, W., Desmet, T. Engineering the acceptor specificity of trehalose phosphorylase for the production of trehalose analogs. Biotechnol. Progr. 28, 1257-1262 (2012).
- Kouril, T., Zaparty, M., Marrero, J., Brinkmann, H., Siebers, B. A novel trehalose synthesizing pathway in the hyperthermophilic Crenarchaeon Thermoproteus tenax: the unidirectional TreT pathway. Arch. Microbiol. 190, 355-369 (2008).
- Urbanek, B. L., et al. Chemoenzymatic synthesis of trehalose analogues: rapid access to chemical probes for investigating mycobacteria. ChemBioChem. 15, 2066-2070 (2014).
- Rostovtsev, V. V., Green, L. G., Fokin, V. V., Sharpless, K. B. A stepwise Huisgen cycloaddition process: copper(I)-catalyzed regioselective “ligation” of azides and terminal alkynes. Angew. Chem. Int. Ed. 41, 2596-2599 (2002).
- Tornøe, C. W., Christensen, C., Meldal, M. Peptidotriazoles on solid phase: [1,2,3]-triazoles by regiospecific copper(I)-catalyzed 1,3-dipolar cycloadditions of terminal alkynes to azides. J. Org. Chem. 67, 3057-3064 (2002).
- Kalscheuer, R., Weinrick, B., Veeraraghavan, U., Besra, G. S., Jacobs, W. R. Trehalose-recycling ABC transporter LpqY-SugA-SugB-SugC is essential for virulence of Mycobacterium tuberculosis. Proc. Natl. Acad. Sci. U. S. A. 107, 21761-21766 (2010).

