Сочетание микрофлюидика и микрореологию определить реологических свойств мягкой материи во время неоднократных фазовых переходов
Summary
Мы показываем, изготовление и использование microfluidic устройство, которое позволяет несколько частиц, отслеживание измерений микрореологию изучить реологические эффекты неоднократные фазовых переходов на мягкой материи.
Abstract
Микроструктура мягкой материи напрямую влияет на реологические свойства макроскопических и может быть изменено факторами, включая коллоидных перегруппировки в ходе предыдущего этапа изменения и применяется при сдвиге. Чтобы определить масштабы этих изменений, мы разработали microfluidic устройство, что позволяет повторять фазовых переходов, индуцированных обмена окружающих жидкости и микрореологических характеристика ограничивая сдвига на образце. Эта техника является реология2мкг, сочетание микрофлюидика и микрореологию. Microfluidic устройство это двухслойная конструкция с симметричный вход потоков ввода пример камеры, что ловушки гель образца в месте в ходе обмена жидкости. Всасывания могут применяться далеко от камеры образец тянуть жидкостях в камеру образец. Реологические свойства материала характеризуются использованием нескольких частиц, отслеживания микрореологию (MPT). В МРТ флуоресцентный зонд частицы внедряются в материал и броуновское движение зондов записывается с помощью видео микроскопии. Отслеживается движение частиц и рассчитывается среднее квадрат перемещения (MSD). Урс связано с макроскопических реологические свойства, используя обобщенные Стоукс-Эйнштейна отношения. Фазы материала определяется сравнением для критических отдыха экспоненты, определяется с использованием время отверждения суперпозиции. Измерения волокнистый гель коллоидных проиллюстрировать полезность технику. Этот гель имеет нежный структуру, которая может необратимо изменено когда применяется сдвига. мкг2реология данных показывает, что материал неоднократно уравновешивает же реологических свойств после каждого этапа перехода, указав, что фазовых переходов не играют роль в микроструктурных изменения. Чтобы определить роль сдвига, образцы можно стриженый до инъекции в нашей microfluidic устройство. Реология2мкг широко применяется методика для характеризации мягкой материи, позволяя определение реологических свойств деликатный микроструктур в одном образце при фазовых переходов в ответ на неоднократные изменения в окружающих условий окружающей среды.
Introduction
Фазовые переходы в мягкой материи можно изменить структуру леса, которая имеет последствия в переработки и окончательной стабильности материала1,2,3. Характеристика мягких материалов во время динамического фазовых переходов предоставляет важную информацию о взаимосвязи между структурной эволюции и равновесная структура и реологические свойства. Например многие уход на дому продукты требуют изменения фазы во время использования потребителем. Кроме того в процессе производства, шагов обработки, включая разбавления и смешивания, может распространять сдвига, влияющих на реологические свойства и окончательной микроструктуры продукта. Понимание всей фазы изменения реологических свойств гарантирует, что продукт выполняет как конструировано. Кроме того если силы изменить начальную реология материала в процессе производства, фазовых переходов может принести непредвиденные и нежелательные результаты, изменения функции и эффективность. В точке критического гелеобразования, определяется как точки, где материал переход от решения связанных коллоиды или полимеров к охватывающих образец гель сети свойств материала резко изменить с незначительными изменениями в ассоциацию. Любые изменения в структуре в точке критического гель может повлиять на конечный продукт4. В ходе этих динамических переходов мягкие материалы имеют слабые механических свойств и измерений, которые используют классические экспериментальные методы можно в пределах измерения шума предел5,6,7. С учетом этого, методы, такие как микрореологию, который чувствителен в диапазоне низких модули (10-3 – 4 Па), используются для характеристики слабых зарождающегося гель во время динамической эволюции. Некоторые материалы чувствительны к изменениям в микроструктуры вследствие внешних сил, которое представляет собой проблему во время определения характеристик, как любой передачи материала или жидкости может повлиять на структуру и, в конечном счете, окончательный свойства материала. Чтобы избежать изменения микроструктуры материала, мы разработали microfluidic устройство, которое можно обменять природоохранных жидкость вокруг образца при сведении к минимуму сдвига. Путем обмена жидкости окружающей среды, изменения реологических свойств и микроструктуры измеряются при фазовых переходах с минимальным вкладом от сдвига. Устройство в сочетании с несколько частиц, отслеживание микрореологию (MPT) в технике называется мкг2реологии. Этот метод используется для количественного определения свойств материала во время последовательных фазовых геля в ответ на внешние движущей силой. Техника будет проиллюстрировано с помощью волокнистых коллоидных гель, гидрогенизированное касторовое масло (HCO)9,10,11.
Подмости гель может претерпеть изменения в ассоциации и диссоциации вследствие их образец среды12,13,,1415. Движущей силой для гелеобразования и деградации материал конкретными и должны быть адаптированы для каждого материала интерес. Реология мкг2может использоваться для характеризуют гель систем, которые реагировать на внешние стимулы, включая коллоидных и полимерные сети. Изменение рН, осмотическое давление или концентрации соли являются примерами движущих сил, которые могут вызвать изменения микроструктуры материала. К примеру HCO подвергается контролируемые фазовых переходов, создав градиент осмотического давления. Когда образец концентрированной HCO гель (4 wt % HCO) погружен в воду, ослабляют сил притяжения между коллоидных частиц, вызывающих деградацию. Кроме того когда разбавленный раствор HCO (0,125 wt % HCO) связывается с гидрофильной материала (упоминаемый как желеобразователь и состоит главным образом глицерин и ПАВ), привлекательной силы вернуться, вызывая гелеобразование. Этот гель системы будет использоваться для отображения операции устройства как инструмент для измерения последовательных фазовых переходов на одном образце9,10. Охарактеризовать эти леса гель во время динамические переходы и деликатный гель зарождающиеся структуры на критическом этапе перехода, мы используем MPT характеризовать эти материалы с высоким пространственно временным разрешением.
Микрореологию используется для определения свойств геля и структуры, особенно в критических перехода массива мягких материалов, в том числе коллоидных и полимерных гелей5,6,9,16. МРТ является пассивным микрореологических техника, которая использует видео микроскопии броуновского движения частиц флуоресцентного зонда, внедренные в образец записи. В пределах 1/10й пикселей с использованием классических отслеживания алгоритмы17,18точно намерены частиц позиции на протяжении всего видео. Ансамбль в среднем среднего квадрата смещения (MSD, (Δr2(t))) рассчитывается из этих траекторий частиц. Урс связано с свойств материала, например соблюдение ползучести, используя обобщенные Стоукс-Эйнштейна отношения17,19,20,21,22, 23. Состояние материала определяется путем вычисления логарифмической наклон кривой MSD как функция времени задержки, α,
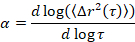
где t — время запаздывания и сравнивая его с критической отдыха экспоненты, n. n определяется с помощью время отверждения суперпозиции, документально технику, которая была изменена для анализа данных MPT Ларсен и Ферст6. Сравнения из n для α количественно определить состояние материала. При α > n материал является соль и когда α < n материал представляет собой гель. Предыдущая работа характеризуется HCO системы с помощью микрореологию для определения критических отдыха экспоненты9. Используя эту информацию, мы точно определить, когда материал перехода от геля соль во время эксперимента. Кроме того параметр негауссовских, αнг, могут быть рассчитаны для определения степени структурной неоднородности системы,
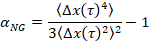
где Δx(t) — одномерный частиц движение в направлении x . С помощью MPT, мы может характеризовать одного фазового перехода, однако, характеризующих материалов с MPT microfluidic устройства, мы способны манипулировать окружающей жидкости и собирать данные нескольких фазовых переходов на выборке одного гель.
Этот microfluidic устройство предназначено для изучения важнейших переходы образец единого гель, который претерпевает изменения фазы в ответ на изменения в окружающей жидкости. Устройство обменивается жидкости вокруг образца, когда это либо в состоянии геля или соль, заблокировав образца в место, чтобы побудить фазового перехода при сведении к минимуму сдвига. Растворитель бассейна расположен непосредственно над образца камеры, которые соединены шесть симметрично расположенными подводящих каналов. Эта симметрия позволяет для обмена жидкости из растворителя бассейна в камеру образец при создании равных давления вокруг образца, фиксировать его на месте. Там было несколько исследований, которые используют этот метод для одной частицы и треппинг ДНК, но эта работа шкалы громкости от одной молекулы для образцов, которые являются приблизительно 10 мкл24,25,26. Этот уникальный дизайн также позволяет в реальном времени микрореологических характеристика во время фазовых переходов.
Реология2µ-это надежная техника, которая применима для многих систем мягкой материи. Метод, описанный в этом документе был разработан для коллоидных гели, но она может быть легко адаптирована для других материалов, таких как полимер или мицеллярный решения. С этой техникой, мы определить не только как фазовых переходов влияют на свойства материала равновесия, но шаги также как различные обработки может иметь долгосрочные эффекты на реологические эволюции материала и окончательный эшафот структуры и Свойства.
Protocol
Representative Results
Discussion
Два слоя microfluidic устройство (рис. 1) могут быть легко сделаны следующие документально microfluidic изготовление техники29. Стеклянные подставки добавляются к нижней части устройства для уменьшения колебательных влияние на движения зонда. Стеклянное скольжение яв?…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Финансовые средства для этой работы были предоставлены Procter & Gamble Co. и американского химического общества нефтяной научный фонд (54462-DNI7). Уведомление производится донорам американского химического общества нефтяной научный фонд для частичной поддержке этого исследования. Авторы хотели бы признать д-р Марко Caggioni для полезной дискуссии.
Materials
| 150 x 15 mm Petri Dish | Corning, Inc. | 351058 | |
| 75 x 50 x 0.15 mm glass slide | Fisher Scientific | Custom | |
| 75 x 50 x 1.0 mm glass slide | Fisher Scientific | 12-550-C | |
| 75 x 25 x 1.0 mm glass Slide | Fisher Scientific | 12-550-A3 | |
| 22 x 22 Glass cover slips | Fisher Scientific | 12-542-B | |
| Acetone, 99.5% | VWR Analytical | 67-64-1 | |
| Low intensity UV source | UVP | UVL-56 | |
| Chloroform, 99.9% | Fisher Chemical | C298-500 | |
| Cotton Swabs | Q-tips | 83289205 | |
| Ethanol, 90% | Fisher Chemical | A962-4 | |
| Fluoresbrite® YG Carboxylate Microspheres 0.50µm | Polysciences, Inc. | 15700-10 | |
| High-Intensity UV Lamp | Spectroline Corp. | SB-100P | |
| Hot plate | Corning, Inc. | PC-420 | |
| Hydrochloric Acid, 6N | Ricca Chemical Company | 3750-32 | |
| Methyltriethyoxysilane, 98% | Acros Organics | 174622500 | |
| Microcentrifuge | Eppendorf | 5424 | |
| Plasma cleaner | Harrick Plasma, Inc. | PDC-32G | |
| Polydimethylsiloxane (PDMS) | Robert McKwown Company | 2065622 | |
| Sonicator | Branson, Emerson Electric | 1800 | |
| Steel connectors, ID 0.023 inch | New England Small Tube Corp. | Custom | |
| Tetraethoxysilane, 98% | Alfa Aesar | A14965 | |
| Thiol-ene Resin (UV curable) | Norland Products, Inc. | NOA81 | |
| Transparency | Staples Inc. | 21828 | |
| Tygon tubing, ID 1/32 inch | McMaster-Carr | E-3603 | |
| Vacuum oven | Fisher Scientific | 282A | |
| Biopsy punch 8 mm | World Precision Instruments | 504535 | |
| Bioposy punch 0.5 mm | World Precision Instruments | 504528 | |
| Syringe, 30 mL | BD | 309659 | |
| Syringe, 3 mL | BD | 309651 | |
| Needle, 18 gauge | BD | 305195 | |
| Microcentrifuge tube, 1.5 mL | Eppendorf | 22-36-320-4 | |
| High-speed Camera | Vision Research | Miro M120 | |
| Microscope | Carl Zeiss AG | Zeiss Observer, Z1 | |
| Syringe pump | New Era Pump Systems | NE-300 | |
| Hydrogenated castor oil | Procter & Gamble | N/A | |
| Afício MP 6002 Printer | Ricoh Company, Ltd. | 415877 |
References
- Mitchell, P. Microfluidics-downsizing large-scale biology. Nat. Biotech. 19, 717-721 (2001).
- Haber, C. Microfluidics in commercial applications; an industry perspective. Lab Chip. 6, 1118-1121 (2006).
- Whitesides, G. M. The origins and the future of microfluidics. Nature. 442, 368-373 (2006).
- Huang, X., Raghavan, S. R., Terech, P., Weiss, R. G. Distinct kinetic pathways generate organogel networks with contrasting fractality and thixotropic properties. J. Am. Chem. Soc. 128, 15341-15352 (2006).
- Larsen, T. H., Schultz, K. M., Furst, E. M. Hydrogel microrheology near the liquid-solid transition. Korea-Aust. Rheol. J. 20, 165-173 (2008).
- Larsen, T. H., Furst, E. M. Microrheology of the liquid-solid transition during gelation. Phys. Rev. Lett. 100, 146001 (2008).
- Schultz, K. M., Baldwin, A. D., Kiick, K. L., Furst, E. M. Rapid rheological screening to identify conditions of biomaterial hydrogelation. Soft Matter. 5, 740-742 (2009).
- Switzer, L. H., Klingenberg, D. J. Flocculation in simulations of sheared fiber suspensions. Int. J. Multiph. Flow. 30, 67-87 (2004).
- Wehrman, M. D., Lindberg, S., Schultz, K. M. Quantifying the dynamic transition of hydrogenated castor oil gels measured via multiple particle tracking microrheology. Soft Matter. 12, 6463-6472 (2016).
- Wehrman, M. D., Milstrey, M. J., Lindberg, S., Schultz, K. M. Using µ2rheology to quantify rheological properties during repeated reversible phase transitions of soft matter. Lab Chip. 17, 2085-2094 (2017).
- Wehrman, M. D., Lindberg, S. E., Schultz, K. M. Impact of shear on the structure and rheological properties of a hydrogenated castor oil colloidal gel during dynamic phase transitions. J. Rheol. , (2018).
- Loh, X. J. Dual-responsive “reversible micelles”. J. Appl. Polym. Sci. 127, 992-1000 (2013).
- Kern, F., Zana, R., Candau, S. J. Rheological properties of semidilute and concentrated aqueous solutions of cetyltrimethylammonium chloride in the presence of sodium salicylate and sodium chloride. Langmuir. 7, 1344-1351 (1991).
- Trappe, V., Prasad, V., Cipelletti, L., Segre, P. N., Weitz, D. A. Jamming phase diagram for attractive particles. Nature. 411, 772-775 (2001).
- Philipse, A. P., Wierenga, A. M. On the density and structure formation in gels and clusters of colloidal rods and fibers. Langmuir. 14, 49-54 (1998).
- Schultz, K. M., Bayles, A. V., Baldwin, A. D., Kiick, K. L., Furst, E. M. Rapid, high resolution screening of biomaterial hydrogelators by mu2rheology. Biomacromolecules. 12, 4178-4182 (2011).
- Crocker, J. C., Grier, D. G. Methods of digital video microscopy for colloidal studies. J. Colloid Interface Sci. 179, 298-310 (1996).
- Mason, T. G. Estimating the viscoelastic moduli of complex fluids using the generalized Stokes–Einstein equation. Rheol. Actac. 39, 371-378 (2000).
- Mason, T. G., Ganesan, K., van Zanten, J. H., Wirtz, D., Kuo, S. C. Particle tracking microrheology of complex fluids. Phys. Rev. Lett. 79, 3282-3285 (1997).
- Mason, T. G., Weitz, D. A. Optical measurements of frequency-dependent linear viscoelastic moduli of complex fluids. Phys. Rev. Lett. 74, 1250-1253 (1995).
- Squires, T. M., Mason, T. G. Fluid mechanics of microrheology. Annu. Rev. Fluid Mech. 42, 413-438 (2010).
- Gittes, F., Schnurr, B., Olmsted, P. D., MacKintosh, F. C., Schmidt, C. F. Microscopic viscoelasticity: shear moduli of soft materials determined from thermal fluctuations. Phys. Rev. Lett. 79, 3286-3289 (1997).
- Mai, D. J., Brockman, C., Schroeder, C. M. Microfluidic systems for single DNA dynamics. Soft Matter. 8 (41), 10560-10572 (2012).
- Tanyeri, M., Ranka, M., Sittipolkul, N., Schroeder, C. M. A microfluidic-based hydrodynamic trap: design and implementation. Lab Chip. 11, 1786-1794 (2011).
- Lee, J. S., Dylla-Spears, R., Teclemariam, N. P., Muller, S. J. Microfluidic four-roll mill for all flow types. Appl. Phys. Lett. 90, 074103 (2007).
- Crocker, J. C., Grier, D. G. Methods of digital video microscopy for colloidal studies. J. Colloid Interface Sci. 179 (1), 298-310 (1996).
- Mason, T. G., Weitz, D. Optical measurements of frequency-dependent linear viscoelastic moduli of complex fluids. Phys. Rev. Lett. 74 (7), 1250 (1995).
- Schultz, K. M., Furst, E. M. High-throughput rheology in a microfluidic device. Lab on a chip. 11, 3802-3809 (2011).
- Abate, A. R., Lee, D., Do, T., Holtze, C., Weitz, D. A. Glass coating for PDMS microfluidic channels by sol-gel methods. Lab Chip. 8, 516-518 (2008).
- Happel, J., Brenner, H. . Low Reynolds Number Hydrodynamics: with special applications to particulate media. , (1965).

