Fremstilling af amyloid-β-udskilning af Alginat-Mikroperler til brug ved modellering af Alzheimers sygdom
Summary
Denne protokol illustrerer en celle indkapsling metode ved hurtig fysisk gelering af alginat at immobilisere celler. Opnåede mikroperler tillader kontrolleret og vedvarende sekretion af amyloid-β over tid og kan anvendes til at studere virkningerne af udskillet amyloid-β i in vitro-og in vivo-modeller.
Abstract
Ifølge amyloid Cascade hypotese, den tidligste udløsende faktor i udviklingen af Alzheimers sygdom (AD) er ophobning af giftige amyloid-β (Aβ) fragmenter, i sidste ende fører til de klassiske egenskaber af sygdommen: amyloid plaques, neurofibrillære tangles og synaptisk og neuronal tab. Manglen på relevante ikke-transgene prækliniske modeller, der afspejler sygdomsprogression, er en af de vigtigste faktorer, der hindrer opdagelsen af effektive lægemiddelbehandlinger. Med henblik herpå har vi udviklet en protokol til fremstilling af alginat-mikroperler, der indeholder amyloid-udskilnings celler, som er nyttige til undersøgelse af virkningerne af kronisk Aβ-produktion.
Ovarieceller fra kinesisk hamster, der tidligere var transficeret med et humant APP-gen, som udskilning Aβ (dvs. 7PA2 celler), blev anvendt i dette studie. En tredimensionel (3D) in vitro model for vedvarende frigivelse af Aβ blev fremstillet ved indkapsling af 7PA2 celler i alginat. Processen blev optimeret til at målrette en perle diameter på 500-600 μm for yderligere in vivo undersøgelser. Optimering af 7pa2 celle indkapsling i alginat blev udført ændre fabrikations parametre, fx alginat koncentration, gel flow rate, elektrostatisk potentiale, hoved vibrationsfrekvens, gelerings løsning. Niveauer af udskilt Aβ blev analyseret over tid og sammenlignet mellem alginat perler og standard cellekultur metoder (op til 96 h).
En koncentration på 1,5 x 106 7pa2 celler/ml og en alginatkoncentration på 2% (w/v) bufferet med Hepes og efterfølgende gelering i 0,5 M calciumchlorid i 5 min blev fundet for at fremstille de mest stabile mikroperler. Fremstillede mikroperler var 1) af ensartet størrelse, 2) med en gennemsnitlig diameter på 550 μm, 3) indeholdende omkring 100-150 celler pr. mikroperle og 4) i stand til at udskilte Aβ.
Afslutningsvis, vores optimerede metode til produktion af stabile alginat mikroperler indeholdende amyloid-producerende 7PA2 celler kan gøre det muligt modellering af vigtige aspekter af AD både in vitro og in vivo.
Introduction
Modellering neurodegenerative sygdomme er udfordrende på grund af den komplekse og indviklede karakter af hjernen. I Alzheimers sygdom (AD), det progressive tab af synaptisk funktion og død af neuroner menes at være en downstream effekt af vedvarende overproduktion og ophobning af amyloid beta (Aβ) peptider efter unormal behandling af amyloid forløber protein (APP) i henhold til amyloid Cascade hypotese1.
For at forstå mekanismerne i denne amyloid-induceret patologi og for at hjælpe med at identificere nye behandlingsmål har forskerne udviklet forskellige in vivo prækliniske modeller. En kategori af modeller anvender en bolt injektion af et syntetisk Aβ peptid i rotte hjernen2,3,4. Den vigtigste begrænsning af sådanne modeller er, at de er afhængige af en enkelt-punkt eller gentagne behandlinger med Aβ peptider i høje koncentrationer deponeret alle på én go. Dette er uforeneligt med den kroniske, vedvarende karakter af frigivelsen af Aβ i sygdom5. En anden kategori af in vivo-modeller er transgene dyremodeller, der udtrykker en eller flere genetiske mutationer i forbindelse med sygdommens familiale variationer6,7,8,9, 10. da familial annonce dog kun tegner sig for mindre end 5% af alle Alzheimers tilfælde11, er relevansen af disse modeller i at oversætte til sporadisk annonce hos mennesker tvivlsom12. En anden ulempe ved den transgene tilgang er den accelererede Aβ dannelse fra fødslen, hvilket udmønter sig i underskud i kognitiv funktion og patologiske ændringer for hurtigt og aggressivt at ligne sygdomsprogression i sporadiske AD hos patienter12 . For eksempel, 5x FAD model producerer plaques i så lidt som 1,5 måneder13.
Interessant, begge disse kategorier resulterer i ændringer i kognitiv funktion af relevans for ad forskning2,3,4,5,6, og nogle gange er de ledsaget af fremkomsten af patologiske kendetegn af sygdommen, såsom amyloid plaques6,8, Tau fosforylering6,7 og/eller synaptisk og neuronal tab7,9, 14. Men mens disse typer af modeller kan give os et indblik i virkningerne af høje niveauer af amyloid i hjernen, som ofte er forbundet med senere stadier af AD, de undlader at afspejle de tidligere ændringer udstillet som reaktion på den kroniske og vedvarende eksponering for Aβ peptid12, såsom ændret ekspression af synaptiske markører15 og komponenter i den ekstracellulære matrix16. Derfor er der stadig et behov for at skabe en kronisk model, der mere præcist illustrerer virkningerne af vedvarende Aβ sekretion på in vivo kognition og illustrerer ændringer i patologi.
Til dette formål har vi udviklet et system, der tillader konstant, vedvarende sekretion af Aβ på en kontrolleret måde ved at immobilisere amyloid-udskilning af celler inden for hydrogel-mikroperlerne, som efterfølgende kan implanteres i den voksne rotte hjerne for at modellere aspekter af sporadisk annonce.
Alginat var det udvalgte biomateriale, da det er biokompatibelt og ikke inducerer nogen bivirkninger, når det implanteres i vivo17. Celle indkapsling i alginat silicagelrogeler er blevet veletableret i løbet af de sidste fire årtier. Det første eksempel på dets oversættelse til klinikken blev rapporteret til behandling af type 1 diabetes mellitus17. Den tidligste rapport om vellykket indkapsling af Holme af Langerhans stammer tilbage til 1980. Transplantation af mikroperler indeholdende insulin-udskilning celler revolutionerede behandlingsmuligheder for diabetiske patienter, da det restaureret pancreas funktion, eliminerer behovet for insulin injektion terapi18. Disse værker rapporterer om, hvordan celle indkapsling kan beskytte dem mod ydre belastninger, uanset om de er mekaniske eller kemiske. Faktisk, alginat perler fungere som en barriere og isolere celler fra det omgivende miljø bevare deres fænotype, samtidig give tilstrækkelig adgang til de omgivende medier for næringsstoffer og clearance af cellulære biprodukter19. Desuden, brugen af alginat tillader matching af mekaniske egenskaber af blødt væv20. Alginat silicagelrogeler kan indstilles til at have en stivhed på 1-30 kPa, ved blot varierende alginat koncentration og Cross-Linking tæthed20,21. Dette er et væsentligt aspekt, ikke kun for at opretholde det fænotypiske udtryk for indkapslede celler in vitro, men også for at undgå eventuelle inflammatoriske virkninger efter engraftment in vivo22.
I denne protokol, 7pa2 celler-en kinesisk hamster ovarie cellelinje, der er stabilt transficeret med en menneskelig app V717F muteret gen23 -anvendes. Disse celler producerer kontinuerligt katalytiske produkter af app, herunder Aβ1-4224,25, og er blevet brugt til at generere Aβ som et alternativ til syntetisk produktion i prækliniske, akutte in vivo-studier26. Vi beskriver en fabrikationsmetode til immobilisering af 7PA2-celler inden for “bløde” alginat-mikroperler, der er designet til at tillade vedvarende sekretion af biomolekyler. Som et bevis på koncept, rapporterer vi om frigivelsen af Aβ1-42 peptid over tid. Det alginat, der anvendes, er en alginat med lav viskositet med en molekylvægt på 120000-190000 g/mol og et mannuronært til guluronisk forhold på 1,56 (M/G).
I yderligere undersøgelser kan disse mikroperler sikkert transplanteres i områder af rotte hjernen af relevans for AD (f. eks hippocampus) at studere virkningerne af kronisk Aβ sekretion på adfærd in vivo og patologi ex vivo. Desuden kan dette system anvendes til at undersøge virkningerne af kronisk Aβ-frigivelse i in vitro-og ex vivo-applikationer. For eksempel, 7PA2-holdige alginat mikroperler kan være co-dyrket in vitro med neuronal eller astrocytiske kulturer til at vurdere virkningerne af kronisk Aβ eksponering på cellulære mekanismer forbundet med AD. Desuden kan denne metode anvendes til at undersøge forholdet mellem kronisk Aβ produktion og langsigtede potensering i ex vivo Elektrofysiologi.
Højdepunktet i denne protokol er fremstillings metodens modularitet og fleksibilitet, som gør det muligt at fremstilling af alginat perler med en måldimension ved finjustering af fabrikations parametrene. Afhængigt af applikationen kan protokollen justeres for at opnå skræddersyede mål med hensyn til mikrovulst størrelse, tæthed af de indkapslede celler og mikrovulst stivhed. Denne protokol kan bruges til indkapsling af en række forskellige celletyper, udvikle mere relevante tredimensionelle (3D) in vitro-modeller til at studere forskellige patologier. Vi rapporterede for nylig om, hvordan alginat-indkapslede celler kan bruges til at modellere tidlige stadier af kræft progression20.
Konceptet med indkapsling proces er baseret på ekstrudering af en laminar stråle af celler suspenderet i alginat opløsning gennem en dyse. Et vibrerende hoved forstyrrer strålen med en kontrolleret frekvens, der resulterer i lige store alginat-baserede dråber. En ekstern elektrisk felt tillader adskillelse af de dannede alginat-baserede dråber, som ved kontakt med en opløsning beriget i Divalente ioner, såsom calcium ioner, kan hurtigt kryds-link, bevare deres sfæriske form. Inkubation i gelations opløsningen giver mulighed for dannelse af sfæriske mikroperler, der indeholder celler inden for en homogen fysisk hydrogel27. Target størrelse af mikroperler og alginat silicagelrogeler tillader næringsstoffers og ilt udveksling med cellekultur medier i lange perioder (uger). Figur 1 A viser en skematisk gengivelse af det anvendte indkapsling apparat (figur 1B).
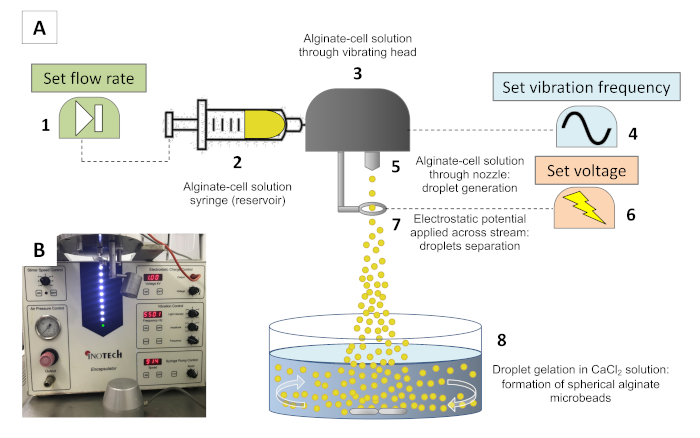
Figur 1 : Indkapsling system. (A) skematisk gengivelse af indkapsling systemet. En alginat-cellesuspension indlæses i en sprøjte (2) og fodres gennem et reservoir ved en ekstruderinghastighed indstillet ved sprøjtepumpe (1). I reservoiret vibrerer en vibrations hat (3) med en frekvens, der er indstillet af en bølgeform generator (4) for at forstyrre strømmen med lige store intervaller, der danner samme størrelse dråber. Da opløsningen fodres gennem en dyse (5), og der dannes dråber, påføres et elektrostatisk potentiale på tværs af en elektrode (7), som indstilles af en spændings generator (6), som let oplader overfladen af dråberne, så strømmen kan spredes som følge af frastøde elektrostatiske kræfter. Som dråber engagere sig med gelering bad (8), ca2 +-drevet Cross-Linking af alginat resultater i dannelsen af sfæriske mikroperler. B) fotografi af indkapmen før fremstilling af alginat-mikroperler. Venligst klik her for at se en større version af dette tal.
Mikroperlens størrelse kan ændres afhængigt af den tilsigtede anvendelse. For at kontrollere størrelsen af mikroperlen justeres de forskellige parametre, der er skitseret i figur 1A og i protokollen, tilsvarende. Den indvendige diameter af den anvendte dyse har en væsentlig indvirkning på størrelsen af dråberne; yderligere justering af indkapsling parametre, nemlig ekstrudering hastighed, vibration frekvens og spænding, er nøglen til at opnå en ensartet størrelsesfordeling. Tabel 1 skitserer, hvordan de forskellige parametre kan ændre størrelsen af mikroperler opnået med dette system.
| Parameter | Dyse størrelse | Vibrationsfrekvens | Strømningshastighed | Elektrode spænding |
 |
 |
 |
 |
|
| Perle størrelse |
 
|
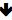 |
 |
– |
Tabel 1: Fabrikations parametre og deres indflydelse på mikroperlens størrelse. Tabellen illustrerer, hvordan hver parameter kan påvirke den resulterende størrelse af fremstillede mikroperler, uanset dysen og viskositeten af den anvendte opløsning.
Protocol
Representative Results
Discussion
Den metode, der er skitseret i denne artikel, er nyttig til indkapsningceller, der opnår en smal størrelsesfordeling af alginat-mikroperler27. Det giver også fordelen af voksende celler i et immuno-isoleret miljø17,19, beskytte dem mod ekstern stress. Desuden, indkapsling af celler i alginat nøjere efterligner fysiologiske forhold, specielt med hensyn til celle-til-celle interaktioner og matrix stivhed20. Disse faktorer er alle særligt afgørende for efterfølgende anvendelse i relevante anvendelser, såsom in vivo engraftment, der udelukker potentielle immunreaktioner i det omgivende væv17. Desuden er en stor fordel ved denne protokol den nemme mulighed for at tilpasse sig efter anvendelse af renter: det er muligt at ændre protokollen og optimere parametrene for fabrikation af større eller mindre, og blødere eller stivere perler. Den beskrevne metode bruges til at fremstille perler, der er små nok til at blive injiceret med minimalt invasive metoder, og tilstrækkeligt store nok til at være vært for en række celler og give en tilstrækkelig frigivelse af Aβ til at resultere i observerbare adfærdsmæssige og patologiske virkninger ved injektion i dyremodeller.
Succesen med denne protokol afhænger af en række kritiske trin. Omhyggelig celle håndtering og optimale celledyrkning teknikker er vigtige for at opretholde cellernes levedygtighed og funktion20,28. Ved hjælp af standard dyrkningsbetingelser sikrer bevarelsen af normal funktion af 7PA2 celler, som observeret. Dette tillader en lignende Release profil for Aβ1-42 fra indkapslede celler sammenlignet med 2D kulturer. For at protokollen skal fungere optimalt, garanterer en alginat-opløsning med lav viskositet desuden bedre resultater sammenlignet med en alginat-opløsning med høj viskositet. Dette sikrer, at en homogen laminar jet ekstruderes gennem dysen og en jævn fordeling af celler inden for matrixen af de fremstillede perler27. Materialer, der anvendes til indkapsling af celler skal have en meget hurtig gelering mekanisme, tillader fastholdelse af form.
Et andet kritisk skridt i denne protokol er håndteringen af fabrikerede mikroperler efter gelering. Her viser vi hentning af mikroperler ved hjælp af en stor blænde plastik pipette til at overføre perlerne. Alternativt kan hælde calciumchloridopløsningen, der indeholder mikroperlerne i et mesh-filter, bruges til perle udtagning. En stor (5, 10 eller 25 mL) serologisk pipette kan bruges til at tegne mikroperlerne og derefter vaskes gennem maske filteret i stedet for at hælde. Fordelen ved dette er en højere tillid til steriliteten af proceduren i forhold til hælde. Men af begrænsningerne er, at nogle perler kan blive forvrænget, hvis de komprimeres af pipetten, ud over at risikere et lavere udbytte, hvis en stor del af mikroperler ikke er reddet.
Denne fremgangsmåde er blevet brugt til at indkapslede forskellige cellelinjer til model og studere forskellige sygdomme (f. eks. frigivelse af insulin fra indkapslet Pankreatisk ø). Det nye ved vores tilgang er engraftment af mikroperlerne genereret ved hjælp af denne protokol som en nyttig metode i modellering vigtige aspekter af Alzheimers sygdom in vivo. Ved sammenligning af udgivelsesprofilen for Aβ fra indkapslede celler (figur 4) til niveauerne af Aβ genereret ved en bolt indsprøjtning (som den, der er indberettet i andre undersøgelser3,26), kan en mere kronisk og vedvarende frigivelse af Aβ Forventede. Figur 6 illustrerer den forventede tendens, der kan opnås. Ved hjælp af dette system til in vivo modellering er mere relevant for den måde, sygdommen skrider frem, og kan være mere nyttigt i narkotika opdagelse og udvikling.
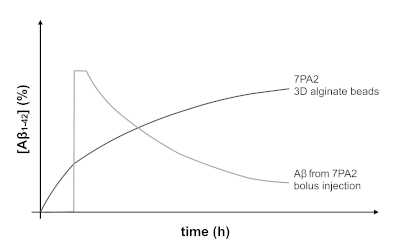
Figur 6 : Forventet frigivelses profil for Aβ1-42 fra INDKAPSLEDE 7pa2-celler sammenlignet med en Profilen af Aβ frigivelse fra engrafted 7PA2-holdige mikroperler tillader afprøvning af virkningerne af kronisk og vedvarende Aβ i en dyremodel af relevans for AD. Omvendt ville en bolt indsprøjtning skabe en stigning i Aβ niveauer over en kort periode, efterfulgt af en hurtig clearance af Aβ fra hjernen. Venligst klik her for at se en større version af dette tal.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Forfatterne vil gerne takke hr. kajen Suresparan, Dr. Jonathan Wubetu, hr. Dominik Grudzinski, Miss Chen Zhao og Dr. Thierry pilot for deres hjælp til optimering af alginat mikroperle fabrikation, cellekultur og Aβ-detektion og nyttige videnskabelige Diskussioner.
Materials
| µManager software | Vale Lab, UCSF, USA | v.1.46 | |
| 0.22 um PES filter | Merck, UK | SLGP033RS | |
| 15mm Netwell insert 74 um mesh filter | Constar, usa | #3477 | |
| Alginic acid sodium salt from brown algae | Sigma-Aldrich,uk | A0682 | |
| Calcium chloride | Sigma-Aldrich,uk | C1016 | |
| CellTiter96 AQueous One Solution cell proliferation assay | Promega, USA | G3580 | |
| Encapsulator | Inotech | IE-50 | serial no. 05.002.01-2005 |
| HEPES | Sigma-Aldrich,uk | H4024 | |
| Hu Aβ 1-42 ELISA | ThermoFisher, UK | KHB3441 | |
| ImageJ software | ImageJ | v1.49p | |
| Inverted light microscope | Olympus | CKX41 | |
| Leica microscope | Leica microsystems, UK | DMI6000B | |
| Neo sCMOS Camera | Ander, UK | 5.5 | |
| Phosphate buffered saline | Sigma-Aldrich,uk | D1408 | |
| Sodium chloride | Sigma-Aldrich,uk | 433209 | |
| Trispdium citrate dihydrate | Sigma-Aldrich,uk | W302600-K | |
| Trypsin-EDTA solution | Sigma-Aldrich,uk | T4049 |
References
- Hardy, J. A., Higgins, G. A. Alzheimer’s disease: the amyloid cascade hypothesis. Science. 256, 184-185 (1992).
- Karthick, C., et al. Time-dependent effect of oligomeric amyloid-β (1-42)-induced hippocampal neurodegeneration in rat model of Alzheimer’s disease. Neurological Research. 41 (2), 139-150 (2018).
- Watremez, W., et al. Stabilized Low-n Amyloid-β Oligomers Induce Robust Novel Object Recognition Deficits Associated with Inflammatory, Synaptic, and GABAergic Dysfunction in the Rat. Journal of Alzheimer’s Disease. 62 (1), 213-226 (2018).
- Brouillette, J., et al. Neurotoxicity and memory deficits induced by soluble low-molecular-weight amyloid-β1-42 oligomers are revealed in vivo by using a novel animal model. Journal of Neurosciences. 32 (23), 7852-7861 (2012).
- Solana, C., Tarazona, R., Solana, R. Immunosenescence of Natural Killer Cells, Inflammation, and Alzheimer’s Disease. International Journal of Alzheimer’s Disease. , 3128758 (2018).
- Sturchler-Pierrat, C., et al. Two amyloid precursor protein transgenic mouse models with Alzheimer disease-like pathology. Proceedings of the National Academy of Sciences of the United States of America. 94 (24), 13287-13292 (1997).
- Tomiyama, T., et al. A mouse model of amyloid beta oligomers: their contribution to synaptic alteration, abnormal tau phosphorylation, glial activation, and neuronal loss in vivo. Journal of Neurosciences. 30 (14), 4845-4856 (2010).
- Saito, T., et al. Single App knock-in mouse models of Alzheimer’s disease. Nature Neurosciences. 17 (5), 661-663 (2014).
- Oddo, S., et al. Triple-Transgenic Model of Alzheimer’s Disease with Plaques and Tangles: Intracellular A and Synaptic Dysfunction. Neuron. 39 (3), 409-421 (2003).
- Leon, W. C., et al. A Novel Transgenic Rat Model with a Full Alzheimer’s-Like Amyloid Pathology Displays Pre-Plaque Intracellular Amyloid-β-Associated Cognitive Impairment. Journal of Alzheimer’s Disease. 20 (1), 113-126 (2010).
- Prince, M., et al. Dementia UK: Second Edition – Overview. Alzheimer’s Society. , 61 (2007).
- Cavanaugh, S. E., Pippin, J. J., Barnard, N. D. Animal models of Alzheimer disease: historical pitfalls and a path forward. Alternatives to animal experimentation. 31 (3), 279-302 (2014).
- Oakley, H., et al. Intraneuronal β-Amyloid Aggregates, Neurodegeneration, and Neuron Loss in Transgenic Mice with Five Familial Alzheimer’s Disease Mutations: Potential Factors in Amyloid Plaque Formation. The Journal of Neuroscience. 26 (40), 10129-10140 (2006).
- Forny-Germano, L., et al. Alzheimer’s Disease-Like Pathology Induced by Amyloid-β Oligomers in Nonhuman Primates. Journal of Neuroscience. 34 (41), 13629-13643 (2014).
- Masliah, E., et al. Altered expression of synaptic proteins occurs early during progression of Alzheimer’s disease. Neurology. 56 (1), 127-129 (2001).
- Lepelletier, F. X., Mann, D. M. A., Robinson, A. C., Pinteaux, E., Boutin, H. Early changes in extracellular matrix in Alzheimer’s disease. Neuropathology and Applied Neurobiology. 43 (2), 167-182 (2017).
- Calafiore, R., Basta, G. Clinical application of microencapsulated islets: Actual prospectives on progress and challenges. Advanced Drug Delivery Reviews. 67-68, 84-92 (2014).
- Lim, F., Sun, A. M. Microencapsulated islets as bioartificial endocrine pancreas. Science. 210 (4472), 908-910 (1980).
- Tran, N. M., et al. Alginate hydrogel protects encapsulated hepatic HuH-7 cells against hepatitis C virus and other viral infections. PLoS One. 9 (10), 109969 (2014).
- Rios de la Rosa, J. M., Wubetu, J., Tirelli, N., Tirella, A. Colorectal tumor 3D in vitro models: advantages of biofabrication for the recapitulation of early stages of tumour development. Biomedical Physics & Engineering Express. 4 (4), 045010 (2018).
- Tirella, A., Orsini, A., Vozzi, G., Ahluwalia, A. A phase diagram for microfabrication of geometrically controlled hydrogel scaffolds. Biofabrication. 1 (4), 045002 (2009).
- Smalley, K. S. M., Lioni, M., Herlyn, M. Life ins’t flat: Taking cancer biology to the next dimension. In Vitro Cellular & Developmental Biology – Animal. 42 (8-9), 242-247 (2006).
- Podlisny, M. B., et al. Aggregation of secreted amyloid beta-protein into sodium dodecyl sulfate-stable oligomers in cell culture. Journal of Biological Chemistry. 270 (16), 9564-9570 (1995).
- Portelius, E., et al. Mass spectrometric characterization of amyloid-β species in the 7PA2 cell model of Alzheimer’s disease. Journal of Alzheimer’s Disease. 33 (1), 85-93 (2013).
- Welzel, A. T., et al. Secreted amyloid β-proteins in a cell culture model include N-terminally extended peptides that impair synaptic plasticity. Biochemistry. 53 (24), 3908-3921 (2014).
- O’Hare, E., et al. Orally bioavailable small molecule drug protects memory in Alzheimer’s disease models. Neurobiology of Aging. 34 (4), 1116-1125 (2013).
- Nedović, V., Willaert, R. Fundamentals of Cell Immobilisation Biotechnology. Methods and Technologies for Cell Immobilisation/Encapsulation. , 185-204 (2004).
- Omer, A., et al. Long-term Normoglycemia in Rats Receiving Transplants with Encapsulated Islets. Transplantation. 79 (1), 52-58 (2005).

