Struktureret motorisk rehabilitering efter selektive nerve overførsler
Summary
Her præsenterer vi en protokol for motor rehabilitering af patienter med svære nerveskader og selektiv nerve overførsel kirurgi. Det sigter mod at genoprette motorisk funktion, der foreslår flere stadier i patientuddannelse, tidlig fase terapi efter kirurgi og interventioner til rehabilitering efter vellykket re-innervation af nervens mål.
Abstract
Efter svære nerveskader giver selektive nerve overførsler mulighed for at genoprette motoriske og sensoriske funktioner. Funktionel genopretning afhænger både af den vellykkede re-innervation af målene i periferien og på den motoriske re-Learning proces, som medfører kortikal plasticitet. Mens der er et stigende antal metoder til at forbedre rehabilitering, deres rutinemæssige gennemførelse i en klinisk indstilling er fortsat en udfordring på grund af deres kompleksitet og lang varighed. Derfor er anbefalinger til Rehabiliteringsstrategier præsenteret med det formål at vejlede læger og terapeuter gennem den langvarige rehabiliteringsproces og give trin-for-trin instruktioner til at støtte motor re-Learning.
Umiddelbart efter nerve overførsel kirurgi, ingen motorisk funktion er til stede, og terapi bør fokusere på at fremme aktiviteten i den sensoriske-motoriske cortex områder i den paralyserede kropsdel. Efter omkring to til seks måneder (afhængigt af sværhedsgraden og modalitet af skade, afstanden af nerve regenerering og mange andre faktorer), den første motoriske aktivitet kan påvises via Elektromyografi (EMG). Inden for denne fase af rehabilitering bruges multimodal feedback til at genlære motor funktionen. Dette er især kritisk efter nerve overførsler, som muskel aktiverings mønstre ændre sig på grund af den ændrede neurale forbindelse. Endelig bør muskelstyrke være tilstrækkelig til at overvinde tyngdekraften/modstanden af antagonistiske muskler og ledstivhed, og flere funktionelle opgaver kan implementeres i rehabilitering.
Introduction
Selektive nerve overførsler giver mulighed for at genoprette motorens funktion efter nerveskader, når genvinding ved brug af neurolyse, nerve reparation eller nerve transplantation ikke kan forventes1,2. Mulige indikationer for nerve overførsler er alvorlige distale nerveskader, avulsion-type skader, manglen på tilgængelige nerve rødder til podning, den omfattende ardannelse på skades stedet og forsinket genopbygning3,4. Efter motor nerveskade, genopbygning er tidskritisk som degeneration af muskelvæv og motor ende plader kun giver mulighed for vellykket muskel re-innervation inden for 1-2 år efter skaden5,6. Her, nerve overførsler giver fordelen af en relativt kort re-innervation tid efter operationen, da de tillader nerve coaptation tæt på målet. Denne procedure, også kendt som Neuro bilisering, involverer kirurgisk omdirigering af en intakt nerve (donor nerve) til den distale del af recipient nerven. Da denne forbindelse er distale til den beskadigede stedet for modtageren nerve, det giver omgå den skadede nerve segment7.
Da neurale veje er ændret efter nerve overførsel kirurgi, patienter kan ikke behandles med standardpost-operative terapi protokoller ellers anvendes efter direkte nerve reparation8,9. Mens donor axoner vokse ind i det nye mål, de overtager en funktion, de ikke har før, mens kortikerisk stadig er forbundet til deres oprindelige funktion. Som et eksempel, er Oberlin caput ulnare nerve overførsel bruges til at genoprette albue flekon efter uoprettelig skade på den øvre Trunk eller nerve rødder C5 og C61. Som vist i figur 1, det indebærer at overføre en eller flere caput ulnare nerve fascicles til musculocutaneous motor gren af biceps muskel10. Men efter den vellykkede re-innervation, disse fascikler af caput ulnare nerve er kortikulært stadig forbundet med deres tidligere funktion af finger fleksering og/eller caput ulnare bortførelse og bøjning af håndleddet. På et funktionelt niveau dette indebærer, at i begyndelsen af rehabilitering, patienten har brug for at fokusere på den tidligere nerve funktion (hånd lukning) for at aktivere og styrke recipient musklen (biceps sammentrækning). Denne tilgang er også kendt som “donor aktivering fokuseret rehabilitering tilgang”9.
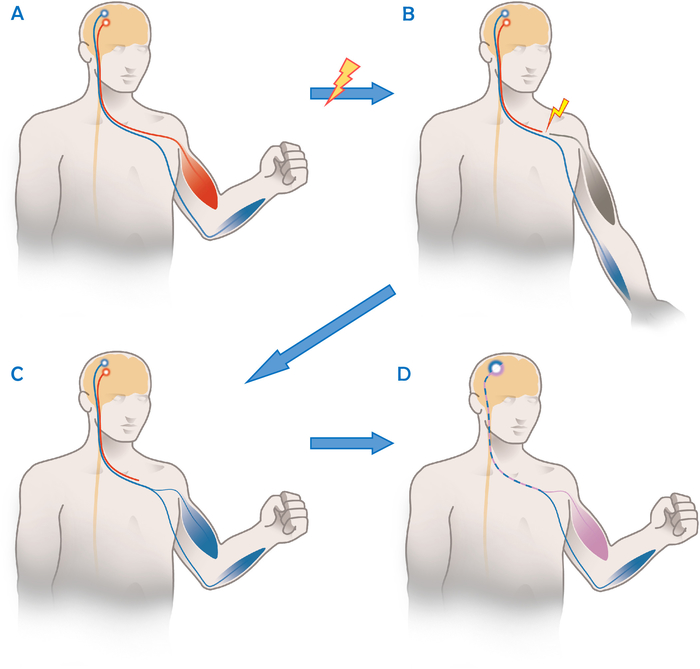
Figur 1: skematisk illustration af det funktionelle princip for en caput ulnare til musculocutaneous nerve overførsel. (A) i en sund person, er der en klar adskillelse mellem aktivitet i motorisk cortex for funktioner af forskellige nerver/leddene som her den musculocutaneous nerve (rød) og caput ulnare nerve (blå). (B) efter en skade af musculocutaneous nerve, biceps musklen kan ikke aktiveres, mens den ubeskadigede caput ulnare nerve (i blåt) stadig funktioner. (C). efter oberlins nerve overførsel og re-innervation, fascikler af caput ulnare nerve styre biceps muskler samt alle andre muskler anatomisk innerveret af caput ulnare nerve. Før kortikal reorganisering sker, er begge muskler aktiveret sammen, da der ikke er nogen kortikal adskillelse mellem disse nervefibre (i blåt). (D) med vellykket rehabilitering har patienten lært at bruge visse kortikale axoner til “normale” caput ulnare nerve funktioner (i blåt), mens andre (i lilla) nu styrer biceps-musklen. Dette giver mulighed for uafhængig bevægelse af begge muskelgrupper. Venligst klik her for at se en større version af dette tal.
Selv om forståelsen af dette koncept er grundlaget for vellykket rehabilitering, kan Genindlæring af nye motor mønstre være udfordrende for patienter og klinikere. Dette skyldes den lange varighed af rehabilitering, kompleksiteten af nerve regenerering og re-innervation og den begrænsede mængde direkte observerbare muskuløs aktivitet under tidlig re-innervation8. Bortset fra de ændringer i det perifere nervesystem, der er en stigende bevidsthed blandt kirurger og terapeuter for relevansen af ændringer i centralnervesystemet (CNS), dvs re-organisering af hånd motor og sensoriske kortikale områder forekommer som en konsekvens af denervering11. Når neurale input til CNS er berøvet, det associerede kortikale område mindskes til en vis grad på bekostning af tilstødende områder12. Restaurering af funktion, derfor afhænger af den centrale genopretning af sin repræsentation i hjernen. Inden for de seneste år har brugen af biofeedback metoder8 og tilgange til at støtte kortikale re-organisation13,14,15 ført til udvidede muligheder for rehabilitering efter nerve overførsler. Men på grund af kompleksiteten af post-kirurgisk terapi, er det vigtigt at give de rigtige interventioner på det rigtige tidspunkt13.
Derfor er formålet med denne strukturerede protokol til rehabilitering efter selektive nerve overførsler at tilvejebringe en realistisk og holistisk tilgang til at støtte motor opsving. Det er baseret på aktuelle anbefalinger og forfatternes erfaring med at indarbejde det i en klinisk indstilling. Protokollen er beregnet til at vejlede læger, arbejds-og fysioterapeuter samt andre sundhedspersonale gennem den langvarige rehabiliteringsproces.
Denne strukturerede protokol for motor rehabilitering blev evalueret i en gennemførlighedsundersøgelse8 hos fem patienter med brachialis plexus-skader som vist i tabel 1. Alle af dem fik flere nerve overførsler (nogle i kombination med nerve grafts) at genoprette øvre ekstremitet funktion. Af klarhedshensyn, når de beskriver specifikke indgreb i denne protokol, henviser de derfor til det øvre led. I detaljer, vi tager Oberlin caput ulnare nerve overførsel10 som et eksempel, som blev udført hos patienter 1-3. Til dette refererer vi til dele af caput ulnare nerven som donor nerven og musculocutaneous nerve er modtager nerven. Således biceps og brachialis muskler er modtageren muskler bliver re-innerveret af dele af caput ulnare nerve. Funktionelt, betyder det, at efter en donor aktivering fokuseret tilgang9, bevægelser forbundet med caput ulnare nerve aktivitet (såsom hånd lukning eller caput ulnare bortførelse af håndleddet) anvendes til aktivering af biceps muskel direkte efter re-innervation. Øvelser baseret på denne fremgangsmåde kan dog også udføres i andre kropsdele. Hvis det er nødvendigt med særlige hensyn for at gennemføre dette i andre dele af kroppen (f. eks. den nedre ekstremitet), påpeges dette i protokollen.
Uafhængig af kroppen del påvirket, terapi sessioner bør ikke overstige 30 min som muskler bliver let trætte kort efter re-innervation8 og vellykket træning kræver en patients fulde engagement og fokus.
Protocol
Representative Results
Discussion
For nylig er nerve overførsler i stigende grad blevet brugt til at genoprette funktionen efter svære proksimale nerveskader med lovende resultater1,4,31,32. Men selv om der er enighed om, at strukturerede uddannelsesprogrammer er nødvendige for at fremme gavnlige Neuro plastic ændringer33,34,35, er der ingen struktureret protokol tilgængelig til at beskrive motor rehabilitering tilgange efter nerve overførsler trin-for-trin. Derfor, formålet med den præsenterede protokol var at give detaljerede instruktioner til post-kirurgisk rehabilitering til at omfavne kortikale ændringer og forbedre kirurgiske resultater. I modsætning til andre protokoller9,36, visualisering af muskuløs aktivitet via Surface EMG Biofeedback er et centralt element i den præsenterede protokol.
Inden for terapi, patientuddannelse er et kritisk skridt, som patienten har brug for at forstå den temmelig komplekse kirurgiske procedure og blive uddannet på aktiviteter, der forbedrer sundhedstilstanden for at være aktivt involveret i den lange rehabilitering proces8 , 13 , 37. der er bred enighed om, at gentagelse er grundlæggende, og daglige hjem øvelser er nødvendige for at styrke en veletableret kortikal repræsentation af hånd8,34,38,39 . Bortset fra ren patientinformation, forfatterne stærkt anbefale en patient-centreret tilgang til rehabilitering. Dette indebærer desuden behandling af patienten som en unik person, inddragelse af patienten i pleje, god kliniker-patient kommunikation og bemyndigelse af patienten. I medicinsk rehabilitering, denne tilgang positivt påvirker patienttilfredshed og resultater40. Med hensyn til selve motoren rehabilitering, anbefales det at starte interventioner før re-innervation af musklerne og til at følge en donor aktivering fokuseret tilgang9. For at sikre, at der opdages muskuløs aktivitet så tidligt som muligt, kan der anvendes EMG Biofeedback-anordninger. Mens forfatterne er klar over, at EMG Biofeedback enheder er endnu ikke klinisk standard, deres anvendelse anbefales stærkt, da de tillader at starte tidlig aktiv motor rehabilitering og give værdifuld feedback på nyligt re-innervated muskler8.
De principper, der er beskrevet i denne protokol, kan anvendes for forskellige typer af nerve overførsler, selv om det kan være nødvendigt at foretage ændringer i protokollen. Mens motorisk re-Learning er relativt let, hvis synergistiske muskler/nerver blev brugt, brug af antagonistiske muskler/nerver kræver en længere rehabilitering tid og brugen af biofeedback kan være af endnu større betydning3,8. Især i de tilfælde, hvor en større mængde af gentagelser er nødvendig, kan fremtidige protokoller også omfatte alvorlige spil for at opretholde patientens motivation41.
Da timingen af nerve regenerering og mængden af nyttiggørelse enormt afhænger af skaden og kirurgiske indgreb, er der ingen streng tidsplan for rehabilitering. I stedet, terapeuten er bedt om at fortsætte afhængigt af tegn på motor opsving som anført i protokollen. På samme måde, er det vigtigt at bemærke, at succesen med nerve Transfer kirurgi er baseret på mange faktorer, herunder type og sværhedsgraden af skaden, kirurgens færdigheder, og ekspertise samt patientens alder, helbredstilstand, kognition og motivation8 , 13 , 42 , 43. mens rehabilitering er en hovedsøjle for genvinde funktion efter alvorlige nerveskader, selv det bedste program for motor re-uddannelse kan ikke forbedre funktionen, hvis der er utilstrækkelig perifer nerve regenerering og muskel re-innervation. Således forfatterne stærkt anbefale at se patienterne regelmæssigt sammen inden for en tværfaglig Team at være i stand til at diskutere, hvis nyttiggørelse går som forventet, eller hvis yderligere medicinske indgreb er nødvendige. Men, især efter alvorlige skader såsom C8 og Th1 nerve rod avulsioner, realistiske resultater kan ikke omfatte fuld helbredelse af ekstremitet funktion3,30. I disse tilfælde skal det kliniske team kommunikere dette til patienten, så snart en realistisk prognose kan angives (ca. et år efter nerve overførslerne). På dette tidspunkt, yderligere muligheder i rehabilitering, hjælpemidler eller kirurgiske indgreb (som senen overførsler) skal diskuteres. I tilfælde, hvor absolut ingen hånd funktion returnerer, kan udskiftning af funktionsløs lemmer med en protesfri anordning betragtes som en mulighed samt44,45. Dette er dog kun anbefales som en sidste udvej og efter dybtgående fysisk og psykologisk vurdering46.
Mens fokus for perifer nerve kirurgi normalt ligger på genopbygningen af motorisk funktion, sensoriske nerve overførsler er undertiden bruges til at genoprette fornemmelsen i hånden efter svær median eller caput ulnare nerveskade4,47. Svarende til motoriske nerve overførsler, dette skaber ændrede sensoriske neurale veje og resulterer i fornemmelser, der mærkes som om de var stammer fra den tidligere innervation område af donor nerven. Selv om der ikke blev udført sensoriske nerve overførsler, kan man stadig ændre/nedsætte følelsen enten på grund af selve skaden27 eller på grund af sygelighed på donor siden48. I disse tilfælde, rettidig re-uddannelse kan bidrage til at forbedre den sensoriske funktion49, og reducere uønsket hyper-følsomhed og smerte, der ofte opstår efter sådanne skader. For at sikre god motorisk og sensorisk funktion, anbefaler forfatterne stærkt at supplere motor genuddannelse med skræddersyede terapi tilgange for at fremme re-organisation i den tilsvarende sensoriske cortex samt39,50, 51. med hensyn til sensorisk reuddannelse anbefales det at starte interventioner før re-innervation af huden49,52,53. Dette kan omfatte substitution af sensation med andre sanser som vision53 eller auditiv feedback54, samt at gøre brug af overlapningen af sensoriske innervation områder27,52. Så snart patienten har genvundet en vis følsomhed, kan taktile Gnosis og objekt genkendelse uddannes, samtidig med at der opretholdes en høj mængde sensorisk input34. Typiske materialer, der kan anvendes til dette, omfatter selv lavede plader med forskellige overflader, der skal genkendes med lukkede øjne (Se figur 2) eller en æske fyldt med bønner/linser/ris (Se figur 3).

Figur 2: forskellige overflader kan anvendes til at støtte genvundne følsomhed. Normalt, patienten bliver bedt om at røre ved disse med begge hænder først, mens han/hun kan forsøge bagefter at genkende de forskellige overflader uden vision ved hjælp af kun hånd med begrænset følsomhed. Venligst klik her for at se en større version af dette tal.
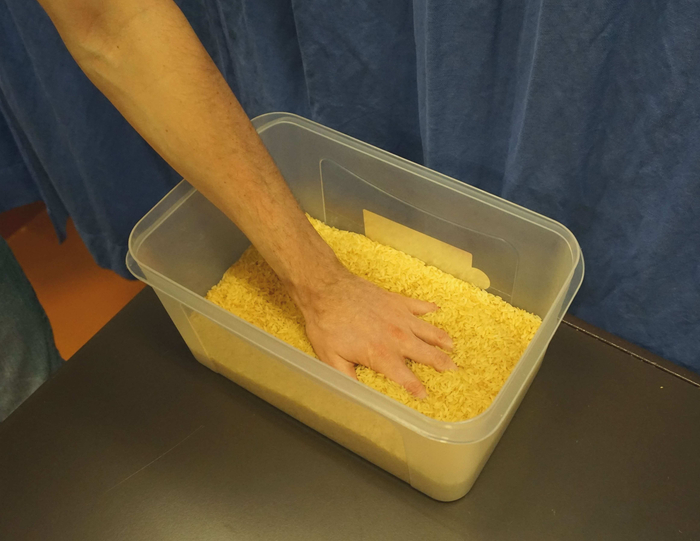
Figur 3: en æske fyldt med ris til sensorisk genuddannelse af hånden. I terapi, patienten kan sætte sin hånd med nedsat følsomhed omhyggeligt i denne boks og langsomt flytte hånden. For at fokusere patientens opmærksomhed kan terapeuten sætte nogle små genstande (f. eks. træblokke eller papirclips) i denne boks og bede om at finde dem uden visuel kontrol. Venligst klik her for at se en større version af dette tal.
Men i både sensorisk og motorisk genuddannelse er der kun begrænset evidens for valget af interventioner, som er nødvendige for at fremme god bedring34. Dette begrænser gyldigheden af den foreslåede rehabiliterings protokol som for andre protokoller. Mens den beskrevne protokol blev vurderet i en gennemførlighedsundersøgelse, og motoriske resultater var ens eller lidt bedre end dem, der blev rapporteret i litteraturen8, blev denne undersøgelse udført på en lille stikprøvestørrelse og uden en kontrolgruppe. Dette gør det umuligt at sammenligne resultater, fordele og ulemper ved denne protokol med hensyn til tidligere. Yderligere forskning skal omfatte kontrollerede undersøgelser for at sammenligne de mulige fordele ved at bruge overflade EMG Biofeedback til konventionelle tilgange.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Denne undersøgelse blev finansieret af Christian Doppler Research Foundation fra det østrigske råd for forskning og teknologisk udvikling og det østrigske Forbundsministerium for videnskab, forskning og økonomi. Vi takker Petra Gettinger for hendes hjælp til at forberede optagelserne og Aron Cserveny til forberedelsen af illustrationerne i manuskriptet og revaliderings sedlen. Grænser for neurovidenskab givet tilladelse til at gengive de data, der præsenteres i det oprindelige papir.
Materials
| EMG electrodes | Otto bock Healthcare, Duderstadt, Germany | electrodes 13E202 = 50 | The EMG electrodes used in this study were bipolar and included a ground and a 50 Hz filter. They were used with the Moby. |
| Folding Mirror Therapy Box (Arm/Foot/Ankle) | Reflex Pain Management Therapy Store | This box was used for mirror therapy. | |
| Myoboy | Otto bock Healthcare, Duderstadt, Germany | Myoboy | This EMG Biofeedback device that can be used as stand alone device or with a computer. While this device was used in the presented pilot study, other (cheaper) devices for sEMG biofeedback training are available as well. |
| Recognise[TM] Flash Cards | noigroup | If no self-made cards for left-right discrimination are used, these can be purchased from noigroup.com. There, a mobile app for training is available as well. |
References
- Rohde, R. S., Wolfe, S. W. Nerve transfers for adult traumatic brachial plexus palsy (brachial plexus nerve transfer). HSS Journal. 3 (1), 77-82 (2007).
- Ray, W. Z., Mackinnon, S. E. Management of nerve gaps: Autografts, allografts, nerve transfers, and end-to-side neurorrhaphy. Experimental Neurology. 223 (1), 77-85 (2010).
- Tung, T. H., Mackinnon, S. E. Nerve Transfers: Indications, Techniques, and Outcomes. The Journal of Hand Surgery. 35 (2), 332-341 (2010).
- Isaacs, J., Cochran, A. R. Nerve transfers for peripheral nerve injury in the upper limb. Bone Joint Journal. 101 (2), 124-131 (2019).
- Terzis, J. K., Papakonstantinou, K. C. The surgical treatment of brachial plexus injuries in adults. Plastic and Reconstruction Surgery. 106 (5), (2000).
- Ray, W. Z., Mackinnon, S. E. Clinical Outcomes Following Median to Radial Nerve Transfers. The Journal of Hand Surgery. 36 (2), 201-208 (2011).
- Liu, Y., Lao, J., Gao, K., Gu, Y., Xin, Z. Outcome of nerve transfers for traumatic complete brachial plexus avulsion: results of 28 patients by DASH and NRS questionnaires. Journal of Hand Surgery European. 37 (5), 413-421 (2012).
- Sturma, A., Hruby, L. A., Prahm, C., Mayer, J. A., Aszmann, O. C. Rehabilitation of Upper Extremity Nerve Injuries Using Surface EMG Biofeedback: Protocols for Clinical Application. Frontiers in Neuroscience. 12 (906), (2018).
- Kahn, L. C., Moore, A. M. Donor Activation Focused Rehabilitation Approach: Maximizing Outcomes After Nerve Transfers. Hand Clinics. 32 (2), 263-277 (2016).
- Oberlin, C., et al. Nerve transfer to biceps muscle using a part of ulnar nerve for C5-C6 avulsion of the brachial plexus: anatomical study and report of four cases. Journal of Hand Surgery American. 19 (2), 232-237 (1994).
- Karl, A., Birbaumer, N., Lutzenberger, W., Cohen, L. G., Flor, H. Reorganization of motor and somatosensory cortex in upper extremity amputees with phantom limb pain. Journal of Neurosciences. 21 (10), 3609-3618 (2001).
- Makin, T. R., Bensmaia, S. J. Stability of Sensory Topographies in Adult Cortex. Trends in Cognitive Science. 21 (3), 195-204 (2017).
- Novak, C. B., Lvonder Heyde, R. Rehabilitation of the upper extremity following nerve and tendon reconstruction: when and how. Seminars in Plastic Surgery. 29 (1), 73-80 (2015).
- Lundborg, G. Brain plasticity and hand surgery: an overview. Journal of Hand Surgery Bristish. 25 (3), 242-252 (2000).
- Novak, C. B. Rehabilitation Following Motor Nerve Transfers. Hand Clinics. 24 (4), 417-423 (2008).
- Miller, C., Peek, A. L., Power, D., Heneghan, N. R. Psychological consequences of traumatic upper limb peripheral nerve injury: A systematic review. Hand Therapy. 22 (1), 35-45 (2016).
- Bailey, R., Kaskutas, V., Fox, I., Baum, C. M., Mackinnon, S. E. Effect of Upper Extremity Nerve Damage on Activity Participation, Pain, Depression, and Quality of Life. The Journal of Hand Surgery. 34 (9), 1682-1688 (2009).
- Moseley, G. L. . The graded motor imagery handbook. , (2012).
- Ramachandran, V. S., Rogers-Ramachandran, D. Synaesthesia in phantom limbs induced with mirrors. Proceedings of the Royal Society of Biological Sciences. 263 (1369), 377-386 (1996).
- Rothgangel, A. S., Braun, S. M., Beurskens, A. J., Seitz, R. J., Wade, D. T. The clinical aspects of mirror therapy in rehabilitation. International Journal of Rehabilitation Research. 34 (1), 1-13 (2011).
- Ramachandran, V. S., Hirstein, W. The perception of phantom limbs. The D. O. Hebb lecture. Brain. 121 (Pt 9), 1603-1630 (1998).
- Hubatka, G., Meyer, V. E. Immobilization of the injured hand. Helvetica Chirurgica Acta. 47 (1-2), 81-84 (1980).
- Merletti, R., Parker, P. A. Electromyography: Physiology, Engineering, and Non-Invasive Applications. Wiley IEEE-Press Verlag. , (2004).
- Götz-Neumann, K. . Gehen verstehen. Ganganalyse in der Physiotherapie. , (2016).
- Perry, J., Burnfield, J. M. . Gait Analysis: Normal and Pathological Function. , (2010).
- James, M. A. Use of the Medical Research Council muscle strength grading system in the upper extremity. The Journal of Hand Surgery American. 32 (2), 154-156 (2007).
- Bertelli, J. A., Ghizoni, M. F., Loure Iro Chaves, D. P. Sensory disturbances and pain complaints after brachial plexus root injury: a prospective study involving 150 adult patients. Microsurgery. 31 (2), 93-97 (2011).
- Ray, W. Z., Pet, M. A., Yee, A., Mackinnon, S. E. Double fascicular nerve transfer to the biceps and brachialis muscles after brachial plexus injury: clinical outcomes in a series of 29 cases. Journal of Neurosurgery. 114 (6), 1520-1528 (2011).
- Bertelli, J. A., Ghizoni, M. F. Reconstruction of C5 and C6 brachial plexus avulsion injury by multiple nerve transfers: spinal accessory to suprascapular, ulnar fascicles to biceps branch, and triceps long or lateral head branch to axillary nerve. The Journal of Hand Surgery American. 29 (1), 131-139 (2004).
- Wong, A. H., Pianta, T. J., Mastella, D. J. Nerve transfers. Hand Clinics. 28 (4), 571-577 (2012).
- Colbert, S. H., Mackinnon, S. E. Nerve Transfers for Brachial Plexus Reconstruction. Nerve Transfers. 24 (4), 341-361 (2008).
- Brown, J. M., Mackinnon, S. E. Nerve Transfers in the Forearm and Hand. Nerve Transfers. 24 (4), 319-340 (2008).
- Beisteiner, R., et al. New type of cortical neuroplasticity after nerve repair in brachial plexus lesions. Archives in Neurology. 68 (11), 1467-1470 (2011).
- Novak, C. B., von der Heyde, R. L. Evidence and techniques in rehabilitation following nerve injuries. Hand Clinics. 29 (3), 383-392 (2013).
- Dahlin, L. B., Andersson, G., Backman, C., Svensson, H., Bjorkman, A. Rehabilitation, Using Guided Cerebral Plasticity, of a Brachial Plexus Injury Treated with Intercostal and Phrenic Nerve Transfers. Frontiers in Neurology. 8, 72 (2017).
- Hill, J., et al. . The stages of rehabilitation following motor nerve transfer surgery. , (2019).
- Vikstrom, P., Carlsson, I., Rosen, B., Bjorkman, A. Patients’ views on early sensory relearning following nerve repair-a Q-methodology study. The Journal of Hand Therapy. 31 (4), 443-450 (2018).
- Anastakis, D. J., Malessy, M. J., Chen, R., Davis, K. D., Mikulis, D. Cortical plasticity following nerve transfer in the upper extremity. Hand Clinics. 24 (4), 425-444 (2008).
- Oud, T., Beelen, A., Eijffinger, E., Nollet, F. Sensory re-education after nerve injury of the upper limb: a systematic review. Clinical Rehabilitation. 21 (6), 483-494 (2007).
- Plewnia, A., Bengel, J., Korner, M. Patient-centeredness and its impact on patient satisfaction and treatment outcomes in medical rehabilitation. Patient Education Counselling. 99 (12), 2063-2070 (2016).
- Prahm, C., Kayali, F., Sturma, A., Aszmann, O. PlayBionic: Game-Based Interventions to Encourage Patient Engagement and Performance in Prosthetic Motor Rehabilitation. Physical Medicine & Rehabilitation. 10 (11), 1252-1260 (2018).
- Rosen, B., Lundborg, G., Dahlin, L. B., Holmberg, J., Karlson, B. Nerve repair: correlation of restitution of functional sensibility with specific cognitive capacities. Journal of Hand Surgery. 19 (4), 452-458 (1994).
- Lundborg, G., Rosen, B. Sensory relearning after nerve repair. Lancet. 358 (9284), 809-810 (2001).
- Aszmann, O. C., et al. Bionic reconstruction to restore hand function after brachial plexus injury: a case series of three patients. Lancet. 385 (9983), 2183-2189 (2015).
- Hruby, L. A., et al. Algorithm for bionic hand reconstruction in patients with global brachial plexopathies. Journal of Neurosurgery. , 1-9 (2017).
- Hruby, L. A., Pittermann, A., Sturma, A., Aszmann, O. C. The Vienna psychosocial assessment procedure for bionic reconstruction in patients with global brachial plexus injuries. PloS One. 13 (1), e0189592 (2018).
- Soldado, F., Bertelli, J. A., Ghizoni, M. F. High Median Nerve Injury: Motor and Sensory Nerve Transfers to Restore Function. Hand Clinics. 32 (2), 209-217 (2016).
- Li, X. M., et al. Donor-side morbidity after contralateral C-7 nerve transfer: results at a minimum of 6 months after surgery. Journal of Neurosurgery. 124 (5), 1434-1441 (2016).
- Rosen, B., Lundborg, G. Sensory re-education after nerve repair: aspects of timing. Handchirurgie Mikrochirurgie Plastiche Chirurgie. 36 (1), 8-12 (2004).
- Jerosch-Herold, C. Sensory relearning in peripheral nerve disorders of the hand: a web-based survey and delphi consensus method. Journal of Hand Therapy. 24 (4), 292-298 (2011).
- Rosén, B., Lundborg, G., Skirven, T. M., Osterman, A. L., Fedorczyk, J. M., Amadio, P. C. . Rehabilitation of the Hand and Upper Extremity. 6, (2011).
- Daniele, H. R., Aguado, L. Early compensatory sensory re-education. Journal of Reconstructive Microsurgery. 19 (2), 107-110 (2003).
- Rosen, B., et al. Enhanced early sensory outcome after nerve repair as a result of immediate post-operative re-learning: a randomized controlled trial. Journal of Hand Surgery European Volume. 40 (6), 598-606 (2015).
- Rosen, B., Lundborg, G. Early use of artificial sensibility to improve sensory recovery after repair of the median and ulnar nerve. Scandinavian Journal of Plastic and Reconstructive Surgery and Hand Surgery. 37 (1), 54-57 (2003).

