Användning av en perkutan ventrikulär hjälpanordning/vänster atrium till lårbensartär bypasssystem för kardiogen chock
Summary
Följande artikel beskriver det stegvisa förfarandet för placering av en enhet (t.ex. Tandemheart) i kardiogen chock (CS) som är en perkutan vänster ventrikulärt stödanordning (pLVAD) och en vänster förmaksling till femorala gatan bypass (LAFAB) system som kringgår och stöder den vänstra ventrikel (LV) i CS.
Abstract
Den vänstra förmakseln till lårbens gatan bypass (LAFAB) systemet är en mekanisk cirkulation stöd (MCS) enhet som används i kardiogen chock (CS) som kringgår den vänstra ventrikeln genom att tömma blod från vänster atrium (LA) och återföra det till systemisk kranskärlens cirkulation via lårbensartären. Det kan ge flöden från 2,5-5 L/min beroende på kanylens storlek. Här diskuterar vi verkningsmekanismen för LAFAB, tillgängliga kliniska data, indikationer för dess användning i kardiogenic chock, steg för implantation, post-procedurell vård och komplikationer i samband med användningen av denna enhet och deras hantering.
Vi tillhandahåller också en kort video av den procedurmässiga komponenten i enhetsterapi, inklusive förberedelse före placering, perkutan placering av enheten via transseptal punktering under ekokardiografisk vägledning och postoperativ hantering av enhetsparametrar.
Introduction
Kardiogen chock (CS) är ett tillstånd av vävnad hypoperfusion med eller utan samtidig hypotension, där hjärtat inte kan leverera tillräckligt med blod och syre för att möta kroppens krav, vilket resulterar i organsvikt. Det klassificeras i steg A till E av Society of Cardiovascular Angiography and Interventions (SCAI): steg A – patienter i riskzonen för CS; steg B – patienter i början av CS med hypotoni eller takykardi utan hypoperfusion; steg C – klassisk CS med kall och våt fenotyp som kräver inotroper/vasopressorer eller mekaniskt stöd för att upprätthålla perfusion; steg D – försämras på nuvarande medicinskt eller mekaniskt stöd som kräver eskalering till mer avancerade enheter; och steg E – inkluderar patienter med cirkulationskollaps och eldfasta arytmier som aktivt upplever hjärtstillestånd med pågående hjärt-lungräddning1. De vanligaste orsakerna till CS är akut MI (AMI) som representerar 81% av fallen i en nyligen rapporterad analys2 och akut dekompenserad hjärtsvikt (ADHF). CS kännetecknas klassiskt av överbelastning och nedsatt perfusion, manifesterat av förhöjt fyllningstryck (pulmonell kapillär kiltryck [PCWP], vänster ventrikulärt enddiastoliskt tryck [LVEDP], centralt ventryck [CVP] och höger ventrikulärt enddiastoliskt tryck [RVEDP]), minskad hjärtutgång (CO), hjärtindex (CI), hjärteffekt (CPO) och endorganfel3 . Tidigare var de enda tillgängliga behandlingarna för AMI kompliceras av CS tidiga revascularization och medicinsk förvaltning med inotropes och/eller vasopressors4. Mer nyligen, med tillkomsten av mekanisk cirkulationsstöd (MCS) enheter och erkännandet att eskalering av vasopressorer är associerad med ökad dödlighet, har det skett ett paradigmskifte i behandlingen av både AMI och ADHF relaterade CS5,6.
I den nuvarande eran av perkutan ventrikulära hjälpanordningar (pVAD) finns det ett antal MCS-enhetsplattformar/ konfigurationer tillgängliga, som ger univentricular eller biventricular cirkulations- och ventrikulärt stöd med och utan syresättningsförmåga7. Trots stadiga ökningar av användningen av pVADs för att behandla både AMI och ADHF CS, dödligheten har varit i stort sett oförändrad5. Med framväxande bevis för möjliga kliniska fördelar för tidig lossning av vänster ventrikel (LV) i AMI8 och tidig användning av MCS i AMI CS9, fortsätter användningen av MCS att öka.
Vänster förmaks- till lårartär bypass (LAFAB) MCS-enhet kringgår LV genom att tömma blod från vänster förmak (LA) och återföra det till den systemiska arteriell cirkulationen via lårbensartären (figur 1). Det stöds av en extern centrifugalpump som erbjuder 2,5-5,0 liter per minut (L/m) flöde (ny generation pump, betecknad som LifeSPARC, som kan upp till 8 L / m flöde) beroende på kanylernas storlek. När blodet extraheras från LA via transseptal venös kanyl passerar det genom den yttre centrifugalpumpen som återcirkulerar blodet tillbaka in i patientens kropp via artär cannula placerad i lårartären.
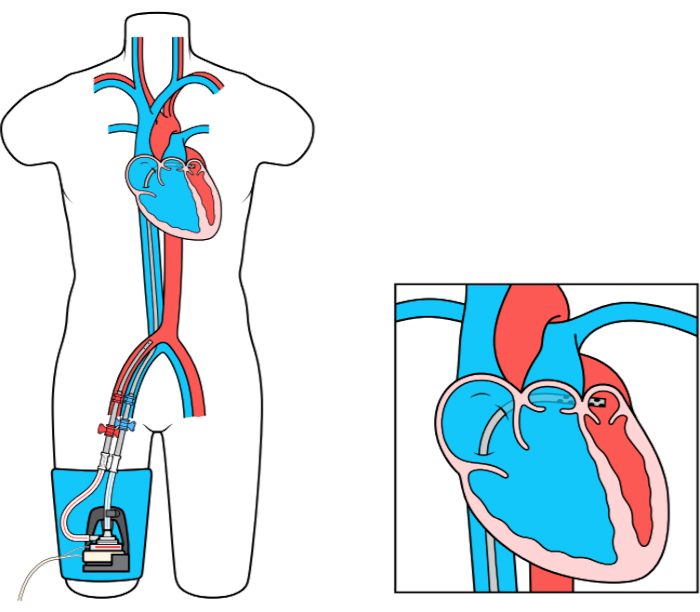
Bild 1: LAFAB-inställning. Klicka här för att se en större version av denna siffra.
Protocol
Representative Results
Discussion
Hemodynamik för LAFAB-enhet:
LAFAB-enhetens hemodynamiska profil skiljer sig från andra pVADs. Genom att tömma blod direkt från LA och återföra det till lårbensartären kringgår enheten LV helt. På så sätt minskar det LV-ändens diastoliska volym och tryck, vilket bidrar till förbättrad LV-geometri och därmed påverkar en minskning av LV-slagarbetet. Men genom att återföra blodet tillbaka till iliaca gatan/fallande stora kroppspulsådern ökar dock efterbelastningen. D…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Till TandemHeart-teamet på LifeSparc.
Materials
| For LAFAB (TandemHeart) | |||
| Factory Supplied Equipment for circuit connections. | TandemLife | ||
| ProtekSolo 15 Fr or 17 Fr Arterial Cannula | TandemLife | ||
| ProtekSolo 62 cm or 72 cm Transseptal Cannula | TandemLife | ||
| TandemHeart Controller | TandemLife | For adjusting flows/RPM | |
| TandemHeart Pump | LifeSPARC | Centrifugal pump | |
| For RAPAB (ProtekDuo) | |||
| Factory Supplied Equipment to complete the circuit. | TandemLife | ||
| ProtekDuo 29 Fr or 31 Fr Dual Lumen Cannula | TandemLife | ||
| TandemHeart Controller | TandemLife | For adjusting flows/RPM | |
| TandemHeart Pump | LifeSPARC | Centrifugal pump |
References
- Baran, D. A., et al. SCAI clinical expert consensus statement on the classification of cardiogenic shock. Catheterization and Cardiovascular Interventions. 94 (1), 29-37 (2019).
- Harjola, V. -. P., et al. Clinical picture and risk prediction of short-term mortality in cardiogenic shock. European Journal of Heart Failure. 17 (5), 501-509 (2015).
- Furer, A., Wessler, J., Burkhoff, D. Hemodynamics of Cardiogenic Shock. Interventional Cardiology Clinics. 6 (3), 359-371 (2017).
- Hochman, J. S., et al. Cardiogenic shock complicating acute myocardial infarction–etiologies, management and outcome: a report from the SHOCK Trial Registry. SHould we emergently revascularize Occluded Coronaries for cardiogenic shocK. Journal of the American College of Cardiology. 36 (3), 1063-1070 (2000).
- Shah, M., et al. Trends in mechanical circulatory support use and hospital mortality among patients with acute myocardial infarction and non-infarction related cardiogenic shock in the United States. Clinical Research in Cardiology. 107 (4), 287-303 (2018).
- van Diepen, S., et al. Contemporary Management of Cardiogenic Shock: A Scientific Statement From the American Heart Association. Circulation. 136 (16), 232-268 (2017).
- Alkhouli, M., et al. Mechanical Circulatory Support in Patients with Cardiogenic Shock. Current Treatment Options in Cardiovascular Medicine. 22 (2), 4 (2020).
- Basir, M. B., et al. Feasibility of early mechanical circulatory support in acute myocardial infarction complicated by cardiogenic shock: The Detroit cardiogenic shock initiative. Catheterization and Cardiovascular Interventions. 91 (3), 454-461 (2018).
- Basir, M. B., et al. Improved Outcomes Associated with the use of Shock Protocols: Updates from the National Cardiogenic Shock Initiative. Catheterization and Cardiovascular Interventions. 93 (7), 1173-1183 (2019).
- Alkhouli, M., Rihal, C. S., Holmes, D. R. Transseptal Techniques for Emerging Structural Heart Interventions. JACC: Cardiovascular Interventions. 9 (24), 2465-2480 (2016).
- Dennis, C., et al. Clinical use of a cannula for left heart bypass without thoracotomy: experimental protection against fibrillation by left heart bypass. Annals of Surgery. 156 (4), 623-637 (1962).
- Dennis, C., et al. Left atrial cannulation without thoracotomy for total left heart bypass. Acta Chirurgica Scandinavica. 123, 267-279 (1962).
- Fonger, J. D., et al. Enhanced preservation of acutely ischemic myocardium with transseptal left ventricular assist. Annals of Thoracic Surgery. 57 (3), 570-575 (1994).
- Thiele, H., et al. Reversal of cardiogenic shock by percutaneous left atrial-to-femoral arterial bypass assistance. Circulation. 104 (24), 2917-2922 (2001).
- Burkhoff, D., et al. A randomized multicenter clinical study to evaluate the safety and efficacy of the TandemHeart percutaneous ventricular assist device versus conventional therapy with intraaortic balloon pumping for treatment of cardiogenic shock. American Heart Journal. 152 (3), 469 (2006).
- Thiele, H., et al. Randomized comparison of intra-aortic balloon support with a percutaneous left ventricular assist device in patients with revascularized acute myocardial infarction complicated by cardiogenic shock. European Heart Journal. 26 (13), 1276-1283 (2005).
- Gregoric, I. D., et al. TandemHeart as a rescue therapy for patients with critical aortic valve stenosis. Annals of Thoracic Surgery. 88 (6), 1822-1826 (2009).
- Kar, B., et al. The percutaneous ventricular assist device in severe refractory cardiogenic shock. Journal of the American College of Cardiology. 57 (6), 688-696 (2011).
- Patel, C. B., Alexander, K. M., Rogers, J. G. Mechanical Circulatory Support for Advanced Heart Failure. Current Treatment Options in Cardiovascular Medicine. 12 (6), 549-565 (2010).
- Tempelhof, M. W., et al. Clinical experience and patient outcomes associated with the TandemHeart percutaneous transseptal assist device among a heterogeneous patient population. Asaio Journal. 57 (4), 254-261 (2011).
- Gregoric, I. D., et al. The TandemHeart as a bridge to a long-term axial-flow left ventricular assist device (bridge to bridge). Texas Heart Institute Journal. 35 (2), 125-129 (2008).
- Bruckner, B. A., et al. Clinical experience with the TandemHeart percutaneous ventricular assist device as a bridge to cardiac transplantation. Texas Heart Institute Journal. 35 (4), 447-450 (2008).
- Agarwal, R., et al. Successful treatment of acute left ventricular assist device thrombosis and cardiogenic shock with intraventricular thrombolysis and a tandem heart. Asaio Journal. 61 (1), 98-101 (2015).
- Vetrovec, G. W. Hemodynamic Support Devices for Shock and High-Risk PCI: When and Which One. Current Cardiology Reports. 19 (10), 100 (2017).
- Al-Husami, W., et al. Single-center experience with the TandemHeart percutaneous ventricular assist device to support patients undergoing high-risk percutaneous coronary intervention. Journal of Invasive Cardiology. 20 (6), 319-322 (2008).
- Vranckx, P., et al. Clinical introduction of the Tandemheart, a percutaneous left ventricular assist device, for circulatory support during high-risk percutaneous coronary intervention. International Journal of Cardiovascular Interventions. 5 (1), 35-39 (2003).
- Vranckx, P., et al. The TandemHeart, percutaneous transseptal left ventricular assist device: a safeguard in high-risk percutaneous coronary interventions. The six-year Rotterdam experience. Euro Intervention. 4 (3), 331-337 (2008).
- Vranckx, P., et al. Assisted circulation using the TandemHeart during very high-risk PCI of the unprotected left main coronary artery in patients declined for CABG. Catheterization and Cardiovascular Interventions. 74 (2), 302-310 (2009).
- Thomas, J. L., et al. Use of a percutaneous left ventricular assist device for high-risk cardiac interventions and cardiogenic shock. Journal of Invasive Cardiology. 22 (8), 360 (2010).
- Vranckx, P., et al. Assisted circulation using the Tandemhear , percutaneous transseptal left ventricular assist device, during percutaneous aortic valve implantation: the Rotterdam experience. Euro Intervention. 5 (4), 465-469 (2009).
- Pitsis, A. A., et al. Temporary assist device for postcardiotomy cardiac failure. The Annals of Thoracic Surgery. 77 (4), 1431-1433 (2004).
- Singh, G. D., Smith, T. W., Rogers, J. H. Targeted Transseptal Access for MitraClip Percutaneous Mitral Valve Repair. Interventional Cardiology Clinics. 5 (1), 55-69 (2016).
- Subramaniam, A. V., et al. Complications of Temporary Percutaneous Mechanical Circulatory Support for Cardiogenic Shock: An Appraisal of Contemporary Literature. Cardiology and Therapy. 8 (2), 211-228 (2019).
- Morley, D., et al. Hemodynamic effects of partial ventricular support in chronic heart failure: Results of simulation validated with in vivo data. The Journal of Thoracic and Cardiovascular Surgery. 133 (1), 21-28 (2007).
- Naidu, S. S. Novel Percutaneous Cardiac Assist Devices. Circulation. 123 (5), 533-543 (2011).
- Kapur, N. K., et al. Hemodynamic Effects of Left Atrial or Left Ventricular Cannulation for Acute Circulatory Support in a Bovine Model of Left Heart Injury. ASAIO Journal. 61 (3), 301-306 (2015).
- Smith, L., et al. Outcomes of patients with cardiogenic shock treated with TandemHeart percutaneous ventricular assist device: Importance of support indication and definitive therapies as determinants of prognosis. Catheterization and Cardiovascular Interventions. 92 (6), 1173-1181 (2018).
- Ergle, K., Parto, P., Krim, S. R. Percutaneous Ventricular Assist Devices: A Novel Approach in the Management of Patients With Acute Cardiogenic Shock. The Ochsner Journal. 16 (3), 243-249 (2016).
- Sultan, I., Kilic, A., Kilic, A.Short-Term Circulatory and Right Ventricle Support in Cardiogenic Shock: Extracorporeal Membrane Oxygenation, Tandem Heart, CentriMag, and Impella. Heart Failure Clinics. 14 (4), 579-583 (2018).
- Bermudez, C., et al. . Percutaneous right ventricular support: Initial experience from the tandemheart experiences and methods (THEME) registry. , (2018).
- Aggarwal, V., Einhorn, B. N., Cohen, H. A. Current status of percutaneous right ventricular assist devices: First-in-man use of a novel dual lumen cannula. Catheterization and Cardiovascular Interventions. 88 (3), 390-396 (2016).
- Kapur, N. K., et al. Mechanical circulatory support devices for acute right ventricular failure. Circulation. 136 (3), 314-326 (2017).
- Kapur, N. K., et al. Mechanical Circulatory Support for Right Ventricular Failure. JACC: Heart Failure. 1 (2), 127-134 (2013).
- Geller, B. J., Morrow, D. A., Sobieszczyk, P. Percutaneous Right Ventricular Assist Device for Massive Pulmonary Embolism. Circulation: Cardiovascular Interventions. 5 (6), 74-75 (2013).
- Bhama, J., et al. Initial Experience with a Percutaneous Dual Lumen Single Cannula Strategy for Temporary Right Ventricular Assist Device Support Following Durable LVAD Therapy. The Journal of Heart and Lung Transplantation. 35 (4), 323 (2013).
- O’Neill, B., et al. Right ventricular hemodynamic support with the PROTEKDuo Cannula. Initial experience from the tandemheart experiences and methods (THEME) registry category. Miscellaneous. , (2018).
- O’Brien, B., et al. Fluoroscopy-free AF ablation using transesophageal echocardiography and electroanatomical mapping technology. Journal of Interventional Cardiac Electrophysiology. 50 (3), 235-244 (2017).
- O’Brien, B., et al. Transseptal puncture — Review of anatomy, techniques, complications and challenges. International Journal of Cardiology. 233, 12-22 (2017).

