Forbedre reproduserbarheten for å møte minimal informasjon for studier av ekstracellulære vesicles 2018 retningslinjer i nanopartikkelsporingsanalyse
Summary
Nanopartikkelsporingsanalyse (NTA) er en mye brukt metode for å karakterisere ekstracellulære vesikler. Dette dokumentet fremhever NTA eksperimentelle parametere og kontroller pluss en ensartet metode for analyse og karakterisering av prøver og fortynningsstoffer som er nødvendige for å supplere retningslinjene foreslått av MISEV2018 og EV-TRACK for reproduserbarhet mellom laboratorier.
Abstract
Nanopartikkelsporingsanalyse (NTA) har vært en av flere karakteriseringsmetoder som er brukt til ekstracellulær vesicle (EV) forskning siden 2006. Mange anser at NTA-instrumenter og deres programvarepakker lett kan brukes etter minimal opplæring, og at størrelseskalibrering er mulig internt. Siden både NTA-anskaffelse og programvareanalyse utgjør EV-karakterisering, blir de adressert i Minimal informasjon for studier av extracellulære vesikler 2018 (MISEV2018). I tillegg har de blitt overvåket av Transparent Reporting and Centralizing Knowledge in Extracellular Vesicle Research (EV-TRACK) for å forbedre robustheten til EV-eksperimenter (f.eks. minimere eksperimentell variasjon på grunn av ukontrollerte faktorer).
Til tross for arbeidet med å oppmuntre til rapportering av metoder og kontroller, klarer mange publiserte forskningsartikler ikke å rapportere kritiske innstillinger som trengs for å reprodusere de opprinnelige NTA-observasjonene. Få artikler rapporterer NTA-karakterisering av negative kontroller eller fortynningsmidler, noe som tydeligvis antar at kommersielt tilgjengelige produkter, som fosfatbufret saltvann eller ultrarent destillert vann, er partikkelfrie. På samme måte rapporteres positive kontroller eller størrelsesstandarder sjelden av forskere for å verifisere partikkelstørrelse. Stokes-Einstein-ligningen inneholder prøveviskositet og temperaturvariabler for å bestemme partikkelforskyvning. Rapportering av stabil laserkammertemperatur under hele prøvevideosamlingen er derfor et viktig kontrollmål for nøyaktig replikering. Filtrering av prøver eller fortynningsstoffer rapporteres heller ikke rutinemessig, og i så fall er spesifikasjonene til filteret (produsent, membranmateriale, porestørrelse) og lagringsforhold sjelden inkludert. International Society for Extracellular Vesicle (ISEV)s minimale standarder for akseptable eksperimentelle detaljer bør inneholde en veldokumentert NTA-protokoll for karakterisering av elbiler. Følgende eksperiment gir bevis på at en NTA-analyseprotokoll må etableres av den enkelte forsker og inkluderes i metodene for publikasjoner som bruker NTA-karakterisering som et av alternativene for å oppfylle MISEV2018-krav for enkelt vesicle karakterisering.
Introduction
Nøyaktig og repeterbar analyse av elbiler og andre nanometerskalerte partikler byr på mange utfordringer på tvers av forskning og industri. Replikering av EV-forskning har blant annet vært vanskelig på grunn av manglende ensartethet i rapportering av nødvendige parametere knyttet til datainnsamling. For å løse disse manglene foreslo ISEV bransjeretningslinjer som et minimalt sett med biokjemiske, biofysiske og funksjonelle standarder for EV-forskere og publiserte dem som en posisjonserklæring, ofte referert til som MISEV20141. Det akselererende tempoet i EV-forskningen krevde en oppdatert retningslinje, og “MISEV2018: a position statement of the ISEV” utvidet MISEV2014-retningslinjene2. MISEV2018-artikkelen inkluderte tabeller, disposisjoner av foreslåtte protokoller og trinn du må følge for å dokumentere spesifikk EV-tilknyttet karakterisering. Som et ytterligere tiltak for å legge til rette for tolkning og replikering av eksperimenter, ble EV-TRACK utviklet som en crowd-sourcing kunnskapsbase (http://evtrack.org) for å muliggjøre mer gjennomsiktig rapportering av EV-biologi og metodikken som brukes for publiserte resultater3. Til tross for disse anbefalingene for standardisert rapportering av metoder, fortsetter feltet å lide når det gjelder replikering og bekreftelse av publiserte resultater.
I henhold til National Institutes of Health’s og National Science Foundations innsats for kvalitetskontrollverktøy, antyder dette dokumentet at ISEV krever standardisert rapportering av metoder og detaljer slik at datavurderingsverktøy kan brukes med mål om å replikere resultater mellom laboratorier. Rapportering av cellekilder, cellekulturprosedyrer og EV-isolasjonsmetoder er viktige faktorer for å definere kvalitetene til EV-befolkningen. Blant NTA-instrumenter gjør faktorer som deteksjonsinnstillinger, brytningsindeksen for bærervæske, heterogene partikkelpopulasjoner som bidrar til polydispersitet, mangel på standardiserte rapporteringskrav og fraværende intra- og interobservatørmålingsresultater NTA-sammenligning mellom laboratorier vanskelig eller umulig.
I bruk siden 2006 er NTA en populær metode for nanopartikkelstørrelse og konsentrasjonsbestemmelse som i dag brukes av omtrent 80% av EV-forskere4. MISEV2018-retningslinjene krever to former for enkelt vesicle-analyse, hvorav NTA er et av de populære alternativene. NTA fortsetter å være i vanlig bruk for EV-karakterisering på grunn av sin brede tilgjengelighet, lave kostnader per prøve og dens enkle grunnteori (Stokes-Einstein-ligningen). EV-vurdering fra NTA genererer en partikkelstørrelsesfordeling og konsentrasjonsestimat ved hjelp av laserlysspredning og Brownian bevegelsesanalyse, med den nedre grensen for deteksjon bestemt av den brytningsindeksen til EV. Ved bruk av en væskeprøve av kjent viskositet og temperatur spores banene til ELBIL-ene for å bestemme deres gjennomsnittlige firkantede forskyvning i to dimensjoner. Dette gjør at partikkeldiffusjonskoeffisienten kan beregnes og omdannes til en sfæreekvivalent hydrodynamisk diameter ved en modifisert Stokes-Einstein-ligning 5,6,7. NTA’s partikkel-til-partikkelanalyse har mindre interferens ved agglomerater eller større partikler i en heterogen populasjon av elbiler enn andre karakteriseringsmetoder7. Mens noen få større partikler har minimal innvirkning på størrelsesnøyaktigheten, resulterer tilstedeværelsen av jevne minuttmengder med store, høye lysspredningspartikler i en merkbar reduksjon i påvisning av mindre partikler på grunn av redusert programvare EV-deteksjon og sporing8. Som måleteknikk anses NTA generelt ikke å være partisk mot større partikler eller aggregater av partikler, men kan løse flere størrelser gjennom individuell partikkelanalyse9. På grunn av bruk av lysspredning av partikler, er en av begrensningene ved NTA-analyse at eventuelle partikler som støv, plast eller pulver med lignende brytning og størrelsesattributter sammenlignet med elbiler ikke kan skilles fra faktiske elbiler ved denne karakteriseringsmetoden.
NanoSight LM10 (nanopartikkelstørrelsesanalysator) og LM14 (lasermodul) har blitt solgt siden 2006, og selv om nyere modeller av dette instrumentet er utviklet, finnes denne modellen i mange kjerneanlegg og regnes som en pålitelig arbeidshest. Opplæring er nødvendig for å optimalisere NTA-innstillingene riktig for høyoppløselige målinger av størrelse og konsentrasjon. De to viktige innstillingene som trengs for optimale videoopptak er (1) kameranivået og (2) deteksjonsterskelen. Disse må angis av operatøren basert på utvalgets egenskaper. En av de viktigste begrensningene ved NTA-analyse er anbefalingen av prøvekonsentrasjoner mellom 107 og 109 partikler/ml, for å oppnå denne prøvefortynning kan være nødvendig10. Løsninger som brukes til fortynning, som fosfatbufret saltvann, 0,15 M saltvann eller ultrarent vann, er sjelden fri for partikler som er mindre enn 220 μm i størrelse, noe som kan påvirke NTA-målingene. NTA-karakterisering av løsningene som brukes til fortynning, bør utføres på samme kameranivå og deteksjonsterskel som nanopartikkelprøvene som analyseres. Størrelsen og konsentrasjonen av nanopartikler tilstede i fortynningsstoffer som brukes til EV-prøvefortynning er sjelden inkludert i publikasjoner som involverer NTA-analyse av elbiler.
Denne protokollen bruker NTA-analyse av syntetiske EV-lignende liposomer evaluert ved hjelp av utvalgte kameranivåer, deteksjonsterskler og mekanisk filtrering av prøvene for å analysere de systematiske effektene av kameranivå, deteksjonsterskel eller prøvefiltrering på NTA-datasettet. Liposomer ble syntetisert som beskrevet i Supplemental File S1. Syntetiske liposomer ble brukt i dette eksperimentet på grunn av deres størrelse ensartethet, fysiske egenskaper og stabilitet i lagring ved 4 °C. Selv om faktiske prøver av elbiler kunne ha blitt brukt, kan heterogeniteten og stabiliteten til elbiler under lagring ha komplisert denne studien og dens tolkning. Likheter i NTA-rapportene fra (A) liposomer og (B) elbiler tyder på at de systematiske effektene som avdekkes for liposomer i dette papiret, sannsynligvis også vil gjelde for EV-karakterisering (figur 1). Sammen støtter disse funnene forestillingen om at fullstendig rapportering av kritiske programvareinnstillinger og beskrivelsen av prøvebehandling, for eksempel fortynning, fortynning og filtrering, påvirker reproduserbarheten av NTA-data.
Formålet med dette dokumentet er å demonstrere at varierende NTA-innstillinger (temperatur, kameranivå og deteksjonsterskel) og prøvepreparering endrer resultatene som samles inn: systematiske, betydelige forskjeller i størrelse og konsentrasjon ble oppnådd. Siden NTA er et av de populære alternativene for å oppfylle MISEV2018-karakteriseringsspesifikasjonen, viser disse resultatene viktigheten av å rapportere prøvepreparering og NTA-innstillinger for å sikre reproduserbarhet.
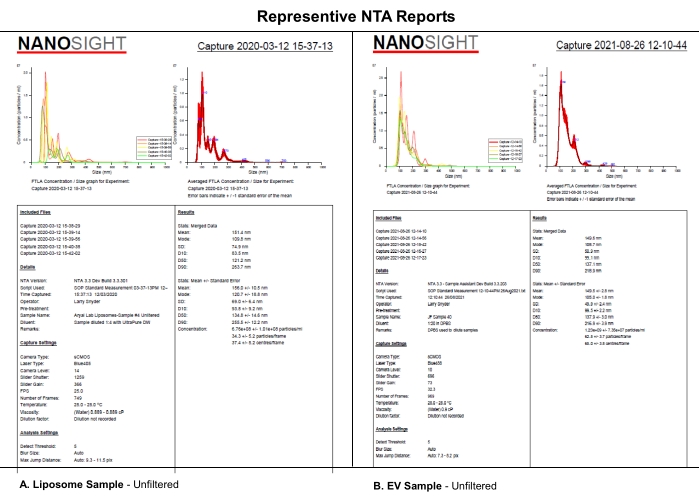
Figur 1: Representative NTA-rapporter for å sammenligne liposomer med elbiler. (A) Liposomer: ufiltrert prøve karakterisert på NTA 12. (B) Elbiler: ufiltrert prøve karakterisert på NTA 26. Forkortelser: NTA = Nanopartikkelsporingsanalyse; Elbiler = ekstracellulære vesicles. Klikk her for å se en større versjon av denne figuren.
Protocol
Representative Results
Discussion
Det finnes flere metoder for å estimere størrelsen og konsentrasjonen av nanopartikler11. Disse inkluderer ensemblemetoder som genererer et størrelsesestimat fra en populasjon, inkludert dynamisk lysspredning (DLS), sentrifugalsedimentering og analyse-elektronmikroskopi på enkeltpartikkelnivå, NTA, mikroskopi og justerbar resistiv pulsmåling. Av disse er DLS og NTA mye brukt, ikke-ødeleggende størrelse og konsentrasjonsmålingsmetoder, basert på brownsk bevegelse i et ideelt medium. DLS e…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Arbeidet ble støttet av staten Kansas til Midwest Institute for Comparative Stem Cell Biology (MICSCB), Johnson Cancer Research Center til MLW og NIH R21AG066488 til LKC. OLS mottok GRA-støtte fra MICSCB. Forfatterne takker Dr. Santosh Aryal for å ha gitt liposomene som brukes i dette prosjektet og medlemmene av Weiss- og Christenson-laboratoriene for nyttige samtaler og tilbakemeldinger. Dr. Hong Han er takket for teknisk støtte. MLW takker Betti Goren Weiss for hennes støtte og råd.
Materials
| Automatic Pipetter | |||
| Centrifuge Tubes, Conical, Nunc 15 mL | Thermo Sci. | 339650 | |
| Kimwipes | |||
| Lens Cleaner | |||
| Lens Paper | |||
| NanoSight LM-10 | Malvern Panalytical | ||
| NanoSight LM-14 Laser Module | Malvern Panalytical | ||
| Nanosight NTA Software Ver. 3.2 | Malvern Panalytical | ||
| Paper Towels | |||
| Pipette Tips, 1-200 µL, Filtered, Sterile, Low Binding | BioExpress | P -3243-200X | |
| Pipette Tips, 50-1,000 µL, Filtered, Sterile | BioExpress | P-3243-1250 | |
| Saline, Dulbecco's Phosphate Buffered (No Ca or Mg) | Gibco | 14190-144 | |
| Standards, Latex Transfer- 100 nm (3 mL) | Malvern | NTA4088 | |
| Standards, Latex Transfer- 50 nm (3 mL) | Malvern | NTA4087 | |
| Syringe Filter, 33 mm, .22 µm, MCE, Sterile | Fisher brand | 09-720-004 | |
| Syringe, TB, 1 mL, slip tip | Becton Dickinson | 309659 | |
| Waste fluid container |
References
- Lotvall, J., et al. Minimal experimental requirements for definition of extracellular vesicles and their functions: a position statement from the International Society for Extracellular Vesicles. Journal of Extracellular Vesicles. 3 (1), (2014).
- Thery, C., et al. Minimal information for studies of extracellular vesicles 2018 (MISEV2018): a position statement of the International Society for Extracellular Vesicles and update of the MISEV2014 guidelines. Journal of Extracellular Vesicles. 7 (1), 1535750 (2018).
- Consortium, E. -. T., et al. EV-TRACK: transparent reporting and centralizing knowledge in extracellular vesicle research. Nature Methods. 14 (3), 228-232 (2017).
- Gardiner, C., et al. Techniques used for the isolation and characterization of extracellular vesicles: results of a worldwide survey. Journal of Extracellular Vesicles. 5, 32945 (2016).
- Maas, S. L., et al. Possibilities and limitations of current technologies for quantification of biological extracellular vesicles and synthetic mimics. Journal of Controlled Release. 200, 87-96 (2015).
- Danaei, M., et al. Impact of particle size and polydispersity index on the clinical applications of lipidic nanocarrier systems. Pharmaceutics. 10 (2), 57 (2018).
- Kestens, V., Bozatzidis, V., De Temmerman, P. J., Ramaye, Y., Roebben, G. Validation of a particle tracking analysis method for the size determination of nano- and microparticles. Journal of Nanoparticle Research. 19 (8), 271 (2017).
- Filipe, V., Hawe, A., Jiskoot, W. Critical evaluation of nanoparticle tracking analysis (NTA) by NanoSight for the measurement of nanoparticles and protein aggregates. Pharmaceutical Research. 27 (5), 796-810 (2010).
- Hole, P., et al. Interlaboratory comparison of size measurements on nanoparticles using nanoparticle tracking analysis (NTA). Journal of Nanoparticle Research. 15 (12), 2101 (2013).
- Malvern analytical Ltd. . NanoSight LM10 Operating Manual-P550H. , (2013).
- Kim, A., Ng, W. B., Bernt, W., Cho, N. J. Validation of size estimation of nanoparticle tracking analysis on polydisperse macromolecule assembly. Scientific Reports. 9 (1), 2639 (2019).
- Gollwitzer, C., et al. A comparison of techniques for size measurement of nanoparticles in cell culture medium. Analytical Methods. 8 (26), 5272-5282 (2016).
- vander Pol, E., et al. Particle size distribution of exosomes and microvesicles determined by transmission electron microscopy, flow cytometry, nanoparticle tracking analysis, and resistive pulse sensing. Journal of Thrombosis and Haemostasis. 12 (7), 1182-1192 (2014).

