Förbättra reproducerbarheten för att möta minimal information för studier av extracellulära vesiklar 2018 riktlinjer i nanopartikelspårningsanalys
Summary
Nanopartikelspårningsanalys (NTA) är en allmänt använd metod för att karakterisera extracellulära vesiklar. Detta dokument belyser NTA-experimentella parametrar och kontroller plus en enhetlig metod för analys och karakterisering av prover och utspädningsmedel som är nödvändiga för att komplettera de riktlinjer som föreslås av MISEV2018 och EV-TRACK för reproducerbarhet mellan laboratorier.
Abstract
Nanopartikelspårningsanalys (NTA) har varit en av flera karakteriseringsmetoder som används för forskning om extracellulär vesikel (EV) sedan 2006. Många anser att NTA-instrument och deras mjukvarupaket enkelt kan användas efter minimal utbildning och att storlekskalibrering är möjlig internt. Eftersom både NTA-förvärv och mjukvaruanalys utgör EV-karakterisering behandlas de i Minimal Information for Studies of Extracellular Vesicles 2018 (MISEV2018). Dessutom har de övervakats av Transparent Reporting and Centralizing Knowledge in Extracellular Vesicle Research (EV-TRACK) för att förbättra robustheten hos EV-experiment (t.ex. minimera experimentell variation på grund av okontrollerade faktorer).
Trots ansträngningar för att uppmuntra rapportering av metoder och kontroller misslyckas många publicerade forskningsartiklar med att rapportera kritiska inställningar som behövs för att reproducera de ursprungliga NTA-observationerna. Få artiklar rapporterar NTA-karakteriseringen av negativa kontroller eller utspädningsmedel, uppenbarligen förutsatt att kommersiellt tillgängliga produkter, såsom fosfatbuffrad saltlösning eller ultrarent destillerat vatten, är partikelfria. På samma sätt rapporteras positiva kontroller eller storleksstandarder sällan av forskare för att verifiera partikelstorlek. Stokes-Einstein-ekvationen innehåller provviskositet och temperaturvariabler för att bestämma partikelförskjutning. Att rapportera den stabila laserkammartemperaturen under hela provvideoinsamlingen är därför en viktig kontrollåtgärd för korrekt replikering. Filtrering av prover eller utspädningsmedel rapporteras inte heller rutinmässigt, och i så fall ingår sällan filtrets detaljer (tillverkare, membranmaterial, porstorlek) och lagringsförhållanden. International Society for Extracellular Vesicle (ISEV) minimala standarder för acceptabla experimentella detaljer bör innehålla ett väldokumenterat NTA-protokoll för karakterisering av elbilar. Följande experiment ger bevis för att ett NTA-analysprotokoll måste upprättas av den enskilda forskaren och inkluderas i metoderna för publikationer som använder NTA-karakterisering som ett av alternativen för att uppfylla MISEV2018-kraven för enstaka vesiklarakterisering.
Introduction
Noggrann och repeterbar analys av elbilar och andra partiklar i nanometerskala utgör många utmaningar inom forskning och industri. Replikering av EV-forskning har varit svårt, delvis på grund av bristen på enhetlighet i rapporteringen av nödvändiga parametrar i samband med datainsamling. För att ta itu med dessa brister föreslog ISEV branschriktlinjer som en minimal uppsättning biokemiska, biofysiska och funktionella standarder för EV-forskare och publicerade dem som ett ställningstagande, vanligen kallat MISEV20141. Den accelererande takten i EV-forskningen krävde en uppdaterad riktlinje, och “MISEV2018: a position statement of the ISEV” utvidgade MISEV2014-riktlinjerna2. MISEV2018-papperet innehöll tabeller, konturer av föreslagna protokoll och steg att följa för att dokumentera specifik EV-associerad karakterisering. Som en ytterligare åtgärd för att underlätta tolkning och replikering av experiment utvecklades EV-TRACK som en crowdsourcing-kunskapsbas (http://evtrack.org) för att möjliggöra en mer transparent rapportering av EV-biologi och den metod som används för publicerade resultat3. Trots dessa rekommendationer för standardiserad rapportering av metoder fortsätter fältet att lida när det gäller replikering och bekräftelse av publicerade resultat.
I överensstämmelse med National Institutes of Healths och National Science Foundations ansträngningar för kvalitetsbedömningsverktyg, föreslår detta dokument att ISEV kräver standardiserad rapportering av metoder och detaljer så att databedömningsverktyg kan tillämpas med målet att replikera resultat mellan laboratorier. Rapportering av cellkällor, cellodlingsförfaranden och EV-isoleringsmetoder är viktiga faktorer för att definiera EV-populationens egenskaper. Bland NTA-instrument gör faktorer som detektionsinställningar, brytningsindex för bärarvätska, heterogena partikelpopulationer som bidrar till polydispersitet, brist på standardiserade rapporteringskrav och frånvarande mätresultat inom och mellan observatörer NTA-jämförelse mellan laboratorier svår eller omöjlig.
NTA har använts sedan 2006 och är en populär metod för nanopartikelstorlek och koncentrationsbestämning som för närvarande används av cirka 80% av EV-forskarna4. MISEV2018-riktlinjerna kräver två former av en-vesiklaranalys, varav NTA är ett av de populära alternativen. NTA fortsätter att vara i allmänt bruk för EV-karakterisering på grund av dess breda tillgänglighet, låga kostnad per prov och dess enkla grundteori (Stokes-Einstein-ekvationen). EV-bedömning av NTA genererar en partikelstorleksfördelning och koncentrationsuppskattning med hjälp av laserljusspridning och brunisk rörelseanalys, med den nedre detektionsgränsen bestämd av EV: s brytningsindex. Vid användning av ett vätskeprov med känd viskositet och temperatur spåras EV: s banor för att bestämma deras genomsnittliga kvadratiska förskjutning i två dimensioner. Detta gör att partikeldiffusionskoefficienten kan beräknas och omvandlas till en sfärekvivalent hydrodynamisk diameter med en modifierad Stokes-Einstein-ekvation 5,6,7. NTA:s partikel-till-partikelanalys har mindre interferens av agglomerat eller större partiklar i en heterogen population av elbilar än andra karakteriseringsmetoder7. Medan några större partiklar har minimal inverkan på storleksnoggrannheten, resulterar närvaron av jämna små mängder stora, höga ljusspridningspartiklar i en anmärkningsvärd minskning av detekteringen av mindre partiklar på grund av minskad programvara EV-detektering och spårning8. Som mätteknik anses NTA i allmänhet inte vara partisk mot större partiklar eller aggregat av partiklar utan kan lösa populationer av flera storlekar genom individuell partikelanalys9. På grund av användningen av ljusspridning av partiklar är en av begränsningarna med NTA-analys att alla partiklar som damm, plast eller pulver med liknande brytnings- och storleksattribut jämfört med elbilar inte kan särskiljas från faktiska elbilar med denna karakteriseringsmetod.
NanoSight LM10 (nanopartikelstorleksanalysator) och LM14 (lasermodul) har sålts sedan 2006, och även om nyare modeller av detta instrument har utvecklats, finns just denna modell i många kärnanläggningar och anses vara en pålitlig arbetshäst. Utbildning behövs för att korrekt optimera NTA-inställningarna för högupplösta mätningar av storlek och koncentration. De två viktiga inställningar som behövs för optimala videoinspelningar är (1) kameranivån och (2) detekteringströskeln. Dessa måste fastställas av operatören på grundval av provets egenskaper. En av de största begränsningarna med NTA-analys är rekommendationen av provkoncentrationer mellan 107 och 109 partiklar/ml, för att uppnå detta kan provutspädning krävas10. Lösningar som används för utspädning, såsom fosfatbuffrad saltlösning, 0,15 M saltlösning eller ultrarent vatten, är sällan fria från partiklar som är mindre än 220 μm stora, vilket kan påverka NTA-mätningarna. NTA-karakterisering av de lösningar som används för utspädning bör utföras på samma kameranivå och detektionströskel som de nanopartikelprover som analyseras. Storleken och koncentrationen av nanopartiklar som finns i utspädningsmedel som används för ev-provutspädningar ingår sällan i publikationer som involverar NTA-analys av elfordon.
Detta protokoll använder NTA-analys av syntetiska EV-liknande liposomer utvärderade med hjälp av utvalda kameranivåer, detektionströsklar och mekanisk filtrering av proverna för att analysera de systematiska effekterna av kameranivå, detektionströskel eller provfiltrering på NTA-datasetet. Liposomer syntetiserades enligt beskrivningen i tilläggsfil S1. Syntetiska liposomer användes i detta experiment på grund av deras storleksenhetlighet, fysiska egenskaper och stabilitet vid lagring vid 4 ° C. Även om faktiska prover av elbilar kunde ha använts, kan heterogeniteten och stabiliteten hos elbilar under lagring ha komplicerat denna studie och dess tolkning. Likheter i NTA-rapporterna från (A) liposomer och (B) EVs indikerar att de systematiska effekterna som avslöjas för liposomer i detta papper sannolikt också kommer att gälla för EV-karakterisering (Figur 1). Tillsammans stöder dessa resultat uppfattningen att fullständig rapportering av kritiska programvaruinställningar och beskrivningen av provbehandling, såsom utspädningsmedel, utspädning och filtrering, påverkar reproducerbarheten av NTA-data.
Syftet med detta dokument är att visa att varierande NTA-inställningar (temperatur, kameranivå och detektionströskel) och provberedning förändrar de insamlade resultaten: systematiska, signifikanta skillnader i storlek och koncentration erhölls. Eftersom NTA är ett av de populära alternativen för att uppfylla MISEV2018-karakteriseringsspecifikationen, visar dessa resultat vikten av att rapportera provberedning och NTA-inställningar för att säkerställa reproducerbarhet.
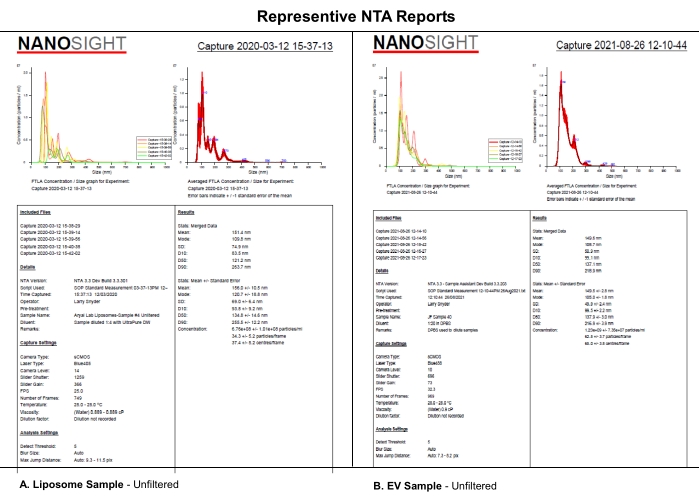
Figur 1: Representativa NTA-rapporter för att jämföra liposomer med elbilar. A) Liposomer: ofiltrerat prov som karakteriseras på NTA den 12 mars 2020. (B) Elfordon: ofiltrerat prov som karakteriserades på NTA den 26 augusti 2021. Förkortningar: NTA = Nanopartikelspårningsanalys; EVs = extracellulära vesiklar. Klicka här för att se en större version av denna figur.
Protocol
Representative Results
Discussion
Det finns flera metoder tillgängliga för att uppskatta storleken och koncentrationen av nanopartiklar11. Dessa inkluderar ensemblemetoder som genererar en storleksuppskattning från en population, inklusive dynamisk ljusspridning (DLS), centrifugalsedimentering och enpartikelnivåanalys-elektronmikroskopi, NTA, atomkraftsmikroskopi och avstämbar resistiv pulsavkänning. Av dessa används DLS och NTA i stor utsträckning, icke-destruktiva storleks- och koncentrationsmätningsmetoder, baserade p?…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Arbetet stöddes av delstaten Kansas till Midwest Institute for Comparative Stem Cell Biology (MICSCB), Johnson Cancer Research Center till MLW och NIH R21AG066488 till LKC. OLS fick GRA-stöd från MICSCB. Författarna tackar Dr. Santosh Aryal för att ha tillhandahållit liposomerna som används i detta projekt och medlemmarna i Weiss och Christenson-laboratorierna för hjälpsamma samtal och feedback. Dr. Hong Han tackas för teknisk support. MLW tackar Betti Goren Weiss för hennes stöd och råd.
Materials
| Automatic Pipetter | |||
| Centrifuge Tubes, Conical, Nunc 15 mL | Thermo Sci. | 339650 | |
| Kimwipes | |||
| Lens Cleaner | |||
| Lens Paper | |||
| NanoSight LM-10 | Malvern Panalytical | ||
| NanoSight LM-14 Laser Module | Malvern Panalytical | ||
| Nanosight NTA Software Ver. 3.2 | Malvern Panalytical | ||
| Paper Towels | |||
| Pipette Tips, 1-200 µL, Filtered, Sterile, Low Binding | BioExpress | P -3243-200X | |
| Pipette Tips, 50-1,000 µL, Filtered, Sterile | BioExpress | P-3243-1250 | |
| Saline, Dulbecco's Phosphate Buffered (No Ca or Mg) | Gibco | 14190-144 | |
| Standards, Latex Transfer- 100 nm (3 mL) | Malvern | NTA4088 | |
| Standards, Latex Transfer- 50 nm (3 mL) | Malvern | NTA4087 | |
| Syringe Filter, 33 mm, .22 µm, MCE, Sterile | Fisher brand | 09-720-004 | |
| Syringe, TB, 1 mL, slip tip | Becton Dickinson | 309659 | |
| Waste fluid container |
References
- Lotvall, J., et al. Minimal experimental requirements for definition of extracellular vesicles and their functions: a position statement from the International Society for Extracellular Vesicles. Journal of Extracellular Vesicles. 3 (1), (2014).
- Thery, C., et al. Minimal information for studies of extracellular vesicles 2018 (MISEV2018): a position statement of the International Society for Extracellular Vesicles and update of the MISEV2014 guidelines. Journal of Extracellular Vesicles. 7 (1), 1535750 (2018).
- Consortium, E. -. T., et al. EV-TRACK: transparent reporting and centralizing knowledge in extracellular vesicle research. Nature Methods. 14 (3), 228-232 (2017).
- Gardiner, C., et al. Techniques used for the isolation and characterization of extracellular vesicles: results of a worldwide survey. Journal of Extracellular Vesicles. 5, 32945 (2016).
- Maas, S. L., et al. Possibilities and limitations of current technologies for quantification of biological extracellular vesicles and synthetic mimics. Journal of Controlled Release. 200, 87-96 (2015).
- Danaei, M., et al. Impact of particle size and polydispersity index on the clinical applications of lipidic nanocarrier systems. Pharmaceutics. 10 (2), 57 (2018).
- Kestens, V., Bozatzidis, V., De Temmerman, P. J., Ramaye, Y., Roebben, G. Validation of a particle tracking analysis method for the size determination of nano- and microparticles. Journal of Nanoparticle Research. 19 (8), 271 (2017).
- Filipe, V., Hawe, A., Jiskoot, W. Critical evaluation of nanoparticle tracking analysis (NTA) by NanoSight for the measurement of nanoparticles and protein aggregates. Pharmaceutical Research. 27 (5), 796-810 (2010).
- Hole, P., et al. Interlaboratory comparison of size measurements on nanoparticles using nanoparticle tracking analysis (NTA). Journal of Nanoparticle Research. 15 (12), 2101 (2013).
- Malvern analytical Ltd. . NanoSight LM10 Operating Manual-P550H. , (2013).
- Kim, A., Ng, W. B., Bernt, W., Cho, N. J. Validation of size estimation of nanoparticle tracking analysis on polydisperse macromolecule assembly. Scientific Reports. 9 (1), 2639 (2019).
- Gollwitzer, C., et al. A comparison of techniques for size measurement of nanoparticles in cell culture medium. Analytical Methods. 8 (26), 5272-5282 (2016).
- vander Pol, E., et al. Particle size distribution of exosomes and microvesicles determined by transmission electron microscopy, flow cytometry, nanoparticle tracking analysis, and resistive pulse sensing. Journal of Thrombosis and Haemostasis. 12 (7), 1182-1192 (2014).

