In vitro - och in vivo-utvärdering av fotokontrollerade biologiskt aktiva substanser - potentiella läkemedelskandidater för cancerfotofarmakologi
Summary
Detta protokoll presenterar en uppsättning experiment som antagits för utvärdering av fotoswitchbara anticancerpeptider, som kan användas vid preklinisk screening av sådana föreningar. Detta inkluderar cytotoxicitetsbedömning i 2D- och 3D-cellkulturer, utvärdering av fotoisomeriseringseffektivitet ex vivo (modellvävnad) och in vivo-effekt .
Abstract
Fotokontrollerade, biologiskt aktiva substanser är en framväxande klass av “smarta” läkemedelskandidater. De ger ytterligare säkerhet vid systemisk kemoterapi på grund av deras exakta spatiotemporala aktivering genom att rikta ett godartat, icke-joniserbart ljus till en specifik plats i patientens kropp. Denna artikel presenterar en uppsättning metoder för att utvärdera in vitro-potensen och ex vivo-effektiviteten av fotoaktivering av fotokontrollerade, biologiskt aktiva föreningar samt in vivo-effekten i tidiga stadier av läkemedelsutveckling. Metoden tillämpas på cytotoxiska peptider mot cancer, nämligen de diaryleteninnehållande analogerna av ett känt antibiotikum, gramicidin S. Experimenten utförs med användning av 2D (vidhäftande celler) och 3D (sfäroider) cellkulturer av en cancercellinje (Lewis lungkarcinom, LLC), levande vävnadsurrogat (fläskköttfärs) och en allograftcancermodell (subkutan LLC) i immunkompetenta möss. Valet av de mest effektiva föreningarna och uppskattningen av realistiska fototerapeutiska fönster utförs via automatiserad fluorescensmikroskopi. Fotoaktiveringseffektiviteten vid varierande belysningsregimer bestäms på olika djup i en modellvävnad, och den optimala ljusdosen appliceras i det slutliga terapeutiska in vivo-experimentet .
Introduction
Fotokontrollerade biologiskt aktiva föreningar har uppstått under de senaste decennierna som en lovande komponent i säkra kemoterapier för mänskliga sjukdomar och för att specifikt utrota maligna solida tumörer1. Dessa föreningar innehåller reversibelt fotoisomerbara fragment (molekylära fotoswitchar) och kan växla mellan inaktiva och aktiva fotoisomerer vid bestrålning med ljus av olika våglängder.
Jämfört med deras icke-fotokontrollerbara analoger kan fotokontrollerade läkemedel vara säkrare eftersom de systemiskt kan införas i patientens kropp i mindre aktiva och väsentligen icke-toxiska former och aktiveras sedan av ljus endast vid behov, såsom i tumörer, sår och sår. Även om flera spännande demonstrationer av sådana molekylära läkemedelsprototyper kan hittas i de senaste akademiska artiklarna 2,3,4,5,6,7, existerar inte fältet klinisk fotofarmakologi – en tillämpning av godkända kombinationer av läkemedel / medicinsk utrustning / sjukdom. Fotofarmakologi är ännu i läkemedelsupptäcktsstadiet, och systematiska prekliniska studier är okända.
Vi visade nyligen säkerhetsfördelen in vivo för vissa fotokontrollerade cancerpeptider, nämligen analogerna till peptidantibiotikumet gramicidin S8. Dessa fotokontrollerade derivat innehåller en diaryleten (DAE) fotoswitch, som genomgår reversibla fotoinducerade transformationer mellan de så kallade röda ljusgenererade “ringöppna” och UV-genererade “ringstängda” fotoformerna (illustrerad i figur 1 för ett av derivaten, förening LMB002).
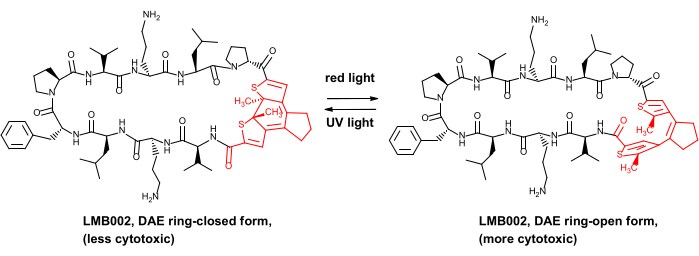
Figur 1: Fotokontrollerad cytotoxisk peptid LMB002 och dess fotoisomerisering. Dagbokletenfragmentet visas i rött. Förkortning: DAE = diaryleten. Klicka här för att se en större version av denna figur.
Att hitta träffar och utföra hit-to-lead-optimering kräver ofta in vitro– och in vivo-screening av lämpliga föreningsbibliotek 9,10. Här demonstrerar vi en metodik som lämpar sig för systematisk high-throughput screening av cytotoxicitet hos fotokontrollerade substanser. Vi bestämmer också fotoisomeriseringseffektiviteten, uppskattar ljusdosen i modellvävnader och utvärderar in vivo-effekten hos de bäst presterande kandidaterna. Tillvägagångssättet är förenligt med bioetik och djurvård.
I detta arbete modifieras traditionella prekliniska metoder för att undvika okontrollerad fotoisomerisering av testade substanser. Det övergripande målet med att tillämpa dessa modifierade metoder här är att utveckla en allmän strategi som är enkel och snabb och ger statistiskt signifikanta data för att på ett tillförlitligt sätt jämföra in vitro-aktiviteter och rationalisera in vivo-effektivitetstestningen av fotoswitchbara föreningar för blyidentifiering och vidareutveckling.
Strategin består av tre på varandra följande steg. Det första steget innefattar bestämning av IC 50 (skenbar50 % cellviabilitet) i serieutspädningar för aktiva och inaktiva fotoformer av utvalda fotokontrollerade biologiskt aktiva föreningar med användning av tvådimensionella (2D, monolager) och tredimensionella (3D, sfäroid) cellkulturer och konfokal automatiserad fluorescensmikroskopi med hög genomströmning. Fototerapeutiska fönster jämförs med avseende på IC50-skillnaden mellan de två fotoformerna, och de bäst presterande kandidaterna väljs. Det finns ingen specifik fördel med toxicitetsbedömning med hjälp av automatiserad mikroskopi och andra plattformar för screening av cytotoxicitet (assays)11. Mer komplexa cellbaserade tumörmodeller12 skulle lätt kunna implementeras i detta skede.
För de föreningar som valts ut i steg 1 är det andra steget att realistiskt uppskatta deras fotoväxlingseffektivitet inuti vävnaderna som en funktion av djupet från den bestrålade vävnadsytan genom att kvantifiera fotoväxlingseffektiviteten hos de mindre aktiva fotoformerna i ett vävnadsurrogat med hjälp av UV-detekterad högpresterande vätskekromatografi (HPLC) av bestrålade provextrakt. In vivo kan fotoväxlingseffektivitet studeras, men vi föreslår att man använder ett enkelt vävnadsurrogat – fläskfärskött. Vi har testat giltigheten av detta tillvägagångssätt. Vi mätte omvandlingen av våra fotoswitchbara föreningar in vivo på en muscancermodell och observerade ungefär samma fotokonvertering på ett djup uppmätt i tidigare experiment med möss8. Alla lämpliga alternativa konstgjorda vävnader13, 3D-bioprintade vävnader/organ14, biopsimaterial eller annat undantaget animaliskt material kan användas. Denna inställning är dock en bra kompromiss eftersom den är ekonomisk, snabb och etisk.
Det tredje steget är bestämningen av in vivo anticancereffekt i en murin cancermodell. De föreningar som uppvisar överlägsna egenskaper i in vitro-experimenten och effektivt fotoväxlar på ett djup av minst 1-1,5 cm i modellvävnaderna väljs ut för detta experiment.
Detta protokoll kan tillämpas på föreningar som har olika typer av fotoswitchar, förutsatt att deras fotoformer (eller deras fotostationära tillstånd, PSS) är stabila under en rimlig tid (några dagar eller längre). Som illustration används en tidigare beskriven DAE-härledd LMB00215. LMB002-fotoformerna är termiskt stabila och kan lagras vid −20 °C i minst ett år utan väsentlig nedbrytning. Lewis lungkarcinom (LLC) -celler väljs för denna in vitro- och in vivo-demonstration, men inga begränsningar införs för celltypen. LLC-celler är vidhäftande, lätt odlingsbara i 3D och används för att generera tumöroider (som beskrivs i referens16). In vivo LLC-celler används för att modellera metastatiska processer och kan lätt generera solida tumörer hos immunkompetenta möss efter subkutan injektion. Denna in vivo-metod kan tillämpas universellt på andra cancermodeller17,18. Det detaljerade genomförandet av denna strategi beskrivs nedan.
Protocol
Representative Results
Discussion
Fotokontrollerade föreningar saknar motstycke i läkemedelsutveckling; Inga metoder har dock fastställts för deras prekliniska och kliniska utvärdering. Den närmaste monoterapianalogen, fotodynamisk terapi (PDT), är den behandlingsmodalitet för klinisk användning som antagits av många länder mot cancer och är under utveckling för andra indikationer19,20. I likhet med fotofarmakologi är PDT också baserat på användningen av ljus för att aktivera den bioaktiva substansen (singlettsyre). Därför kan vissa experimentella metoder som används för prekliniska och kliniska studier i PDT antas för fotofarmakologi. Till exempel är ljuskällor, ljusleveransmetoder och medicintekniska produkter välutvecklade och godkända för PDT; De kan användas direkt för utvärdering av fotokontrollerade läkemedel. PDT och fotofarmakologi har emellertid många skillnader från varandra4, vilket motiverar behovet av att fastställa specifika metoder för den senare.
För det första är den icke-aktiverade substansen i PDT (syre) alltid närvarande i levande vävnader vid icke-toxiska koncentrationer. Däremot kan icke-aktiverade fotokontrollerade biologiskt aktiva föreningar ha kvarvarande aktivitet och oönskad toxicitet. Därför bör ideala fotofarmakologiska läkemedel ha minimerat biologisk aktivitet i sin administrerade form och måste vara mycket aktiva i sin ljusgenererade form, det “fototerapeutiska fönstret”21 måste vara så stort som möjligt. Att hitta träffen och utföra hit-to-lead-optimering kräver identifiering av lämpliga föreningar och screening av relativt stora bibliotek, redan i tidiga stadier av läkemedelsutveckling. Här föreslog vi en automatiserad konfokal fluorescerande mikroskopi med hög genomströmning för att identifiera effektiva fotoväxlingsföreningar.
Den valda metoden för utvärdering av cytotoxicitet möjliggör enkel implementering av det mest kritiska kravet – underhåll av PSS eller stabilitet hos den synliga ljuskänsliga fotoisomeren. Detta beror på att ljusexponeringen minimeras vid genomförandet. Därför, om du väljer alternativa metoder, bör automatiserade metoder föredras. Detta tillvägagångssätt är tillförlitligt och informativt. Användningen av 3D-cellkulturer (sfäroider) i detta skede ger en holistisk förståelse för cellens svar på behandlingen i en mer realistisk vävnadsliknande mikromiljö. Dessutom kan värdefulla insikter i föreningarnas verkningsmekanism erhållas med hjälp av mikroskopi som den direkta metoden. Den konfokala fluorescerande mikroskopin med korrekt färgningsprotokoll möjliggör visuell bedömning av cellernas och sfäroidernas morfologi; Viktiga detaljer om celldöd och förändringar inuti cellerna kan också detekteras.
För det andra kräver lätt applicering ett noggrant val av ljusdosering. Vid PDT är lätt överdosering extremt skadlig för vävnader22. Fotofarmakologisk behandling kan vara fördelaktig vid överdriven ljusbestrålning. Den aktiva substansens övre gräns bestäms av den administrerade dosen av den icke-aktiverade substansen och dess farmakokinetik. Emellertid, ljus dosering är fortfarande ett problem i fotofarmakologi. Försiktighet bör iakttas för att säkerställa att bestrålningseffekttätheten och exponeringstiden inte är mindre än kravet för behandlingen. I princip kan genereringen av den aktiverade substansen övervakas in vivo. Av bioetiska skäl föreslog vi dock ett experiment med en modellvävnad (färskt malet kött) blandat med den icke-aktiverade föreningen15. Detta experiment är enkelt och kan modifieras för att använda olika ljuskällor. Den kan också anpassas för fotofysisk uppskattning av ljusdosering och mätning av termisk påverkan. Även här, genom att använda modellvävnader, är ljusexponeringen möjlig att minimera, jämfört med till exempel den mer exakta fotoswitchningseffektivitetsbestämningen i in vivo-förhållandena , ett alternativ som alltid kan vara intressant att överväga.
Slutligen kan de föreningar som uppvisar överlägsna egenskaper i in vitro-toxicitetsskärmarna och effektivt fotoväxlar minst 1-1,5 cm djupt i modellvävnaden väljas för kostsamma, mödosamma och långa in vivo-studier. I detta protokoll använde vi samma cellinje (LLC) som i in vitro-bedömningen för att generera allograftcancermodellen. Tumörtillväxtdynamiken, dödligheten och antalet metastaser är de parametrar som är mest lämpade för att bedöma effekten mot cancer. Jämfört med konventionell kemoterapi appliceras en ytterligare faktor i den fotofarmakologiska behandlingen – ljuset. Därför behövs två kontrolldjurgrupper: en som endast tar emot fordonet och den andra som tar emot fordonet och bestrålning. Denna inställning möjliggör utvärdering av ljusets inverkan på de uppmätta parametrarna. I vårt experiment mottog djuren i de två experimentgrupperna den icke-aktiverade föreningen, och tumörerna hos mössen i en grupp bestrålades. Bestrålningsregimen var identisk för kontroll- och behandlingsgrupperna. Jämförelse med benchmarkkemoterapi är inte nödvändig i detta skede eftersom huvudsyftet med experimentet är att visa den kombinerade effekten av ljus- och sammansatt applikation. De bäst presterande föreningarna som uppvisar denna effekt kan sedan väljas ut för vidare studier av deras in vivo-toxicitet och jämförelse med riktmärken för att fatta viktiga go-no-go-beslut om deras utveckling. Tekniskt sett kan in vivo-experimentet som vi beskriver enkelt anpassas till farmakokinetiska eller farmakodynamiska studier, till exempel av en förening som redan är vald som läkemedelsledare.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Författarna erkänner EU-finansiering från H2020-MSCA-RISE-programmet genom projekten PELICO (#690973) och ALISE (#101007256). Detta arbete stöddes av DFG-GRK 2039 (SA, TS och ASU), NACIP-programmet för Helmholtz Society (SA och ASU) och VIP+ för BMBF (OB och ASU). Vi erkänner Dr. Serhii Koniev, Karlsruhe Institute of Technology, som har syntetiserat föreningen LMB002, renat den och vänligen tillhandahållit föreningen för studien. Författarna tackar också Chupryna Maksym som filmade och sammanställde videon i Ukraina, och till alla modiga försvarare av Ukraina som gjorde det experimentella arbetet, skrivandet och filmningen av denna publikation möjlig.
Materials
| Agilent 1100 Series capillary LC system | ALSI-Chrom (Agilent distributor) | – | |
| ATCC CRL-1642, LL/2 (LLC1) Lewis lung carcinoma cell line | ECACC | 90020104 | |
| C57BL/6NCrl mice, female, inbred | Charles River | Strain code: 027 | |
| CelCulture, CO2 incubator | Esco Micro | CCL-170B | |
| Corning Matrigel Basement membrane matrix | Merck | CLS354234 | |
| Corning, 384- well spheroid microplates | Merck | CLS3830 | |
| Fetal bovine serum | Merck | F7524 | |
| Gibco, DPBS | Thermo Fisher Scientific | 21600044 | |
| Gramicidin S | Lumobiotics | Custom synthesis | |
| HyClone, DMEM/high glucose | Cytiva | SH30003.04 | |
| IN Cell Analyzer 6500HS, imaging system | Cytiva | 29240358 | |
| Invitrogen, Calcein AM | Thermo Fisher Scientific | C1430 | |
| Isoflurane anesthesia machine | ASA | S/N ASA 1305 | |
| L-glutamine, 200 mM solution | Merck | G7513 | |
| LIKA-surgeon, diode surgery laser | Fotonika plus | – | |
| LMB002 | Lumobiotics | Custom synthesis | |
| Penicillin–Streptomycin, solution stabilized | Merck | P4333 | |
| PhenoPlate, 96-well plates | PerkinElmer | 6055302 | |
| Photometer PCE-LED 20 | PCE Instruments | PCE-LED 20 | |
| Thermo Scientific, Hoechst 33342 | Thermo Fisher Scientific | 62249 | |
| Thermo Scientific, Propidium iodide | Thermo Fisher Scientific | J66764-MC | |
| Trypan blue, 0.4% solution | Merck | T8154 | |
| Trypsin–EDTA, 10 x solution | Merck | T4174 | |
| UltraCruz Cell culture flasks with vented caps, 75 cm2 | Santa Cruz Biotechnology | sc-200263 | |
| UltraCruz, bottle top filters, PES, 0.22 μm | Santa Cruz Biotechnology | sc-360882 | |
| Vydac 218TP, C18 HPLC column (4.6 mm × 250 mm, 5 µm) | Altmann Analytik (Avantor distributor) | GR5103827 |
References
- Fuchter, M. J. On the promise of photopharmacology using photoswitches: a medicinal chemist’s perspective. Journal of Medicinal Chemistry. 63 (20), 11436-11447 (2020).
- Volarić, J., Szymanski, W., Simeth, N. A., Feringa, B. L. Molecular photoswitches in aqueous environments. Chemical Society Reviews. 50, 12377-12449 (2021).
- Paoletti, P., Ellis-Davies, G. C. R., Mourot, A. Optical control of neuronal ion channels and receptors. Nature Reviews Neuroscience. 20, 514-532 (2019).
- Hüll, K., Morstein, J., Trauner, D. In Vivo Photopharmacology. Chemical Reviews. 118 (21), 10710-10747 (2018).
- Ma, X., et al. In vivo photopharmacology with a caged mu opioid receptor agonist drives rapid changes in behavior. Nature Methods. 20, 682-685 (2023).
- Sarabando, S. N., Palmeira, A., Sousa, M. E., Faustino, M. A. F., Monteiro, C. J. P. Photomodulation Approaches to Overcome Antimicrobial Resistance. Pharmaceuticals. 16 (5), 682 (2023).
- Kolarski, D., Szymanski, W., Feringa, B. L., Hirota, T., Hatori, M., Panda, S. Chronophotopharmacology: Methodology for high spatiotemporal control over the circadian rhythm with light. Neuromethods. 186, (2022).
- Babii, O., et al. Peptide drugs for photopharmacology: how much of a safety advantage can be gained by photocontrol. Future Drug Discovery. 2 (1), FDD28 (2020).
- Davis, A. M., Keeling, D. J., Steele, J., Tomkinson, N. P., Tinker, A. C. Components of successful lead generation. Current Topics in Medicinal Chemistry. 5 (4), 421-439 (2005).
- Balani, S. K., Miwa, G. T., Gan, L., Wu, J., Lee, F. W. Strategy of utilizing in vitro and in vivo adme tools for lead optimization and drug candidate selection. Current Topics in Medicinal Chemistry. 5 (11), 1033-1038 (2005).
- Kleijn, A., et al. A Systematic comparison identifies an ATP-based viability assay as most suitable read-out for drug screening in glioma stem-like cells. Stem Cells International. 2016, (2016).
- Rodrigues, J., Heinrich, M. A., Teixeira, L. M., Prakash, J. 3D in vitro model revolution: unveiling tumor-stroma interactions. Trends in Cancer. 7 (3), 249-264 (2021).
- Sittinger, M., et al. Tissue engineering and autologous transplant formation: practical approaches with resorbable biomaterials and new cell culture techniques. Biomaterials. 17 (3), 237-242 (1996).
- Matai, I., Kaur, G., Seyedsalehi, A., McClinton, A., Laurencin, C. T. Progress in 3D bioprinting technology for tissue/organ regenerative engineering. Biomaterials. 226, 119536 (2020).
- Babii, O., et al. Direct photocontrol of peptidomimetics: an alternative to oxygen-dependent photodynamic cancer therapy. Angewandte Chemie International Edition. 55 (18), 5493-5496 (2016).
- De Ridder, K., et al. Novel 3D lung tumor spheroids for oncoimmunological assays. Advanced NanoBiomed Research. 2 (4), 2100124 (2022).
- Pauli, C., et al. Personalized in vitro and in vivo cancer models to guide precision medicine. Cancer Discovery. 7 (5), 462-477 (2017).
- Van Straten, D., Mashayekhi, V., De Bruijn, H. S., Oliveira, S., Robinson, D. J. Oncologic photodynamic therapy: basic principles, current clinical status and future directions. Cancers. 9 (2), 19 (2017).
- Li, X., Kwon, N., Guo, T., Liu, Z., Yoon, J. Innovative strategies for hypoxic-tumor photodynamic therapy. Angewandte Chemie International Edition. 57 (36), 11522-11531 (2018).
- Hull, K., Morstein, J., Trauner, D. In vivo photopharmacology. Chemical Reviews. 118 (21), 10710-10747 (2018).
- Babii, O., et al. Structure-activity relationships of photoswitchable diarylethene-based β-hairpin peptides as membranolytic antimicrobial and anticancer agents. Journal of Medicinal Chemistry. 61 (23), 10793-10813 (2018).
- Heckl, C., Aumiller, M., Rühm, A., Sroka, R., Stepp, H. Fluorescence and treatment light monitoring for interstitial photodynamic therapy. Photochemistry and Photobiology. 96 (2), 388-396 (2020).

