양이온 펩타이드 캐리어의 인트라-연골 수송 특성의 특성화
Summary
이 프로토콜은 연골에서 양이온 펩티드 캐리어에 대한 평형 섭취량, 침투 깊이 및 비 평형 확산 속도를 결정합니다. 운송 특성의 특성화는 효과적인 생물학적 반응을 보장하는 데 중요합니다. 이러한 방법은 음전하 조직을 대상으로 최적의 충전 약물 운반사업자를 설계하는 데 적용될 수 있다.
Abstract
연골과 같은 신체의 여러 부정적 충전 조직은 음전하 아그레칸의 고밀도로 인해 표적 약물 전달에 장벽을 제시하고, 따라서 치료 반응을 높이기 위해 향상된 표적 타겟팅 방법이 필요합니다. 연골은 높은 음의 고정 전하 밀도를 가지고 있기 때문에, 약물은 정전기 상호 작용을 활용하기 위해 양전하 약물 캐리어로 수정 할 수 있습니다, 향상된 연골 약물 수송을 허용. 따라서 약물 운반선의 수송을 연구하는 것은 생물학적 반응을 유도하는 약물의 효능을 예측하는 데 중요합니다. 연골 연동에서 양양 펩티드 운반선의 평형 섭취량, 침투 깊이 및 비평형 확산 속도를 정량화할 수 있는 세 가지 실험의 설계를 보여줍니다. 평형 섭취 실험은 주변 목욕에 비해 연골 내의 용성 농도의 척도를 제공하며, 이는 연골에서 약물의 치료 농도를 향상시키는 데 약물 운반체의 잠재력을 예측하는 데 유용합니다. 공초점 현미경을 이용한 침투 연구의 깊이는 solutes가 그들의 매트릭스 및 세포 표적 사이트에 도달하는지 여부를 평가하는 데 중요한 연골의 깊은 영역에 피상에서 1D solute 확산의 시각적 표현을 허용합니다. 맞춤형 수송 챔버를 이용한 비평형 확산 속도 연구는 조직 전반에 걸쳐 형광으로 표지된 솔루트의 확산 속도를 특성화함으로써 조직 매트릭스와의 결합 상호 작용강도의 측정을 가능하게 한다. 이것은 연골과 최적의 결합 강도의 캐리어를 설계하는 데 도움이됩니다. 함께, 3개의 수송 실험에서 얻은 결과는 약물 전달 애플리케이션을 위한 약하고 가역적인 충전 상호작용을 활용하는 최적으로 충전된 약운반사업자를 설계하기 위한 가이드라인을 제공한다. 이러한 실험적 방법은 또한 약물 및 약물-약물 운반체 컨쥬게이트의 수송을 평가하기 위해 적용될 수 있다. 또한, 이러한 방법은 반월 상 연골, 각막 및 유리체 유머와 같은 다른 부정적인 충전 조직을 대상으로 하는 데 사용할 수 있습니다.
Introduction
본문에 부정적인 충전된 조직에 약물 전달은 세포 및 매트릭스 표적 부위1에도달하기 위해 조직 깊숙이 침투하는 약물의 무능력으로 인해 어려움을 유지하고 있다. 이들 조직 중 일부는 조직 내에서 높은 음전하 고정 전하 밀도(FCD)2를 생성하고 대부분의 거대 분자3,,4의전달을 위한 장벽역할을 하는 조밀하게 포장된 음전하 아그레칸으로 구성된다. 그러나, 양전하 약물 운반선의 도움으로, 이러한 음전하 조직 장벽은 실제로 지속적인 약물전달을위한 정전기 전하 상호작용을 통해 약물 창고로 변환될 수 있다1,5,,6,,7(도 1).
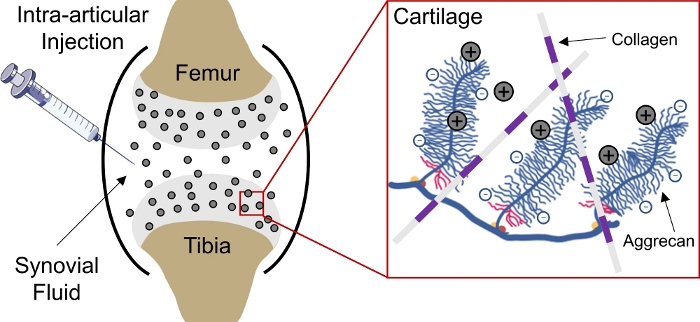
그림 1: CPC의 충전 기반 연골 전달. 무릎 관절 공간에 CPC의 관절 내 주입. 양전하 CPC와 음전하 아그레칸 그룹 간의 정전기 상호 작용은 연골을 통해 신속하고 완전한 깊이 침투를 가능하게 합니다. 이 그림은 Vedadghavami 외4에서수정되었습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
최근에는 단길이 의 양이온 펩티드 캐리어(CC)가 음전하 연골4로전달하기 위해 더 큰 크기의 치료제를 운반할 수 있는 작은 양이온 영역을 만드는 것을 목표로 설계되었다. 골관절염(OA)10과같은만연성8,9 및 퇴행성 질환을 치료하기 위한 연골에 효과적인 약물 전달을 위해서는, 약물의 치료 농도가 조직 내 깊숙이 침투하는 것이 중요하며, 여기서 대부분의 연골세포(chondrocytes)가 놓여 있다.11 몇몇 잠재적인 질병 수정 약유효하더라도, 이들이 효과적으로 연골을 표적으로 할 수 없기 때문에 아무도 FDA 승인을 얻지 못했습니다12,,13. 따라서, 치료 반응을 유도하는 약물의 효과를 예측하기 위해서는 약물 운반선의 수송 성질에 대한 평가가 필요하다. 여기서, 우리는 CPC4의평형 섭취량, 침투 깊이 및 비 평형 확산 속도를 평가하기 위해 활용할 수있는 세 가지 별도의 실험을 설계했습니다.
최적의 치료 반응을 제공할 수 있는 연골 내에 충분한 약물 농도가 있는지 확인하기 위해, 섭취 실험은 연골4에서평형 CPC 농도를 정량화하도록 설계되었다. 이 설계에서는 연골과 주변 목욕 사이의 평형에 따라 연골 내부의 총 솔직량(매트릭스에 결합되거나 프리)을 사용하여 결정할 수 있다. 이 비율은 연골 내부의 솔틸테 농도를 평형 욕조의 농도로 정상화하여 계산됩니다. 원칙적으로 연골을 통한 확산이 전하 상호 작용에 의해 지원되지 않는 중성 솔루트는 1 미만의 섭취 비율을 가질 것입니다. 반대로, 정전기 상호 작용을 통해 운송이 향상된 양이온 솔루트는 1보다 큰 섭취 비율을 보여줍니다. 그러나 CPC와 마찬가지로 최적의 양전하를 사용하면 훨씬 더 높은 흡기 비율(300보다 큰)4를초래할 수 있습니다.
연골 내의 높은 약물 농도는 치료 적 이점을 달성하는 데 중요하지만, 연골의 전체 두께를 통해 약물확산도 중요합니다. 따라서, 단백질과 세포 표적 부위에 도달할 수 있도록 약물이 연골 깊숙이 도달하도록 침투깊이를 보여주는 연구가 요구되어 보다 효과적인 치료법을 제공한다. 이 실험은 연골을 통해 솔틸테의 단방향 확산을 평가하도록 설계되었으며, 생체 내에서 관절 내 주입에 이어 연골으로 약물의 확산을 시뮬레이션합니다. 공초점 현미경 검사를 이용한 형광 화상 진찰은 연골으로 침투의 깊이의 평가를 허용합니다. 순 입자 충전은 심층 약물이 매트릭스를 통해 확산될 수 있는 방법을 조정하는 데 핵심적인 역할을 합니다. 조직 FCD에 기초한 최적의 순 전하는 양이온 입자와 음이온 조직 매트릭스 사이의 약한 가역적 결합 상호 작용을 허용하기 위해 요구된다. 이는 입자가 매트릭스에서 분리할 수 있지만 조직에서 다른 매트릭스 결합 부위에 더 깊이 결합할 수 있도록 모든 상호 작용이 충분히 약하다는 것을의미한다. 반대로, 너무 강한 매트릭스 결합으로 인해 연골의 피상 영역에서 초기 결합 부위에서 입자의 분리를 방지하므로 입자의 과도한 양성 순 전하가 확산쪽으로 해로울 수 있습니다. 이것은 표적 사이트의 대다수가 조직11내 깊은 거짓말로 불충분 한 생물학적 반응을 초래할 것이다.
결합 상호 작용의 강도를 더욱 정량화하기 위해 연골을 통한 약물 확산 률 분석이 유리하다. 비 평형 확산 연구는 다른 솔루트 사이의 실시간 확산 속도의 비교를 허용합니다. 약물이 연골의 피상적, 중간 및 깊은 영역을 통해 확산됨에 따라 결합 상호 작용의 존재는 확산 속도를 크게 변경할 수 있습니다. 결합 상호 작용이 약물과 연골 매트릭스 사이에 존재하는 경우, 효과적인 확산성 (DEFF)로정의됩니다. 이 경우, 일단 모든 결합 부위가 점유되면 약물의 확산 속도는 정상 상태 확산 (DSS)에의해 지배됩니다. 다른 솔루트의 DEFF 간의 비교는 매트릭스와 솔루트의 상대적 결합 강도를 결정합니다. 주어진 솔루트의 경우, DEFF와 DSS가 동일한 크기의 순서 내에 있는 경우 확산 시 약물과 매트릭스 사이에 최소한의 결합이 존재한다는 것을 의미한다. 그러나 DEFF가 DSS보다큰 경우 행렬에 대한 입자의 실질적인 결합이 존재합니다.
설계된 실험은 연골을 통한 용성 수송의 특성화를 개별적으로 허용하지만, 최적으로 충전된 약물 운반체를 설계하기 위해서는 모든 결과를 포함하는 전체적인 분석이 필요하다. 전하 상호 작용의 약하고 가역적 특성은 입자 확산 속도를 제어하고 연골을 통해 높은 평형 섭취와 빠른 전체 깊이 침투를 허용합니다. 평형 섭정 섭취 실험을 통해 비평형 확산 률 연구를 사용하여 확인할 수 있는 전하 상호 작용의 결과로 높은 섭취량을 보이는 운반체를 찾아야 합니다. 그러나 이러한 결합 상호 작용은 연골을 통해 솔ute의 전체 두께 침투를 허용하기 위해 자연에서 약하고 뒤집을 수 있어야합니다. 이상적인 약물 운반대는 섭취와 높은 연골 약물 농도에 충분한 결합을 가능하게 하는 최적의 전하를 가지고 있지만, 전체 두께 확산을 방해하기에는 너무 강하지않다 4. 제시된 실험은 약물 운반체를 표적으로 하는 충전 기지를 둔 조직을 위한 디자인 특성에 도움이 될 것입니다. 이러한 프로토콜은 연골4를통한 CPC 수송을 특성화하는 데 사용되었지만, 이들은 연골 및 기타 음전하 조직을 통해 다양한 약물 및 약물 운반기에적용될 수 있다.
Protocol
Representative Results
Discussion
여기에 설명된 방법 및 프로토콜은 부정적으로 충전된 조직에 표적 약물 전달 분야에 중요합니다. 이 조직에 존재하는 부정적인 충전 된 aggrecans의 높은 밀도로 인해 장벽이 생성되므로 약물이 매트릭스 내에서 깊숙이 놓여있는 세포 표적 부위에 도달하지 못하게합니다. 이러한 뛰어난 과제를 해결하기 위해, 약물은 조직 1,3,,4,,14,<…
Disclosures
The authors have nothing to disclose.
Acknowledgements
이 작품은 W81XWH-17-1-0085 계약에 따라 의회 지시 의학 연구 프로그램 (CDMRP)과 국립 보건 R03 EB025903-1을 통해 미국 국방부에 의해 지원되었다. AV는 노스이스턴 대학의 공학 학장 펠로우십 대학의 지원을 받았습니다.
Materials
| 316 Stainless Steel SAE Washer | McMaster-Carr | 91950A044 | For number 5 screw size, 0.14" ID, 0.312" OD |
| 96-Well Polystyrene Plate | Fisherbrand | 12566620 | Black |
| Acrylic Thick Gauge Sheet | Reynolds Polymer | N/A | For non-equilibrium diffusion and 1-D diffusion transport chamber |
| Antibiotic-Antimycotic | Gibco | 15240062 | 100x |
| Bovine Cartilage | Research 87 | N/A | 2-3 weeks old, femoropatellar groove |
| Bovine Serum Albumin | Fisher BioReagents | BP671-1 | |
| CPC+14 | LifeTein | LT1524 | Custom designed peptide |
| CPC+20 | LifeTein | LT1525 | Custom designed peptide |
| CPC+8 | LifeTein | LT1523 | Custom designed peptide |
| Delicate Task Wipers | Kimberly-Clark Professional | 34155 | |
| Dermal Punch | MedBlades | MB5-1 | 3, 4 and 6 mm |
| Economy Plain Glass Microscope Slides | Fisherbrand | 12550A3 | |
| Flat Bottom Cell Culture Plates | Corning Costar | 3595 | Clear, 96 well |
| Flexible Wrapping Film | Bemis Parafilm M Laboratory | 1337412 | |
| Gold Seal Cover Glass | Electron Microscopy Sciences | 6378701 | # 1.5, 18×18 mm |
| Hammer-Driven Hole Punch | McMaster-Carr | 3427A15 | 1/2" Diameter |
| Hammer-Driven Hole Punch | McMaster-Carr | 3427A19 | 3/4" Diameter |
| Laser | Chroma Technology | AT480/30m | Spectrophotometer Laser Light |
| Low-Strength Steel Hex Nut | McMaster-Carr | 90480A007 | 6-32 Thread size |
| LSM 700 Confocal Microscope | Zeiss | LSM 700 | |
| Micro Magnetic Stirring Bars | Bel-Art Spinbar | F37119-0007 | 7×2 mm |
| Multipurpose Neoprene Rubber Sheet | McMaster-Carr | 1370N12 | 1/32" Thickness |
| Non-Fat Dried Bovine Milk | Sigma Aldrich | M7409 | |
| Petri Dish | Chemglass Life Sciences | CGN1802145 | 150 mm diameter |
| Phosphate-Buffered Saline | Corning | 21-040-CMR | 1x |
| Plate Shaker | VWR | 89032-088 | |
| Protease Inhibitors | Thermo Scientific | A32953 | |
| Razor Blades | Fisherbrand | 12640 | |
| R-Cast Acrylic Thin Gauge Sheet | Reynolds Polymer | N/A | Black transport chamber inserts |
| RTV Silicone | Loctite | 234323 | Epoxy, Non-corrosive, clear |
| Scalpel | TedPella | 549-3 | #10, #11 blades |
| Signal Receiver | Chroma Technology | ET515lp | Spectrophotometer Laser Signal Receiver |
| Snap-Cap Microcentrifuge Tubes | Eppendorf | 22363204 | 1.5 mL |
| Spatula | TedPella | 13508 | |
| Synergy H1 Microplate Reader | Biotek | H1M | |
| Zinc-Plated Alloy Steel Socket Head Screw | McMaster-Carr | 90128A153 | 6-32 Thread size, 1" Long |
References
- Bajpayee, A. G., Grodzinsky, A. J. Cartilage-targeting drug delivery: can electrostatic interactions help. Nature Reviews Rheumatology. 13 (3), 183-193 (2017).
- Maroudas, A. Transport of solutes through cartilage: permeability to large molecules. Journal of Anatomy. 122, 335-347 (1976).
- Bajpayee, A. G., Wong, C. R., Bawendi, M. G., Frank, E. H., Grodzinsky, A. J. Avidin as a model for charge driven transport into cartilage and drug delivery for treating early stage post-traumatic osteoarthritis. Biomaterials. 35 (1), 538-549 (2014).
- Vedadghavami, A., et al. Cartilage penetrating cationic peptide carriers for applications in drug delivery to avascular negatively charged tissues. Acta Biomaterialia. 93, 258-269 (2019).
- Mehta, S., Akhtar, S., Porter, R. M., Önnerfjord, P., Bajpayee, A. G. Interleukin-1 receptor antagonist (IL-1Ra) is more effective in suppressing cytokine-induced catabolism in cartilage-synovium co-culture than in cartilage monoculture. Arthritis Research & Therapy. 21 (1), 238 (2019).
- Vedadghavami, A., Zhang, C., Bajpayee, A. G. Overcoming negatively charged tissue barriers: Drug delivery using cationic peptides and proteins. Nano Today. 34, 100898 (2020).
- Young, C. C., Vedadghavami, A., Bajpayee, A. G. Bioelectricity for Drug Delivery: The Promise of Cationic Therapeutics. Bioelectricity. , (2020).
- Felson, D. T. Osteoarthritis of the knee. New England Journal of Medicine. 354 (8), 841-848 (2006).
- Wieland, H. A., Michaelis, M., Kirschbaum, B. J., Rudolphi, K. A. Osteoarthritis – An untreatable disease. Nature Reviews Drug Discovery. 4 (4), 331-344 (2005).
- Martel-Pelletier, J. Pathophysiology of osteoarthritis. Osteoarthritis and Cartilage. 7 (4), 371-373 (1999).
- Sophia Fox, A. J., Bedi, A., Rodeo, S. A. The basic science of articular cartilage: Structure, composition, and function. Sports Health. 1 (6), 461-468 (2009).
- Chevalier, X., et al. Intraarticular injection of anakinra in osteoarthritis of the knee: A multicenter, randomized, double-blind, placebo-controlled study. Arthritis Care and Research. 61 (3), 344-352 (2009).
- Cohen, S. B., et al. A randomized, double-blind study of AMG 108 (a fully human monoclonal antibody to IL-1R1) in patients with osteoarthritis of the knee. Arthritis Research and Therapy. 13 (4), 125 (2011).
- Evans, C. H., Kraus, V. B., Setton, L. A. Progress in intra-articular therapy. Nature Reviews Rheumatology. 10 (1), 11-22 (2014).
- He, T., et al. Multi-arm Avidin nano-construct for intra-cartilage delivery of small molecule drugs. Journal of Controlled Release. 318, 109-123 (2020).
- Bajpayee, A. G., Scheu, M., Grodzinsky, A. J., Porter, R. M. A rabbit model demonstrates the influence of cartilage thickness on intra-articular drug delivery and retention within cartilage. Journal of Orthopaedic Research. 33 (5), 660-667 (2015).
- Bajpayee, A. G., Quadir, M. A., Hammond, P. T., Grodzinsky, A. J. Charge based intra-cartilage delivery of single dose dexamethasone using Avidin nano-carriers suppresses cytokine-induced catabolism long term. Osteoarthritis and Cartilage. 24 (1), 71-81 (2016).
- Zhang, C., et al. Avidin-biotin technology to synthesize multi-arm nano-construct for drug delivery. MethodsX. , 100882 (2020).
- Wagner, E. K., et al. Avidin grafted dextran nanostructure enables a month-long intra-discal retention. Scientific Reports. 10.1, 1-14 (2020).
- Troeberg, L., Nagase, H. Proteases involved in cartilage matrix degradation in osteoarthritis. Biochimica et Biophysica Acta – Proteins and Proteomics. 1824 (1), 133-145 (2012).
- Kirk, T. B., Wilson, A. S., Stachowiak, G. The effects of dehydration on the surface morphology of articular cartilage. Journal of Orthopaedic Rheumatology. 6 (2-3), 75-80 (1993).
- Ateshian, G. A., Maas, S., Weiss, J. A. Solute transport across a contact interface in deformable porous media. Journal of Biomechanics. 45 (6), 1023-1027 (2012).
- Arbabi, V., Pouran, B., Weinans, H., Zadpoor, A. A. Multiphasic modeling of charged solute transport across articular cartilage: Application of multi-zone finite-bath model. Journal of Biomechanics. 49 (9), 1510-1517 (2016).
- Arbabi, V., Pouran, B., Zadpoor, A. A., Weinans, H. An experimental and finite element protocol to investigate the transport of neutral and charged solutes across articular cartilage. Journal of Visualized Experiments. 2017 (122), (2017).
- Sampson, S. L., Sylvia, M., Fields, A. J. Effects of dynamic loading on solute transport through the human cartilage endplate. Journal of Biomechanics. 83, 273-279 (2019).
- Bajpayee, A. G., Scheu, M., Grodzinsky, A. J., Porter, R. M. Electrostatic interactions enable rapid penetration, enhanced uptake and retention of intra-articular injected avidin in rat knee joints. Journal of Orthopaedic Research : Official Publication of the Orthopaedic Research Society. 32 (8), 1044-1051 (2014).
- Bajpayee, A. G., et al. Sustained intra-cartilage delivery of low dose dexamethasone using a cationic carrier for treatment of post traumatic osteoarthritis. European Cells & Materials. 34, 341-364 (2017).
- Malda, J., et al. Of Mice, Men and Elephants: The Relation between Articular Cartilage Thickness and Body Mass. PLoS One. 8 (2), 57683 (2013).
- Frisbie, D. D., Cross, M. W., McIlwraith, C. W. A comparative study of articular cartilage thickness in the stifle of animal species used in human pre-clinical studies compared to articular cartilage thickness in the human knee. Veterinary and Comparative Orthopaedics and Traumatology. 19 (3), 142-146 (2006).

