Caractérisation des systèmes complexes à l'aide de la conception des expériences approche: l'expression transitoire de protéines dans le tabac comme une étude de cas
Summary
Nous décrivons une conception de l'approche des expériences qui peuvent être utilisés pour déterminer et modéliser l'influence des éléments de régulation du transgène, les paramètres de croissance et de développement des plantes, et des conditions d'incubation sur l'expression transitoire des anticorps monoclonaux et des protéines rapporteurs dans les plantes.
Abstract
Les plantes apportent de multiples avantages pour la production de produits biopharmaceutiques, y compris de faibles coûts, l'évolutivité et la sécurité. L'expression transitoire offre l'avantage supplémentaire de développement à court et temps de production, mais les niveaux d'expression peut varier considérablement entre les lots donnant ainsi naissance à des préoccupations d'ordre réglementaire dans le cadre de bonnes pratiques de fabrication. Nous avons utilisé un plan d'expériences (DoE) approche pour déterminer l'impact des principaux facteurs tels que des éléments de régulation dans la construction d'expression, la croissance des plantes et les paramètres de développement, et les conditions d'incubation pendant expression, sur la variabilité d'expression entre les lots. Nous avons testé des plantes exprimant un anticorps anti-VIH modèle monoclonal (2G12) et une protéine marqueur fluorescent (DsRed). Nous discutons de la justification du choix des propriétés du modèle et identifier ses limites éventuelles. L'approche générale peut facilement être transférée à d'autres problèmes parce que les principes du modèle dere largement applicable: le choix des paramètres de la connaissance, la réduction de la complexité en divisant le problème initial en petits modules, configuration logicielle guidée de combinaisons optimales d'expérimentation et par étapes de conception augmentation. Par conséquent, la méthode n'est pas seulement utile pour caractériser l'expression des protéines dans les plantes mais aussi pour l'étude d'autres systèmes complexes qui n'ont pas une description mécaniste. Les équations de prédiction décrivant l'interconnectivité entre les paramètres peuvent être utilisés pour établir des modèles mécanistes pour d'autres systèmes complexes.
Introduction
La production de protéines biopharmaceutiques dans les plantes est avantageux parce que les plantes sont peu coûteux à développer, la plate-forme peut être étendu simplement en cultivant plus de plantes, et les agents pathogènes humains sont incapables de se répliquer 1,2. Stratégies d'expression transitoire sur la base par exemple sur l'infiltration des feuilles avec Agrobacterium tumefaciens offre des avantages supplémentaires parce que le temps entre le point de livraison de l'ADN et la livraison d'un produit purifié est réduite de quelques années à moins de 2 mois 3. L'expression transitoire est également utilisée pour l'analyse fonctionnelle, par exemple pour tester des gènes pour leur capacité à compléter les mutants perte de fonction ou pour étudier les interactions entre protéines 6.4. Cependant, les niveaux d'expression transitoire ont tendance à montrer une plus grande variation de lot à lot que les niveaux d'expression dans des plantes transgéniques 9.7. Ceci réduit la probabilité que les processus de fabrication de produits biopharmaceutiques basés sur l'expression transitoire will être approuvé dans le cadre des bonnes pratiques de fabrication (BPF), parce que la reproductibilité est un attribut de qualité critique et est soumis à une évaluation des risques 10. Cette variation peut également masquer toutes les interactions que les chercheurs ont l'intention d'enquêter. Par conséquent, nous avons décidé d'identifier les principaux facteurs qui influent sur les niveaux d'expression transitoire dans les usines et de construire un modèle prédictif quantitatif de haute qualité.
Le (OFAT) approche à un facteur-à-un-temps est souvent utilisé pour caractériser l'impact (effet) de certains paramètres (facteurs) sur le résultat (réponse) d'une expérience 11. Mais ce n'est pas optimal parce que les tests individuels (courses) pendant une enquête (expérience) seront alignés comme des perles sur une ficelle à travers la zone potentiel engendré par les facteurs qui sont testés (espace de conception). La couverture de l'espace de conception et, partant, le degré de l'information dérivée de l'expérience estfaible, comme le montre la Figure 1A 12. En outre, les interdépendances entre les différents facteurs (interactions de facteurs) peuvent rester cachées dans les modèles résultant pauvres et / ou la prédiction de la fausse optima, comme le montre la Figure 1B 13.
Les inconvénients décrits ci-dessus peuvent être évités en utilisant une conception d'expériences (DoE) approche dans laquelle les pistes d'une expérience sont dispersées plus uniformément dans l'espace de conception, ce qui signifie que plus d'un facteur varie entre deux pistes 14. Il ya des dessins spécialisées pour les mélanges, les facteurs (dessins factoriels) et la quantification des impacts de facteurs sur les réponses (méthodes de surface de réponse, RSM s) 15 de dépistage. En outre, SMR peuvent être réalisées que des dessins centraux-composite mais peuvent également être atteints de manière efficace en utilisant un logiciel spécialisé qui peut appliquer des critères différents pour la sélection des pistes. Par exemple, ce qu'on appelle le D-OptimalITcritère d'y sélectionnera pistes afin de minimiser l'erreur dans les coefficients du modèle qui en résulte, tandis que le critère d'optimalité sélectionne IV-séries qui permettent d'atteindre le plus faible variance de prédiction dans tout l'espace de conception 15,16. Le RSM nous décrivons ici permet la quantification précise de l'expression de la protéine transitoire chez les plantes, mais il peut facilement être transférée à tout système impliquant plusieurs (~ 5-8) facteurs numériques (tels que la température, le temps, la concentration) et quelques-uns (~ 2 – 4) facteurs catégoriques (par exemple promoteur, couleur) dans lequel une description mécaniste n'est pas disponible ou trop complexes à modéliser.
L'approche DoE origine dans les sciences agricoles, mais s'est étendu à d'autres domaines, car il est transférable à toute situation où il est utile de réduire le nombre de cycles nécessaires pour obtenir des données fiables et générer des modèles descriptifs des processus complexes. Cela a conduit à l'inclusion de DoE dans les "Directives pourIndustrie, Q8 (R2) Développement pharmaceutique », publié par la Conférence internationale sur l'harmonisation des exigences techniques pour l'enregistrement des produits pharmaceutiques à usage humain (ICH) 17. DoE est maintenant largement utilisé dans la recherche scientifique et de l'industrie 18. Cependant, il faut prendre soin lors de la planification et l'exécution de l'expérience, car le choix d'un polynôme de degré mauvaise pour le modèle linéaire multiple régression (modèle de base) peuvent introduire une nécessité pour des courses supplémentaires pour modéliser correctement les effets des facteurs. Par ailleurs, corrompus ou des données manquantes génèrent des modèles erronés et défectueux prédictions, et peuvent même empêcher tout modèle tentative de construction comme décrit dans les sections de protocole et de discussion 18. Dans la section de protocole, nous allons d'abord définir les étapes de planification les plus importants pour une expérience à base de RSM et ensuite expliquer la conception basée sur le DoE logiciel DesignExpert v8.1. Mais les conceptions semblables peuvent être construites avec d'autres includi logicielng JMP, Modde, et STATISTICA. Les procédures expérimentales sont suivies par des instructions pour l'analyse et l'évaluation des données.
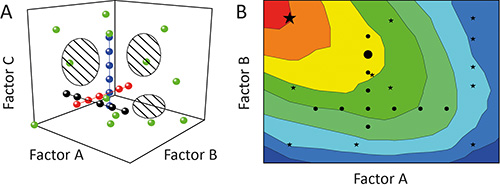
Figure 1. Comparaison des OFAT et DoE. A. Variation séquentielle d'un facteur à la fois (OFAT) dans une expérience (cercles noirs, rouges et bleues) réalise une faible couverture de l'espace de conception (des zones hachurées). En revanche, la variation de plus d'un facteur à la fois en utilisant la conception des expériences de stratégie (DoE) (cercles verts) améliore la couverture et donc la précision des modèles issus. B. La couverture de l'espace de conception biaisée signifie que les expériences OFAT (cercles noirs) peuvent aussi échouer à identifier les régions d'exploitation optimales (en rouge) et de prévoir des solutions sous-optimales (grand cercle noir), alors que DoE stratégiquementes (étoiles noires) sont plus susceptibles d'identifier les conditions préférables (grande étoile noire).
Protocol
Representative Results
Discussion
Chaque expérience nécessite une planification minutieuse, car les ressources sont souvent rares et chers. Cela est particulièrement vrai pour les stratégies DoE car les erreurs au cours de la phase de planification (par exemple, la sélection d'un modèle de base qui ne couvre pas toutes les interactions de facteurs importants) peuvent sensiblement diminuer le pouvoir prédictif des modèles issus et donc dévaluer toute l'expérience. Cependant, ces erreurs peuvent être facilement évitées en sui…
Divulgations
The authors have nothing to disclose.
Acknowledgements
Les auteurs tiennent à remercier le Dr Thomas Rademacher pour fournir le vecteur d'expression PPAM végétale et Ibrahim Al Amedi pour cultiver les plants de tabac utilisées dans cette étude. Nous tenons à remercier le Dr Richard M. Twyman pour son aide dans l'édition du manuscrit. Ce travail a été en partie financé par le Conseil européen de la recherche avancée Grant "Future-Pharma", la proposition n ° 269110 et le Fraunhofer Zukunftsstiftung (Fondation Fraunhofer avenir).
Materials
| Design-Expert(R) 8 | Stat-Ease, Inc. | n.a. | DoE software |
| Tryptone | Carl Roth GmbH | 8952.2 | Media component |
| Yeast extract | Carl Roth GmbH | 2363.2 | Media component |
| Sodium chloride | Carl Roth GmbH | P029.2 | Media component |
| Ampicillin | Carl Roth GmbH | K029.2 | Antibiotic |
| Agar-Agar | Carl Roth GmbH | 5210.2 | Media component |
| Escherichia coli K12 DH5a | Life technologies | 18263-012 | Microorganism |
| pPAM | GenBank | AY027531 | Cloning/expression vector; |
| NucleoSpin Plasmid | MACHEREY-NAGEL GmbH | 740588.250 | Plasmid DNA isolation kit |
| NucleoSpin Gel and PCR Clean-up | MACHEREY-NAGEL GmbH | 740609.250 | Plasmid DNA purification kit |
| NanoDrop 2000 | Thermo Scientific | n.a. | Spectrophotometer |
| NcoI | New England Biolabs Inc. | R3193L | Restrictionendonuclease |
| EcoRI | New England Biolabs Inc. | R3101L | Restrictionendonuclease |
| AscI | New England Biolabs Inc. | R0558L | Restrictionendonuclease |
| NEB 4 | New England Biolabs Inc. | B7004S | Restrictionendonuclease buffer |
| TRIS | Carl Roth GmbH | 4855.3 | Media component |
| Disodium tetraborate | Carl Roth GmbH | 4403.3 | Media component |
| EDTA | Carl Roth GmbH | 8040.2 | Media component |
| Agarose | Carl Roth GmbH | 6352.4 | Media component |
| Bromophenol blue | Carl Roth GmbH | A512.1 | Color indicator |
| Xylene cyanol | Carl Roth GmbH | A513.1 | Color indicator |
| Glycerol | Carl Roth GmbH | 7530.2 | Media component |
| Mini-Sub Cell GT Cell | BioRad | 170-4406 | Gel electrophoresis chamber |
| Agrobacterium tumefaciens strain GV3101:pMP90RK | DSMZ | 12365 | Microorganism |
| Electroporator 2510 | Eppendorf | 4307000.658 | Electroporator |
| Beef extract | Carl Roth GmbH | X975.2 | Media component |
| Peptone | Carl Roth GmbH | 2365.2 | Media component |
| Sucrose | Carl Roth GmbH | 4621.2 | Media component |
| Magnesium sulfate | Carl Roth GmbH | 0261.3 | Media component |
| Carbenicillin | Carl Roth GmbH | 6344.2 | Antibiotic |
| Kanamycin | Carl Roth GmbH | T832.3 | Antibiotic |
| Rifampicin | Carl Roth GmbH | 4163.2 | Antibiotic |
| FWD primer | Eurofins MWG Operon | n.a. | CCT CAG GAA GAG CAA TAC |
| REV primer | Eurofins MWG Operon | n.a. | CCA AAG CGA GTA CAC AAC |
| 2720 Thermal cycler | Applied Biosystems | 4359659 | Thermocycler |
| RNAfold webserver | University of Vienna | n.a. | Software |
| Ferty 2 Mega | Kammlott | 5.220072 | Fertilizer |
| Grodan Rockwool Cubes 10x10cm | Grodan | n.a. | Rockwool block |
| Greenhouse | n.a. | n.a. | For plant cultivation |
| Phytotron | Ilka Zell | n.a. | For plant cultivation |
| Omnifix-F Solo | B. Braun | 6064204 | Syringe |
| Murashige and Skoog salts | Duchefa | M 0222.0010 | Media component |
| Glucose | Carl Roth GmbH | 6780.2 | Media component |
| Acetosyringone | Sigma-Aldrich | D134406-5G | Phytohormon analogon |
| BioPhotometer plus | Eppendorf | 6132 000.008 | Photometer |
| Osram cool white 36 W | Osram | 4930440 | Light source |
| Disodium phosphate | Carl Roth GmbH | 4984.3 | Media component |
| Centrifuge 5415D | Eppendorf | 5424 000.410 | Centrifuge |
| Forma -86C ULT freezer | ThermoFisher | 88400 | Freezer |
| Synergy HT | BioTek | SIAFRT | Fluorescence plate reader |
| Biacore T200 | GE Healthcare | n.a. | SPR device |
| Protein A | Life technologies | 10-1006 | Antibody binding protein |
| HEPES | Carl Roth GmbH | 9105.3 | Media component |
| Tween-20 | Carl Roth GmbH | 9127.3 | Media component |
| 2G12 antibody | Polymun | AB002 | Reference antibody |
References
- Fischer, R., Emans, N. Molecular farming of pharmaceutical proteins. Transgenic research. 9, 277-299 (2000).
- Commandeur, U., Twyman, R. M., Fischer, R. The biosafety of molecular farming in plants. AgBiotechNet. 5, 9 (2003).
- Shoji, Y., et al. A plant-based system for rapid production of influenza vaccine antigens. Influenza Other Resp. 6, 204-210 (2012).
- Goodin, M. M., Zaitlin, D., Naidu, R. A., Lommel, S. A. Nicotiana benthamiana: Its history and future as a model for plant-pathogen interactions. Mol Plant Microbe In. 21, 1015-1026 (2008).
- Berg, R. H., Beachy, R. N. Fluorescent protein applications in plants. Method Cell Biol. 85, 153 (2008).
- Chung, S. M., Vaidya, M., Tzfira, T. Agrobacterium is not alone: gene transfer to plants by viruses and other bacteria. Trends in plant science. 11, 1-4 (2006).
- Sheludko, Y. V., Sindarovska, Y. R., Gerasymenko, I. M., Bannikova, M. A., Kuchuk, N. V. Comparison of several Nicotiana species as hosts for high-scale Agrobacterium-mediated transient expression. Biotechnology and Bioengineering. 96, 608-614 (2007).
- Wydro, M., Kozubek, E., Lehmann, P. Optimization of transient Agrobacterium-mediated gene expression system in leaves of Nicotiana benthamiana. Acta Biochimica Polonica. 53, 289-298 (2006).
- Buyel, J. F., Fischer, R. Processing heterogeneous biomass: Overcoming the hurdles in model building. Bioengineered. 4, (2013).
- Fischer, R., Schillberg, S., Hellwig, S., Twyman, R. M., Drossard, J. GMP issues for recombinant plant-derived pharmaceutical proteins. Biotechnol Adv. 30, 434-439 (2012).
- Daniel, C. One-at-a-time plans. Journal of the American Statistical Association. 68, 353-360 (1973).
- Czitrom, V. One-Factor-at-a-Time versus Designed Experiments The American Statistician. 53, 6 (1999).
- Anderson, M. J., Kraber, S. L. Keys to successful designed experiments. ASQ – The global voice of quality. 6, 6 (1999).
- Montgomery, D. C. . Design and Analysis of Experiments. , (2007).
- Myers, R. H., Montgomery, D. C., Anderson-Cook, C. M. . Response Surface Methodology: Process and Product Optimization Using Designed Experiments. , (2009).
- Piepel, G. F. Programs for generating extreme vertices and centroids of linearly constrained experimental regions. J Qual Technol. 20, 15 (1988).
- . . FDA. , (2009).
- Shivhare, M., McCreath, G. Practical Considerations for DoE Implementation in Quality By Design. BioProcess International. 8, 9 (2010).
- Buyel, J. F., Fischer, R. Predictive models for transient protein expression in tobacco (Nicotiana tabacum L.) can optimize process time, yield, and downstream costs. Biotechnology and bioengineering. 109, 2575-2588 (2012).
- Buyel, J. F., Kaever, T., Buyel, J. J., Fischer, R. Predictive models for the accumulation of a fluorescent marker protein in tobacco leaves according to the promoter/5’UTR combination. Biotechnology and bioengineering. 110, 471-482 (2013).
- Anderson, M. J., Whitcomb, P. J. . DOE Simplified: Practical Tools for Effective Experimentation. , (2000).
- Anderson, M. J., Whitcomb, P. J. . Response Surface Methods Simplified. , (2005).
- De Gryze, S., Langhans, I., Vandebroek, M. Using the correct intervals for prediction: A tutorial on tolerance intervals for ordinary least-squares regression. Chemometr Intell Lab. 87, 147-154 (2007).
- . . Plasmid DNA purification User manual. , (2012).
- . . PCR clean-up Gel extraction User manual. , (2012).
- . . Quick Ligation Protocol. 4, (2009).
- Inoue, H., Nojima, H., Okayama, H. High-Efficiency Transformation of Escherichia-Coli with Plasmids. Gene. 96, 23-28 (1990).
- Main, G. D., Reynolds, S., Gartland, J. S. Electroporation protocols for Agrobacterium. Methods in Molecular Biology. 44, 405-412 (1995).
- Gruber, A. R., Lorenz, R., Bernhart, S. H., Neubock, R., Hofacker, I. L. The Vienna RNA websuite. Nucleic acids research. 36, 70-74 (2008).
- Howell, S., Kenmore, M., Kirkland, M., Badley, R. A. High-density immobilization of an antibody fragment to a carboxymethylated dextran-linked biosensor surface. J Mol Recognit. 11, 200-203 (1998).
- Newcombe, A. R., et al. Evaluation of a biosensor assay to quantify polyclonal IgG in ovine serum used for the production of biotherapeutic antibody fragments. Process Biochem. 41, 842-847 (2006).
- Peixoto, J. L. Hierarchical Variable Selection in Polynomial Regression-Models. Am Stat. 41, 311-313 (1987).
- Peixoto, J. L. A Property of Well-Formulated Polynomial Regression-Models. Am Stat. 44, 26-30 (1990).
- Sanders, P. R., Winter, J. A., Barnason, A. R., Rogers, S. G., Fraley, R. T. Comparison of cauliflower mosaic virus 35S and nopaline synthase promoters in transgenic plants. Nucleic acids research. 15, 1543-1558 (1987).
- Ma, J. K. C., et al. Generation and Assembly of Secretory Antibodies in Plants. Science. 268, 716-719 (1995).
- Wycoff, K. L. Secretory IgA antibodies from plants. Curr Pharm Design. 11, 2429-2437 (2005).
- Pace, C. N., Vajdos, F., Fee, L., Grimsley, G., Gray, T. How to measure and predict the molar absorption coefficient of a protein. Protein Sci. 4, 2411-2423 (1995).

