Инструменты для оценки в режиме реального времени модели инфекции Pseudomonas aeruginosa
Summary
Синтетическая среда мокроты при муковисцидозе (SCFM2) может быть использована в сочетании как с конфокальной лазерной сканирующей микроскопией, так и с флуоресцентно-активированной сортировкой клеток для наблюдения бактериальных агрегатов с высоким разрешением. В этой статье подробно описываются методы оценки совокупных популяций во время антимикробного лечения в качестве платформы для будущих исследований.
Abstract
Pseudomonas aeruginosa (Pa) является одним из наиболее распространенных условно-патогенных микроорганизмов, связанных с муковисцидозом (МВ). Как только колонизация Па установлена, большая часть инфекционных бактерий образует биопленки в мокроте дыхательных путей. Было показано, что биопленки Па, выделенные из мокроты муковисцидного средства, растут в небольших, плотных агрегатах ~ 10-1000 клеток, которые пространственно организованы и демонстрируют клинически значимые фенотипы, такие как устойчивость к противомикробным препаратам. Одной из самых больших проблем при изучении того, как агрегаты Pa реагируют на изменение среды мокроты, является отсутствие питательных и надежных систем, которые способствуют образованию агрегатов. Используя синтетическую среду мокроты CF (SCFM2), историю жизни агрегатов Pa можно наблюдать с помощью конфокальной лазерной сканирующей микроскопии (CLSM) и анализа изображений с разрешением одной клетки. Эта система in vitro позволяет наблюдать тысячи агрегатов различного размера в режиме реального времени, трех измерениях и в микроном масштабе. На индивидуальном и популяционном уровнях способность группировать агрегаты по фенотипу и положению облегчает наблюдение агрегированных агрегатов на разных стадиях развития и их реакцию на изменения в микросреде, такие как лечение антибиотиками, которые должны быть дифференцированы с точностью.
Introduction
Pseudomonas aeruginosa (Pa) является оппортунистическим патогеном, который устанавливает хронические инфекции у людей с ослабленным иммунитетом. Для людей с генетическим заболеванием муковисцидоз (МВ) эти инфекции могут охватывать всю жизнь. Муковисцидоз вызывает накопление вязкой, богатой питательными веществами мокроты в дыхательных путях, которая со временем колонизируется различными микробными патогенами. Па является одним из наиболее распространенных патогенов муковисцидоза, колонизируя дыхательные пути в раннем детстве и устанавливая трудноизуемые инфекции1. Па остается значительной клинической проблемой и считается ведущей причиной смертности у лиц с муковисцидозом, несмотря на улучшение схем терапии в последниегоды2,3. Этот фенотип персистенции и повышение толерантности к антибиотикам принесли Па место в группе патогенов, идентифицированных как Центрами по контролю и профилактике заболеваний (CDC), так и Всемирной организацией здравоохранения (ВОЗ) в качестве исследовательских приоритетов для разработки новых терапевтических стратегий – патогенов ESKAPE4.
Как и другие патогены ESKAPE, приобретенная устойчивость к антибиотикам распространена в Pa,но есть также много внутренних свойств, которые способствуют антимикробной толерантности Pa. Среди них способность Па образовывать агрегаты — высокоплотные кластеры из ~10-1000 клеток, которые могут наблюдаться при множественных инфекциях, в том числе при МВ мокроте больного5,6. Подобно Pa, изученным в других системах биопленки, агрегаты Pa демонстрируют клинически значимые фенотипы, такие как повышенная устойчивость к антибиотикам и активация клеточно-клеточной коммуникации (кворум-зондирование (QS)). Например, было показано, что агрегаты Па используют QS-регулируемое поведение для борьбы с другими микробами, а также переносят антимикробные методы лечения, такие как производство пиоцианина7. Способность изучать такое поведение дает захватывающее представление о бактериальных экосистемах в среде, подобной той, в которой они существуют в организме человека.
Одной из самых больших проблем при изучении того, как агрегаты Pa реагируют на изменение среды мокроты, является отсутствие питательных и надежных систем, которые способствуют образованию агрегатов. Многое из того, что известно о Па, было обнаружено с использованием систем in vitro, в которых клетки растут планктонально или в характерной поверхностно-прикрепленной, «грибной» архитектуре, которая не наблюдалась in vivo8. В то время как классические модели роста биопленки, такие как прототочные клетки или твердый агар, дали обширные и ценные знания о поведении бактерий и механизмах толерантности к антибиотикам, эти результаты не всегда переводятся in vivo. Многие модели in vitro имеют ограниченную способность имитировать среду роста места инфекции человека, что требует дорогостоящих исследований in vivo. В свою очередь, многим моделям in vivo не хватает гибкости и разрешения, предоставляемых методами in vitro.
Синтетический муковисцидоз мокроты (SCFM2) предназначен для обеспечения среды для роста Па, аналогичной той, которая наблюдается во время хронической инфекции в легких муковисцидоза. SCFM2 включает источники питания, идентифицированные в отхаркиваемой смуте CF в дополнение к муцину, липидам и ДНК. Рост Pa в SCFM2 требует почти идентичного набора генов, необходимых для роста фактической мокроты, и поддерживает естественное образование агрегата Pa 9,10. После инокуляции планктонные клетки образуют агрегаты, которые увеличиваются в размерах за счет расширения. Отдельные клетки (называемые мигрантами) высвобождаются из агрегатов, мигрируют в неколонизированные районы и образуют новые агрегаты10. Эту историю жизни можно наблюдать с помощью CLSM и анализа изображений с разрешением одной клетки. Агрегаты Па, образующиеся в SCFM2, имеют размеры, аналогичные тем, которые наблюдаются в легкомCF 10. Эта модель позволяет наблюдать несколько агрегатов различного размера в режиме реального времени и в трех измерениях в микроновом масштабе. Покадровая микроскопия позволяет отслеживать тысячи (~50 000) агрегатов в одном эксперименте. Использование программного обеспечения для анализа изображений позволяет количественно оценить совокупные фенотипы по микроснимкам, включая совокупный объем, площадь поверхности и положение в трех измерениях до ближайших 0,1 мкм, как на индивидуальном агрегированном, так и на популяционном уровнях. Наличие способности группировать агрегаты по фенотипу и положению позволяет с точностью дифференцировать агрегаты на разных стадиях развития, а также их реакцию на изменениемикросреды 6,11.
Применение SCFM2 для изучения агрегатов Pa в анализах с низким объемом и высокой пропускной способностью делает его гибкой и экономически эффективной моделью. В качестве определенной среды SCFM2 обеспечивает однородность и воспроизводимость на нескольких платформах, обеспечивая питательную и физически релевантную методику изучения агрегатов Pa in vitro9. Приложения включают его использование в сочетании с CLSM для наблюдения пространственной организации и толерантности к антибиотикам при высоком разрешении (как описано в этой статье о методах). Возможность проводить эксперименты, которые предоставляют данные в микроновом масштабе в режиме реального времени, позволяет изучать внутривидовые и межвидовые взаимодействия, поскольку они могут происходить in vivo. Например, SCFM2 ранее использовался для изучения пространственной динамики клеточно-клеточной коммуникации в совокупных популяциях через сеть систем, используемых Pa для регулирования нескольких генов, которые способствуют вирулентности и патогенезу6.
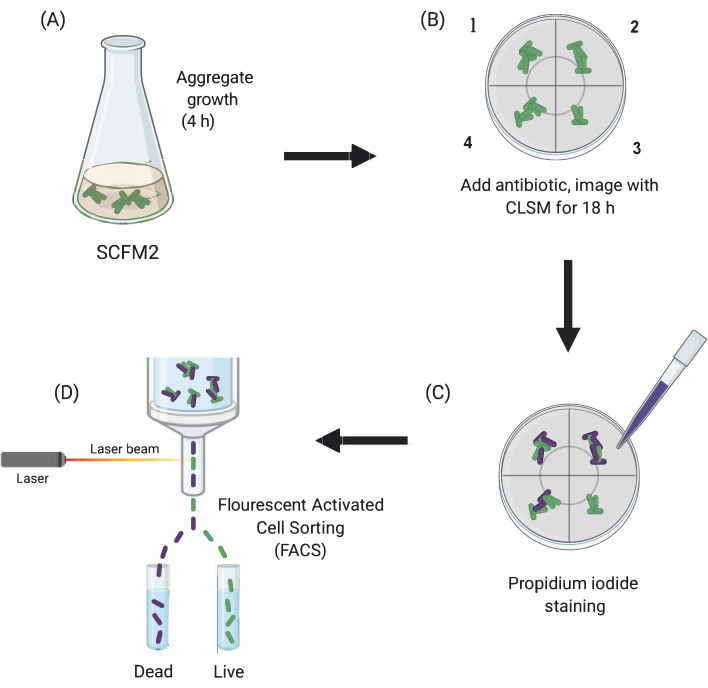
Рисунок 1:Графическое изображение основных экспериментальных этапов. (A)SCFM2 инокулируют Па-клетками и позволяют формировать агрегаты в чашке со стеклянным дном. (B) Агрегаты переносятся в конфокальный микроскоп и добавляют антибиотик. Изображены три технические реплики (камеры 1-3) и контрольная скважина (4) инокулированного SCFM2 без лечения антибиотиками. Агрегаты визуализируются с использованием CLSM в течение 18 ч. (C) После первоначальной 18-ч визуализации агрегаты обрабатывают йодидом пропидия для визуализации мертвых клеток и визуализируют с помощью CLSM (D) Агрегаты с желаемым фенотипом отделяют от SCFM2 с помощью FACS. Сокращения: SCFM2 = синтетический муковисцидоз мокроты; Pa = Синегнойная палочка; CLSM = конфокальная лазерная сканирующая микроскопия; FACS = флуоресцентная сортировка клеток. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Здесь демонстрируется полезность SCFM2 для изучения влияния лечения антибиотиками на агрегаты Pa в режиме реального времени, за которым следует использование клеточного подхода для выделения популяций агрегатов с различными фенотипами для последующего анализа(рисунок 1).
Protocol
Representative Results
Discussion
Эта работа представила методологии, которые могут быть объединены для изучения бактериальных совокупных популяций при наличии и отсутствии лечения антибиотиками. CLSM с высоким разрешением позволяет визуализировать изменения в совокупной биомассе и структурной ориентации агрегатов ?…
Divulgations
The authors have nothing to disclose.
Acknowledgements
S.E.D поддерживается стартовыми фондами, предоставляемыми Департаментом молекулярной медицины Университета Южной Флориды, а также исследовательским грантом CFF (DARCH19G0) N.I.H (5R21AI147654 – 02 (PI, Chen)) и Институтом микробиомов USF. Мы благодарим лабораторию Уайтли за постоянное сотрудничество с наборами данных, связанных с этой рукописью. Мы благодарим д-ра Чарльза Секереса за содействие в сортировке FACS. Рисунки были созданы A.D.G и S.E.D с использованием Biorender.com.
Materials
| Amino acids | |||
| Alanine | Acr s Organics s Organics |
56-41-7 | |
| Arginine HCl | MP | 1119-34-2 | |
| Asparagine | Acr s Organics s Organics |
56-84-8 | Prepared in 0.5 M NaOH |
| Cystine HCl | Alfa Aesar | L06328 | |
| Glutamic acid HCl | Acr s Organics s Organics |
138-15-8 | |
| Glycine | Acr s Organics s Organics |
56-40-6 | |
| Histidine HCl H2O | Alfa Aesar | A17627 | |
| Isoleucine | Acr s Organics s Organics |
73-32-5 | |
| Leucine | Alfa Aesar | A12311 | |
| Lysine HCl | Alfa Aesar | J62099 | |
| Methionine | Acr s Organics s Organics |
63-68-3 | |
| Ornithine HCl | Alfa Aesar | A12111 | |
| Phenylalanine | Acr s Organics s Organics |
63-91-2 | |
| Proline | Alfa Aesar | A10199 | |
| Serine | Alfa Aesar | A11179 | |
| Threonine | Acr s Organics s Organics |
72-19-5 | |
| Tryptophan | Acr s Organics s Organics |
73-22-3 | Prepared in 0.2 M NaOH |
| Tyrosine | Alfa Aesar | A11141 | Prepared in 1.0 M NaOH |
| Valine | Acr s Organics s Organics |
72-18-4 | |
| Antibiotic | |||
| Carbenicillin | Alfa Aesar | J6194903 | |
| Day-of Stocks | |||
| CaCl2 * 2H2O | Fisher Chemical | C79-500 | |
| Dextrose (D-glucose) | Fisher Chemical | 50-99-7 | |
| 1,2-dioleoyl-sn-glycero-3-phosphocholine (DOPC) | Fisher (Avanti Polar Lipids) | 4235-95-4 | shake 15-20 min at 37 °C to evaporate chloroform |
| FeSO4 * 7H2O | Acr s Organics s Organics |
7782-63-0 | this stock equals 1 mg/mL, MUST make fresh |
| L-lactic acid | Alfa Aesar | L13242 | pH stock to 7 with NaOH |
| MgCl2 * 6H2O | Acr s Organics s Organics |
7791-18-6 | |
| N-acetylglucosamine | TCI | A0092 | |
| Prepared solids | |||
| Porcine mucin | Sigma | M1778-100G | UV-sterilize |
| Salmon sperm DNA | Invitrogen | 15632-011 | |
| Stain | |||
| Propidium iodide | Alfa Aesar | J66764MC | |
| Salts | |||
| K2SO4 | Alfa Aesar | A13975 | |
| KCl | Alfa Aesar | J64189 | add solid directly to buffered base |
| KNO3 | Acr s Organics s Organics |
7757-79-1 | |
| MOPS | Alfa Aesar | A12914 | add solid directly to buffered base |
| NaCl | Fisher Chemical | S271-500 | add solid directly to buffered base |
| Na2HPO4 | RPI | S23100-500.0 | |
| NaH2PO4 | RPI | S23120-500.0 | |
| NH4Cl | Acr s Organics s Organics |
12125-02-9 | add solid directly to buffered base |
| Consumables | |||
| Conical tubes (15 mL) | Olympus plastics | 28-101 | |
| Conical tubes (50 mL) | Olympus plastics | 28-106 | |
| Culture tubes w/air flow cap | Olympus plastics | 21-129 | |
| 35 mm four chamber glass-bottom dish | CellVis | NC0600518 | |
| Luria Bertani (LB) broth | Genessee Scientific | 11-118 | |
| Phosphate-buffered saline (PBS) | Fisher Bioreagents | BP2944100 | |
| Pipet tips (p200) | Olympus plastics | 23-150RL | |
| Pipet tips (p1000) | Olympus plastics | 23-165RL | |
| Serological pipets (5 mL) | Olympus plastics | 12-102 | |
| Serological pipets (25 mL) | Olympus plastics | 12-106 | |
| Serological pipets (50 mL) | Olympus plastics | 12-107 | |
| Ultrapure water (RNAse/DNAse free); nanopure water | Genessee Scientific | 18-194 | Nanopure water used for preparation of solutions in Table 1 |
| Syringes (10 mL) | BD | 794412 | |
| Syringes (50 mL) | BD | 309653 | |
| 0.22 mm PES syringe filter | Olympus plastics | 25-244 | |
| PS cuvette semi-mico | Olympus plastics | 91-408 | |
| Software | |||
| Biorender | To prepare the figures | ||
| FacsDiva6.1.3 | Becton Dickinson, San Jose, CA | ||
| Imaris | Bitplane | version 9.6 | |
| Zen Black | |||
| Equipment | |||
| FacsAriallu | Becton Dickinson, San Jose, CA | ||
| LSM 880 confocal laser scanning microscope | Zeiss |
References
- Ramsay, K. A., et al. The changing prevalence of pulmonary infection in with fibrosis: A longitudinal analysis. Journal of Cystic Fibrosis. 16 (1), 70-77 (2017).
- Bessonova, L., et al. Data from the US and UK cystic fibrosis registries support disease modification by CFTR modulation with ivacaftor. Thorax. 73 (8), 731-740 (2018).
- Breuer, O., et al. Changing prevalence of lower airway infections in young children with cystic fibrosis. American Journal of Respiratory and Critical Care Medicine. 200 (5), 590-599 (2019).
- O’Donnell, J. N., Bidell, M. R., Lodise, T. P. Approach to the treatment of patients with serious multidrug-resistant Pseudomonas aeruginosa infections. Pharmacotherapy. 40 (9), 952-969 (2020).
- Bjarnsholt, T., et al. The in vivo biofilm. Trends in Microbiology. 21 (9), 466-474 (2013).
- Darch, S. E., et al. Spatial determinants of quorum signaling in a Pseudomonas aeruginosa infection model. Proceedings of the National Academy of Sciences of the United States of America. 115 (18), 4779-4784 (2018).
- Zhu, K., Chen, S., Sysoeva, T. A., You, L. Universal antibiotic tolerance arising from antibiotic-triggered accumulation of pyocyanin in Pseudomonas aeruginosa. PLoS Biology. 17 (12), 3000573 (2019).
- Ciofu, O., Tolker-Nielsen, T. Tolerance and resistance of Pseudomonas aeruginosa biofilms to antimicrobial agents-how P. aeruginosa can escape antibiotics. Frontiers in Microbiology. 10, 913 (2019).
- Turner, K. H., Wessel, A. K., Palmer, G. C., Murray, J. L., Whiteley, M. Essential genome of Pseudomonas aeruginosa in cystic fibrosis sputum. Proceedings of the National Academy of Sciences of the United States of America. 112 (13), 4110-4115 (2015).
- Darch, S. E., et al. Phage inhibit pathogen dissemination by targeting bacterial migrants in a chronic infection model. MBio. 8 (2), 00240 (2017).
- Jorth, P., et al. Regional isolation drives bacterial diversification within cystic fibrosis lungs. Cell Host & Microbe. 18 (3), 307-319 (2015).
- Palmer, K. L., Aye, L. M., Whiteley, M. Nutritional cues control Pseudomonas aeruginosa multicellular behavior in cystic fibrosis sputum. Journal of Bacteriology. 189 (22), 8079-8087 (2007).
- Davies, D. G., et al. The involvement of cell-to-cell signals in the development of a bacterial biofilm. Science. 280 (5361), 295-298 (1998).
- Hartmann, R., et al. Quantitative image analysis of microbial communities with BiofilmQ. Nature Microbiology. 6 (2), 151-156 (2021).
- Stacy, A., et al. Bacterial fight-and-flight responses enhance virulence in a polymicrobial infection. Proceedings of the National Academy of Sciences of the United States of America. 111 (21), 7819-7824 (2014).

