高速超分辨速度显微镜在活原纤毛中的应用
Summary
最近, 我们映射了三维 (3D) 的运输路线的空间位置的各种蛋白质转运内原纤毛的活细胞。本文详细介绍了新应用于活原纤毛的3D 超分辨率荧光成像方法的实验装置、生物样品的处理过程和数据分析。
Abstract
主要纤毛是在许多真核细胞的表面上的 microtubule-based 突起, 它包含了在细胞运动和信号中具有重要作用的独特的蛋白质补充。由于纤毛无法合成自己的蛋白质, 近200独特的睫状蛋白需要在胞和原发纤毛之间进行贩运。然而, 这仍然是一个技术上的挑战, 以地图三维 (3D) 的运输途径的这些蛋白质在活原发纤毛的位置, 由于目前现有的技术的局限性。为了克服这一挑战, 最近我们开发并使用了一个高速虚拟3D 超分辨率显微术, 称为单点边缘激发 sub-diffraction (速度) 显微镜, 以确定3D 空间位置的传输路径胞浆和细胞膜蛋白都是活细胞的主要纤毛。在本文中, 我们将演示的详细设置速度显微镜, 细胞表达荧光蛋白标记的睫状蛋白, real-time 分子跟踪个体蛋白在活纤毛和成就3D 空间概率密度图谱的传输路线的睫状蛋白。
Introduction
自 1873年, 由于来自目标12的光线衍射, 传统光学显微镜的分辨率被认为仅限于大约 200 nm。目前, 超分辨率光显微镜技术打破了这一限制, 并允许捕捉动态图像与 sub-diffraction (< 200 nm) 的决议。该技术一般分为两大类: 受激发射损耗 (STED) 显微镜的方法, 它产生 sub-diffraction 光照体积由于非线性光学响应的荧光在样本3;和光光显微镜 (手掌) 和随机光学重建显微镜 (风暴) 的超分辨率技术, 利用数学功能, 本地化质心的荧光, 然后重建这些质心要形成超分辨率图像4,5。目前, 由于相对简单的光学设置, 棕榈和风暴是广泛使用的只激活一个小子集的荧光在每个帧的一个长视频的生物准备。这使得更精确的定位由2D 高斯拟合的荧光点, 称为点扩散函数 (聚砜), 荧光标记的蛋白质在每个帧的视频。每个荧光标记的分子的2D 位置, 然后可以叠加在一个单一的成像平面上产生一个超分辨率的图像的生物准备1,2。虽然这些分子的本地化, 超分辨率的方法, 以显微镜肯定革命性的生物样品的成像是如何进行的, 仍然有挑战要克服。例如, 风暴和棕榈可以达到他们的最佳空间分辨率后, 固定的生物样品, 从而提出了静态表示的荧光标记蛋白, 这是一个类似的限制电子显微镜。此外, 为了实现在活细胞中每个荧光标记的蛋白质的高空间分辨率, 样品必须成像在非常长的帧, 不能捕捉蛋白质动力学。因此, 有必要克服这些主要的技术障碍。
为了获得一个高时空分辨率, 它非常适合在活细胞中检测快速移动的蛋白质或 rna, 我们在实验室中开发了超分辨速度显微镜 (图 1)6,7,8. 速度显微镜的几个主要技术进步使我们能够成功地追踪小分子、蛋白质、mRNA 和病毒通过本机核孔复合体 (npc) 的 nucleocytoplasmic 传输,6,7,8. 简要地, 以下速度显微镜的特点将用于跟踪快速移动的大分子通过微米旋转对称结构在活细胞, 例如 npc 和主要纤毛: (1) 倾斜或垂直照明, 使在焦平面的小衍射极限体积内的单分子激发 (图 1);(2) 倾斜的聚砜可以极大地避免焦荧光, 从而提高信噪比。(3) 光照中的 100-500 kW/cm2的光学密度允许数千个光子从单个荧光中收集, 并具有快速检测速度 (> 500 Hz)。(4) 快速检测速度还大大降低了分子空间定位错误 (< 10 nm) 在确定活细胞中移动荧光分子的空间轨迹时, 因为分子扩散是主要因素之一造成移动分子分子定位的缺陷。(5) 良好的2D 到3D 转换算法使我们能够为 NPC 或主要纤毛中的分子提供3D 空间概率密度地图。值得注意的是, 我们在笛卡尔和圆柱坐标系之间的转换过程被用来生成3D 空间概率密度图而不是3D 分子跟踪 (图 2)。此前, 电子显微镜数据显示, NPC9、10和主纤毛11都具有旋转对称结构。原则上, 随机扩散分子通过 NPC 或初级纤毛也应该有旋转对称分布。如图 2所示, 大量随机扩散的分子在气缸内将产生旋转对称分布, 在剖面图, 在 NPC, 进一步导致一个近似一致的空间在相邻的两个环之间的每个非常小的子区域中分布 (图 2E)。这种均匀分布导致圆柱系统中θ维数的空间分布是恒定的。然后, 3D 坐标 (r、x、θ) 可以简化为2D 坐标 (r、x、常量)。实际上, 我们在笛卡尔和圆柱系统之间的转换过程是从 2D (x, Y) 到 2D (R, x, 常数)。常数θ, 指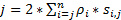 的是空间密度p在图 2E中, 是通过使用等式A来计算的。
的是空间密度p在图 2E中, 是通过使用等式A来计算的。
最终, 分子跟踪在生物研究中有着广泛的应用, 因此, 将开发大量的技术来填充特定的生物龛位12、13、14是很自然的。速度显微镜就是如此。以前, 当与3D 变换算法结合时, 这项技术被开发来解决通过 npc 传递分子的3D 传输路线, 一个 sub-diffraction-sized 和旋转对称的生物结构6。本文中, 原发纤毛也被证明是优秀的模型细胞器。主要纤毛是圆柱形的, 天线状的细胞器 (~ 125 nm 半径), 该项目从大多数哺乳动物的表面15,16,17。它们负责接收外部信号, 并传送通常与生长和新陈代谢相关的细胞内反应15,16。因此, 结构蛋白的通量、跨膜受体的再循环以及细胞内信使的传递是原发性纤毛的重要责任。在主要纤毛和细胞体之间的接合处是一种临界选择性屏障, 称为过渡区或正向, 所有这些蛋白传输必须发生11,18,19, 20。除了 intraflagellar 的浇注功能, 至少有两个传输过程, 即传输和被动扩散, 被认为是负责蛋白质的移动通过这个区域16,21,22. 从人类健康的角度来看, 失去初级纤毛和随后对下游信号的放松管制是许多癌症的特点。此外, 许多遗传性疾病, 如 Bardet Biedl 综合征和多囊肾病, 都与有缺陷的蛋白质转运有关23。sub-diffraction 极限大小和选择性蛋白转运的复杂过程, 使原纤毛成为这项技术的主要目标。在本方法中, 我们将展示一个睫状跨膜蛋白的跟踪, 生长抑素受体 3 (SSTR3)24, 在外部标有 Alexa 氟647和 IFT, IFT2025的成分, 用一个融合的 GFP 分子标记。
Protocol
Representative Results
Discussion
该协议描述了速度显微镜在初级纤毛的应用, 这是一种高度依赖高效蛋白质传输的细胞信号器官。速度显微镜可以提供高分辨率 (< 10 nm) 的位置为荧光标记分子, 因为他们通过单点照明中心的中间。此前它已被应用于研究通过 NPC 的蛋白质贩运6,7,8。然而, 它可以扩展到研究通过任何 sub-diffraction 细胞腔的贩运。该技术比其他高分?…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
我们感谢 Dr. 克里斯汀 Verhey (密歇根大学, 安阿伯) 和 Dr. 格雷戈里 Pazour (马萨诸塞大学医学院) 提供一些质粒。该项目得到了国家卫生研究院 (NIH GM097037、GM116204 和 GM122552 W.Y.) 的资助。
Materials
| 25 cm2 tissue culture dish | Corning | VV-01936-00 | |
| Penicillin/streptomycin | ThermoFisher | 15140122 | |
| Fetal bovine serum | ThermoFisher | 10438018 | |
| DMEM | ThermoFisher | 10566-016 | |
| OPTIMEM | ThermoFisher | 31985062 | |
| Trypsin | ThermoFisher | 25300054 | |
| Phosphate buffered saline | Sigma-Aldrich | P3813-1PAK | |
| Transit LT1 | Mirus | MIR 2300 | |
| 35 mm glass bottom dish | MatTek | P35GCOL-0-14-C | |
| AlexaFluor 647-conjugated streptavidin | ThermoFisher | S21374 | |
| Biotin | Sigma-Aldrich | B4501-100MG | |
| 633 nm He-Ne laser | Melles Griot | 25-LHP-928-249 | |
| 561 nm solid state laser | Coherent | OBIS 561-50 LS | |
| 488 nm solid state laser | Coherent | 1185053 | |
| Inverted fluorescence microscope | Olympus | IX81 | |
| 1.4-NA 100× oil-immersion apochromatic objective | Olympus | UPLSAPO 100× | |
| On-chip multiplication gain charge-coupled-device camera | Roper Scientific | Cascade 128+ | |
| Dichroic filter | Semrock | Di01- R405/488/561/635-25×36 | |
| Emission filter | Semrock | NF01-405/488/561/635-25X5.0 | |
| Slidebook 6.0 | Intelligent Imaging Innovations | digital microscopy software |
Riferimenti
- Huang, B., Bates, M., Zhuang, X. Super-resolution fluorescence microscopy. Annu Rev Biochem. 78, 993-1016 (2009).
- Leung, B. O., Chou, K. C. Review of super-resolution fluorescence microscopy for biology. Appl Spectrosc. 65, 967-980 (2011).
- Willig, K. I., Rizzoli, S. O., Westphal, V., Jahn, R., Hell, S. W. STED microscopy reveals that synaptotagmin remains clustered after synaptic vesicle exocytosis. Nature. 440, 935-939 (2006).
- Betzig, E., et al. Imaging intracellular fluorescent proteins at nanometer resolution. Science. 313, 1642-1645 (2006).
- Rust, M. J., Bates, M., Zhuang, X. Sub-diffraction-limit imaging by stochastic optical reconstruction microscopy (STORM). Nat Meth. 3, 793-796 (2006).
- Ma, J., Yang, W. Three-dimensional distribution of transient interactions in the nuclear pore complex obtained from single-molecule snapshots. Proc Natl Acad Sci USA. 107, 7305-7310 (2010).
- Ma, J., Goryaynov, A., Sarma, A., Yang, W. Self-regulated viscous channel in the nuclear pore complex. Proc Natl Acad Sci USA. 109, 7326-7331 (2012).
- Ma, J., et al. High-resolution three-dimensional mapping of mRNA export through the nuclear pore. Nat Comm. 4, (2013).
- Akey, C. W., Radermacher, M. Architecture of the Xenopus nuclear pore complex revealed by three-dimensional cryo-electron microscopy. J Cell Biol. 122, 1-19 (1993).
- Akey, C. W. Interactions and structure of the nuclear pore complex revealed by cryo-electron microscopy. J Cell Biol. 109, 955-970 (1989).
- Czarnecki, P. G., Shah, J. V. The ciliary transition zone: from morphology and molecules to medicine. Trends Cell Biol. 22, 201-210 (2012).
- Elf, J., Li, G. -. W., Xie, X. S. Probing transcription factor dynamics at the single-molecule level in a living cell. Science. 316, 1191-1194 (2007).
- Anzalone, A., Annibale, P., Gratton, E. 3D orbital tracking in a modified two-photon microscope: an application to the tracking of intracellular vesicles. J Vis Exp. , (2014).
- Ritter, J. G., Veith, R., Veenendaal, A., Siebrasse, J. P., Kubitscheck, U. Light sheet microscopy for single molecule tracking in living tissue. PloS one. 5, 11639 (2010).
- Marshall, W. F., Nonaka, S. Cilia: tuning in to the cell’s antenna. Curr Biol. 16, 604-614 (2006).
- Scholey, J. M., Anderson, K. V. Intraflagellar transport and cilium-based signaling. Cell. 125, 439-442 (2006).
- Yang, T. T., et al. Superresolution pattern recognition reveals the architectural map of the ciliary transition zone. Sci Rep. 5, 14096 (2015).
- Craige, B., et al. CEP290 tethers flagellar transition zone microtubules to the membrane and regulates flagellar protein content. J Cell Biol. 190, 927-940 (2010).
- Kee, H. L., et al. A size-exclusion permeability barrier and nucleoporins characterize a ciliary pore complex that regulates transport into cilia. Nat Cell Biol. 14, 431-437 (2012).
- Najafi, M., Maza, N. A., Calvert, P. D. Steric volume exclusion sets soluble protein concentrations in photoreceptor sensory cilia. Proc Natl Acad Sci USA. 109, 203-208 (2012).
- Nachury, M. V., Seeley, E. S., Jin, H. Trafficking to the ciliary membrane: how to get across the periciliary diffusion barrier. Annu Rev Cell Dev Biol. 26, 59-87 (2010).
- Ye, F., et al. Single molecule imaging reveals a major role for diffusion in the exploration of ciliary space by signaling receptors. Elife. 2, 00654 (2013).
- Ross, A. J., et al. Disruption of Bardet-Biedl syndrome ciliary proteins perturbs planar cell polarity in vertebrates. Nat Genetics. 37, 1135-1140 (2005).
- Handel, M., et al. Selective targeting of somatostatin receptor 3 to neuronal cilia. Neuroscienze. 89, 909-926 (1999).
- Follit, J. A., Tuft, R. A., Fogarty, K. E., Pazour, G. J. The intraflagellar transport protein IFT20 is associated with the Golgi complex and is required for cilia assembly. Mol Biol Cell. 17, 3781-3792 (2006).
- Awata, J., et al. NPHP4 controls ciliary trafficking of membrane proteins and large soluble proteins at the transition zone. J Cell Sci. 127, 4714-4727 (2014).
- Howarth, M., Ting, A. Y. Imaging proteins in live mammalian cells with biotin ligase and monovalent streptavidin. Nat Protoc. 3, 534-545 (2008).
- Huang, B., Wang, W., Bates, M., Zhuang, X. Three-dimensional super-resolution imaging by stochastic optical reconstruction microscopy. Science. 319, 810-813 (2008).

