無細胞再構成のための組換えセプチン複合体の精製と品質管理
Summary
細胞骨格タンパク質のin vitro再構成は、これらのタンパク質の基本的な機能特性を理解するための重要なツールです。本論文は、細胞分裂と遊走において中心的な役割を果たす組換えセプチン複合体の品質を精製および評価するためのプロトコルを記載する。
Abstract
セプチンは、ヘテロオリゴマー複合体から細胞骨格フィラメントおよび高次構造を形成することができる保存された真核生物GTP結合タンパク質のファミリーです。それらは他の細胞骨格成分および細胞膜と相互作用して、遊走および細胞分裂などの重要な細胞機能に関与する。セプチンの多くの相互作用の複雑さ、多数のセプチン遺伝子(ヒトでは13個)、およびセプチンが異なるサブユニット組成を持つヘテロオリゴマー複合体を形成する能力のために、無細胞再構成はセプチン生物学の基礎を理解するための重要な戦略です。本論文では、まず、2段階アフィニティークロマトグラフィーアプローチを使用して、ヘテロオリゴマー形態の組換えセプチンを精製する方法について説明します。次に、セプチン複合体の純度と完全性をチェックするために使用される品質管理のプロセスが詳細に説明されています。このプロセスは、ネイティブおよび変性ゲル電気泳動、負染色電子顕微鏡、および干渉散乱顕微鏡を組み合わせたものです。最後に、ネガ染色電子顕微鏡および蛍光顕微鏡を用いてセプチン錯体の重合能を確認するプロセスについて説明する。これは、ショ ウジョウバエ セプチン六量体と同様に、高品質のヒトセプチン六量体および異なるseptin_9アイソフォームを含む八量体を製造することが可能であることを示している。
Introduction
細胞骨格は、古典的にはアクチンフィラメント、微小管、中間フィラメント1からなる3成分系と記載されてきたが、最近では細胞骨格1の第4成分としてセプチンが認められている。セプチンは、真核生物に保存されているGTP結合タンパク質のファミリーです2。セプチンは、細胞分裂3、細胞間接着4、細胞運動性5、形態形成6、細胞感染7、細胞極性の確立と維持8など、多くの細胞機能に関与しています。それらの重要な機能にもかかわらず、セプチンがそのようなプロセスにどのように関与しているかはよく理解されていません。
セプチンファミリーのタンパク質は、タンパク質配列の類似性に基づいていくつかのサブグループ(分類に応じて4つまたは7つ)に細分されます2。異なるサブファミリーのメンバーは、フィラメントの構成要素であり、次にバンドル、リング、メッシュワークなどの高次構造に集合する回文ヘテロオリゴマー複合体を形成することができます1,9,10,11,12。さらなる分子の複雑さは、異なるスプライス変異体の存在から生じ、その一例はヒトSEPT9であり、そこでは異なるスプライス変異体の特定の機能の証拠がある13、14、15。さらに、ヘテロオリゴマーの長さは、種および細胞型に依存する。例えば、カエノラブディティス・エレガンス・セプチンは四量体16を形成し、ショウジョウバエ・メラノガスター・セプチンは六量体17を形成し(図1A)、サッカロミセス・セレビシエ・セプチンは八量体18を形成し、ヒトセプチンは六量体と八量体19の両方を形成します(図1A)。同じサブファミリー由来のセプチンアイソフォーム、スプライスバリアント、および翻訳後修飾セプチンが複合体内で互いに置換する能力、および異なるサイズのヘテロオリゴマーの(共)存在により、異なるヘテロオリゴマー複合体の細胞機能を描写することが困難になっています12。
セプチンのもう一つの興味深い能力は、細胞内の多くの結合パートナーと相互作用する能力です。セプチンは、間期および細胞分裂中に原形質膜および膜細胞小器官に結合する20,21,22。細胞分裂において、セプチンは細胞質分裂中にアニリン23,24,25ならびにアクチンおよびミオシンと協力する26,27。細胞質分裂の後期段階では、セプチンは中体離脱のための輸送(ESCRT)システムに必要なエンドソーム選別複合体を調節するようである28。さらに、間期細胞のアクチン皮質およびアクチンストレス線維に位置するセプチンの証拠もあります29、30、31。特定の細胞型では、セプチンは微小管細胞骨格にも結合して調節する32,33。
これらすべての特徴により、セプチンは研究するのに非常に興味深いタンパク質システムになりますが、挑戦的なタンパク質システムでもあります。多数のセプチンサブユニット(スプライスバリアント2を数えずにヒトでは13遺伝子)と、同じサブファミリーのセプチンサブユニットが互いに置換し、異なるサイズのヘテロオリゴマーを形成する可能性の組み合わせにより、遺伝子操作によって特定のセプチンの細胞機能について結論を出すことは困難です。さらに、セプチンの複数の相互作用により、細胞骨格または膜成分に向けられた薬物34 などの一般的な研究ツールの効果を解釈することは困難な作業になります。
この状況を克服する方法は、セプチンのin vitro(無細胞)再構成で細胞内の研究を補完することです。インビトロ再構成は、特定のサブユニット組成および長さ18、35、36、37を有する単一タイプのセプチンヘテロオリゴマーの単離を可能にする。この複合体は、セプチン38,39,40の基本的な構造的および物理化学的特性を発見するために単独で、またはモデル生体膜11,41,42、アクチンフィラメント10,27、または微小管32,36などの所望のパートナーと組み合わせて、それらの性質を解読するために、制御された環境で研究することができる。相互 作用。
したがって、さまざまなセプチン複合体を効率的に精製するための信頼性の高い方法は、セプチン研究にとって不可欠です。ただし、同じプロトコルを使用しても、精製が異なれば、活性/機能、さらには完全性が異なるタンパク質が得られる可能性があります。酵素などの市販のタンパク質については、機能性および酵素活性が注意深く検証される43。セプチンなどの細胞骨格タンパク質や構造タンパク質の慎重な品質管理を実施することは困難な場合がありますが、ラボ間での実験を比較可能にすることが不可欠です。
この論文では、大腸菌細胞におけるモノまたはバイシストロン構築物を含む2つのベクター(表1)の同時発現に基づいて、ヘテロオリゴマー形態の高品質の組換えセプチンを精製する堅牢な方法について説明します。この方法は、his6タグセプチンとStrep-IIタグセプチンの両方を含むセプチンヘテロオリゴマーを捕捉するための2段階アフィニティークロマトグラフィーアプローチで構成されています(図1B、C)。Ivら10で最初に記載されたこのプロトコルは、ショウジョウバエセプチン六量体11、27、35、ヒトセプチン六量体10、および異なる天然(アイソフォーム1、3、および5)10,32または変異したSEPT9アイソフォーム32を含むいくつかのヒトセプチン八量体を精製するために使用されています。.さらに、精製されたセプチンの品質を評価するための一連の技術の説明が与えられる。まず、セプチンサブユニットの完全性と正しい化学量論を変性電気泳動と透過型電子顕微鏡(TEM)を使用してチェックします。次に、正しい分子量のヘテロオリゴマーの存在、および複雑な不安定性を示すモノマーまたはより小さなオリゴマーの存在を、ネイティブ電気泳動および干渉散乱顕微鏡(iSCAT)を介した質量測光によって調べます。最後に、最後のステップは、蛍光顕微鏡とTEMを使用したセプチンの重合活性の評価で構成されます。
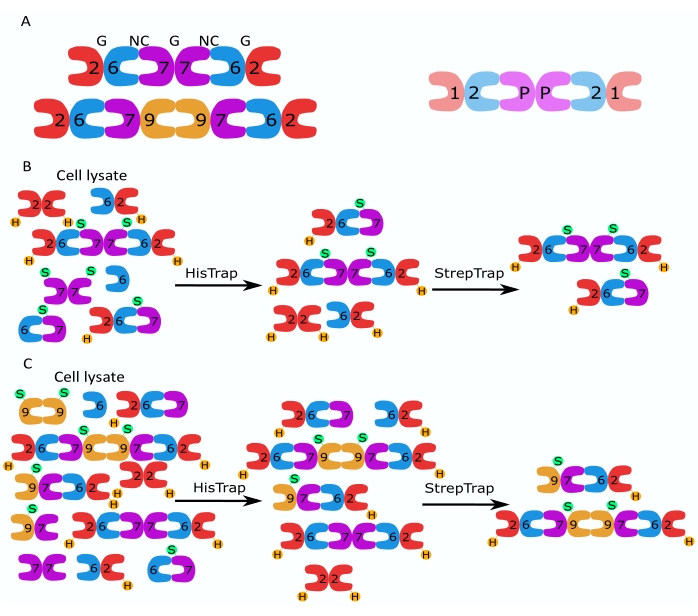
図1:精製戦略 。 (A)ヒト(左)と ショウジョウバエ (右)の細胞に存在するセプチンヘテロオリゴマーの模式図。数字は示されたグループのセプチンサブユニットを示し、Pはピーナッツを示します。ヒトSEPT9は、そのアイソフォームのいずれかであり得る。セプチンサブユニットは非対称形状を有し、ヒト六量体の上にそれぞれNCおよびGで示されるように、2つの異なる界面、NC:NCおよびG:G界面に縦方向に関連付けられる。(B,C)二段階クロマトグラフィー戦略の概略図を、(B)ヒトセプチン六量体および(C)八量体について示す。Hはヒスタグを示し、SはストレプIIタグを示します。 この図の拡大版を表示するには、ここをクリックしてください。
Protocol
Representative Results
Discussion
ここで説明する方法は、予め形成されたセプチンヘテロオリゴマーの堅牢な精製および品質管理を可能にする。この方法を正しく適用するために考慮すべき重要な問題のいくつかは次のとおりです。クロマトグラフィー分離の溶出ステップでは、セプチン複合体の希釈を最小限に抑えるために、推奨される(またはそれより低い)流速を使用することが重要です。さらに、最終濃縮ステップ中のタンパク質の回収率を最大化するために、濃縮カラムは、溶液がフィルターに押し付けられないように配向されています(片側にフィルターしかない場合)。溶液がフィルターに直接送られると、タンパク質はフィルターにはるかに付着し、最終収量が大幅に減少します。濃縮ステップが必ずしも必要ではないことを考慮することも重要です。クロマトグラムのピーク付近の狭い範囲からのみフラクションをピックすると、通常、多くの再構成アプリケーション(通常は10〜300 nM)に十分な高いストック濃度(>3,000 nM)が得られます。最後に、蛍光顕微鏡によるセプチン複合体の機能性の品質管理のためには、セプチン複合体がガラスに熱心に付着するため、顕微鏡スライドの表面を正しく不動態化することが重要です。スライドガラスの不動態化は、PLL−PEG機能化を介して、または中性(100%DOPC)支持脂質二重層の形成のいずれかによって行うことができる11,32。
Ivら10で最初に記載された元の精製プロトコルと比較して、緩衝液組成に変化がある(表2)。MgCl2の濃度は5mMから2mMに減少し、トリス塩酸塩の濃度およびpHはそれぞれ50mMから20mMにおよび8.0から7.4に減少した。これらの変更は、緩衝条件をヒトセプチンと脂質二重層、アクチンフィラメント、および微小管との相互作用の研究に適合させるために行われました10,11,32。これは、著者らがFバッファー中に支持された脂質二重層を形成し、Fバッファー中にATPが存在することを除けば、その組成がdarkSPBの組成と同じであるためである。バッファーの変更は、元のバッファーと比較して精製セプチンの品質または寿命に変化をもたらさなかった。
この精製方法にはまだいくつかの制限があります。第一に、精製の異なる試みは、精製されたセプチン複合体のバンドル形成能力によって確認されるように、収率(0.5〜1mLの2〜5μMセプチン複合体)および機能品質において異なる可能性がある。そのため、このホワイトペーパーで説明されている品質チェックを一貫して実行することが非常に重要です。発現時間と細菌培養物の光学密度を非常によく制御することで、収量の差を軽減することができます。第二に、この精製パイプラインは三量体と六量体、または四量体と八量体を区別できません(図1B)。しかしながら、品質管理実験は、セプチン複合体の大部分がそれらの長いオリゴマー形態であることを証明するために使用することができる。さらに狭いオリゴマーサイズ分布が必要な場合は、ステップ1.6の間にサイズ排除クロマトグラフィーを挿入できます。およびステップ1.7。精製プロトコルの。ただし、このオプションのステップは歩留まりを劇的に低下させるため、厳密に必要な場合を除いて推奨されません。最後の、より根本的な制限は、組換えセプチン複合体の発現系としての大腸菌の使用から来ています。当然のことながら、このシステムは、リン酸化、アセチル化、およびスモイル化などの動物細胞で報告されている翻訳後修飾(PTM)を許可しません6,51,52,53。これらの翻訳後修飾は、昆虫またはヒト細胞において同様の精製戦略を実施することによって追加することができる。さらに、この論文ではセプチンの再構成についてのみ議論しましたが、細胞での研究では、Borgファミリー54,55やアニリン24,25,56のタンパク質などの調節タンパク質は、セプチンの組み立てと機能に実質的でありながら十分に理解されていない影響を与える可能性があるため、最終的にin vitroに組み込むことが重要です。 勉強。Borgタンパク質およびアニリンの精製のためのプロトコールが報告されている54,57。
ここで報告されているセプチン精製プロトコルは、正しいサブユニット化学量論でオリゴマー形態のセプチンを精製するための標準化された方法を提供し、単一のセプチンサブユニットに依存する多くの以前のin vitro研究よりも重要な進歩を提供します。特定の状況におけるいくつかのセプチンは単一のサブユニット2として作用することができるが、現在の文献は、動物細胞において、セプチンが主に複合体9,58で機能することを強く示唆している。したがって、この論文や他の論文10、11、18、32、35、36、37に記載されているような事前に形成されたヘテロオリゴマーの使用は、in vitroを介してセプチンの構造的および生物物理学的特性を研究するために非常に重要です。 細胞内のそれらの機能を解剖するための再構成。さらに、セプチンは、膜や細胞骨格を含む多くの相互作用パートナーを持つ自己組織化タンパク質であり、ボトムアップ合成生物学59,60,61や、湾曲42,62,63などの膜生物物理学的特性におけるタンパク質誘発性変化の研究にとって非常に興味深いものとなっています。
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
我々は、質量測光(iSCAT)実験への協力について、セシリア・デ・アグレラ・ピント氏、トマス・デ・ガライ氏、カタリーナ・ホイサーマン氏に感謝する。アリエン・ヤコビとヴィエル・エヴァースがTEMを手伝ってくれた。TIRFへの支援に対するルシア・バルダウフ。パスカル・ヴェルディエ・ピナール ネイティブ電気泳動に関するアドバイス。ショウジョウバエセプチン精製の取り組みの立ち上げを支援してくれたAgata SzubaとMarjolein Vinkenoog、およびフランス国立研究インフラストラクチャフランスバイオイメージング(ANR10-INBS-04)のメンバーであるキュリー研究所の細胞および組織イメージング(PICT-IBiSA)。この研究は、オランダ科学研究機構(NWO / OCW)から「BaSyC-合成細胞の構築」重力助成金(024.003.019)および国立研究開発庁(ANR助成金ANR-17-CE13-0014:「セプティモルフ」;ANR-13-JSV8-0002-01: “SEPTIME”;およびANR-20-CE11-0014-01:「セプツコート」)。
Materials
| 488nm laser combiner iLAS2 | Gataca | TIRF microscope | |
| 488nm Sapphire laser lines | Coherent | Confocal microscope | |
| 4k X 4k F416 CMOS camera | TVIPS | For JEM-1400plus | |
| 4x sample buffer nativePAGE | Thermo Fisher scientific | BN2003 | |
| 6-Hydroxy-2,5,7,8-tetramethylchromane-2-carboxylic acid (TROLOX) | Sigma-Aldrich | 238813 | To prevent blinking |
| AKTA pure 25 M1 | GE healthcare | 1680311 | |
| Ampicillin | Sigma-Aldrich | A9518-25G | |
| Carbon Type-B, 300 mesh EM grid | Ted pella | 01813-F | |
| Carbon Type-B, 300 mesh EM grid | Electron micoscopy sciences | CF300-Cu | |
| Cover glass #1.5H | Thorslabs | CG15KH | |
| CSU-X1-M1 confocal unit | Yokogawa | Confocal microscope | |
| Desthiobiotin | Sigma-Aldrich | D1411-1G | |
| Dithiothreitol (DTT) | Sigma-Aldrich | D9779 | |
| DNAse | Sigma-Aldrich | 10104159001 | |
| DOPC | Avanti Polar Lipids | 850375C | |
| Eclipse Ti2-E | Nikon instruments | Confocal microscope | |
| EDTA-free protease inhibtor cocktail | Roche | 481761 | |
| HisTrap HP, 5 mL | GE healthcare | 29-0588-3 | |
| iLAS2 azimuthal TIRF illumination system | Gataca | TIRF microscope | |
| Imidazole | Sigma-Aldrich | 1202-1KG | |
| InstantBlue Protein Gel Stain | Westburg Life Sciences | EP ab119211 | |
| Isopropyl β-D-1-thiogalactopyranoside (IPTG) | Thermo Fisher scientific | 10849040 | |
| iXon Ultra 888 EMCCD camera | Andor | Confocal microscope | |
| iXon Ultra 897 EM-CCD | Andor | TIRF microscope | |
| JEM-1400plus | JOEL | TEM microscope TUDelft | |
| kappa-cassein | Sigma-Aldrich | C0406 | |
| LB broth | Sigma-Aldrich | L3022-6X1KG | |
| Lyzozyme | Sigma-Aldrich | 62971-10G-F | |
| Magnesium Chloride | Sigma-Aldrich | M8266-100G | |
| Magnesium sulfate | Sigma-Aldrich | 746452-1KG | |
| Methylecllulose | Sigma-Aldrich | 8074844 | |
| MilliQ system (Integral 10) | Merck-Millipore | I-water dispenser | |
| Mini protean TGX gels | BIORAD | 4561086 | |
| NativeMark unstained protein standard | Invitrogen | LC0725 | For iSCAT and Native gels |
| NativePAGE 4-16% GELS | Thermo Fisher scientific | BN1002BOX | |
| NativePAGE Running Buffer kit | Thermo Fisher scientific | BN2007 | |
| Nikon Ti2-E | Nikon instruments | TIRF microscope | |
| Nr. 1 Menzel coverslips | Thermo Fisher scientific | 11961988 | |
| parafilm | Sigma-Aldrich | P7668 | |
| Plan Apo ×100/1.45 NA oil immersion objective | Nikon instruments | Confocal microscope | |
| PMSF | Sigma-Aldrich | 10837091001 | |
| Poly(L-lysine)-graft-biotinylated PEG (PLL-PEG) | SuSoS | CHF560.00 | |
| Poly-L-lysine solution 0.01% | Sigma-Aldrich | P4832 | For iSCAT glass slides |
| Pottassium Chloride | Sigma-Aldrich | P9541-1KG | |
| Power supply for native gels | CONSORT | S/N 71638 | |
| POWERPAC UNIVERSAL | BIORAD | 042BR31206 | |
| Protocatechuate 3,4-Dioxygenase (PCD) | Sigma-Aldrich | P8279-25UN | oxygen scavenger – enzyme |
| Protocatechuic acid (PCA) | Sigma-Aldrich | 03930590-50MG | oxygen scavenger – reagent |
| Q500 Sonicator | Qsonica | Q500-110 | |
| Quemesa camera | Olympus | For Tecnai Spirit | |
| Refeyn OneMP | Refeyn | ||
| Sample buffer, laemmli 2x concentrate | Sigma-Aldrich | S3401-10vl | |
| Silicon gaskets | Sigma-Aldrich | GBL103250-10EA | |
| Slide-A-Lyzer Dialysis cassettes 30k MWCO 3mL | Thermo Fisher scientific | 66381 | |
| Spectinomycin | Sigma-Aldrich | PHR1441-1G | |
| StrepTrap HP, 1 mL | GE healthcare | 28-9075-46 | |
| Tecnai Spirit microscope | Thermo Scientific, FEI | TEM microscope Institute Curie | |
| Terrific broth | Sigma-Aldrich | T0918-1KG | |
| Tris/Glyine/SDS buffer | BIORAD | 1610772 | |
| Tris-HCl | Sigma-Aldrich | T5941-1KG | |
| Ultrasonic cleaner | Branson | CPX2800H-E | |
| Vivaspin 6, 30,000 MWCO PES | Sartorius | VS0622 |
Riferimenti
- Mostowy, S., Cossart, P. Septins: The fourth component of the cytoskeleton. Nature Reviews Molecular Cell Biology. 13 (3), 183-194 (2012).
- Shuman, B., Momany, M. Septins from protists to people. Frontiers in Cell and Developmental Biology. 9, 3802 (2022).
- Bridges, A. A., Gladfelter, A. S. Septin form and function at the cell cortex. Journal of Biological Chemistry. 290 (28), 17173-17180 (2015).
- Smith, C., et al. Septin 9 exhibits polymorphic binding to F-actin and inhibits myosin and cofilin activity. Journal of Molecular Biology. 427 (20), 3273-3284 (2015).
- Gilden, J. K., Peck, S., Chen, Y. C. M., Krummel, M. F. The septin cytoskeleton facilitates membrane retraction during motility and blebbing. Journal of Cell Biology. 196 (1), 103-114 (2012).
- Marquardt, J., Chen, X., Bi, E. Architecture, remodeling, and functions of the septin cytoskeleton. Cytoskeleton. 76 (1), 7-14 (2018).
- Van Ngo, H., Mostowy, S. Role of septins in microbial infection. Journal of Cell Science. 132 (9), (2019).
- Fung, K. Y. Y., Dai, L., Trimble, W. S. Cell and molecular biology of septins. International Review of Cell and Molecular Biology. 310, 289-339 (2014).
- Kinoshita, M., Field, C. M., Coughlin, M. L., Straight, A. F., Mitchison, T. J. Self- and actin-templated assembly of mammalian septins. Developmental Cell. 3 (6), 791-802 (2002).
- Iv, F., et al. Insights into animal septins using recombinant human septin octamers 2 with distinct SEPT9 isoforms. Journal of Cell Science. 134 (15), (2021).
- Szuba, A., et al. Membrane binding controls ordered self-assembly of animal septins. eLife. 10, 63349 (2021).
- Kinoshita, M. Assembly of mammalian septins. Journal of Biochemistry. 134 (4), 491-496 (2003).
- Connolly, D., et al. Septin 9 isoform expression, localization and epigenetic changes during human and mouse breast cancer progression. Breast Cancer Research. 13 (4), 76 (2011).
- Connolly, D., et al. Septin 9 amplification and isoform-specific expression in peritumoral and tumor breast tissue. Biological Chemistry. 395 (2), 157-167 (2014).
- Estey, M. P., Di Ciano-Oliveira, C., Froese, C. D., Bejide, M. T., Trimble, W. S. Distinct roles of septins in cytokinesis: SEPT9 mediates midbody abscission. Journal of Cell Biology. 191 (4), 741-749 (2010).
- John, C. M., et al. The Caenorhabditis elegans septin complex is nonpolar. EMBO Journal. 26 (14), 3296-3307 (2007).
- Field, C. M., et al. A purified Drosophila septin complex forms filaments and exhibits GTPase activity. Journal of Cell Biology. 133 (3), 605-616 (1996).
- Bertin, A., et al. Saccharomyces cerevisiae septins: Supramolecular organization of heterooligomers and the mechanism of filament assembly. Proceedings of the National Academy of Sciences of the United States of America. 105 (24), 8274-8279 (2008).
- Sellin, M. E., Sandblad, L., Stenmark, S., Gullberg, M. Deciphering the rules governing assembly order of mammalian septin complexes. Molecular Biology of the Cell. 22 (17), 3152-3164 (2011).
- Akil, A., et al. Septin 9 induces lipid droplets growth by a phosphatidylinositol-5-phosphate and microtubule-dependent mechanism hijacked by HCV. Nature Communications. 7, 12203 (2016).
- Tanaka-Takiguchi, Y., Kinoshita, M., Takiguchi, K. Septin-mediated uniform bracing of phospholipid membranes. Current Biology. 19 (2), 140-145 (2009).
- Omrane, M., et al. Septin 9 has two polybasic domains critical to septin filament assembly and Golgi integrity. iScience. 13, 138-153 (2019).
- Carim, S. C., Kechad, A., Hickson, G. R. X. Animal cell cytokinesis: The rho-dependent actomyosin-anilloseptin contractile ring as a membrane microdomain gathering, compressing, and sorting machine. Frontiers in Cell and Developmental Biology. 8, 575226 (2020).
- El Amine, N., Kechad, A., Jananji, S., Hickson, G. R. X. Opposing actions of septins and Sticky on Anillin promote the transition from contractile to midbody ring. Journal of Cell Biology. 203 (3), 487-504 (2013).
- Renshaw, M. J., Liu, J., Lavoie, B. D., Wilde, A. Anillin-dependent organization of septin filaments promotes intercellular bridge elongation and Chmp4B targeting to the abscission site. Open Biology. 4 (1), 130190 (2014).
- Vogt, E. T., et al. The ultrastructural organization of actin and myosin II filaments in the contractile ring: new support for an old model of cytokinesis. Molecular Biology of the Cell. 28 (5), 613-623 (2017).
- Mavrakis, M., et al. Septins promote F-actin ring formation by crosslinking actin filaments into curved bundles. Nature Cell Biology. 16 (4), 322-334 (2014).
- Karasmanis, E. P., et al. A septin double ring controls the spatiotemporal organization of the ESCRT machinery in cytokinetic abscission. Current Biology. 29 (13), 2174-2182 (2019).
- Hagiwara, A., et al. Submembranous septins as relatively stable components of actin-based membrane skeleton. Cytoskeleton. 68 (9), 512-525 (2011).
- Calvo, F., et al. Cdc42EP3/BORG2 and septin network enables mechano-transduction and the emergence of cancer-associated fibroblasts. Cell Reports. 13 (12), 2699-2714 (2015).
- Salameh, J., Cantaloube, I., Benoit, B., Poüs, C., Baillet, A. Cdc42 and its BORG2 and BORG3 effectors control the subcellular localization of septins between actin stress fibers and microtubules. Current Biology. 31 (18), 4088-4103 (2021).
- Kuzmić, M., et al. Septin-microtubule association via a motif unique to isoform 1 of septin 9 tunes stress fibers. Journal of Cell Science. 135 (1), (2022).
- Shindo, A., et al. Septin-dependent remodeling of cortical microtubule drives cell reshaping during epithelial wound healing. Journal of Cell Science. 131 (12), (2018).
- Hu, Q., Nelson, W. J., Spiliotis, E. T. Forchlorfenuron alters mammalian septin assembly, organization, and dynamics. Journal of Biological Chemistry. 283 (43), 29563-29571 (2008).
- Mavrakis, M., Tsai, F. C., Koenderink, G. H. Purification of recombinant human and Drosophila septin hexamers for TIRF assays of actin-septin filament assembly. Methods in Cell Biology. 136, 199-220 (2016).
- Nakos, K., Radler, M. R., Spiliotis, E. T. Septin 2/6/7 complexes tune microtubule plus-end growth and EB1 binding in a concentration- and filament-dependent manner. Molecular Biology of the Cell. 30 (23), 2913-2928 (2019).
- Kaplan, C., et al. Absolute arrangement of subunits in cytoskeletal septin filaments in cells measured by fluorescence microscopy. Nano Letters. 15 (6), 3859-3864 (2015).
- Castro, D. K. S. V., et al. A complete compendium of crystal structures for the human SEPT3 subgroup reveals functional plasticity at a specific septin interface. IUCrJ. 7, 462-479 (2020).
- Jiao, F., Cannon, K. S., Lin, Y. -. C., Gladfelter, A. S., Scheuring, S. The hierarchical assembly of septins revealed by high-speed AFM. Nature Communications. 11 (1), 1-13 (2020).
- Bertin, A., et al. Phosphatidylinositol-4,5-bisphosphate promotes budding yeast septin filament assembly and organization. Journal of Molecular Biology. 404 (4), 711-731 (2010).
- Bridges, A. A., Jentzsch, M. S., Oakes, P. W., Occhipinti, P., Gladfelter, A. S. Micron-scale plasma membrane curvature is recognized by the septin cytoskeleton. Journal of Cell Biology. 213 (1), 23-32 (2016).
- Beber, A., et al. Membrane reshaping by micrometric curvature sensitive septin filaments. Nature Communications. 10, 420 (2019).
- Zhou, R., Shi, Y., Yang, G. Expression, purification, and enzymatic characterization of intramembrane proteases. Methods in Enzymology. 584, 127-155 (2017).
- Diebold, M. L., Fribourg, S., Koch, M., Metzger, T., Romier, C. Deciphering correct strategies for multiprotein complex assembly by co-expression: Application to complexes as large as the histone octamer. Journal of Structural Biology. 175 (2), 178-188 (2011).
- Lebedeva, M. A., Palmieri, E., Kukura, P., Fletcher, S. P. Emergence and rearrangement of dynamic supramolecular aggregates visualized by interferometric scattering microscopy. ACS Nano. 14 (9), 11160-11168 (2020).
- Ludtke, S. J., Baldwin, P. R., Chiu, W. EMAN: Semiautomated software for high-resolution single-particle reconstructions. Journal of Structural Biology. 128 (1), 82-97 (1999).
- Zivanov, J., et al. New tools for automated high-resolution cryo-EM structure determination in RELION-3. eLife. 7, 42166 (2018).
- Frank, J., et al. SPIDER and WEB: Processing and visualization of images in 3D electron microscopy and related fields. Journal of Structural Biology. 116 (1), 190-199 (1996).
- Young, G., Kukura, P. Interferometric scattering microscopy. Annual Review of Physical Chemistry. 70, 301-322 (2019).
- Young, G., et al. Quantitative mass imaging of single biological macromolecules. Science. 360 (6387), 423-427 (2018).
- Hernández-Rodríguez, Y., Momany, M. Posttranslational modifications and assembly of septin heteropolymers and higher-order structures. Current Opinion in Microbiology. 15 (6), 660-668 (2012).
- Ribet, D., et al. SUMOylation of human septins is critical for septin filament bundling and cytokinesis. Journal of Cell Biology. 216 (12), 4041-4052 (2017).
- Sinha, I., et al. Cyclin-dependent kinases control septin phosphorylation in Candida albicans hyphal development. Developmental Cell. 13 (3), 421-432 (2007).
- Sheffield, P. J., et al. Borg/Septin interactions and the assembly of mammalian septin heterodimers, trimers, and filaments. Journal of Biological Chemistry. 278 (5), 3483-3488 (2003).
- Joberty, G., et al. Borg proteins control septin organization and are negatively regulated by Cdc42. Nature Cell Biology. 3 (10), 861-866 (2001).
- Chen, X., Wang, K., Svitkina, T., Bi, E. Critical roles of a RhoGEF-anillin module in septin architectural remodeling during cytokinesis. Current Biology. 30 (8), 1477-1490 (2020).
- Kučera, O., et al. Anillin propels myosin-independent constriction of actin rings. Nature Communications. 12 (1), 1-12 (2021).
- Hsu, S. C., et al. Subunit composition, protein interactions, and structures of the mammalian brain sec6/8 complex and septin filaments. Neuron. 20 (6), 1111-1122 (1998).
- Olivi, L., et al. Towards a synthetic cell cycle. Nature Communications. 12 (1), 1-11 (2021).
- Hürtgen, D., Härtel, T., Murray, S. M., Sourjik, V., Schwille, P. Functional modules of minimal cell division for synthetic biology. Advanced Biosystems. 3 (6), 1800315 (2019).
- Jia, H., Schwille, P. Bottom-up synthetic biology: Reconstitution in space and time. Current Opinion in Biotechnology. 60, 179-187 (2019).
- Cannon, K. S., Woods, B. L., Crutchley, J. M., Gladfelter, A. S. An amphipathic helix enables septins to sense micrometer-scale membrane curvature. The Journal of Cell Biology. 218 (4), 1128-1137 (2019).
- Lobato-Márquez, D., Mostowy, S. Septins recognize micron-scale membrane curvature. Journal of Cell Biology. 213 (1), 5-6 (2016).

