Malet Tissue i Compressed Kollagen: en cell som innehåller BioTransplant för enkel iscensatt rekonstruktiv Repair
Summary
Vävnadsteknik inkluderar ofta in vitro expansion i syfte att skapa autotransplantat för vävnadsregenerering. I denna studie en metod för vävnadsexpansion, regenerering, och återuppbyggnad in vivo utvecklades för att minimera behandlingen av celler och biologiska material utanför kroppen.
Abstract
Conventional techniques for cell expansion and transplantation of autologous cells for tissue engineering purposes can take place in specially equipped human cell culture facilities. These methods include isolation of cells in single cell suspension and several laborious and time-consuming events before transplantation back to the patient. Previous studies suggest that the body itself could be used as a bioreactor for cell expansion and regeneration of tissue in order to minimize ex vivo manipulations of tissues and cells before transplanting to the patient. The aim of this study was to demonstrate a method for tissue harvesting, isolation of continuous epithelium, mincing of the epithelium into small pieces and incorporating them into a three-layered biomaterial. The three-layered biomaterial then served as a delivery vehicle, to allow surgical handling, exchange of nutrition across the transplant, and a controlled degradation. The biomaterial consisted of two outer layers of collagen and a core of a mechanically stable and slowly degradable polymer. The minced epithelium was incorporated into one of the collagen layers before transplantation. By mincing the epithelial tissue into small pieces, the pieces could be spread and thereby the propagation of cells was stimulated. After the initial take of the transplants, cell expansion and reorganization would take place and extracellular matrix mature to allow ingrowth of capillaries and nerves and further maturation of the extracellular matrix. The technique minimizes ex vivo manipulations and allow cell harvesting, preparation of autograft, and transplantation to the patient as a simple one-stage intervention. In the future, tissue expansion could be initiated around a 3D mold inside the body itself, according to the specific needs of the patient. Additionally, the technique could be performed in an ordinary surgical setting without the need for sophisticated cell culturing facilities.
Introduction
De flesta vävnadstekniska studier transplantation till huden och urogenitalsystemet inkluderar autologa cell skördar från frisk vävnad och cellexpansion i specialutrustade cell odling anläggningar 1,2.
Efter cellexpansion, cellerna vanligtvis lagras för senare användning när patienten är beredd att ta emot den kroppsegna. Kväve frysar tillåta långvarig lagring vid låga temperaturer av -150 ° C eller lägre. Processen för frysning måste vara försiktig och kontrollerad för att inte förlora cellerna. En risk av celldöd är kristallisation av intracellulärt vatten under upptiningsprocessen, vilket kan leda till brott på cellmembranen. Cell frysning utförs vanligtvis genom långsam och kontrollerad kylning (-1 ° C per min), med användning av en hög koncentration av celler, fetalt bovinserum, och dimetylsulfoxid. Efter upptining av cellerna behöver bearbetas på nytt genom att ta bort frysmedium och odling på cellodlings plast eller enbiomaterial innan transplantation tillbaka till patienten.
Alla de ovan nämnda stegen är tidskrävande, arbetskrävande och kostsamma 3. Dessutom, alla in vitro-behandling av celler avsedda för patient transplantation är starkt reglerad och kräver välutbildad och ackrediterade personal och laboratorier 4. Allt som allt, att anskaffa en säker och tillförlitlig tillverkningsprocess, tekniken kan endast fastställas i ett mycket litet antal tekniskt avancerade centra och en bredare användning i vanliga kirurgiska sjukdomar är tveksamt.
I syfte att övervinna begränsningarna hos cellodling i laboratoriemiljön, är konceptet med att transplantera malda vävnaden för cell expansionen in vivo infördes genom att använda kroppen själv som en bioreaktor. För dessa ändamål, skulle auto företrädesvis att transplanteras på en 3D-form enligt den form som behövs för den slutliga rekonstruktionen av organ intresset 5-7.
Ursprungligen var tanken att transplantera malet epitel presenteras av Meek 1958 när han beskrev hur epitel växer från kanterna av ett sår. Han visade att en liten bit hud skulle öka sina marginaler och därmed dess potential för expansion cell med 100% genom att skära bit två gånger i vinkelräta riktningar (Figur 1) 8. Teorin har fått stöd genom användning av nät med partiell tjocklek hudtransplantation för hudtransplantation 9 och i huden sårläkningsmodeller 10.
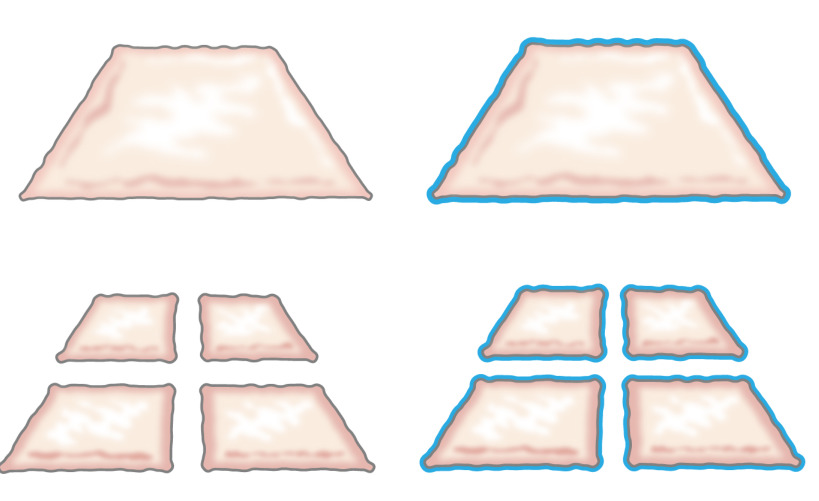
Figur 1:. Meek teori Enligt Meek teori, växer epitel från kanterna av ett sår. Genom att öka området exponeras av malningen teknik, epithelializes malet vävnad sår från många platser.
Den aktuella studien är baserad på hypotesen att samma princip skulle kunna tillämpas på den subkutana vävnaden genom att placera malet epitel runt en form. Epitelcellerna skulle mobilisera från malet transplantationer (omorganisera), täcker de lindade områden (migrerar) och dividera (expandera) i syfte att bilda en kontinuerlig neoepithelium som täcker sårområdet och separerar det främmande föremålet (formen) från den inre kroppen ( Figur 2).

Figur 2:. Tecknad av en 3D-form med malet epitel för in vivo intrakorporeal expansions vävnad enligt teorin om Meek Genom att använda malda vävnaden placeras på en form och därefter transplanteras till den subkutana vävnaden, är hypotesen att epitelcellerna migrera från kanterna av den malda vävnaden, omorganisera, och expandera för att bilda en kontinuerlig neoepithelium som täcker sårområdet och separerar det främmande föremålet (formen) från den inre kroppen.
Även tidigare in vivo-studier visar lovande resultat, kan ytterligare förbättringar uppnås genom att förstärka de auto så att regenere epitel kunde motstå mekanisk trauma bättre 7. För dessa ändamål, var viktiga förutsättningar för en framgångsrik biomaterial identifierats, såsom: enkel diffusion av näringsämnen och avfallsprodukter, möjlighet att mögel i en 3D sätt och enkelheten i kirurgisk behandling. Slutsatser gjordes att dessa behov kan tillgodoses genom att lägga till en sammansatt biomaterial till malet vävnaden.
Den aktuella studien syftar till att utveckla en byggnadsställning som består av malet vävnad i plast-komprimerade kollagen innehållande en förstärkande kärna av en biologiskt nedbrytbar tyg. På detta sätt kan livskraftiga celler migrera från malet vävnadspartiklar och föröka sig med morfologiska egenskaper som kännetecknar den ursprungliga epitel (hud eller urothelium). Med hjälp av plast kompression, ställningen var att minskad i storlek från 1 cm till omkring 420 um som det malda partiklarna var innesluten i det övre skiktet kollagen. Stomfilten kan vara vilken som helst polymer men behöver modifieras med en hydrofil yta i syfte att koppla samman med de täckande kollagenskikt 11.
Metoden gav en förbättrad ställnings integritet genom att införliva en stickad mesh bestående av poly (ε-kaprolakton) (PCL) inom två plast komprimerad kollagengeler använder den som en byggnadsställning för odling malet blåsan slemhinnan eller malet hud från svin. Konstruktet bibehölls i cellodlingsbetingelser i upp till 6 veckor in vitro, vilket demonstrerar framgångsrik bildning av en skiktad, flerskiktad urotelium eller skvamöst huden epitelet på toppen av en väl konsoliderad hybrid konstrukt. Konstruktionen var lätta att hantera och kan sys på plats för blås augmentation ändamål eller beläggning av skalet. Alla delar av vävnadsbyggnadsställning är FDA-godkända och teknikenskulle kunna användas för förfaranden enstegs genom vävnadsskörd, mals, plast kompression, och transplantera tillbaka till patienten som en enda-iscensatt ingripande. Det förfarande skulle kunna utföras för expansion vävnad och rekonstruktion under sterila betingelser i någon allmän kirurgi enhet.
Protocol
Representative Results
Discussion
Denna studie presenteras en enkel att använda tillvägagångssättet för att producera blåsväggen fläckar med autolog vävnad för transplantation vid operationsbordet. Plåstren är bildade genom kombinationen av en biologiskt nedbrytbar polymer stickning i mitten och kollagen med och utan malda vävnaden i de yttre ytorna i kombination med plast komprimering. Plast komprimering är en metod som tidigare beskrivits av andra författare och kan definieras som en snabb utdrivning av vätska från kollagengeler …
Disclosures
The authors have nothing to disclose.
Acknowledgements
The authors thank the Swedish Society for Medical Research, the Promobilia Foundation, the Crown Princess Lovisa Foundation, the Freemason Foundation for Children’s Welfare, the Swedish Society of Medicine, the Solstickan Foundation, Karolinska Institutet, and the Stockholm City Council for financial support.
Materials
| Silicone catheter 10-French | Preparing the animal for surgery , Section 1 | ||
| DMEM 10X | Gibco | 31885-023 | Plastic compression section 4 |
| 24 well plates | Falcon | 08-772-1 | Plastic compression section 4 |
| 3'3,'5-Triiodothyronine | Sigma-Aldrich | IRMM469 | In vitro culture; Section 5 |
| 4% PFA | Labmed Solutions | 200-001-8 | Immunocytochemistry; Section 6 |
| 70% ethanol | Histolab | Immunocytochemistry; Section 6 | |
| ABC Elite kit: Biotin -Streptavidin detection kit | Vector | PK6102 | Immunocytochemistry; Section 6 |
| Absolute ethanol | Histolab | 1399.01 | Immunocytochemistry; Section 6 |
| Adenine | Sigma-Aldrich | A8626 | In vitro culture; Section 5 |
| Atropine 25 μg/kg | Temgesic, RB Pharmaceuticals, Great Britain | Preparing the animal for surgery , Section 1 | |
| Azaperone 2 mg/kg | Stresnil, Janssen-Cilag, Pharma, Austria | Preparing the animal for surgery , Section 1 | |
| Biosafety Level 2 hood | Plastic compression; Section 4 | ||
| Blocking solution: Normal serum from the same species as the secondary secondary antibody was generated in. | Vector | The blocking solution depends of the origin of first antibody | Immunocytochemistry; Section 6 |
| Buprenorphine 45 μg/kg | Atropin, Mylan Inc, Canonsburg, PA | Preparing the animal for surgery , Section 1 | |
| Carprofen 3 mg/kg | Rimadyl, Orion Pharma, Sweden | Preparing the animal for surgery , Section 1 | |
| Chlorhexidine gluconate | Hibiscrub 40 mg/mL, Regent Medical, England | Preparing the animal for surgery , Section 1 | |
| Cholera toxin | Sigma-Aldrich | C8052 | In vitro culture; Section 5 |
| Coplin jar: staining jar for boiling | Histolab | 6150 | Immunocytochemistry; Section 6 |
| Stainless mold (33x22x10 mm) custom made | Plastic compression; Section 4 | ||
| DMEM | Gibco | 3188-5023 | Plastic compression section 4. Keep on ice when using it in plastic compression |
| Epidermal growth factor | Sigma-Aldrich | E9644 | In vitro culture; Section 5 |
| Ethilon (non-absorbable monofilament for skin sutures) | Ethicon | Surgery, Section 1 | |
| Fetal bovine serum (FBS) | Gibco | 10437-036 | Plastic compression section 4 |
| Forceps (Adison with tooth) | Preparing the animal for surgery , Section 1 | ||
| Gauze (Gazin Mullkompresse) | Preparing the animal for surgery , Section 1 | ||
| Ham´s F12 | Gibco | 31765-027 | Plastic compression section 4 |
| Hematoxylin | Histolab | 1820 | Immunocytochemistry; Section 6 |
| Humidity chamber | DALAB | Immunocytochemistry; Section 6 | |
| Hydrocortisone | Sigma-Aldrich | H0888 | In vitro culture; Section 5 |
| Hydrogen peroxide Solution 30% | Sigma-Aldrich | H1009 | Immunocytochemistry; Section 6 |
| Insulin | Sigma-Aldrich | I3536 | In vitro culture; Section 5 |
| Isoflurane | Isoflurane, Baxter, Deerfield, IL | Preparing the animal for surgery , Section 1 | |
| Lidocaine 5 mg/ml | Xylocaine, AstraZeneca, Sweden | Preparing the animal for surgery , Section 1 | |
| Lucose 25 mg/mL | Baxter, Deerfield, IL | Preparing the animal for surgery , Section 1 | |
| Marker pen pap pen | Sigma-Aldrich | Z377821-1EA | Immunocytochemistry; Section 6 |
| Medetomidine 25 μg/kg | Domitor, Orion Pharma, Sweden | Preparing the animal for surgery , Section 1 | |
| Mincing device | Applied Tissue Technologies LLC | Minced tissue preparation, section 2 | |
| Monocryl (absorbable monofilament) | Ethicon | Surgery, Section 1 | |
| NaCl | Sigma-Aldrich | S7653 | Immunocytochemistry; Section 6 |
| NaOH 1N | Merck Millipore | 106462 | Plastic compression section 4 and cell culture |
| Nylon mesh, 110 uM thick pore size 0.04 sqmm | Plastic compression; Section 4 | ||
| Oculentum simplex APL: ointment for eye protection | APL | Vnr 336164 | Surgery, Section 1 |
| PBS | Gibco | 14190-094 | Plastic compression section 4 |
| Penicillin-Streptomycin | Gibco | 15140-122 | Plastic compression section 4 |
| Phenobarbiturate 15 mg/kg | Pentobarbital, APL, Sweden | Preparing the animal for surgery , Section 1 | |
| PLGA Knitted fabric | Plastic compression; Section 4 | ||
| Rat-tail collagen | First LINK, Ltd, UK | 60-30-810 | Plastic compression section 4, keep on ice |
| Scalpel blade – 15 | Preparing the animal for surgery , Section 1 | ||
| Shaving shears | Preparing the animal for surgery , Section 1 | ||
| Stainless stell mesh, 400 uM thick pore size | Plastic compression; Section 4 | ||
| Steril gloves | Preparing the animal for surgery , Section 1 | ||
| Sterile gowns | Preparing the animal for surgery , Section 1 | ||
| Sterile drapes | |||
| Sterilium | Bode Chemie HAMBURG | Preparing the animal for surgery , Section 1 | |
| Suture Thread Ethilon | Preparing the animal for surgery , Section 1 | ||
| TE-solution (antigen unmasking solution) consist of 10 mM Tris and 1 mM EDTA, pH 9.0 | 10 mM Tris/1 mM EDTA, adjust pH to 9.0 | ||
| Tiletamine hypochloride 2,5 mg/kg | Preparing the animal for surgery , Section 1 | ||
| Transferrin | Sigma-Aldrich | T8158 | In vitro culture; Section 5 |
| Trizma Base, H2NC | Sigma-Aldrich | T6066 | Immunocytochemistry; Section 6 |
| Vector VIP kit: Enzyme peroxidase substrate kit | Vector | SK4600 | Immunocytochemistry; Section 6 |
| Vicryl (absorbable braded) | Ethicon | Surgery, Section 1 | |
| Tris buffer pH 7.6 (washing buffer) | TE solution: Make 10X (0,5M Tris, 1,5M NaCl) by mixing: 60,6 g Tris (Trizma Base, H2NC(CH2OH)3, M=121.14 g/mol), add 800 ml distilled water adjust the pH till 7.6, add 87,7 g NaCl and fill to 1000 ml with distilled water. Dilute to 1X with distilled water. | ||
| X-tra solv (solvent) | DALAB | 41-5213-810 | Immunocytochemistry; Section 6. Use under fume hood |
| Zolazepam hypochloride | Zoletil, Virbac, France | Preparing the animal for surgery , Section 1 | |
| Depilatory wax strips | Veet | Preparing the animal for surgery , Section 1 | |
| Pentobarbital sodium | Lundbeck | Termination, Section 3 |
References
- Rheinwald, J. G., Green, H. Serial cultivation of strains of human epidermal keratinocytes: the formation of keratinizing colonies from single cells. Cell. 6, 331-343 (1975).
- Fossum, M., Nordenskjold, A., Kratz, G. Engineering of multilayered urinary tissue in vitro. Tissue Engineering. 10, 175-180 (2004).
- Salmikangas, P., et al. Manufacturing, characterization and control of cell-based medicinal products: challenging paradigms toward commercial use. Regen Med. 10, 65-78 (2015).
- Fossum, M., et al. Minced skin for tissue engineering of epithelialized subcutaneous tunnels. Tissue Engineering. Part A. 15, 2085-2092 (2009).
- Fossum, M., et al. Minced urothelium to create epithelialized subcutaneous conduits. The Journal of Urology. 184, 757-761 (2010).
- Reinfeldt Engberg, G., Lundberg, J., Chamorro, C. L., Nordenskjold, A., Fossum, M. Transplantation of autologous minced bladder mucosa for a one-step reconstruction of a tissue engineered bladder conduit. BioMed Research International. 2013, 212734 (2013).
- Meek, C. P. Successful microdermagrafting using the Meek-Wall microdermatome. Am J Surg. 96, 557-558 (1958).
- Tanner, J. C., Vandeput, J., Olley, J. F. The Mesh skin graft. Plastic and Reconstructive Surgery. 34, 287-292 (1964).
- Svensjo, T., et al. Autologous skin transplantation: comparison of minced skin to other techniques. The Journal of Surgical Research. 103, 19-29 (2002).
- Ajalloueian, F., Zeiai, S., Rojas, R., Fossum, M., Hilborn, J. One-stage tissue engineering of bladder wall patches for an easy-to-use approach at the surgical table. Tissue Engineering. Part C, Methods. 19, 688-696 (2013).
- Engelhardt, E. M., et al. A collagen-poly(lactic acid-co-varepsilon-caprolactone) hybrid scaffold for bladder tissue regeneration. Biomaterials. 32, 3969-3976 (2011).
- Brown, R. A., Wiseman, M., Chuo, C. B., Cheema, U., Nazhat, S. N. Ultrarapid engineering of biomimetic materials and tissues: fabrication of nano- and microstructures by plastic compression. Adv Funct Mater. 15, 1762-1770 (2005).
- Fumagalli Romario, U., Puccetti, F., Elmore, U., Massaron, S., Rosati, R. Self-gripping mesh versus staple fixation in laparoscopic inguinal hernia repair: a prospective comparison. Surg Endosc. 27, 1798-1802 (2013).
- Muangman, P., et al. Complex Wound Management Utilizing an Artificial Dermal Matrix. Annals of Plastic Surgery. 57, 199-202 (2006).
- Ajalloueian, F., Zeiai, S., Fossum, M., Hilborn, J. G. Constructs of electrospun PLGA, compressed collagen and minced urothelium for minimally manipulated autologous bladder tissue expansion. Biomaterials. 35, 5741-5748 (2014).
- Orabi, H., AbouShwareb, T., Zhang, Y., Yoo, J. J., Atala, A. Cell-seeded tubularized scaffolds for reconstruction of long urethral defects: a preclinical study. Eur Urol. 63, 531-538 (2013).
- Blais, M., Parenteau-Bareil, R., Cadau, S., Berthod, F. Concise review: tissue-engineered skin and nerve regeneration in burn treatment. Stem Cells Transl Med. 2, 545-551 (2013).
- Serpooshan, V., Muja, N., Marelli, B., Nazhat, S. N. Fibroblast contractility and growth in plastic compressed collagen gel scaffolds with microstructures correlated with hydraulic permeability. J Biomed Mater Res A. 96, 609-620 (2011).

