Akustik Levitasyon Sisteminde Küresel Olmayan Kabarcık Salınımları ile Mikroakışın İndüksiyonu
Summary
İki kabarcık arasındaki birleşme tekniğine dayanan tek, sıkışmış bir akustik kabarcığın şekil salınımlarını kontrol etmek için hızlı ve güvenilir bir teknik önerilmektedir. Kararlı durum, simetri kontrollü kabarcık şekli salınımları, kabarcık arayüzünün yakınında üretilen sıvı akışının analizine izin verir.
Abstract
Biyolojik bariyerlerin yakınında bulunduğunda, salınımlı mikrokabarcıklar hücre zarı geçirgenliğini artırabilir ve ilaç ve gen içselleştirmesine izin verebilir. Deneysel gözlemler, bu bariyerlerin geçici geçirgenliğinin, kavitasyon mikro akışı ile hücre dokularına uygulanan kesme stresinden kaynaklanabileceğini düşündürmektedir. Kavitasyon mikro akışı, salınımlı ultrason mikro kabarcıkları etrafında ortaya çıkan vorteks akışlarının oluşumudur. Bu tür sıvı akışları üretmek için, kabarcık salınımları tamamen küresel salınımlardan sapmalı ve translasyonel bir kararsızlık veya şekil modları içermelidir. Kabarcık kaynaklı akışlar ve yakındaki yüzeylerdeki kayma gerilmesi üzerine yapılan deneysel çalışmalar, mikro kabarcıkların şekil deformasyonlarını kararlı ve kontrol edilebilir bir şekilde yakalamanın zorluğu nedeniyle genellikle kapsamlarında sınırlıdır. Simetri kontrollü küresel olmayan salınımların incelenmesi için akustik bir kaldırma odasının tasarımını açıklıyoruz. Bu kontrol, yeterince yoğun bir ultrason alanında yaklaşan iki kabarcık arasında bir birleştirme tekniği kullanılarak gerçekleştirilir. Küresel olmayan salınımların kontrolü, serbest yüzey salınımlı bir mikro kabarcığın kontrollü bir kavitasyon mikro akışına giden yolu açar. Yüksek kare hızlı kameralar, akustik zaman ölçeğinde küresel olmayan kabarcık dinamiklerini ve daha düşük bir zaman ölçeğinde sıvı akışını yarı eşzamanlı olarak araştırmaya olanak tanır. Çok çeşitli akışkan desenlerinin elde edilebileceği ve bunların kabarcık arayüzünün modal içeriği ile ilişkili olduğu gösterilmiştir. Arayüz dinamikleri birkaç mod içeriyorsa, yüksek dereceli şekil modlarının bile büyük mesafeli akışkan desenleri oluşturabileceğini gösteriyoruz ve hedeflenen ve lokalize ilaç dağıtımı için küresel olmayan salınımların potansiyelini vurguluyoruz.
Introduction
Tıpta, uygulanan bir ilaç, istenen hedeflere ulaşmadan önce canlı sistemdeki birçok engele nüfuz etmelidir. Bununla birlikte, çoğu ilaç hızla kan dolaşımından uzaklaştırılır. Hedefleme etkinliği düşüktür ve hücre zarlarını kolayca geçemezler, bu da etkisiz ilaç dağıtımına yol açar. Günümüzde, ultrason ile kombinasyon halinde mikrokabarcıkların kullanımı, ilaçların ve genlerin patolojik dokulara ve hücrelere invaziv olmayan, kesin ve hedefe yönelik olarak verilmesi için yenilikçi bir yöntem olarak önerilmiştir1. Bu yaklaşımda, mikro kabarcıklar, serbest ilaçların bir gaz kabarcığı süspansiyonu ile birlikte enjekte edildiği veya yüzeyine yüklendiği taşıyıcılar olarak rol oynayabilir. Mikrokabarcıklar ayrıca hücrelerle etkileşime girmek için ultrason enerjisini yeniden odaklamak için yerel bir vektör görevi görebilir. Temel olarak, ultrasona maruz kalma altında, kabarcıklar kararlı bir şekilde sıkıştırır ve genişler, sıvı akışları üreten ve dolayısıyla yakındaki nesneler üzerinde kayma stresi oluşturan kararlı kavitasyon adı verilen bir rejim. Mikrokabarcıklar ayrıca doğrusal olmayan bir şekilde salınım yapabilir ve atalet kavitasyonu rejiminde çökene kadar genişleyebilir ve çökme bölgesindenradyal olarak yayılan şok dalgaları üretebilir 2. Stabil veya atalet halindeki kavitasyonun, hücre zarlarının geçirgenliğini arttırdığı ve böylece ilaçların hücre içine içselleştirilmesini arttırdığı gösterilmiştir3.
Terapötik uygulamalarda, kabarcık-hücre etkileşiminin mekanizmasını anlamak çok önemlidir, ancak hem bilimsel hem de teknik açıdan, bilgimizin ilerlemesini engelleyen çeşitli engeller vardır. İlk olarak, kabarcık kaynaklı mekanik uyaranlara yanıt olarak hücrelerin dinamiklerini yakalamak çok zordur4. Akustik zaman ölçeğinde, birinci dereceden mikrokabarcık salınımları, membran kanallarının aktivasyonuna yol açarak biyolojik arayüzler arasında moleküler geçişi kolaylaştırabilir. Bu, “hücresel masaj”5 olarak da adlandırılan hücre zarının doğrudan salınımı yoluyla gerçekleşir. Doğrudan mekanik stresi takiben kanal aktivasyonu, ultrason maruziyeti sırasında ve sonrasında hücre zarlarının elektrofizyolojik özelliklerini ölçen yama-kelepçe teknikleri kullanılarak kanıtlanmıştır6. Kabarcık kaynaklı hücre dinamiklerini (hücre zarının deformasyonunun tam alanı anlamına gelir) akustik zaman ölçeğinde ölçmek, gözenekleri hücre zarına indüklemek için gereken membran alanı genişlemesi ΔA / A eşiğinde de içgörüler sağlayacaktır7. İkinci bariyer, mikro kabarcık kaynaklı hücre lizizini önlemek için çöken kabarcık rejimini kontrol etmektir. Kabarcık çökmeleri ve indüklenen mikrojetler, membran perforasyonunun meydana geldiği bir mekanizma olarak tanımlanmıştır 8,9. Geçirgen hale getirildikten sonra, hücre zarı, lipit çift katmanlarının kalsiyumun kendi kendine sızdırmazlığı ve hücre içi veziküllerin füzyonu yoluyla onarılır9. Kabarcık çökmelerinin meydana gelmesi de hücrede ölümcül hasarlara neden olabilir ve çevredekilerde gereksiz yan etkilere neden olabilir. Ultrason aracılı kan-beyin bariyeri açılması gibi hassas uygulamalarda atalet kabarcığı çökmelerinden kaçınılması gerektiği genel kabul görmektedir10.
Bu nedenle, mikrokabarcıkların kararlı salınımlarını sağlamak için pasif kavitasyon izleme ve kontrolü ile birlikte ultrason emisyon dizilerinin tasarımına büyük çabalar harcanmaktadır11. Bu kararlı rejimde, kararlı bir şekilde salınan kabarcıkların, hücre zarı7 üzerinde uzamsal olarak hedeflenmiş kayma stresini teşvik ederek membran geçirgenliğinin tetiklenmesinde güçlü bir rol oynadığı varsayılmıştır. Kayma gerilmesi, salınımlı kabarcıkların yakınında oluşturulan sıvı akışlarından kaynaklanır. Bu sıvı akışlarına kavitasyon mikro akışı denir ve yukarıda belirtildiği gibi, hücre dışı moleküllerin gelişmiş alımından sorumlu olan birkaç olası mekanizmadan biridir. Kabarcıkların veya hücrelerin in-vitro biyolojik transfeksiyon tahlilleri12 gibi süspansiyonu ile uğraşırken, mikro akış ile geçirgenlik, kabarcık çökmesi ile geçirgenlikten çok daha verimli olabilir. Bu, basit bir geometrik düşünceyle gösterilebilir. Hücre süspansiyonlarında, asılı hücrelerin çoğunluğu yeterince büyük mekanik etkilere (membran geçirgenliğine yol açan) gönderilirse sonoporasyon etkili olacaktır. Kabarcık çökmelerinin, kabarcık duvar ekseni13 veya kütle14 merkezlerini birleştiren kabarcık-kabarcık ve kabarcık-hücre çizgisi gibi izotropik simetri kırılma yönü boyunca yönlendirildiği bilinmektedir. Bu nedenle üretilen mikrojet, hücre ve kabarcık merkezlerine katılan sonlu sayıda çizgi boyunca mekansal olarak lokalize bir fenomendir. Hücre ve kabarcık konsantrasyonuna ve ayrıca kabarcık-hücre mesafesine bağlı olarak, bu etki asılı hücrelerin tam sayısını geçirgenleştirmek için en etkili olmayabilir. Buna karşılık, kavitasyon mikro akışı, kabarcık yarıçapına kıyasla büyük bir uzamsal genişleme ile yavaş bir zaman ölçeğinde meydana gelen bir fenomendir. Ayrıca, sıvı akışı kabarcığın her tarafına dağılır ve bu nedenle çok uzun bir aralıkta daha fazla sayıda hücreyi etkileyebilir. Bu nedenle, salınımlı bir kabarcık etrafında üretilen kavitasyon mikroakışını anlamak, hücrelere uygulanan kabarcık kaynaklı kesme stresini kontrol etmek ve ölçmek için bir ön koşuldur.
Bunu yapmak için, bir ön adım, ultrason tahrikli bir kabarcığın küresel ve küresel olmayan salınımlarını kontrol etmekten ibarettir, çünkü üretilen sıvı akışları kabarcık arayüzünün hareketi ile indüklenir15,16. Özellikle, mikro kabarcıkların şekil salınımları tetiklenmeli ve sabit tutulmalıdır. Ayrıca, kabarcık arayüzü dinamikleri ile indüklenen mikro akış paterni arasındaki korelasyonu doğru bir şekilde analiz etmek için kabarcık şekli salınımlarının oryantasyonu kontrol edilmelidir. Mevcut literatürü özetlerken, kavitasyona bağlı mikro akışın ayrıntılı deneysel sonuçlarının yalnızca bir yüzeye bağlı kabarcıklar için mevcut olduğu açıktır. Duvara bağlı mikro kabarcıklar, ultra hızlı bir mikroskopi sistemi altında mikrometre ölçeğinde doğru arayüz dinamiklerini ve hücre etkileşimlerini değerlendirmek için yaygın olarak kullanılır. Bu konfigürasyon, hücre zarı17,18,19 üzerinde bulunan titreşimli mikrokabarcıklar göz önüne alındığında terapötik olarak önemlidir. Bununla birlikte, substrata bağlı kabarcığın incelenmesi, kısmen temas hattı dinamiği20’nin karmaşık doğası ve asimetrik şekil modlarının tetiklenmesi nedeniyle kabarcık dinamiklerinin analizini daha karmaşık hale getirebilir21. Tıbbi ve biyolojik uygulamalarda, bir duvara tutturulmamış kabarcıklar genellikle küçük kaplar gibi sınırlı geometrilerde bulunur. Bu, kabarcık dinamiklerini ve şekil dengesizliklerini önemli ölçüde etkiler. Özellikle, yakındaki bir duvarın varlığı, şekil modu için basınç eşiğini kaydırır ve şekil modu numarasına ve kabarcık boyutu22’ye bağlı olarak basınç değerlerini düşürmek için tetiklenir. Duvar ayrıca, üretilen akış23 için muhtemelen daha yüksek yoğunlukta kabarcık kaynaklı mikro akışı da etkiler.
Mikro kabarcıkların yaşayabileceği tüm olası senaryolar arasında (serbest veya bağlı, bir duvara yakın, çöken veya istikrarlı bir şekilde salınımlı), herhangi bir sınırdan uzak tek bir kabarcığın küresel olmayan dinamiklerini araştırmayı öneriyoruz. Deneysel kurulum, kabarcığı yakalamak için ayakta duran bir ultrason dalgasının kullanıldığı akustik bir kaldırma sistemi24’e dayanmaktadır. Bu senaryo, örneğin bir sonotransfeksiyon odasında asılı kabarcıklar ve hücreler koleksiyonunun bir arada bulunduğu tıbbi uygulamalarla tutarlıdır. Kabarcıklar ve hücreler çok yakın olmadığı sürece, bir hücrenin varlığının kabarcık arayüz dinamiklerini etkilemediği varsayılmaktadır. Hücreler kavitasyona bağlı mikro akışın döngü benzeri yörüngelerini takip ettiklerinde, döngüsel olarak kabarcık konumundan yaklaşır ve itilirler ve hücre varlığının ne akış modelini ne de ortalama hızını etkilemediğini varsayabiliriz. Ek olarak, küresel olmayan dinamikler ve sınırdan uzak tek kabarcıklardan indüklenen mikro akış, teorik bir bakış açısıyla iyi bilinmektedir. Kabarcık kaynaklı sıvı akışını kabarcık kontur dinamiklerine bağlamak için, kabarcık arayüz dinamiklerini doğru bir şekilde karakterize etmek gerekir. Bunu yapmak için, deneysel çalışmalarda mekansal zamansal ölçeğin terapötiklerde kullanılanlara göre uyarlanması tercih edilir, böylece ortak yüksek hızlı kameralarla (1 milyon kare / saniyenin altında) elde etmek, daha düşük frekanslarda uyarılan büyük kabarcıklar kullanılarak elde edilebilir. Kaplanmamış kabarcıklar göz önüne alındığında, belirli bir n modunun özfrekansı ωn, kabarcık boyutu ile 25 olarak 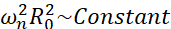 ilişkilidir. Bu yarıçap-özfrekans ilişkisi, kabuklu kabarcıklar26 göz önüne alındığında biraz değiştirilir, ancak özfrekans ωn’nin büyüklük sırası aynı kalır. Bu nedenle, 30 kHz’lik bir ultrason alanında denge yarıçapı ~ 50μm olan kabarcıkların araştırılması, Dollet ve ark.27 tarafından önerildiği gibi, 1.7 MHz’lik bir alanda ~ 3μm yarıçaplı kaplanmış kabarcıkları incelemeye benzer. Bu nedenle benzer şekil modu numaraları ve dolayısıyla mikro akış desenleri beklenir.
ilişkilidir. Bu yarıçap-özfrekans ilişkisi, kabuklu kabarcıklar26 göz önüne alındığında biraz değiştirilir, ancak özfrekans ωn’nin büyüklük sırası aynı kalır. Bu nedenle, 30 kHz’lik bir ultrason alanında denge yarıçapı ~ 50μm olan kabarcıkların araştırılması, Dollet ve ark.27 tarafından önerildiği gibi, 1.7 MHz’lik bir alanda ~ 3μm yarıçaplı kaplanmış kabarcıkları incelemeye benzer. Bu nedenle benzer şekil modu numaraları ve dolayısıyla mikro akış desenleri beklenir.
Kabarcık arayüzünün küresel olmayan salınımlarını tetiklemek için, Şekil 1’de gösterildiği gibi, yarıçapa bağlı belirli bir basınç eşiğini aşmak gerekir. Mevcut deneysel teknikler, yüzey modlarını tetiklemek için akustik basıncın artışına dayanır (Şekil 1’de yol ( 1) ile gösterilmiştir), ya adım adım basınç artışı28 ya da yüzey modlarının periyodik başlangıcından ve yok olmasından sorumlu modüle edilmiş genlik uyarımıile 29. Bu tekniklerin başlıca dezavantajları, (i) görüntüleme düzleminde olması kontrol edilemeyen yüzey salınımlarının simetri ekseninin rastgele yönlendirilmesi, (ii) indüklenen sıvı akışlarının analizini daha büyük zaman ölçeklerinde zorlaştıran kabarcık şekli salınımlarının kısa bir ömrü ve (iii) kararsız şekil modlarının sık sık tetiklenmesidir. Şekil 1’deki yol (2) ile gösterildiği gibi, yarıçap / basınç haritasındaki sabit bir akustik basınçta basınç eşiğini geçmek için alternatif bir teknik öneriyoruz. Bunu yapmak için, kabarcık boyutunu kararsızlık bölgesinde olacak şekilde artırmak gerekir. Böyle bir artış, bir kabarcık birleştirme tekniği ile gerçekleştirilir. Başlangıçta küresel olarak salınım yapan iki mikro kabarcığın birleşmesi, tek bir deforme olmuş kabarcık oluşturmak için kullanılır. Birleştirilmiş kabarcığın akustik basıncı ve kabarcık boyutu kararsızlık bölgesindeyse, yüzey modları tetiklenir. Ayrıca, birleşme tekniğinin, kararlı bir durum rejiminde kararlı şekil salınımlarına ve ayrıca yaklaşan iki kabarcığın doğrusal hareketi ile tanımlanan kontrollü bir simetri eksenine neden olduğunu kanıtladık. Dakikalar içinde kararlı bir şekil salınımı sağlandığından, kabarcık kaynaklı sıvı akışının analizi, sıvı ortamın ince bir lazer tabakası ile aydınlatılan floresan mikropartiküllerle tohumlanmasıyla mümkündür. Kabarcık arayüzünün yakınındaki katı mikropartiküllerin hareketinin kaydedilmesi, indüklenen sıvı akışının30 modelinin tanımlanmasını sağlar. Zamana dayanıklı bir sıvı akışına yol açan kabarcık şekli salınımlarının tetiklenmesinin genel prensibi Şekil 2’de gösterilmiştir.
Aşağıdaki protokolde, birleştirme tekniği ile kararlı kabarcık şekli salınımları oluşturmak için gereken adımları özetliyoruz ve sıvı akışının ölçümlerini açıklıyoruz. Bu, akustik kaldırma sisteminin tasarımını, akustik kalibrasyonu, kabarcık çekirdeklenmesini ve birleştirme tekniğini, kabarcık arayüz dinamiklerinin ve çevresindeki sıvı akışının ölçülmesini ve görüntü işlemeyi içerir.
Protocol
Representative Results
Discussion
Sunulan prosedür, kararlı durum, simetri kontrollü kabarcık şekli salınımlarını tetiklemek için kabarcık birleşmesinin kullanılmasından oluşur ve bu salınımların neden olduğu uzun vadeli sıvı akışının incelenmesine izin verir. Teknikteki ana zorluk, herhangi bir sınırdan uzak, sıkışmış bir kabarcık için küresel olmayan salınımların kontrolüdür.
Literatürde önerilen mevcut tekniklerin çoğu, substrata bağlı kabarcıklar 7…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Bu çalışma Lyon Üniversitesi LabEx CeLyA (ANR-10-LABX-0060 / ANR-11-IDEX-0007) tarafından desteklenmiştir.
Materials
| Aspherical lens | Thorlabs | AL4050 | Lens of focus 40 mm |
| Continuous wave laser source | CNI | MLL6FN | DPSS laser of wavelength 532nm, energy 400 mW |
| Cylindrical plano-concave lens | Thorlabs | LJ1277L1-A | lens of focus -25?4mm |
| Cylindrical plano-concave lens | Thorlabs | LK1900L1 | lens of focus 250 mm |
| Fluorescent particles | Duke Scientific | R700 | Red polymer fluorescent microspheres |
| Function generator | Agilent | HP33120 | Generator of function feeding the ultrasound transducer |
| High-speed camera | Vision Research | Phantom v12.0 | High-speed recording up to 1 Mfps |
| Liquid medium | Carlo Erba | Water for analysis | Demineralized, undegassed water |
| Multiphysics software | Comsol | None | Softwate for simulating the acoustic field of the levitation chamber |
| Nd:Yag pulsed laser | New Wave Research | Solo III-15 | 5 ns pulse duration, λ=532 nm, 3.5 mm beam diameter, up to 50 mJ |
| Plano-concave lens | Thorlabs | N-BK7 | lens of focus 125 mm |
| Spherical concave lens | Thorlabs | N-SF11 | Bi-concave lens of focus -25mm |
| Ultrasound transducer | SinapTec | Custom-made | Nominal frequency 31kHz, active area 35mm diameter |
| Visualization software | NIH | ImageJ | Software for image processing and analysis in Java |
| XY Linear stage | Newport | M-406 | Displacement stage with micrometric screw |
| Z-axis linear stage | Edmund Optics | 62-299 | Vertical displacement stage with micrometric screw |
References
- Roovers, S., et al. The role of ultrasound-driven microbubble dynamics in drug delivery: from microbubble fundamentals to clinical translation. Langmuir. 35 (31), 10173-10191 (2019).
- Liu, H. L., Fan, C. H., Ting, C. Y., Yeh, C. K. Combining microbubbles and ultrasound for drug delivery to brain tumors: current progress and overview. Theranostics. 4 (4), 432-444 (2014).
- Lammertink, B. H. A., et al. Sonochemotherapy: from bench to bedside. Frontiers in Pharmacology. 6, 138 (2015).
- Lajoinie, G., et al. In vitro methods to study bubble-cell interactions: fundamentals and therapeutic applications. Biomicrofluidics. 10, 011501 (2016).
- Van Wamel, A., Bouakaz, A., Versluis, M., de Jong, N. Micromanipulation of endothelial cells: ultrasound-microbubble-cell interaction. Ultrasound in Medicine and Biology. 30, 1255-1258 (2004).
- Tran, T. A., Roger, S., Le Guennec, J. Y., Tranquart, F., Bouakaz, A. Effect of ultrasound-activated microbubbles on the cell electrophysiological properties. Ultrasound in Medicine and Biology. 33, 158-163 (2007).
- Marmottant, P., Hilgenfeldt, S. Controlled vesicle deformation and lysis by single oscillating bubbles. Nature. 423 (6936), 153-156 (2003).
- Prentice, P. A., Cuschieri, K., Dholakia, K., Prausnitz, M., Campbell, P. Membrane disruption by optically controlled microbubble cavitation. Nature Physics. 1, 107-110 (2005).
- Kudo, N., Okada, K., Yamamoto, K. Sonoporation by single-shot pulsed ultrasound with microbubbles adjacent to cells. Biophysical Journal. 96, 4866-4876 (2009).
- Novell, A., et al. A new safety index based on intrapulse monitoring of ultra-harmonic cavitation during ultrasound-induced blood-brain barrier opening procedures. Scientific Reports. 10, 10088 (2020).
- Cornu, C., et al. Ultrafast monitoring and control of subharmonic emissions of an unseeded bubble cloud during pulsed sonication. Ultrasonics Sonochemistry. 42, 697-703 (2018).
- Reslan, L., Mestas, J. L., Herveau, S., Béra, J. C., Dumontet, C. Transfection of cells in suspension by ultrasound cavitation. Journal of Controlled Release. 142 (2), 251-258 (2010).
- Reuter, F., Gonzalez-Avila, S. R., Mettin, R., Ohl, C. D. Flow fields and vortex dynamics of bubbles collapsing near a solid boundary. Physical Review Fluids. 2, 064202 (2017).
- Chew, L. W., Klaseboer, E., Ohl, S. W., Khoo, B. C. Interaction of two differently sized oscillating bubbles in a free field. Physical Review E. 84, 066307 (2011).
- Doinikov, A. A., Bouakaz, A. Acoustic microstreaming around a gas bubble. The Journal of the Acoustical Society of America. 127 (2), 703-709 (2010).
- Tho, P., Manasseh, R., Ooi, A. Cavitation microstreaming patterns in single and multiple bubble systems. Journal of Fluid Mechanics. 576, 191-233 (2007).
- Van Wamel, A., et al. Vibrating microbubbles poking individual cells: Drug transfer into cells via sonoporation. Journal of Controlled Release. 112, 149-155 (2006).
- Helfield, B., Chen, X., Watkins, S. C., Villanueva, F. S. Biophysical insight into mechanisms of sonoporation. PNAS. 113 (36), 9983-9988 (2016).
- Pereno, V., et al. Layered acoustofluidic resonators for the simultaneous optical and acoustic characterization of cavitation dynamics, microstreaming, and biological effects. Biomicrofluidics. 12, 034109 (2018).
- Shklyaev, S., Straube, A. V. Linear oscillations of a compressible hemispherical bubble on a solid substrate. Physics of Fluids. 20, 052102 (2008).
- Fauconnier, M., Bera, J. C., Inserra, C. Nonspherical modes non-degeneracy of a tethered bubble. Physical Review E. 102, 033108 (2020).
- Xi, X., Cegla, F., Mettin, R., Holsteyns, F., Lippert, A. Study of non-spherical bubble oscillations near a surface in a weak acoustic standing wave field. The Journal of the Acoustical Society of America. 135, 1731 (2014).
- Doinikov, A. A., Bouakaz, A. Effect of a distant rigid wall on microstreaming generated by an acoustically driven gas bubble. Journal of Fluid Mechanics. 742, 425-445 (2014).
- Cleve, S., Guédra, M., Inserra, C., Mauger, C., Blanc-Benon, P. Surface modes with controlled axisymmetry triggered by bubble coalescence in a high-amplitude acoustic field. Physical Review E. 98, 033115 (2018).
- Lamb, H. . Hydrodynamics. 6th ed. , (1932).
- Liu, Y., Wang, Q. Stability and natural frequency of nonspherical mode of an encapsulated microbubble in a viscous liquid. Physics of Fluids. 28, 062102 (2016).
- Dollet, B., et al. Nonspherical oscillations of ultrasound contrast agent microbubbles. Ultrasound in Medicine and Biology. 34 (9), 1465-1473 (2008).
- Versluis, M., et al. Microbubble shape oscillations excited through ultrasonic parametric driving. Physical Review E. 82, 026321 (2010).
- Guédra, M., Cleve, S., Mauger, C., Blanc-Benon, P., Inserra, C. Dynamics of nonspherical microbubble oscillations above instability threshold. Physical Review E. 96, 063104 (2017).
- Cleve, S., Guédra, M., Mauger, C., Inserra, C., Blanc-Benon, P. Microstreaming induced by acoustically trapped, non-spherically oscillating microbubbles. Journal of Fluid Mechanics. 875, 597-621 (2019).
- Doinikov, A. A., Cleve, S., Regnault, G., Mauger, C., Inserra, C. Acoustic microstreaming produced by nonspherical oscillations of a gas bubble. I. Case of modes 0 and m. Physical Review E. 100, 033104 (2019).
- Inserra, C., Regnault, G., Cleve, S., Mauger, C., Doinikov, A. A. Acoustic microstreaming produced by nonspherical oscillations of a gas bubble. III. Case of self-interacting modes n-n. Physical Review E. 101, 013111 (2020).
- Prabowo, F., Ohl, C. D. Surface oscillations and jetting from surface attached acoustic driven bubbles. Ultrasonics Sonochemistry. 18 (1), 431-435 (2011).
- Garbin, V., et al. Changes in microbubble dynamics near a boundary revealed by combined; optical micromanipulation and high-speed imaging. Applied Physics Letters. 90, 114103 (2007).
- Collis, J., et al. Cavitation microstreaming and stress fields created by microbubbles. Ultrasonics. 50, 273-279 (2010).
- Loughran, J., Eckersley, R. J., Tang, M. X. Modeling non-spherical oscillations and stability of acoustically driven shelled microbubbles. The Journal of the Acoustical Society of America. 131 (6), 4349-4357 (2012).
- Vos, H. J., Dollet, B., Bosch, J. G., Versluis, M., de Jong, N. Nonspherical vibrations of microbubbles in contact with a wall – a pilot study at low mechanical index. Ultrasound in Medicine and Biology. 34 (4), 685-688 (2008).
- Regnault, G., Mauger, C., Blanc-Benon, P., Inserra, C. Secondary radiation force between two closely spaced acoustic bubbles. Physical Review E. 102, 031101 (2020).

